文档内容
2023-2024学年高三化学下学期开学摸底考(全国卷新教材)
(考试时间:50分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮
擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
4.测试范围:高考全部内容。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Cl 35.5
一、选择题:本题共7小题,每小题6分,共42分。在每小题给出的四个选项中,只有一项是符合题目要
求的。
7.化学与生活、生产及科技密切相关。下列叙述错误的是
A.臭氧可用于自来水消毒
B.奥运火炬“飞扬”外壳采用的耐高温碳纤维材料,属于新型无机非金属材料
C.长征二号F遥十三运载火箭采用的高强度新型钛合金属于金属材料
D.纳米铁粉主要通过物理吸附作用除去污水中的 、 、
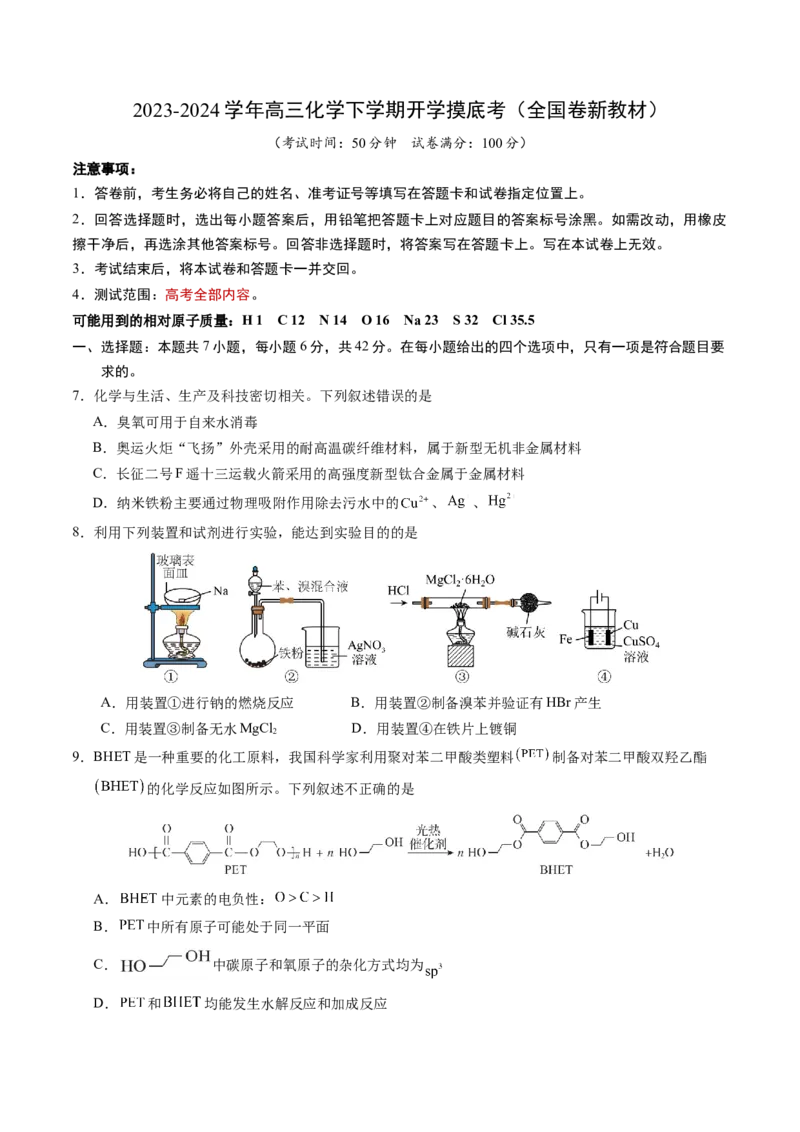
8.利用下列装置和试剂进行实验,能达到实验目的的是
A.用装置①进行钠的燃烧反应 B.用装置②制备溴苯并验证有HBr产生
C.用装置③制备无水MgCl D.用装置④在铁片上镀铜
2
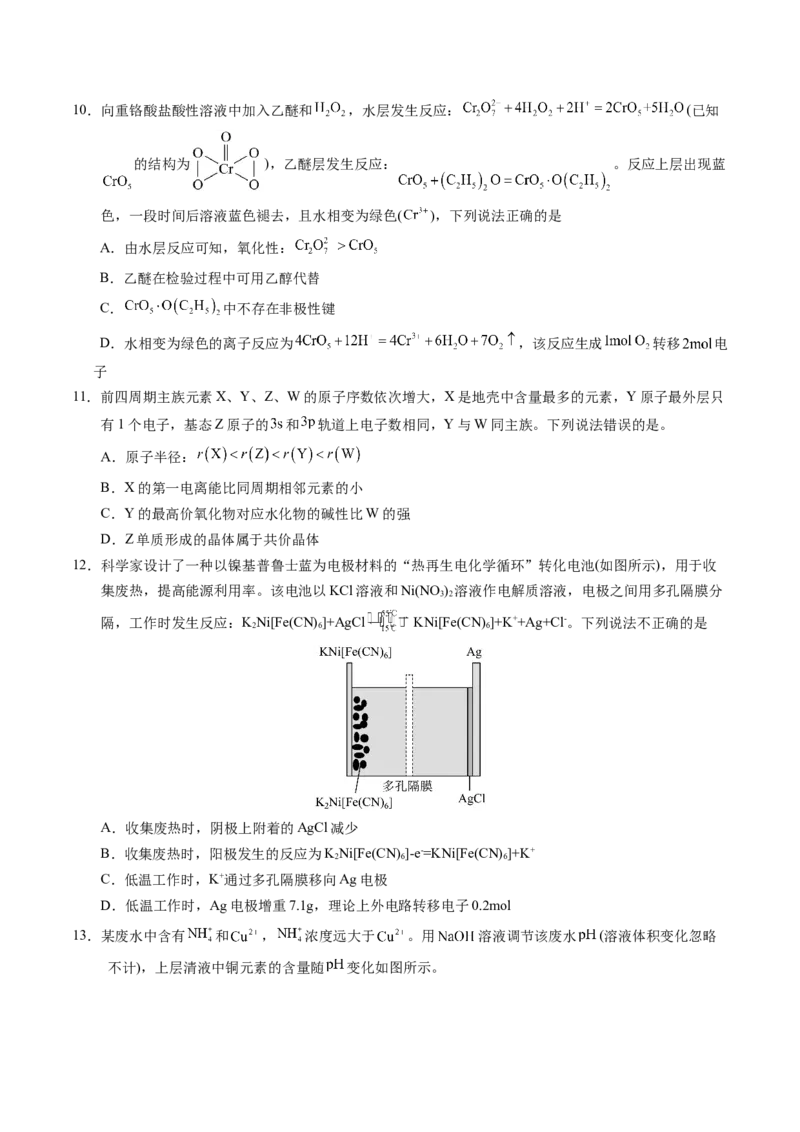
9.BHET是一种重要的化工原料,我国科学家利用聚对苯二甲酸类塑料 制备对苯二甲酸双羟乙酯
的化学反应如图所示。下列叙述不正确的是
A. 中元素的电负性:
B. 中所有原子可能处于同一平面
C. 中碳原子和氧原子的杂化方式均为
D. 和 均能发生水解反应和加成反应
学科网(北京)股份有限公司10.向重铬酸盐酸性溶液中加入乙醚和 ,水层发生反应: (已知
的结构为 ),乙醚层发生反应: 。反应上层出现蓝
色,一段时间后溶液蓝色褪去,且水相变为绿色( ),下列说法正确的是
A.由水层反应可知,氧化性:
B.乙醚在检验过程中可用乙醇代替
C. 中不存在非极性键
D.水相变为绿色的离子反应为 ,该反应生成 转移 电
子
11.前四周期主族元素X、Y、Z、W的原子序数依次增大,X是地壳中含量最多的元素,Y原子最外层只
有1个电子,基态Z原子的 和 轨道上电子数相同,Y与W同主族。下列说法错误的是。
A.原子半径:
B.X的第一电离能比同周期相邻元素的小
C.Y的最高价氧化物对应水化物的碱性比W的强
D.Z单质形成的晶体属于共价晶体
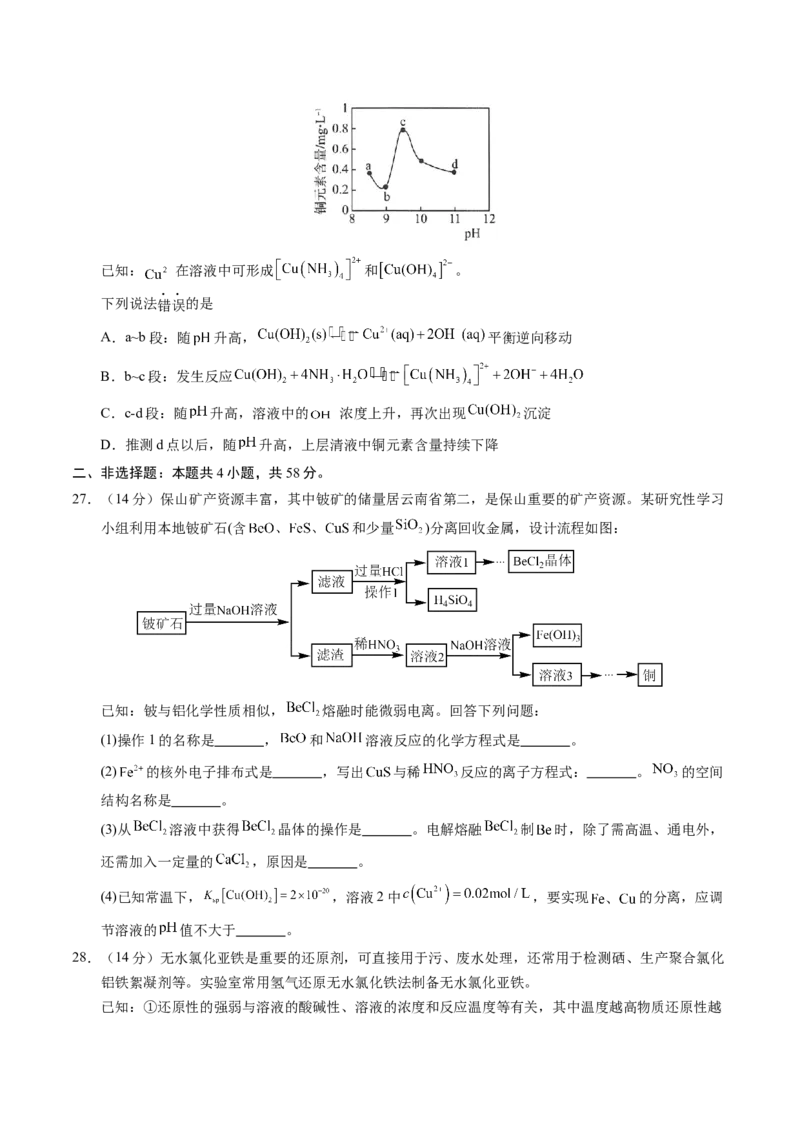
12.科学家设计了一种以镍基普鲁士蓝为电极材料的“热再生电化学循环”转化电池(如图所示),用于收
集废热,提高能源利用率。该电池以KCl溶液和Ni(NO ) 溶液作电解质溶液,电极之间用多孔隔膜分
3 2
隔,工作时发生反应:KNi[Fe(CN) ]+AgCl KNi[Fe(CN) ]+K++Ag+Cl-。下列说法不正确的是
2 6 6
A.收集废热时,阴极上附着的AgCl减少
B.收集废热时,阳极发生的反应为KNi[Fe(CN) ]-e-=KNi[Fe(CN) ]+K+
2 6 6
C.低温工作时,K+通过多孔隔膜移向Ag电极
D.低温工作时,Ag电极增重7.1g,理论上外电路转移电子0.2mol
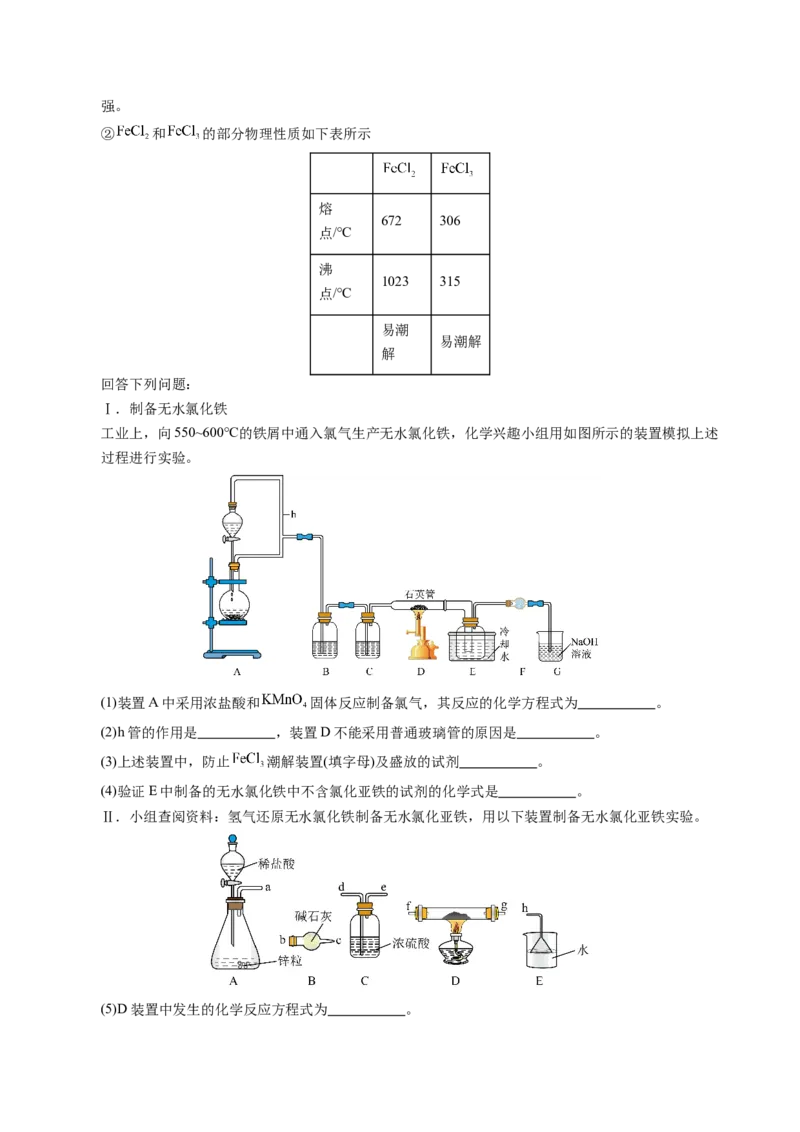
13.某废水中含有 和 , 浓度远大于 。用 溶液调节该废水 (溶液体积变化忽略
不计),上层清液中铜元素的含量随 变化如图所示。
学科网(北京)股份有限公司已知: 在溶液中可形成 和 。
下列说法错误的是
A.a~b段:随 升高, 平衡逆向移动
B.b~c段:发生反应
C.c-d段:随 升高,溶液中的 浓度上升,再次出现 沉淀
D.推测d点以后,随 升高,上层清液中铜元素含量持续下降
二、非选择题:本题共4小题,共58分。
27.(14分)保山矿产资源丰富,其中铍矿的储量居云南省第二,是保山重要的矿产资源。某研究性学习
小组利用本地铍矿石(含 和少量 )分离回收金属,设计流程如图:
已知:铍与铝化学性质相似, 熔融时能微弱电离。回答下列问题:
(1)操作1的名称是 , 和 溶液反应的化学方程式是 。
(2) 的核外电子排布式是 ,写出 与稀 反应的离子方程式: 。 的空间
结构名称是 。
(3)从 溶液中获得 晶体的操作是 。电解熔融 制 时,除了需高温、通电外,
还需加入一定量的 ,原因是 。
(4)已知常温下, ,溶液2中 ,要实现 的分离,应调
节溶液的 值不大于 。
28.(14分)无水氯化亚铁是重要的还原剂,可直接用于污、废水处理,还常用于检测硒、生产聚合氯化
铝铁絮凝剂等。实验室常用氢气还原无水氯化铁法制备无水氯化亚铁。
已知:①还原性的强弱与溶液的酸碱性、溶液的浓度和反应温度等有关,其中温度越高物质还原性越
学科网(北京)股份有限公司强。
② 和 的部分物理性质如下表所示
熔
672 306
点/℃
沸
1023 315
点/℃
易潮
易潮解
解
回答下列问题:
Ⅰ.制备无水氯化铁
工业上,向550~600℃的铁屑中通入氯气生产无水氯化铁,化学兴趣小组用如图所示的装置模拟上述
过程进行实验。
(1)装置A中采用浓盐酸和 固体反应制备氯气,其反应的化学方程式为 。
(2)h管的作用是 ,装置D不能采用普通玻璃管的原因是 。
(3)上述装置中,防止 潮解装置(填字母)及盛放的试剂 。
(4)验证E中制备的无水氯化铁中不含氯化亚铁的试剂的化学式是 。
Ⅱ.小组查阅资料:氢气还原无水氯化铁制备无水氯化亚铁,用以下装置制备无水氯化亚铁实验。
(5)D装置中发生的化学反应方程式为 。
学科网(北京)股份有限公司(6)按气流从左到右的方向,装置接口的连接顺序为a→ ,开始加热前,应先 。
(7)若还原温度高于350℃,无水氯化铁的转化率并未降低,但无水氯化亚铁的产率会明显降低,其原
因是 (已知:实验时D中硬质玻璃管较长,不考虑无水氯化铁逸出对实验结果的影响)。
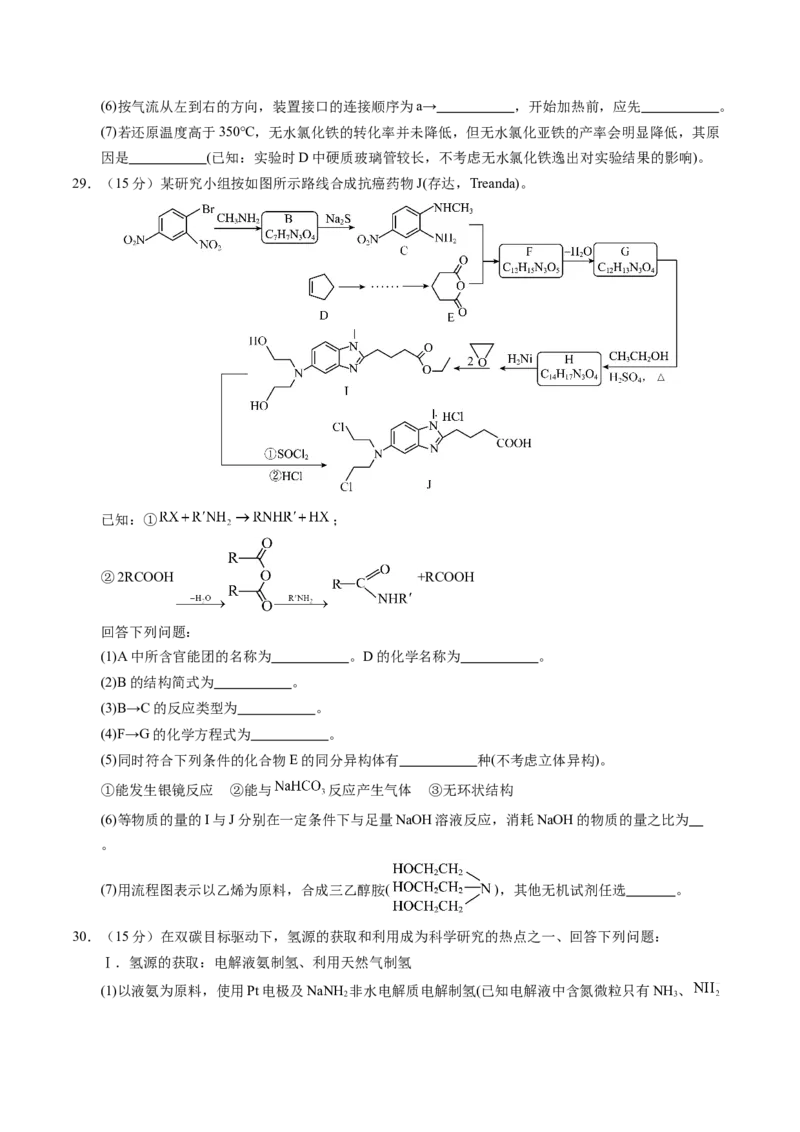
29.(15分)某研究小组按如图所示路线合成抗癌药物J(存达,Treanda)。
已知:① ;
②2RCOOH +RCOOH
回答下列问题:
(1)A中所含官能团的名称为 。D的化学名称为 。
(2)B的结构简式为 。
(3)B→C的反应类型为 。
(4)F→G的化学方程式为 。
(5)同时符合下列条件的化合物E的同分异构体有 种(不考虑立体异构)。
①能发生银镜反应 ②能与 反应产生气体 ③无环状结构
(6)等物质的量的I与J分别在一定条件下与足量NaOH溶液反应,消耗NaOH的物质的量之比为
。
(7)用流程图表示以乙烯为原料,合成三乙醇胺( ),其他无机试剂任选 。
30.(15分)在双碳目标驱动下,氢源的获取和利用成为科学研究的热点之一、回答下列问题:
Ⅰ.氢源的获取:电解液氨制氢、利用天然气制氢
(1)以液氨为原料,使用Pt电极及NaNH 非水电解质电解制氢(已知电解液中含氮微粒只有NH 、
2 3
学科网(北京)股份有限公司和 )。产生H 的电极反应式为 。
2
(2)已知反应1:CH(g)+HO(g) 3H(g)+CO(g) ΔH=+206 kJ·mol-1
4 2 2 1
反应2:CO(g)+HO(g) H(g)+CO(g) ΔH=-41 kJ·mol-1
2 2 2 2
①反应CH(g)+2HO(g) 4H(g) +CO(g)的活化能E -E = 。实际生产中常将
4 2 2 2 正 逆
温度控制在600~900 ℃,从反应的角度分析温度不能过高的主要原因可能是 。
②一定温度下,向1 L的刚性容器中充入1 mol CH 和w mol水蒸气发生上述反应1和反应2,达到平
4
衡时,测得有x mol CO、y mol CO 和相应的H 生成,此时容器内的压强为p Pa(假设没有其他反应发
2 2
生)。在该条件下,CH 的平衡转化率为 %,反应1的平衡常数K= (以分压表
4 p
示,分压=总压×物质的量分数)。
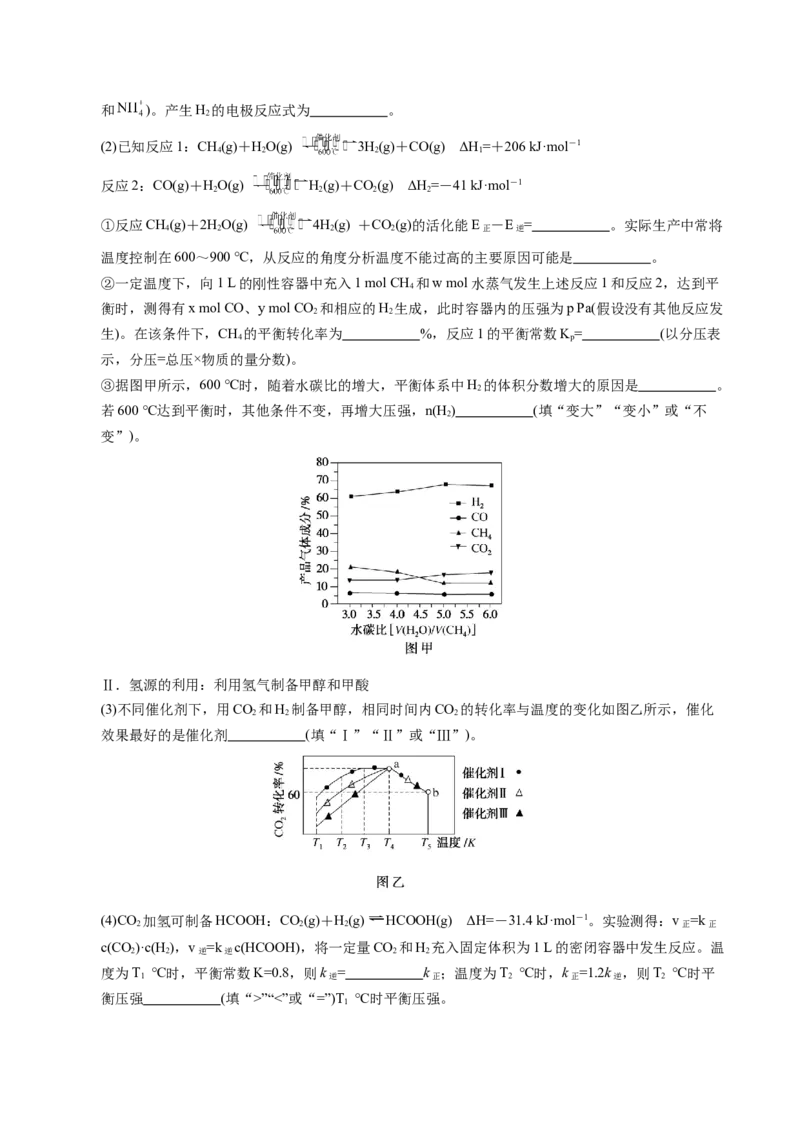
③据图甲所示,600 ℃时,随着水碳比的增大,平衡体系中H 的体积分数增大的原因是 。
2
若600 ℃达到平衡时,其他条件不变,再增大压强,n(H ) (填“变大”“变小”或“不
2
变”)。
Ⅱ.氢源的利用:利用氢气制备甲醇和甲酸
(3)不同催化剂下,用CO 和H 制备甲醇,相同时间内CO 的转化率与温度的变化如图乙所示,催化
2 2 2
效果最好的是催化剂 (填“Ⅰ”“Ⅱ”或“Ⅲ”)。
(4)CO 加氢可制备HCOOH:CO(g)+H(g) HCOOH(g) ΔH=-31.4 kJ·mol-1。实验测得:v =k
2 2 2 正 正
c(CO)·c(H),v =k c(HCOOH),将一定量CO 和H 充入固定体积为1 L的密闭容器中发生反应。温
2 2 逆 逆 2 2
度为T ℃时,平衡常数K=0.8,则k = k ;温度为T ℃时,k =1.2k ,则T ℃时平
1 逆 正 2 正 逆 2
衡压强 (填“>”“<”或“=”)T ℃时平衡压强。
1
学科网(北京)股份有限公司