文档内容
2020 北京市中考化学真题及答案
考生须知
1.本试卷共6页,共两部分,24道小题,满分45分。考试时间:与生物合计90分钟。
2.在试卷和草稿纸上准确填写姓名、准考证号、考场号和座位号。
3.试题答案一律填涂或书写在答题卡上,在试卷上作答无效。
4.在答题卡上,选择题、画图题用2B铅笔作答,其他试题用黑色字迹签字笔作答。
5.考试结束,将本试卷、答题卡和草稿纸一并交回。
可能用到的相对原子质量: 1 12 16 32 23 35.5
第一部分(选择题 共12分)
每小题1份。在每小题给出的四个选项中,选出最符合题目要求的一项。
1.为了防止骨质疏松,人体需要摄入的元素是( )
A. 钙 B. 铁 C. 锌 D. 碘
2.下列气体能供给动植物呼吸的是( )
A. B C D
3.下列含金属元素的物质是( )
A. B. C. D.
4.下列不属于铁丝在氧气中燃烧现象的是( )
A. 放出热量 B. 产生大量白烟
C. 火星四溅 D. 生成黑色固体
5.下列操作不正确的是( )
A.稀释浓硫酸 B.点燃酒精灯
C.加热液体 D.取用固体粉末6.下列不能与稀盐酸反应的金属是( )
A. B. C. D.
7.下列物质含有氧分子的是( )
A. B. C. D.
8.下列物质的用途中,利用其化学性质的是( )
A. 银用于制作导线 B. 干冰用作制冷剂
C. 铜用于制作铜火锅 D. 赤铁矿用于炼铁
9.氯化钯( )可用于检测 。 中 的化合价为( )
A. +1 B. +2 C. +3 D. +4
10.不同温度下 的溶解度如下表所示,下列说法正确的是( )
温度/℃ 20 30 40
溶解度/g 31.6 45.8 63.9
A. 时, 饱和溶液中溶质质量为
B. 时, 饱和溶液的溶质质量分数为45.8%
C. 时,将 放入 水中得到 溶液
D. 时, 水最多溶解
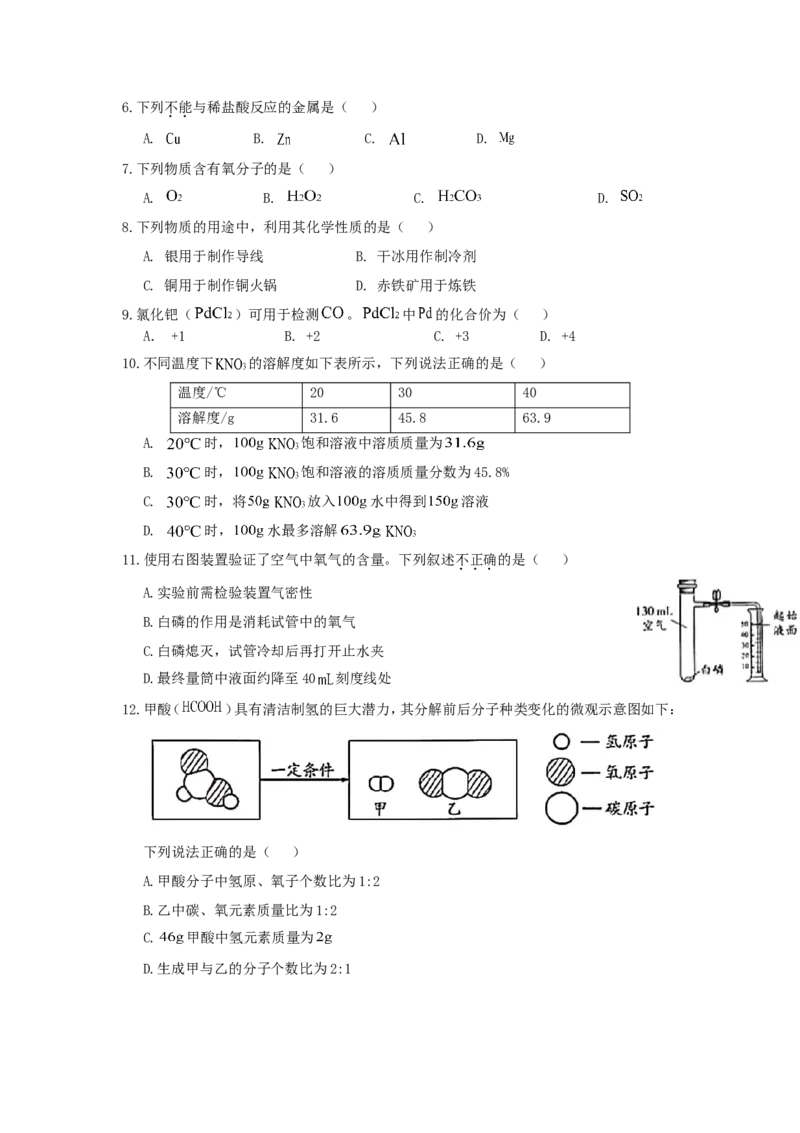
11.使用右图装置验证了空气中氧气的含量。下列叙述不正确的是( )
A.实验前需检验装置气密性
B.白磷的作用是消耗试管中的氧气
C.白磷熄灭,试管冷却后再打开止水夹
D.最终量筒中液面约降至40 刻度线处
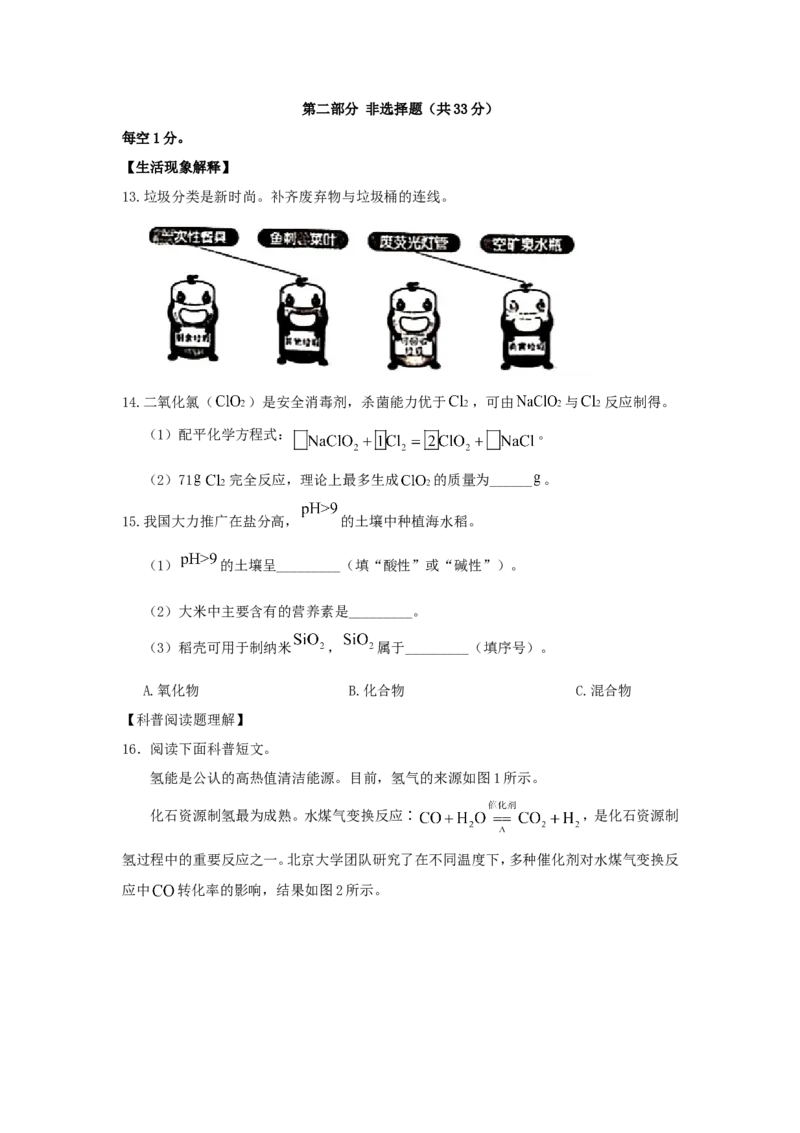
12.甲酸( )具有清洁制氢的巨大潜力,其分解前后分子种类变化的微观示意图如下:
下列说法正确的是( )
A.甲酸分子中氢原、氧子个数比为1:2
B.乙中碳、氧元素质量比为1:2
C. 甲酸中氢元素质量为
D.生成甲与乙的分子个数比为2:1第二部分 非选择题(共33分)
每空1分。
【生活现象解释】
13.垃圾分类是新时尚。补齐废弃物与垃圾桶的连线。
14.二氧化氯( )是安全消毒剂,杀菌能力优于 ,可由 与 反应制得。
(1)配平化学方程式: 。
(2)71 完全反应,理论上最多生成 的质量为______ 。
15.我国大力推广在盐分高, 的土壤中种植海水稻。
(1) 的土壤呈_________(填“酸性”或“碱性”)。
(2)大米中主要含有的营养素是_________。
(3)稻壳可用于制纳米 , 属于_________(填序号)。
A.氧化物 B.化合物 C.混合物
【科普阅读题理解】
16.阅读下面科普短文。
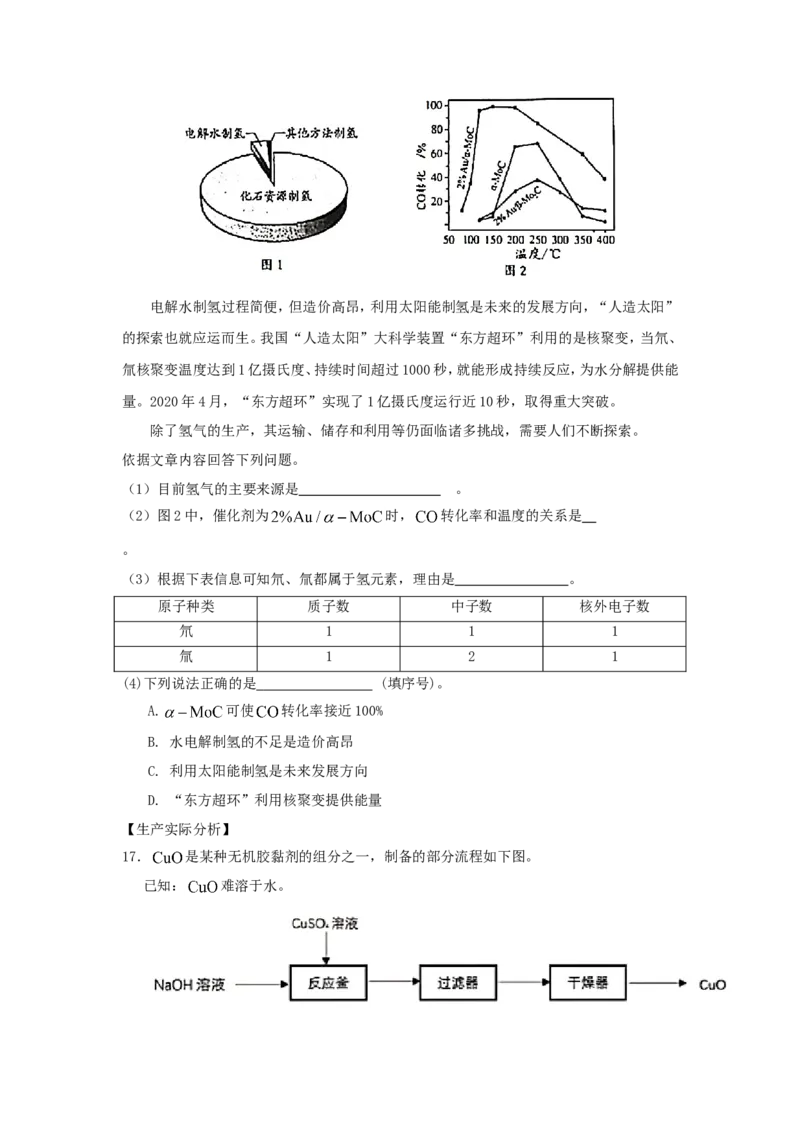
氢能是公认的高热值清洁能源。目前,氢气的来源如图1所示。
化石资源制氢最为成熟。水煤气变换反应∶ ,是化石资源制
氢过程中的重要反应之一。北京大学团队研究了在不同温度下,多种催化剂对水煤气变换反
应中 转化率的影响,结果如图2所示。电解水制氢过程简便,但造价高昂,利用太阳能制氢是未来的发展方向,“人造太阳”
的探索也就应运而生。我国“人造太阳”大科学装置“东方超环”利用的是核聚变,当氘、
氚核聚变温度达到1亿摄氏度、持续时间超过1000秒,就能形成持续反应,为水分解提供能
量。2020年4月,“东方超环”实现了1亿摄氏度运行近10秒,取得重大突破。
除了氢气的生产,其运输、储存和利用等仍面临诸多挑战,需要人们不断探索。
依据文章内容回答下列问题。
(1)目前氢气的主要来源是 。
(2)图2中,催化剂为 时, 转化率和温度的关系是
。
(3)根据下表信息可知氘、氚都属于氢元素,理由是 。
原子种类 质子数 中子数 核外电子数
氘 1 1 1
氚 1 2 1
(4)下列说法正确的是 (填序号)。
A. 可使 转化率接近100%
B. 水电解制氢的不足是造价高昂
C. 利用太阳能制氢是未来发展方向
D. “东方超环”利用核聚变提供能量
【生产实际分析】
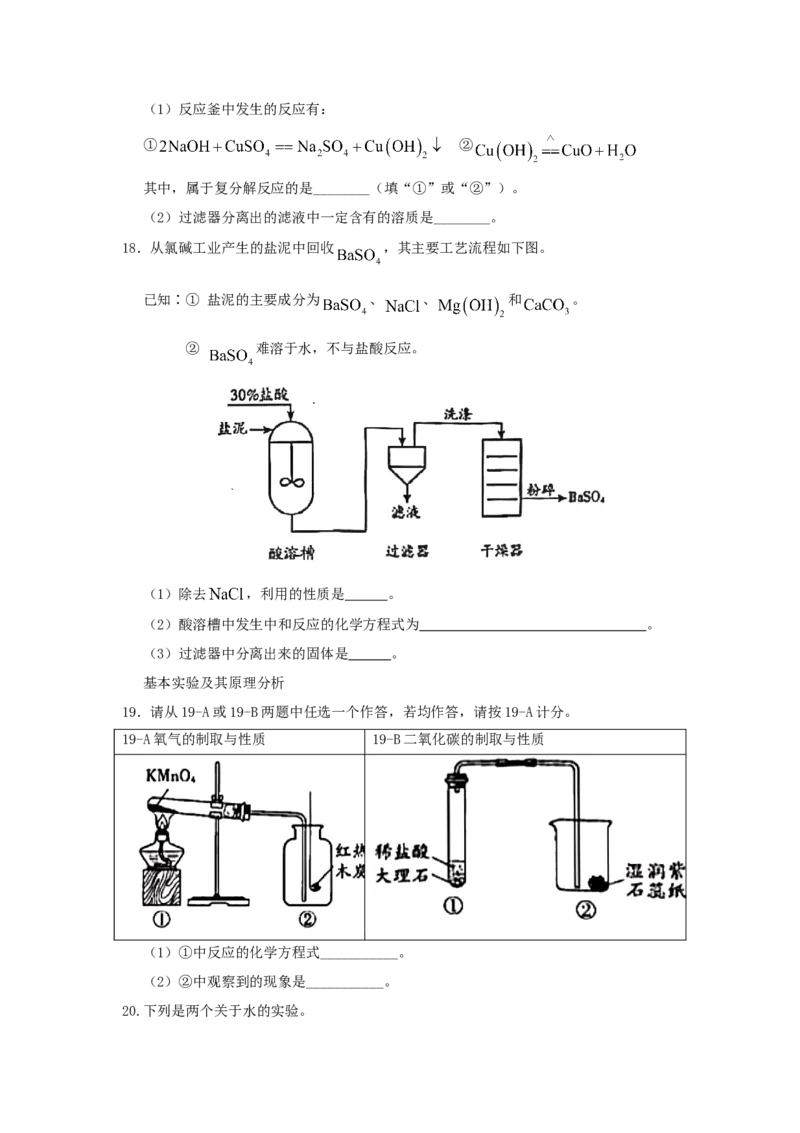
17. 是某种无机胶黏剂的组分之一,制备的部分流程如下图。
已知: 难溶于水。(1)反应釜中发生的反应有:
① ②
其中,属于复分解反应的是________(填“①”或“②”)。
(2)过滤器分离出的滤液中一定含有的溶质是________。
18.从氯碱工业产生的盐泥中回收 ,其主要工艺流程如下图。
已知∶① 盐泥的主要成分为 、 、 和 。
② 难溶于水,不与盐酸反应。
(1)除去 ,利用的性质是 。
(2)酸溶槽中发生中和反应的化学方程式为 。
(3)过滤器中分离出来的固体是 。
基本实验及其原理分析
19.请从19-A或19-B两题中任选一个作答,若均作答,请按19-A计分。
19-A氧气的制取与性质 19-B二氧化碳的制取与性质
(1)①中反应的化学方程式___________。
(2)②中观察到的现象是___________。
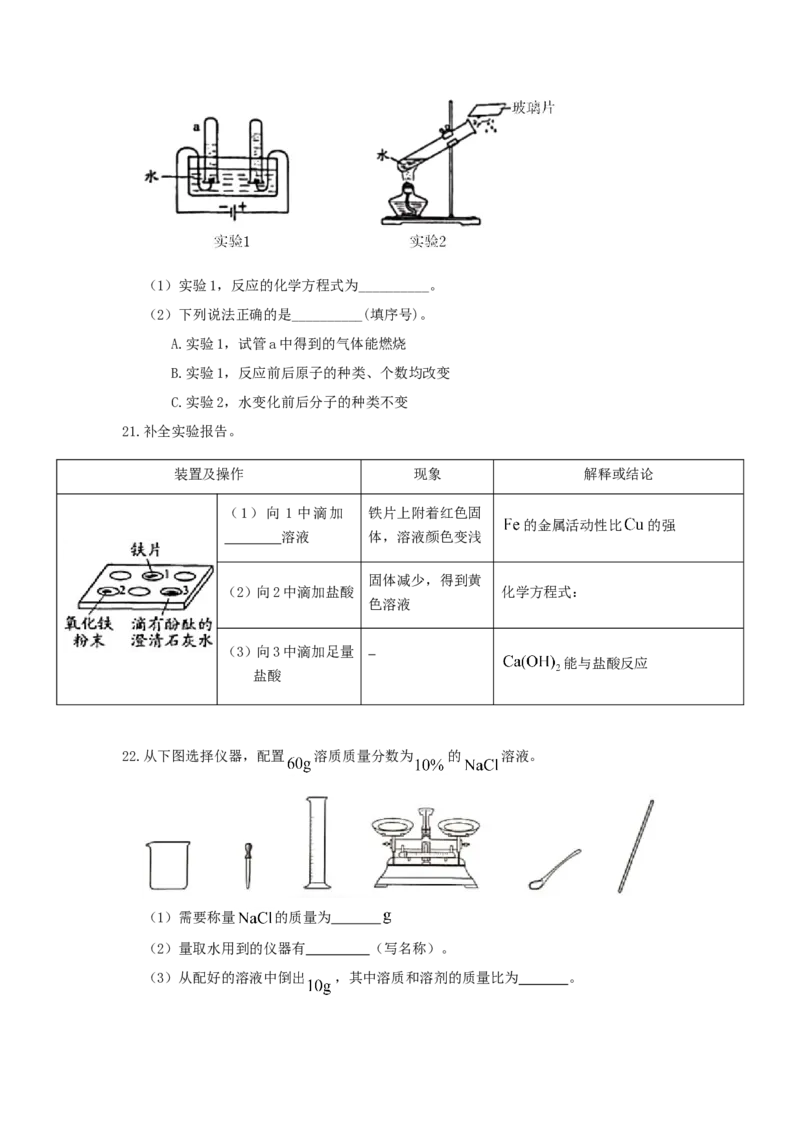
20.下列是两个关于水的实验。(1)实验1,反应的化学方程式为__________。
(2)下列说法正确的是__________(填序号)。
A.实验1,试管a中得到的气体能燃烧
B.实验1,反应前后原子的种类、个数均改变
C.实验2,水变化前后分子的种类不变
21.补全实验报告。
装置及操作 现象 解释或结论
(1)向 1 中滴加 铁片上附着红色固
的金属活动性比 的强
溶液 体,溶液颜色变浅
固体减少,得到黄
(2)向2中滴加盐酸 化学方程式:
色溶液
(3)向3中滴加足量
能与盐酸反应
盐酸
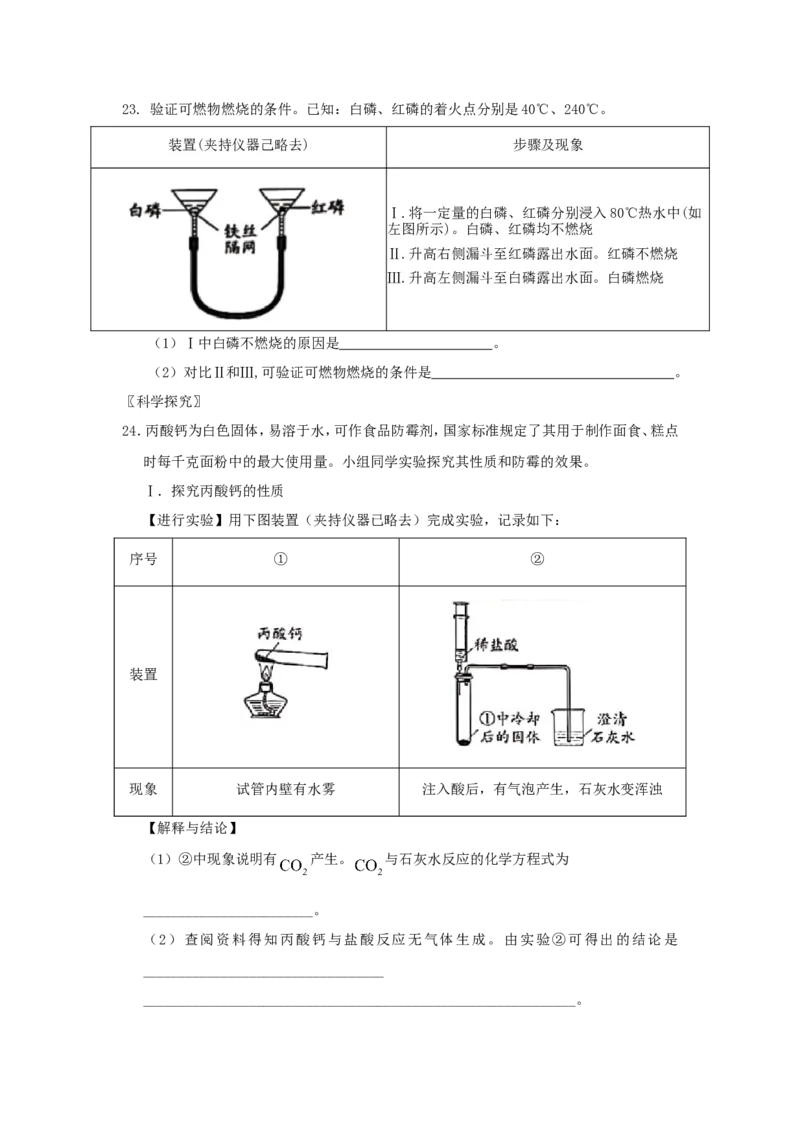
22.从下图选择仪器,配置 溶质质量分数为 的 溶液。
(1)需要称量 的质量为
(2)量取水用到的仪器有 (写名称)。
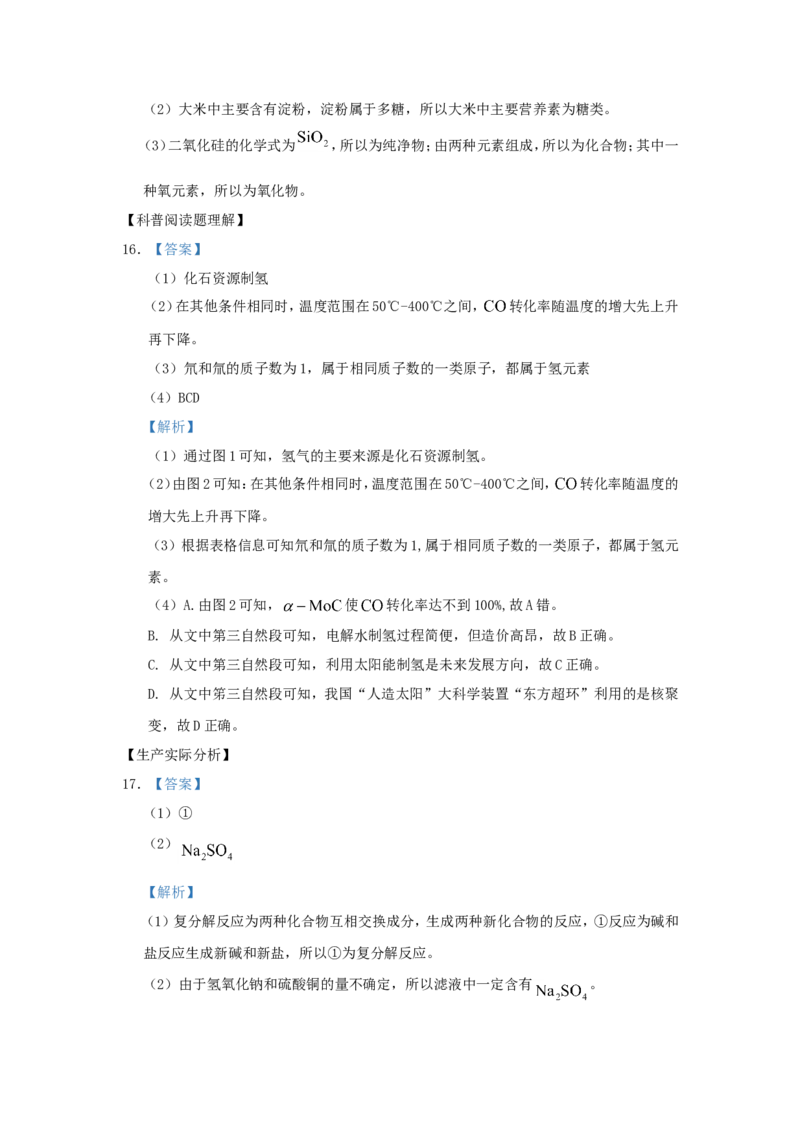
(3)从配好的溶液中倒出 ,其中溶质和溶剂的质量比为 。23. 验证可燃物燃烧的条件。已知:白磷、红磷的着火点分别是40℃、240℃。
装置(夹持仪器己略去) 步骤及现象
Ⅰ.将一定量的白磷、红磷分别浸入80℃热水中(如
左图所示)。白磷、红磷均不燃烧
Ⅱ.升高右侧漏斗至红磷露出水面。红磷不燃烧
Ⅲ.升高左侧漏斗至白磷露出水面。白磷燃烧
(1)Ⅰ中白磷不燃烧的原因是 。
(2)对比Ⅱ和Ⅲ,可验证可燃物燃烧的条件是 。
〖科学探究〗
24.丙酸钙为白色固体,易溶于水,可作食品防霉剂,国家标准规定了其用于制作面食、糕点
时每千克面粉中的最大使用量。小组同学实验探究其性质和防霉的效果。
Ⅰ.探究丙酸钙的性质
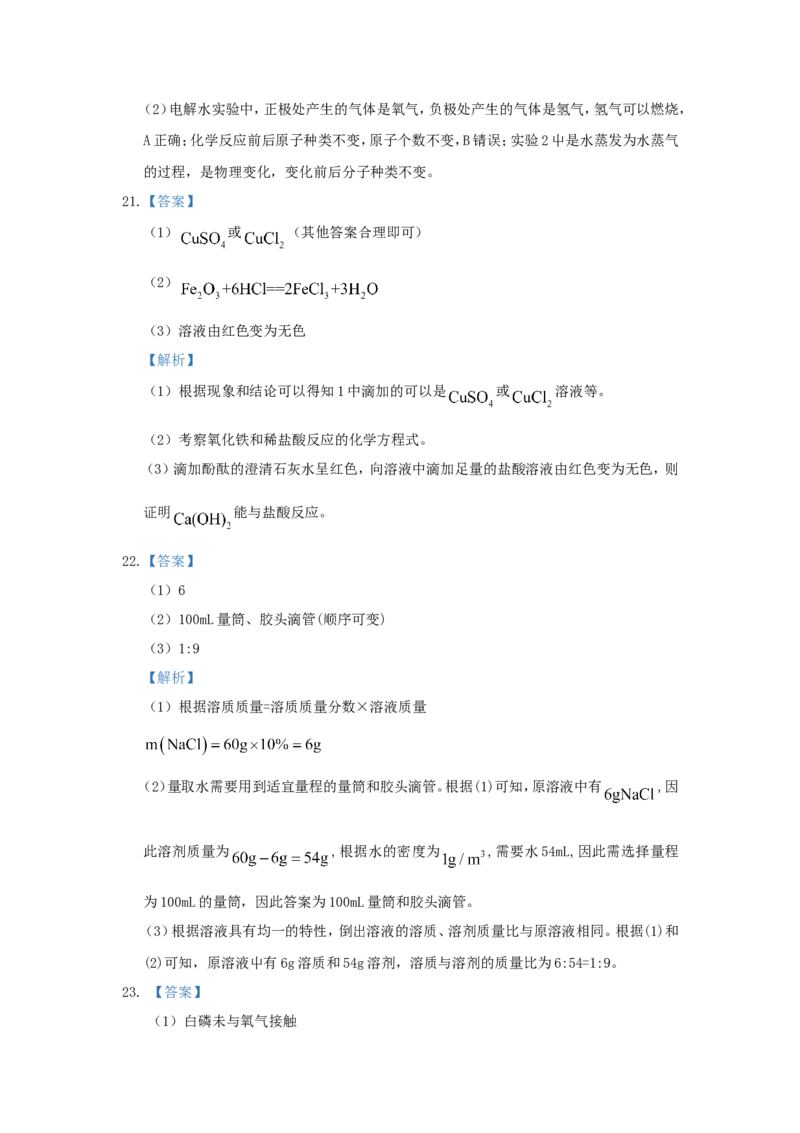
【进行实验】用下图装置(夹持仪器已略去)完成实验,记录如下:
序号 ① ②
装置
现象 试管内壁有水雾 注入酸后,有气泡产生,石灰水变浑浊
【解释与结论】
(1)②中现象说明有 产生。 与石灰水反应的化学方程式为
________________________。
(2)查阅资料得知丙酸钙与盐酸反应无气体生成。由实验②可得出的结论是
__________________________________
_____________________________________________________________。II.探究丙酸钙防霉的效果
【进行实验】分别按下列①~③配方蒸制8个馒头,冷却后置于密封袋中,记录如下:
组别 第1组 第2组
序号 ① ② ③ ④ ⑤ ⑥ ⑦ ⑧
面粉/ 50 50 50 50 50 50 50 50
配 酵母/ 0.75 0.75 0.75 0.75 0.75 0.75 0.75 0.75
方 蔗糖/ 0 0 0 0 5 5 x 5
丙酸钙/ 0 0.06 0.10 0.15 0 0.06 0.10 0.15
开始发霉时间 第3天 第4天 第5天 第6天 第3天 第4天 第5天 第6天
【解释与结论】
(3)设计第1组实验的目的是_____________。
(4)第2组,⑦中x为_____________。
(5)对比第1组、第2组实验可得到的结论是______________。
【反思与评价】
(6)某同学认为“制作面食、糕点时,丙酸钙用量越大越好”,你是否同意此观点,并说明理
由:
______________________________________________________________________________
________。2020年北京市中考考试试卷化学
参考答案
第一部分(选择题 共12分)
每小题1份。在每小题给出的四个选项中,选出最符合题目要求的一项。
1. 【答案】A
【解析】A. 缺钙元素,引起骨质疏松或佝偻病;
B. 缺铁元素,引起贫血;
C. 缺锌元素,引起食欲不振、发育不良;
D. 缺碘元素,引起甲状腺肿大(大脖子病)。
故选A。
2. 【答案】C
【解析】氧气具有供给呼吸的性质。故答案是C。
3. 【答案】C
【解析】
A. 中,氢元素、硫元素均为非金属元素。
B. 中,磷元素、氧元素均为非金属元素。
C. 中,氮元素、氧元素为非金属元素,银元素为金属元素。
D. 中,氢元素、氧元素均为非金属元素。故选C。
4. 【答案】B
【解析】铁丝在氧气中燃烧的现象:剧烈燃烧,火星四射,放出热量,生成黑色固体。其中
不包括产生大量白烟,故选B。
5. 【答案】B
【解析】点燃酒精灯时,不能用酒精灯对点,应该用火柴点燃酒精灯。故选B。
6. 【答案】A
【解析】金属活动顺序表中, 后金属不能与稀酸发生置换反应产生氢气。铜属于 后金
属,不能和稀盐酸发生反应。
故选A。
7. 【答案】A
【解析】只有氧气中含有氧分子,其他物质中含有的为氧元素。故选A。
8. 【答案】D
【解析】
A. 银用于制作导线,体现银具有导电性,体现其物理性质B. 干冰易升华,升华吸热可用作制冷剂,体现其物理性质
C. 铜用于制作铜火锅,体现铜具有导热性,体现其物理性质
D. 赤铁矿用于炼铁,赤铁矿中主要成分为氧化铁,氧化铁在高温条件下可被一氧化碳还
原成铁,体现其化学性质。故选D
9. 【答案】B
【解析】 中 元素为-1价,化合物整体不带电,故 的化合价为+2价。故选B。
10. 【答案】D
【解析】A.溶质质量=溶液质量×溶质质量分数, 时, 饱和溶液中溶质
质量为
,A选项错误;
B. 饱和溶液中溶质质量分数 , 时, 饱和溶液
的溶质质量分数为
,B选项错误;
C.溶液质量=溶质质量+容质质量,由图表可知, 时, 水最多溶解45.8g ,
溶液质量为 ,C选项错误;
D. 由图表可知, 时, 的溶解度为 ,即 时, 水最多溶解
,D选项正确。
故选D。
11. 【答案】D
【解析】A.白磷燃烧有气体参与反应,实验前需要检查装置气密性;A选项正确。
B.利用白磷测定空气中氧气含量,白磷要足量来耗尽氧气;B选项正确。
C.白磷熄灭后,需要装置冷却至室温后再打开止水夹,否则将导致测得氧气的体积分数
偏小;C选项正确。
D.实验中氧气约占试管内空气体积的五分之一,试管内有130 空气,则氧气含量为
;即量筒中有26 水倒吸进入试管中,最终量筒内的水量为
;D选项错误,故选D
12.【答案】C【解析】有微观示意图可写出反应方程式:
A.一个甲酸( )分子中,氢、氧原子个数比为1:1,A选项错误。
B.乙为二氧化碳(CO 2),碳、氧元素质量比为12:(16 2)=12:32=3:8,B选项错误。
C.46g甲酸中氢元素的质量为, C选项
正确。
D.根据方程式可知生成的甲和乙的分子个数比为1:1,D选项错误,故选C。
第二部分 非选择题(共33分)
每空1分。
【生活现象解释】
13.【答案】鱼刺、菜叶——厨余垃圾;
空矿泉水瓶——可回收垃圾。
【解析】鱼刺、菜叶属于厨余垃圾,矿泉水瓶是热塑性塑料属于可回收垃圾。
14.【答案】
(1)2:2
(2)135
【解析】
(1)根据质量守恒定律,化学反应前后原子个数不变,所以反应后氧原子有4个,反应前
也有4个氧原子,则 的化学计量数为2;同理, 的化学计量数也为2。
(2)根据化学方程式可知,每71份质量的 完全反映,生成135份质量的 ,现有
,则最多生成 。
15.【答案】
(1)碱性
(2)糖类
(3)AB
【解析】
(1) 值小于 为酸性,等于 为中性,大于 为碱性,现 ,所以土壤呈碱性。(2)大米中主要含有淀粉,淀粉属于多糖,所以大米中主要营养素为糖类。
(3)二氧化硅的化学式为 ,所以为纯净物;由两种元素组成,所以为化合物;其中一
种氧元素,所以为氧化物。
【科普阅读题理解】
16.【答案】
(1)化石资源制氢
(2)在其他条件相同时,温度范围在50℃-400℃之间, 转化率随温度的增大先上升
再下降。
(3)氘和氚的质子数为1,属于相同质子数的一类原子,都属于氢元素
(4)BCD
【解析】
(1)通过图1可知,氢气的主要来源是化石资源制氢。
(2)由图2可知:在其他条件相同时,温度范围在50℃-400℃之间, 转化率随温度的
増大先上升再下降。
(3)根据表格信息可知氘和氚的质子数为1,属于相同质子数的一类原子,都属于氢元
素。
(4)A.由图2可知, 使 转化率达不到100%,故A错。
B. 从文中第三自然段可知,电解水制氢过程简便,但造价高昂,故B正确。
C. 从文中第三自然段可知,利用太阳能制氢是未来发展方向,故C正确。
D. 从文中笫三自然段可知,我国“人造太阳”大科学装置“东方超环”利用的是核聚
变,故D正确。
【生产实际分析】
17.【答案】
(1)①
(2)
【解析】
(1)复分解反应为两种化合物互相交换成分,生成两种新化合物的反应,①反应为碱和
盐反应生成新碱和新盐,所以①为复分解反应。
(2)由于氢氧化钠和硫酸铜的量不确定,所以滤液中一定含有 。18.【答案】
(1) 可溶于水
(2)
(3)
【解析】
(1)盐泥的主要成分中, 可溶于水且不与盐酸反应, 和 能与盐
酸反应生成可溶于水的物质, 难溶于水且不与盐酸反应。
(2)盐泥的主要成分中只有 为碱,能与盐酸发生中和反应。
(3)盐泥的主要成分中只有 不溶于水,不与盐酸反应。
基本实验及其原理分析
19.【答案】19-A(1)
(2)木炭燃烧,发白光,放热
19-B(1)
(2)湿润紫色石蕊纸花变红
【解析】19-A(1)考察实验室高锰酸钾制氧气的化学方程式。
(2)考察木炭燃烧的现象。
19-B(1)考察实验室制取二氧化碳的化学方程式。
(2)试管中产生的 会沿着导管进入烧杯底部, 遇到湿润的紫色石蕊纸花会生
成碳酸,紫色石蕊遇酸变红。
20.【答案】
(1)
(2)AC
【解析】
(1)考察电解水的化学方程式。(2)电解水实验中,正极处产生的气体是氧气,负极处产生的气体是氢气,氢气可以燃烧,
A正确;化学反应前后原子种类不变,原子个数不变,B锖误;实验2屮是水蒸发为水蒸气
的过程,是物理变化,变化前后分子种类不变。
21.【答案】
(1) 或 (其他答案合理即可)
(2)
(3)溶液由红色变为无色
【解析】
(1)根据现象和结论可以得知1中滴加的可以是 或 溶液等。
(2)考察氧化铁和稀盐酸反应的化学方程式。
(3)滴加酚酞的澄清石灰水呈红色,向溶液中滴加足量的盐酸溶液由红色变为无色,则
证明 能与盐酸反应。
22.【答案】
(1)6
(2)100mL量筒、胶头滴管(顺序可变)
(3)1:9
【解析】
(1)根据溶质质量=溶质质量分数×溶液质量
(2)量取水需要用到适宜量程的量筒和胶头滴管。根据(1)可知,原溶液中有 ,因
此溶剂质量为 ,根据水的密度为 ,需要水54mL,因此需选择量程
为100mL的量筒,因此答案为100mL量筒和胶头滴管。
(3)根据溶液具有均一的特性,倒出溶液的溶质、溶剂质量比与原溶液相同。根据(1)和
(2)可知,原溶液屮有6g溶质和54g溶剂,溶质与溶剂的质量比为6:54=1:9。
23. 【答案】
(1)白磷未与氧气接触(2)燃烧需要温度达到可燃物的着火点
【解析】
(1)白磷浸入 热水中,使白磷无法与氧气接触,因此答案为白磷未与氧气接触。
(2)根据已知:白磷、红磷的着火点分别是 、 , 的温度能达到白磷着火
点,但无法达到红磷着火点,因此验证的燃烧条件是稳定达到可燃物的着火点。
〖科学探究〗
24.【答案】
(1)
(2)丙酸钙受热后产生的物质能与稀盐酸反应生成二氧化碳
(3)探究丙酸钙的质量大小是否对于丙酸钙防霉效果有影响
(4)5
(5)在加入面粉质量相同,酵母质量相同时以及其他条件相同时,有无蔗糖对丙酸钙防霉效
果无影响。
(6)不同意。国家标准规定了丙酸钙用于制作面食、糕点时每千克面粉中的最大使用量,说
明过量使用可能有害。故不是越多越好.
【解析】
(1) 与石灰水反应的化学方程式为: .
(2)丙酸钙受热分解后的固体加入稀盐酸,有气泡产生,石灰水变浑浊,说明该反应有二氧
化碳生成。
(3)根据第1组实验中,通过改变丙酸钙的质量,来探究丙酸钙防霉效果。
(4)第2组实验屮,变量为丙酸钙的质量,蔗糖的质量为定量,故x为5。
(5)根据第1组和第2组的实验数据可知,加入蔗糖不会影响丙酸钙防霉的效果。
(6)国家标准规定了丙酸钙用丁制作面食、糕点时每千克面粉中的最大使用量,说明过量使
用可能有害。不应过量添加.