文档内容
浙江省嘉兴市2018年中考化学真题试题
5.二氧化碳气体既是温室效应的元凶,又是一种潜在的碳资源。实验室里,科学家已成功利
用二氧化碳与环氧丙烷(一种简单有机物)在催化剂的作用下合成“二氧化碳塑料”。
该新型塑料在投入工业生产前,以下不是科学家重点考虑的问题是
A.如何提高催化剂的催化效率 B.新型塑料是否可降解
C.新型塑料的化学性质是否稳定 D.新型塑料生产是否影响碳循环
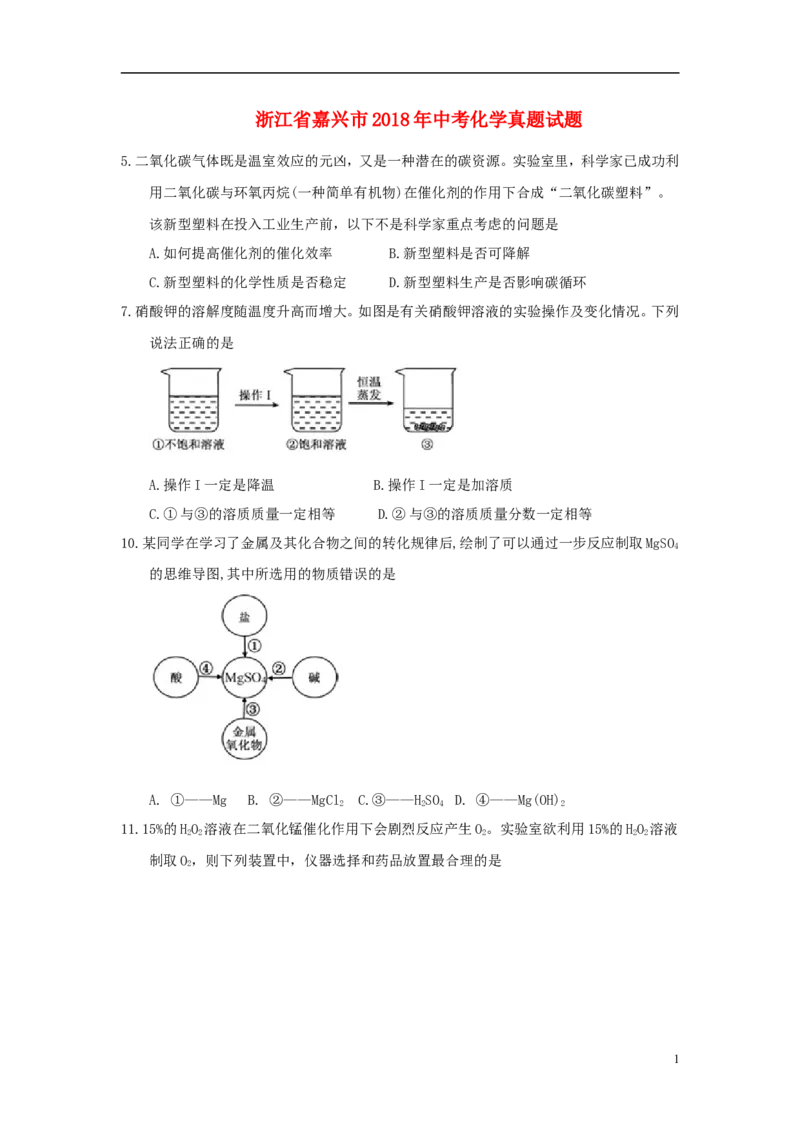
7.硝酸钾的溶解度随温度升高而增大。如图是有关硝酸钾溶液的实验操作及变化情况。下列
说法正确的是
A.操作I一定是降温 B.操作I一定是加溶质
C.①与③的溶质质量一定相等 D.②与③的溶质质量分数一定相等
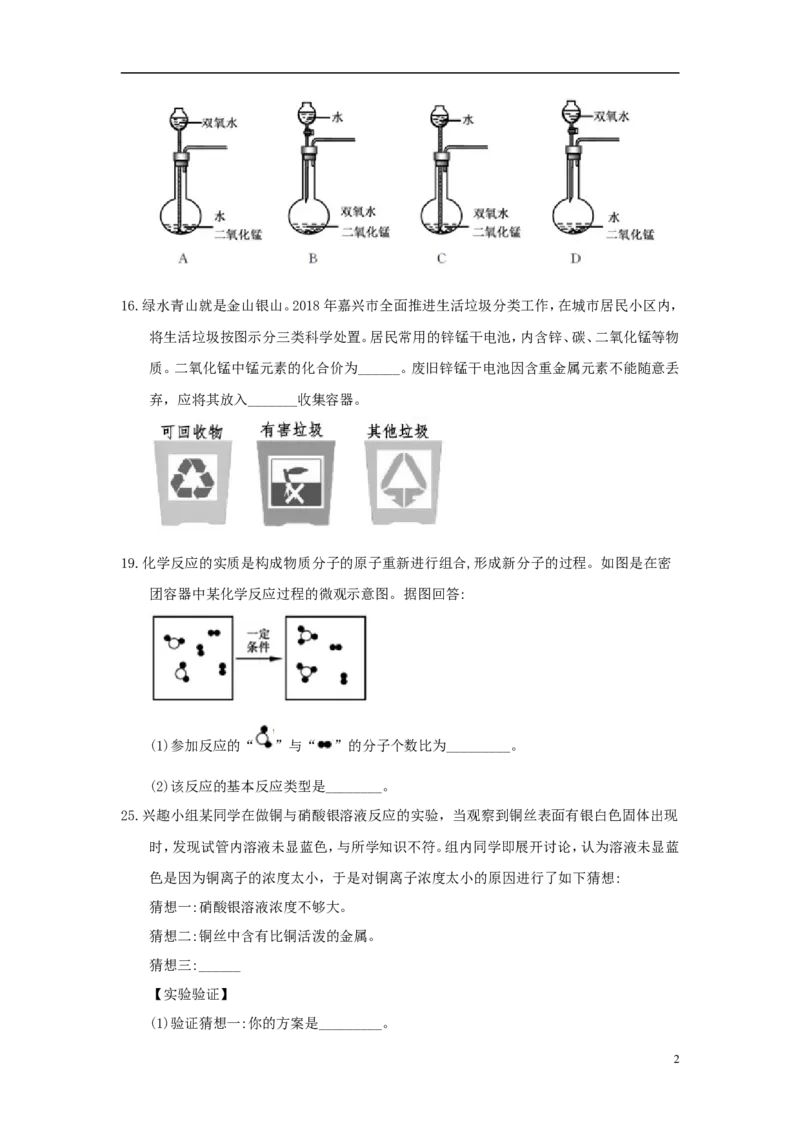
10.某同学在学习了金属及其化合物之间的转化规律后,绘制了可以通过一步反应制取MgSO
4
的思维导图,其中所选用的物质错误的是
A. ①——Mg B. ②——MgCl C.③——HSO D. ④——Mg(OH)
2 2 4 2
11.15%的HO 溶液在二氧化锰催化作用下会剧烈反应产生O。实验室欲利用15%的HO 溶液
2 2 2 2 2
制取O,则下列装置中,仪器选择和药品放置最合理的是
2
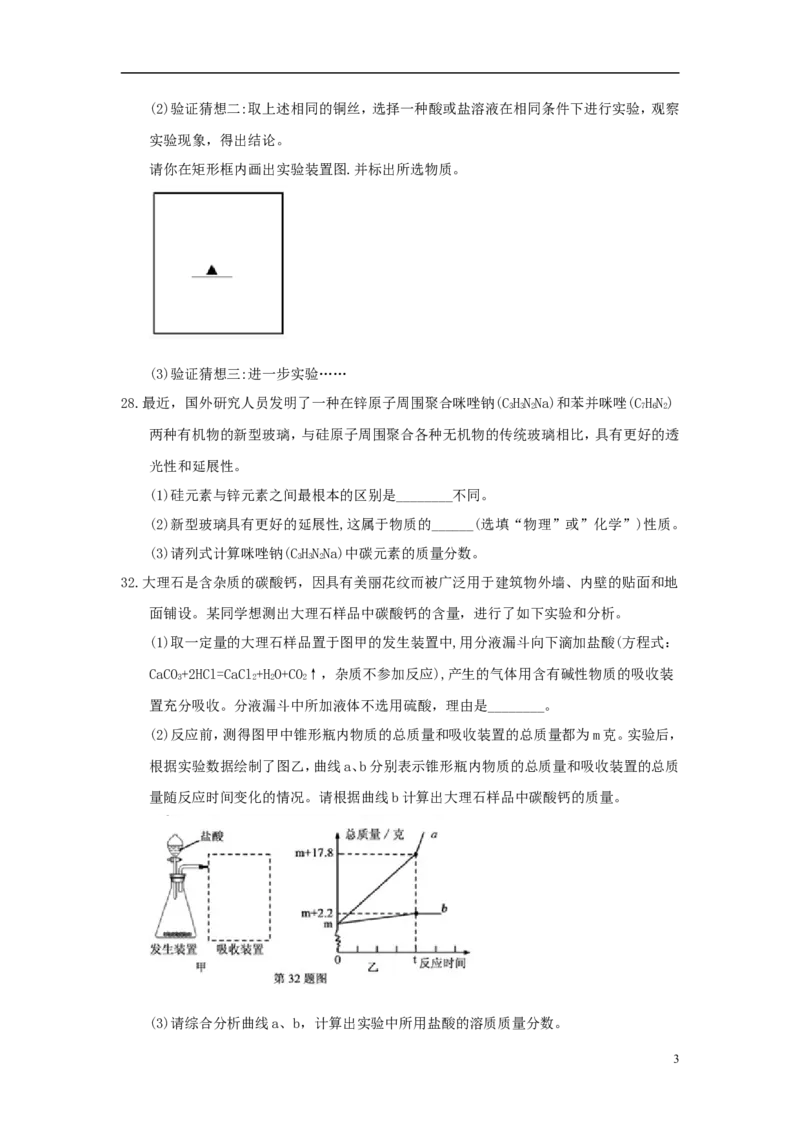
116.绿水青山就是金山银山。2018年嘉兴市全面推进生活垃圾分类工作,在城市居民小区内,
将生活垃圾按图示分三类科学处置。居民常用的锌锰干电池,内含锌、碳、二氧化锰等物
质。二氧化锰中锰元素的化合价为______。废旧锌锰干电池因含重金属元素不能随意丢
弃,应将其放入_______收集容器。
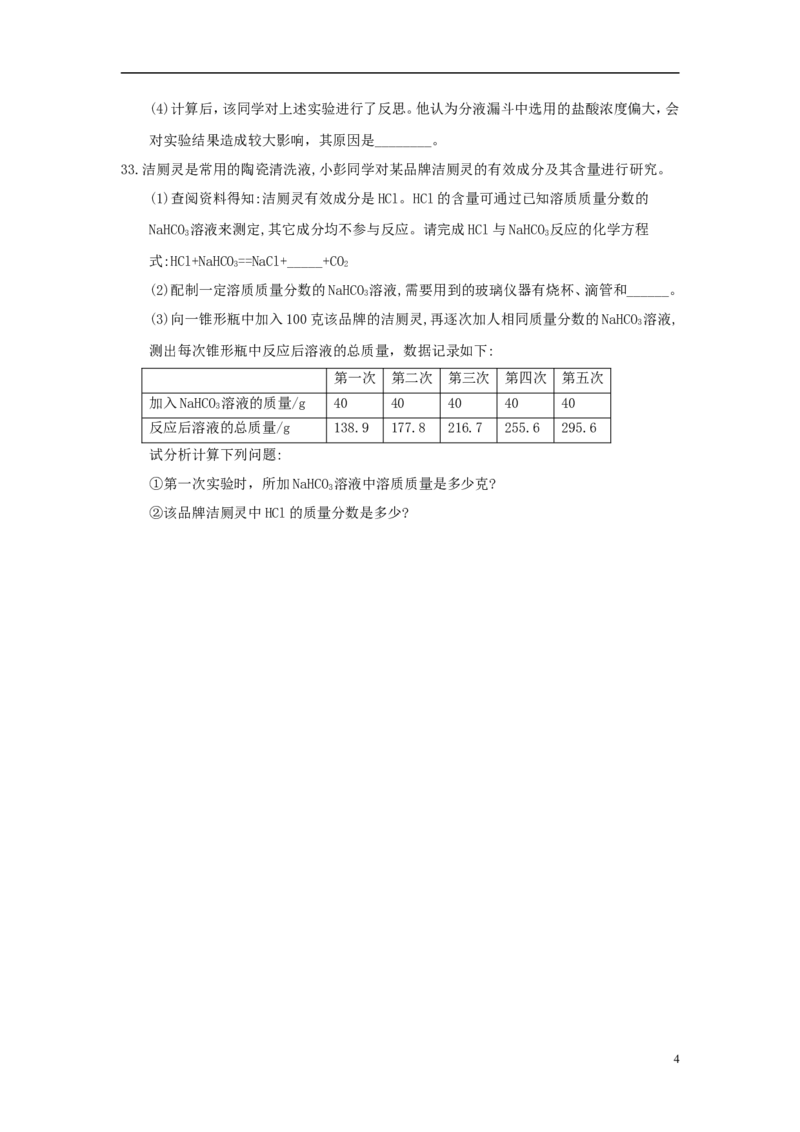
19.化学反应的实质是构成物质分子的原子重新进行组合,形成新分子的过程。如图是在密
团容器中某化学反应过程的微观示意图。据图回答:
(1)参加反应的“ ”与“ ”的分子个数比为_________。
(2)该反应的基本反应类型是________。
25.兴趣小组某同学在做铜与硝酸银溶液反应的实验,当观察到铜丝表面有银白色固体出现
时,发现试管内溶液未显蓝色,与所学知识不符。组内同学即展开讨论,认为溶液未显蓝
色是因为铜离子的浓度太小,于是对铜离子浓度太小的原因进行了如下猜想:
猜想一:硝酸银溶液浓度不够大。
猜想二:铜丝中含有比铜活泼的金属。
猜想三:______
【实验验证】
(1)验证猜想一:你的方案是_________。
2(2)验证猜想二:取上述相同的铜丝,选择一种酸或盐溶液在相同条件下进行实验,观察
实验现象,得出结论。
请你在矩形框内画出实验装置图.并标出所选物质。
(3)验证猜想三:进一步实验……
28.最近,国外研究人员发明了一种在锌原子周围聚合咪唑钠(CHNNa)和苯并咪唑(CHN)
3 3 2 7 6 2
两种有机物的新型玻璃,与硅原子周围聚合各种无机物的传统玻璃相比,具有更好的透
光性和延展性。
(1)硅元素与锌元素之间最根本的区别是________不同。
(2)新型玻璃具有更好的延展性,这属于物质的______(选填“物理”或”化学”)性质。
(3)请列式计算咪唑钠(CHNNa)中碳元素的质量分数。
3 3 2
32.大理石是含杂质的碳酸钙,因具有美丽花纹而被广泛用于建筑物外墙、内壁的贴面和地
面铺设。某同学想测出大理石样品中碳酸钙的含量,进行了如下实验和分析。
(1)取一定量的大理石样品置于图甲的发生装置中,用分液漏斗向下滴加盐酸(方程式:
CaCO+2HCl=CaCl+HO+CO↑,杂质不参加反应),产生的气体用含有碱性物质的吸收装
3 2 2 2
置充分吸收。分液漏斗中所加液体不选用硫酸,理由是________。
(2)反应前,测得图甲中锥形瓶内物质的总质量和吸收装置的总质量都为m克。实验后,
根据实验数据绘制了图乙,曲线a、b分别表示锥形瓶内物质的总质量和吸收装置的总质
量随反应时间变化的情况。请根据曲线b计算出大理石样品中碳酸钙的质量。
(3)请综合分析曲线a、b,计算出实验中所用盐酸的溶质质量分数。
3(4)计算后,该同学对上述实验进行了反思。他认为分液漏斗中选用的盐酸浓度偏大,会
对实验结果造成较大影响,其原因是________。
33.洁厕灵是常用的陶瓷清洗液,小彭同学对某品牌洁厕灵的有效成分及其含量进行研究。
(1)查阅资料得知:洁厕灵有效成分是HCl。HCl的含量可通过已知溶质质量分数的
NaHCO 溶液来测定,其它成分均不参与反应。请完成HCl与NaHCO 反应的化学方程
3 3
式:HCl+NaHCO==NaCl+_____+CO
3 2
(2)配制一定溶质质量分数的NaHCO 溶液,需要用到的玻璃仪器有烧杯、滴管和______。
3
(3)向一锥形瓶中加入100克该品牌的洁厕灵,再逐次加人相同质量分数的NaHCO 溶液,
3
测出每次锥形瓶中反应后溶液的总质量,数据记录如下:
第一次 第二次 第三次 第四次 第五次
加入NaHCO 溶液的质量/g 40 40 40 40 40
3
反应后溶液的总质量/g 138.9 177.8 216.7 255.6 295.6
试分析计算下列问题:
①第一次实验时,所加NaHCO 溶液中溶质质量是多少克?
3
②该品牌洁厕灵中HCl的质量分数是多少?
4参考答案
5.D 7.D 10.B 11.D
16. +4;有害垃圾。
19.(1)2 :1;(2)化合反应
25.猜想三:铜与硝酸银溶液反应的时间太短(合理即可)
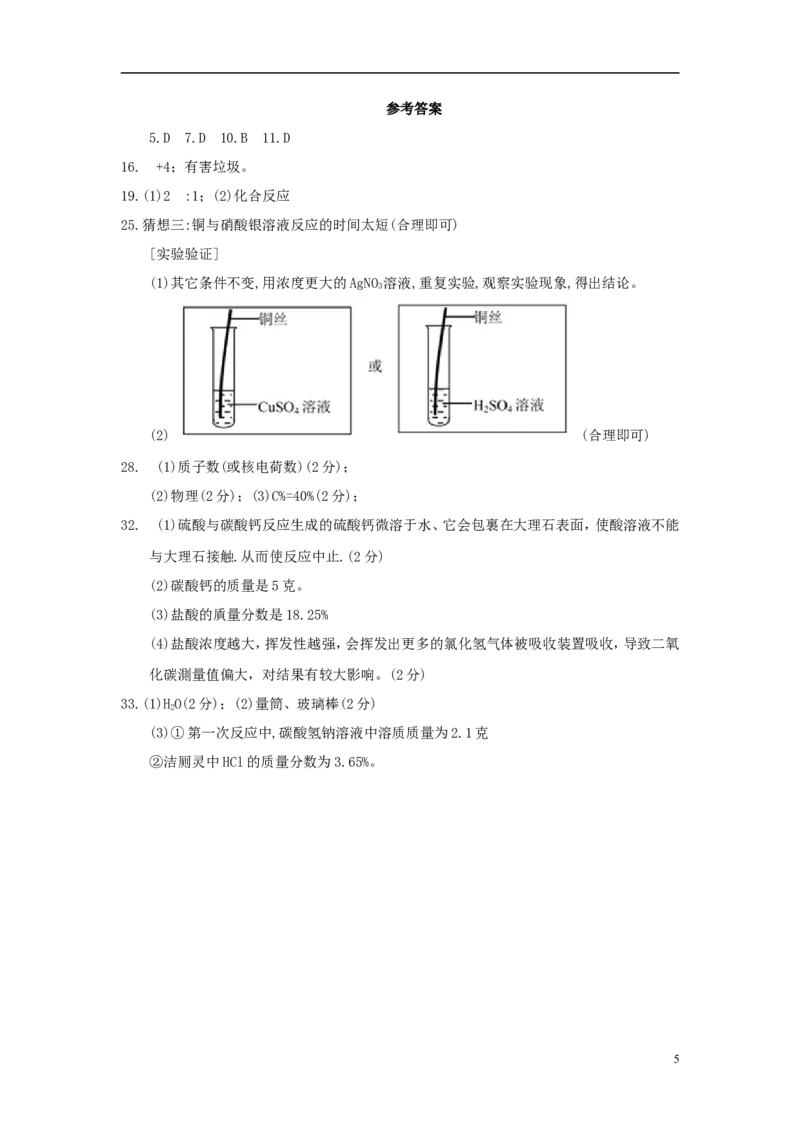
[实验验证]
(1)其它条件不变,用浓度更大的AgNO 溶液,重复实验,观察实验现象,得出结论。
3
(2) (合理即可)
28. (1)质子数(或核电荷数)(2分);
(2)物理(2分);(3)C%=40%(2分);
32. (1)硫酸与碳酸钙反应生成的硫酸钙微溶于水、它会包裏在大理石表面,使酸溶液不能
与大理石接触.从而使反应中止.(2分)
(2)碳酸钙的质量是5克。
(3)盐酸的貭量分数是18.25%
(4)盐酸浓度越大,挥发性越强,会挥发出更多的氯化氢气体被吸收装置吸收,导致二氧
化碳測量值偏大,对结果有较大影响。(2分)
33.(1)HO(2分);(2)量筒、玻璃棒(2分)
2
(3)①第一次反应中,碳酸氢钠溶液中溶质质量为2.1克
②洁厕灵中HCl的质量分数为3.65%。
5