文档内容
湖北省荆州市2018年中考化学真题试题
一、单项选择题(本大题包括12小题,每小题2分,共24分)
1.下列典故中,主要体现化学变化的是
A.火烧赤壁 B.刻舟求剑 C.司马光砸缸 D.铁杵磨成针
2.下列物质属于纯净物的是
A.空气 B.河水 C.臭氧 D.石油
3.下列金属中,金属活动性最强的是
A.铁 B.镁 C.锌 D.铜
4.“创建全国卫生城市,做文明荆州人”,下列做法不符合这一主题的是
A.生活垃圾分类投放 B.骑共享单车出行,节能减排
C.推广使用太阳能等清洁能源 D.生活污水直接排入长江
5.下列实验操作中,正确的是
6.尿素[CO(NH)]是一种化肥,它属于
2 2
A.氮肥 B.磷肥 C.钾肥 D.复合肥料
7.根据化学方程式不能获得的信息有
A.化学反应发生的条件 B.化学反应的快慢
C.反应物和生成物的质量比 D.化学反应的反应物和生成物
8.下列物质的用途与性质对应关系错误的是
A.熟石灰可用来改良酸性土壤---熟石灰呈碱性
B.氮气常用作保护气---氮气化学性质不活泼
C.铁粉可做食品保鲜剂---铁粉可以和空气中的氧气和水反应
D.金刚石能裁玻璃---金刚石是硬度最大的金属
9.下列说法正确的是
A.生成盐和水的反应一定是中和反应 B.有发光放热现象的变化一定是燃烧
C.不同种元素组成的纯净物一定是化合物 D.催化剂一定能加快化学反应速率
10.下列各组物质在水溶液中能大量共存且形成无色溶液的是
1A.NaCl BaCl NaCO B.KNO HCl CaCl
2 2 3 3 2
C.HSO FeCl NaNO D.NaOH HNO NHNO
2 4 3 3 3 4 3
11.实验室有四瓶失去标签的无色溶液,分别是碳酸钠溶液、氯化钡溶液、硫酸钠溶液和稀盐
酸中的一种。为了鉴别它们,将上述溶液分别标记为甲、乙、丙、丁,做如下实验:各取少许,
将甲分别滴加到另外三种溶液中,观察到乙和丁中产生白色沉淀,丙中无明显现象。据此可
判断甲是
A.碳酸钠溶液 B.氯化钡溶液 C.硫酸钠溶液 D.稀盐酸
12.将乙酸(CHCOOH)和葡萄糖(CH O)溶于水得到混合溶液,测得溶液中氢元素的质量分数
3 6 12 6
为a,则溶液中碳元素的质量分数为
A.1﹣9a B.1﹣8a C.12a D.8a
二、填空题(本大题包括5小题,共20分)
13.(4分)厨房中,蕴藏着很多化学知识:
(1)活性炭常用于冰箱内除异味,是利用了它的 性。
(2)炒菜时油锅中的油不慎着火,可用锅盖盖灭,其灭火原理为 。
(3)蛋白质是构成细胞的基本物质。下列食品中富含蛋白质的是 (填字母序号)。
A.米饭和馒头 B.花生油和大豆油
C.鸡蛋和牛肉 D.水果和蔬菜
(4)厨房中能用来除去水壶中水垢的物质是 (填字母序号)。
A.食醋 B.食盐水 C.食用油 D.洗洁精
14.(4分)用化学用语表示:
(1)2个氢氧根离子 。
(2)“可燃冰”的主要成分是甲烷水合物,甲烷的化学式是 。
(3)次氯酸钠( NaClO)是“84消毒液”的有效成分,次氯酸钠中氯元素的化合价是
价。
(4)服用含小苏打( NaHCO)的药物来治疗胃酸过多,其化学方程式为 。
3
15.(4分)图中A、B、C、D是四种粒子的结构示意图,请回答下列问题:
+12 2 8 +6 2 4 +17 2 8 8 +12 2 8 2
A B C D
(1)图中A、B、C、D四种粒子共表示 种元素。
(2)A、B、C、D中的阳离子与阴离子所形成的化合物的化学式为 。
2(3)晶体硅是制造半导体芯片的原料,如图是硅原子的结构示意图,
+x 2 8 4
图中x的值是 。
(4)硅元素的化学性质与A、B、C、D中 (填字母序号)对应的元素的化学性质相似。
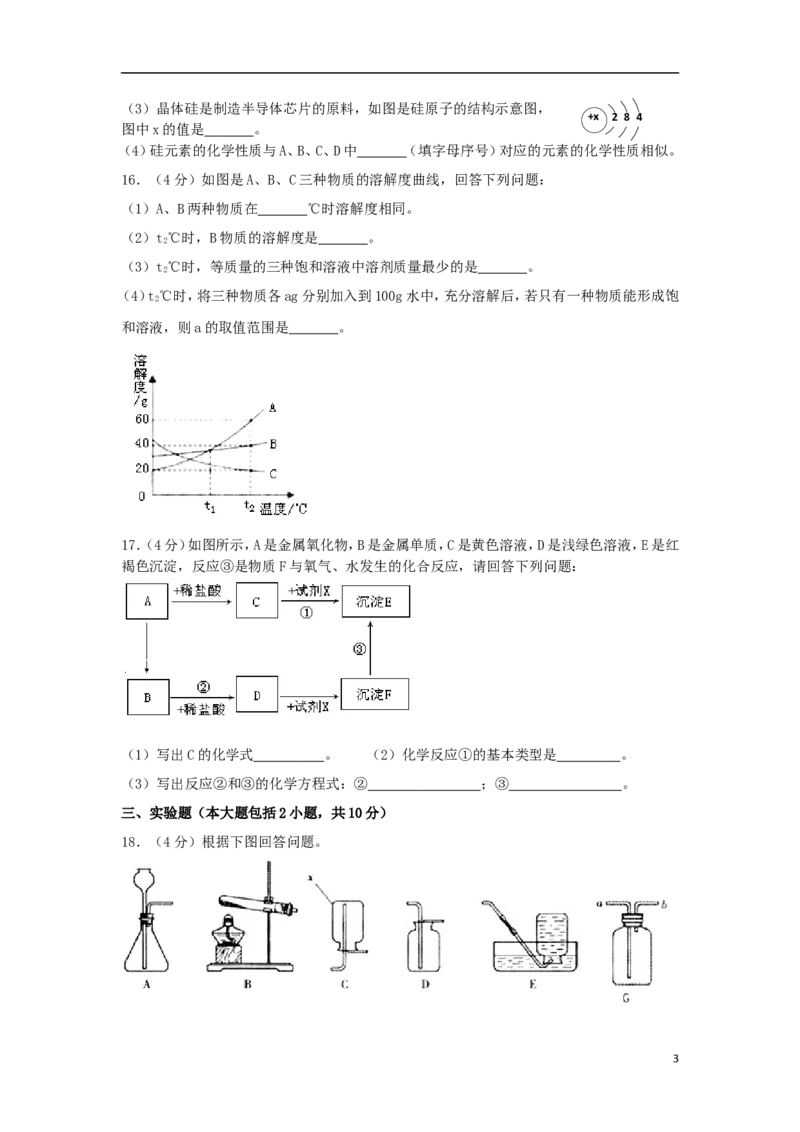
16.(4分)如图是A、B、C三种物质的溶解度曲线,回答下列问题:
(1)A、B两种物质在 ℃时溶解度相同。
(2)t℃时,B物质的溶解度是 。
2
(3)t℃时,等质量的三种饱和溶液中溶剂质量最少的是 。
2
(4)t℃时,将三种物质各ag分别加入到100g水中,充分溶解后,若只有一种物质能形成饱
2
和溶液,则a的取值范围是 。
17.(4分)如图所示,A是金属氧化物,B是金属单质,C是黄色溶液,D是浅绿色溶液,E是红
褐色沉淀,反应③是物质F与氧气、水发生的化合反应,请回答下列问题:
(1)写出C的化学式 。 (2)化学反应①的基本类型是 。
(3)写出反应②和③的化学方程式:② ;③ 。
三、实验题(本大题包括2小题,共10分)
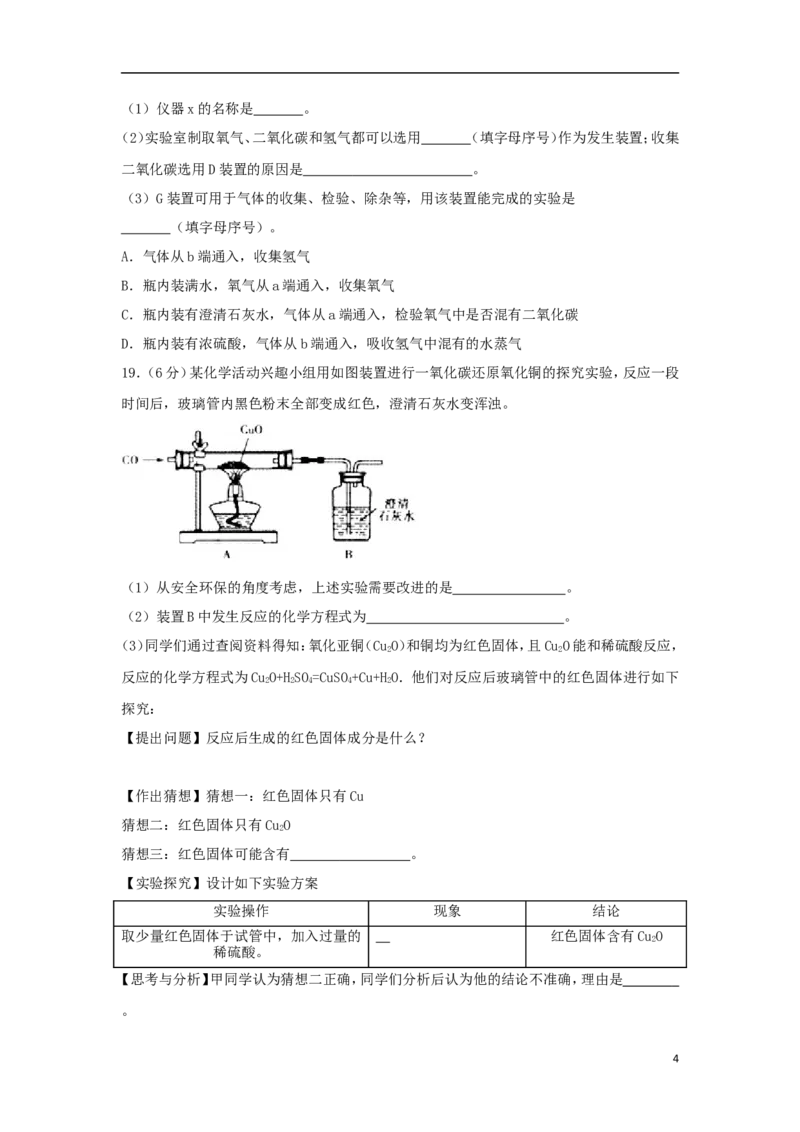
18.(4分)根据下图回答问题。
3(1)仪器x的名称是 。
(2)实验室制取氧气、二氧化碳和氢气都可以选用 (填字母序号)作为发生装置;收集
二氧化碳选用D装置的原因是 。
(3)G装置可用于气体的收集、检验、除杂等,用该装置能完成的实验是
(填字母序号)。
A.气体从b端通入,收集氢气
B.瓶内装满水,氧气从a端通入,收集氧气
C.瓶内装有澄清石灰水,气体从a端通入,检验氧气中是否混有二氧化碳
D.瓶内装有浓硫酸,气体从b端通入,吸收氢气中混有的水蒸气
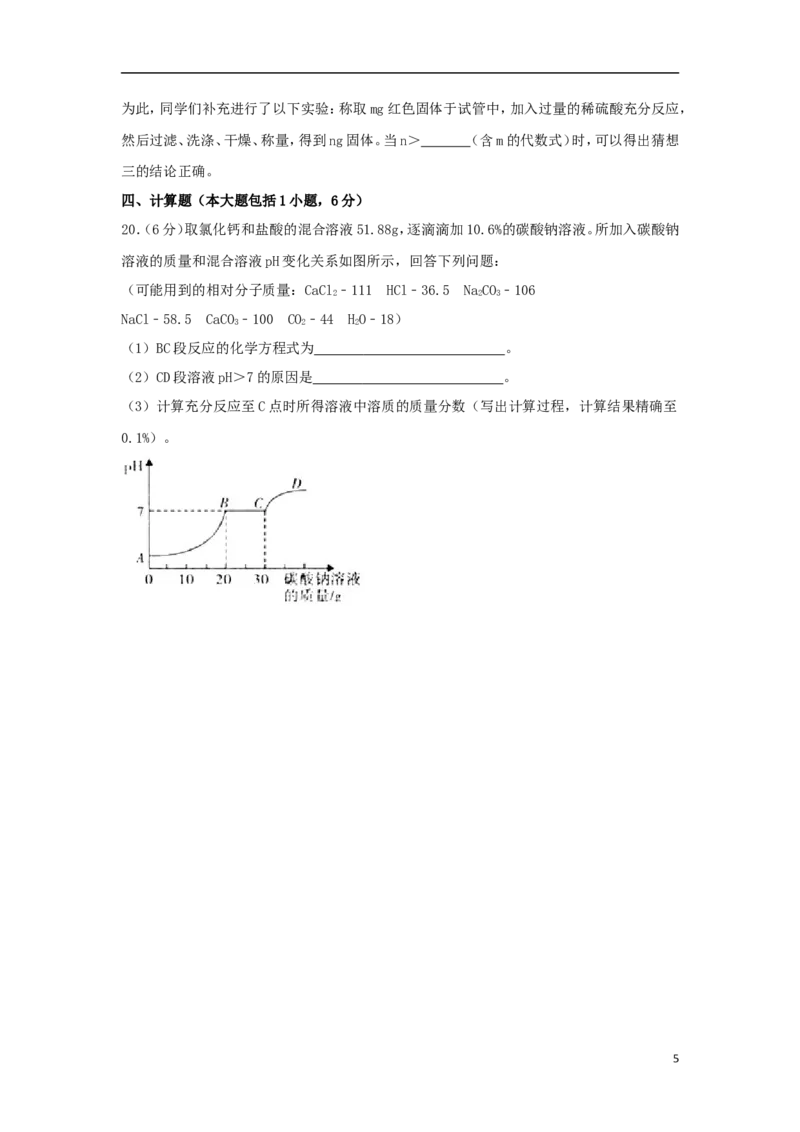
19.(6分)某化学活动兴趣小组用如图装置进行一氧化碳还原氧化铜的探究实验,反应一段
时间后,玻璃管内黑色粉末全部变成红色,澄清石灰水变浑浊。
(1)从安全环保的角度考虑,上述实验需要改进的是 。
(2)装置B中发生反应的化学方程式为 。
(3)同学们通过查阅资料得知:氧化亚铜(CuO)和铜均为红色固体,且CuO能和稀硫酸反应,
2 2
反应的化学方程式为CuO+HSO=CuSO+Cu+HO.他们对反应后玻璃管中的红色固体进行如下
2 2 4 4 2
探究:
【提出问题】反应后生成的红色固体成分是什么?
【作出猜想】猜想一:红色固体只有Cu
猜想二:红色固体只有CuO
2
猜想三:红色固体可能含有 。
【实验探究】设计如下实验方案
实验操作 现象 结论
取少量红色固体于试管中,加入过量的 红色固体含有CuO
2
稀硫酸。
【思考与分析】甲同学认为猜想二正确,同学们分析后认为他的结论不准确,理由是
。
4为此,同学们补充进行了以下实验:称取mg红色固体于试管中,加入过量的稀硫酸充分反应,
然后过滤、洗涤、干燥、称量,得到ng固体。当n> (含m的代数式)时,可以得出猜想
三的结论正确。
四、计算题(本大题包括1小题,6分)
20.(6分)取氯化钙和盐酸的混合溶液51.88g,逐滴滴加10.6%的碳酸钠溶液。所加入碳酸钠
溶液的质量和混合溶液pH变化关系如图所示,回答下列问题:
(可能用到的相对分子质量:CaCl﹣111 HCl﹣36.5 NaCO﹣106
2 2 3
NaCl﹣58.5 CaCO﹣100 CO﹣44 HO﹣18)
3 2 2
(1)BC段反应的化学方程式为 。
(2)CD段溶液pH>7的原因是 。
(3)计算充分反应至C点时所得溶液中溶质的质量分数(写出计算过程,计算结果精确至
0.1%)。
5参考答案
一、单项选择题(本大题包括12小题,每小题2分,共24分)
1.A 2.C 3.B 4.D 5.C 6.A 7.B 8.D 9.C 10.B 11.B 12.A
二、填空题(本大题包括5小题,共20分)
13.(1)吸附 (2)隔绝氧气 (3)C (4)A
14.(1)2OH- (2)CH (3)+1 (4)NaHCO+HCl=NaCl+HO+CO↑
4 3 2 2
15. (1)三 (2)MgCl (3)14 (4)B
2
16.(1)t (2)40g (3)A (4) 20g≤a<40g
1
17.(1)FeCl (2)复分解反应
3
(3)Fe+2HCl=FeCl+H↑ 4Fe(OH)+O+2HO=4Fe(OH)
2 2 2 2 2 3
三、实验题(本大题包括2小题,共10分)
18.(1)集气瓶 (2)A 二氧化碳的密度比空气大 (3)AC
19.(1)将尾气点燃或增加尾气处理装置
(2)CO+Ca(OH)=CaCO↓+HO
2 2 3 2
(3)Cu和CuO 溶液变蓝色,有红色固体剩余
2
铜和氧化亚铜的混合物与足量稀硫酸反应,也能观察到溶液变蓝色,有红色固体剩余
四、计算题(本大题包括1小题,6分)
20. (1)NaCO+CaCl═CaCO↓+2NaCl
2 3 2 3
(2)碳酸钠溶液显碱性,pH>7
(3)【解】设碳酸钠和盐酸反应生成二氧化碳的质量为x,生成氯化钠的质量为y。而碳酸钠和
氯化钙反应生成碳酸钙的质量为z,生成氯化钠的质量为w。
NaCO+2HCl═2NaCl+HO+CO↑
2 3 2 2
106 117 44
20g×10.6% y x
= =
x=0.88g y=2.34g
NaCO+CaCl═CaCO↓+2NaCl
2 3 2 3
106 100 117
610g×10.6% z w
z=1g w=1.17g
充分反应至C点时所得溶液中溶质的质量分数为
×100%=4.4%
答:充分反应至C点时所得溶液中溶质的质量分数为4.4%
7