文档内容
2022 年广东省初中学业水平考试
化学
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Fe-56 Cu-64 Zn-65
一、选择题:本大题共15小题,每小题3分,共45分,在每小题给出的四个选项中,只有
一项是符合题目要求的。
1. 下列涉及化学变化的是
A. 光合作用 B. 冰雪融化 C. 海水蒸发 D. 溪水流淌
2. 学校采购了一批含75%酒精的免洗消毒喷雾。你建议在存放处张贴的警示标识是
A. B. C. D.
3. 下列属于纯净物的是
A. 汽水 B. 氢气 C. 黄铜 D. 空气
4. 我国自主研制的“极目一号”Ⅲ型浮空艇的锚泊主系缆由聚乙烯纤维制成,该材料属于
A. 天然橡胶 B. 天然纤维 C. 合成材料 D. 金属材料
5. 下列化学用语表示两个分子的是
A. O2- B. 2O C. SO D. 2O
3 2
6. 科学家对人类文明和社会可持续发展作出了重要贡献。下列选项正确的是
A. 拉瓦锡编制了元素周期表 B. 门捷列夫提出了近代原子学说
C. 道尔顿确定了空气的组成 D. 屠呦呦因研究青蒿素获诺贝尔奖
7. 荔枝生长过程中,需要施肥为果树补充营养。下列属于复合肥的是
.
A NH HPO B. CO(NH ) C. NH NO D. KCl
4 2 4 2 2 4 3
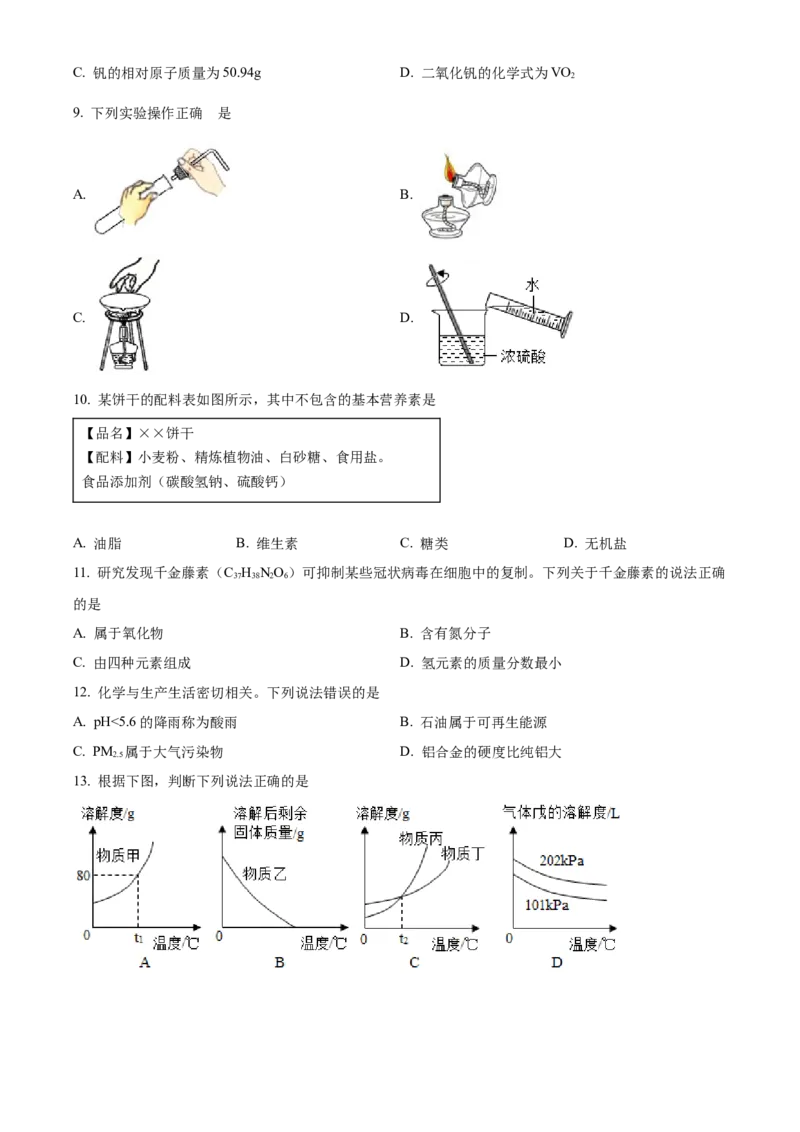
8. 我国科学家开发了一种基于二氧化钒的“冷热双吸”材料,有望助力实现“双碳”目标。钒元素在周期
表中的信息如图所示。下列说法错误的是
A. 钒为金属元素 B. 钒原子核外电子数为23C. 钒的相对原子质量为50.94g D. 二氧化钒的化学式为VO
2
的
9. 下列实验操作正确 是
A. B.
C. D.
10. 某饼干的配料表如图所示,其中不包含的基本营养素是
【品名】××饼干
【配料】小麦粉、精炼植物油、白砂糖、食用盐。
食品添加剂(碳酸氢钠、硫酸钙)
A. 油脂 B. 维生素 C. 糖类 D. 无机盐
11. 研究发现千金藤素(C H NO)可抑制某些冠状病毒在细胞中的复制。下列关于千金藤素的说法正确
37 38 2 6
的是
A. 属于氧化物 B. 含有氮分子
C. 由四种元素组成 D. 氢元素的质量分数最小
12. 化学与生产生活密切相关。下列说法错误的是
A. pH<5.6的降雨称为酸雨 B. 石油属于可再生能源
C. PM 属于大气污染物 D. 铝合金的硬度比纯铝大
2.5
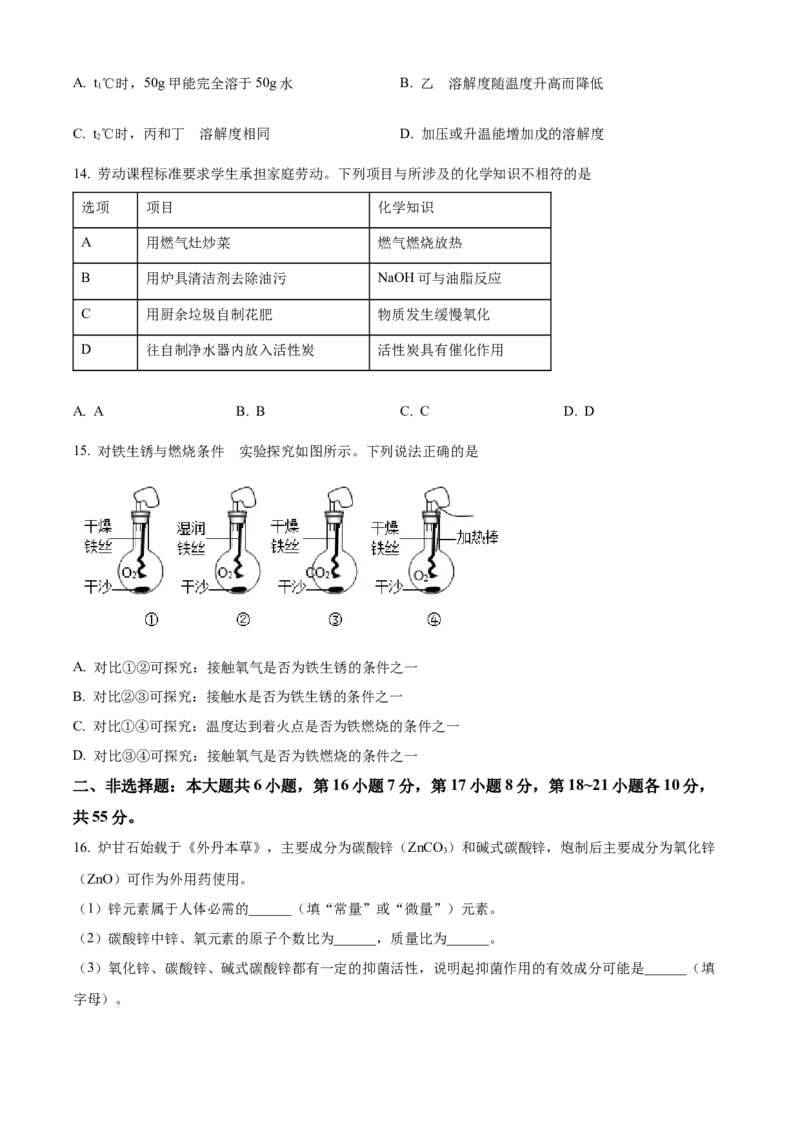
13. 根据下图,判断下列说法正确的是的
A. t℃时,50g甲能完全溶于50g水 B. 乙 溶解度随温度升高而降低
1
的
C. t℃时,丙和丁 溶解度相同 D. 加压或升温能增加戊的溶解度
2
14. 劳动课程标准要求学生承担家庭劳动。下列项目与所涉及的化学知识不相符的是
选项 项目 化学知识
A 用燃气灶炒菜 燃气燃烧放热
B 用炉具清洁剂去除油污 NaOH可与油脂反应
C 用厨余垃圾自制花肥 物质发生缓慢氧化
D 往自制净水器内放入活性炭 活性炭具有催化作用
A. A B. B C. C D. D
的
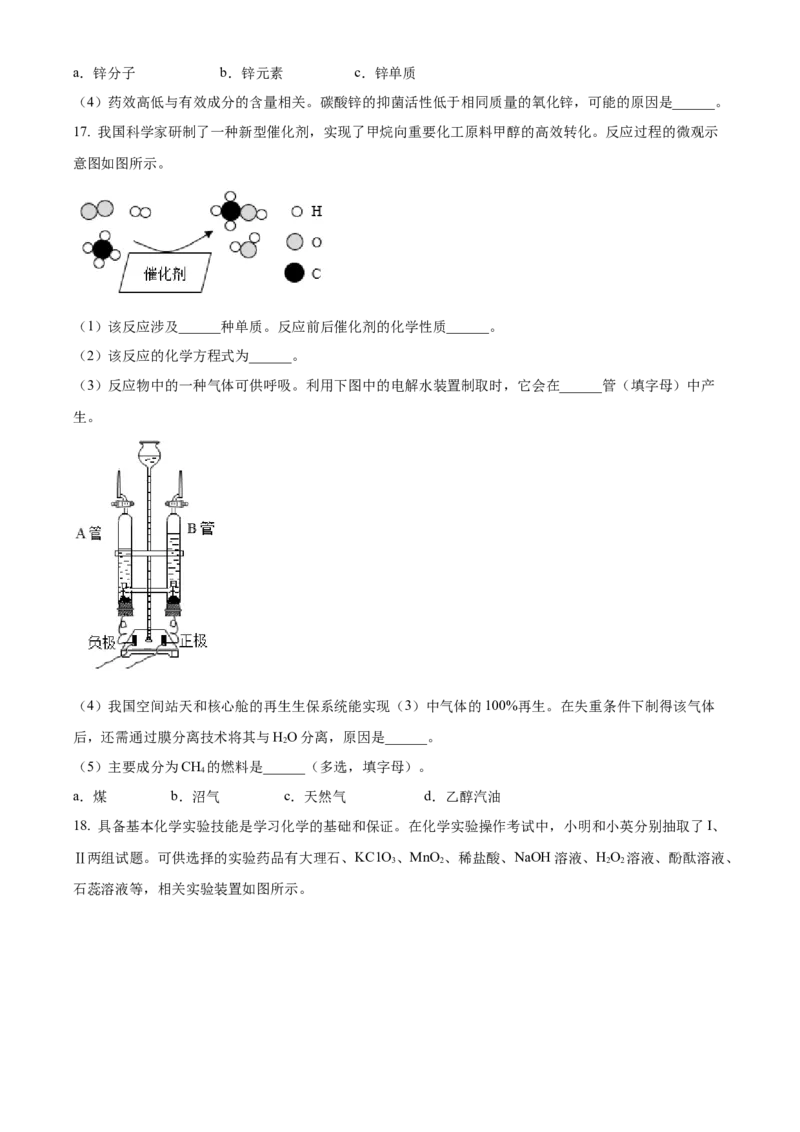
15. 对铁生锈与燃烧条件 实验探究如图所示。下列说法正确的是
A. 对比①②可探究:接触氧气是否为铁生锈的条件之一
B. 对比②③可探究:接触水是否为铁生锈的条件之一
C. 对比①④可探究:温度达到着火点是否为铁燃烧的条件之一
D. 对比③④可探究:接触氧气是否为铁燃烧的条件之一
二、非选择题:本大题共6小题,第16小题7分,第17小题8分,第18~21小题各10分,
共55分。
16. 炉甘石始载于《外丹本草》,主要成分为碳酸锌(ZnCO )和碱式碳酸锌,炮制后主要成分为氧化锌
3
(ZnO)可作为外用药使用。
(1)锌元素属于人体必需的______(填“常量”或“微量”)元素。
(2)碳酸锌中锌、氧元素的原子个数比为______,质量比为______。
(3)氧化锌、碳酸锌、碱式碳酸锌都有一定的抑菌活性,说明起抑菌作用的有效成分可能是______(填
字母)。a.锌分子 b.锌元素 c.锌单质
(4)药效高低与有效成分的含量相关。碳酸锌的抑菌活性低于相同质量的氧化锌,可能的原因是______。
17. 我国科学家研制了一种新型催化剂,实现了甲烷向重要化工原料甲醇的高效转化。反应过程的微观示
意图如图所示。
(1)该反应涉及______种单质。反应前后催化剂的化学性质______。
(2)该反应的化学方程式为______。
(3)反应物中的一种气体可供呼吸。利用下图中的电解水装置制取时,它会在______管(填字母)中产
生。
(4)我国空间站天和核心舱的再生生保系统能实现(3)中气体的100%再生。在失重条件下制得该气体
后,还需通过膜分离技术将其与HO分离,原因是______。
2
(5)主要成分为CH 的燃料是______(多选,填字母)。
4
a.煤 b.沼气 c.天然气 d.乙醇汽油
18. 具备基本化学实验技能是学习化学的基础和保证。在化学实验操作考试中,小明和小英分别抽取了I、
Ⅱ两组试题。可供选择的实验药品有大理石、KC1O 、MnO 、稀盐酸、NaOH溶液、HO 溶液、酚酞溶液、
3 2 2 2
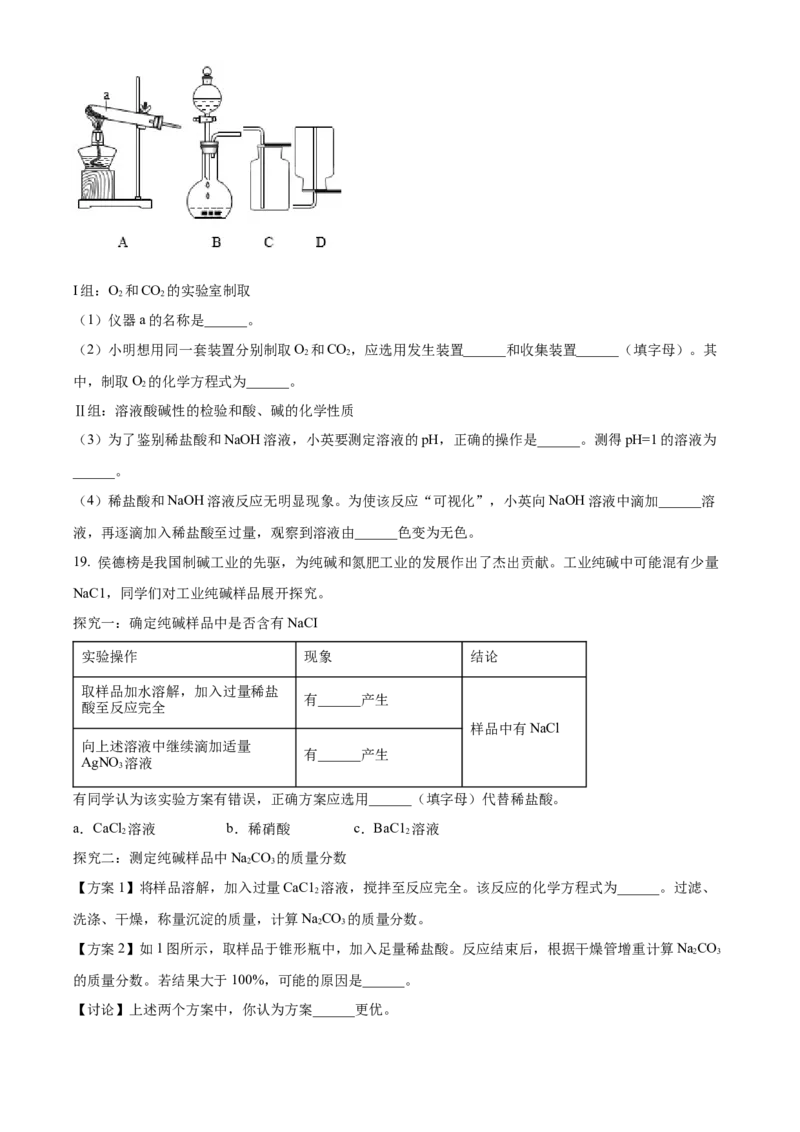
石蕊溶液等,相关实验装置如图所示。I组:O 和CO 的实验室制取
2 2
(1)仪器a的名称是______。
(2)小明想用同一套装置分别制取O 和CO,应选用发生装置______和收集装置______(填字母)。其
2 2
中,制取O 的化学方程式为______。
2
Ⅱ组:溶液酸碱性的检验和酸、碱的化学性质
(3)为了鉴别稀盐酸和NaOH溶液,小英要测定溶液的pH,正确的操作是______。测得pH=1的溶液为
______。
(4)稀盐酸和NaOH溶液反应无明显现象。为使该反应“可视化”,小英向NaOH溶液中滴加______溶
液,再逐滴加入稀盐酸至过量,观察到溶液由______色变为无色。
19. 侯德榜是我国制碱工业的先驱,为纯碱和氮肥工业的发展作出了杰出贡献。工业纯碱中可能混有少量
NaC1,同学们对工业纯碱样品展开探究。
探究一:确定纯碱样品中是否含有NaCI
实验操作 现象 结论
取样品加水溶解,加入过量稀盐
有______产生
酸至反应完全
样品中有NaCl
向上述溶液中继续滴加适量
有______产生
AgNO 溶液
3
有同学认为该实验方案有错误,正确方案应选用______(填字母)代替稀盐酸。
a.CaCl 溶液 b.稀硝酸 c.BaC1 溶液
2 2
探究二:测定纯碱样品中NaCO 的质量分数
2 3
【方案1】将样品溶解,加入过量CaC1 溶液,搅拌至反应完全。该反应的化学方程式为______。过滤、
2
洗涤、干燥,称量沉淀的质量,计算NaCO 的质量分数。
2 3
【方案2】如1图所示,取样品于锥形瓶中,加入足量稀盐酸。反应结束后,根据干燥管增重计算NaCO
2 3
的质量分数。若结果大于100%,可能的原因是______。
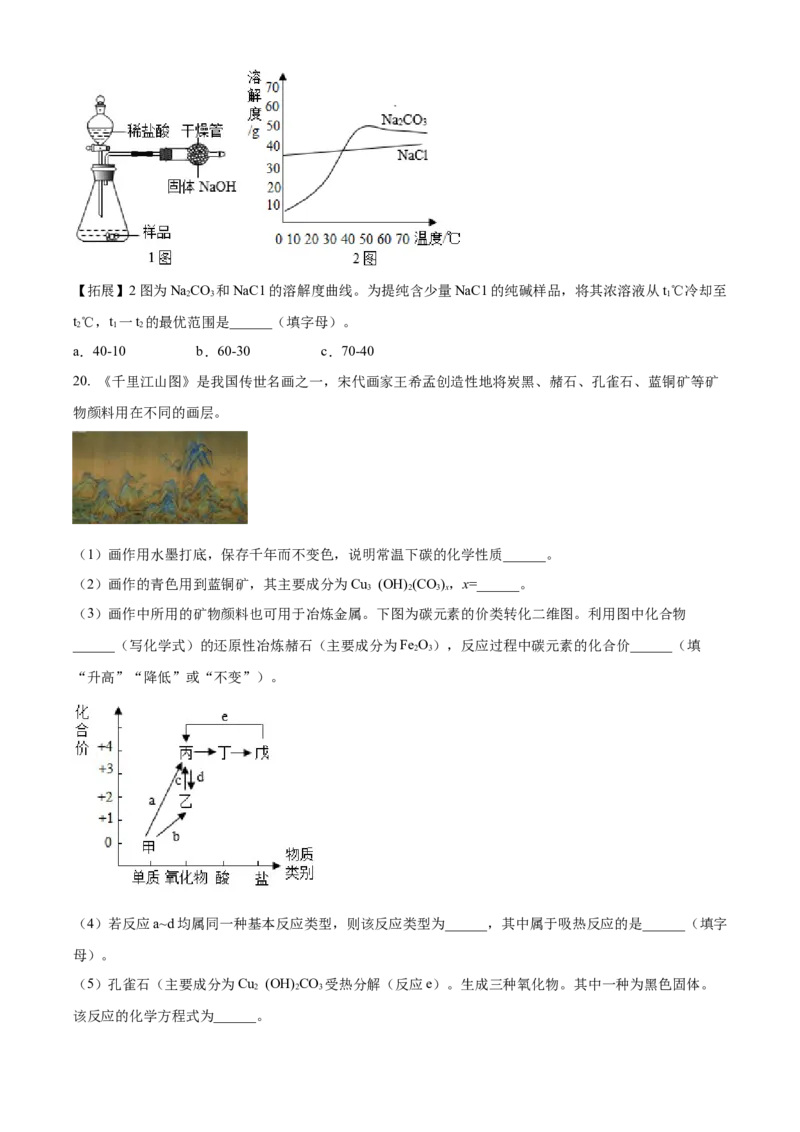
【讨论】上述两个方案中,你认为方案______更优。【拓展】2图为NaCO 和NaC1的溶解度曲线。为提纯含少量NaC1的纯碱样品,将其浓溶液从t℃冷却至
2 3 1
t℃,t 一t 的最优范围是______(填字母)。
2 1 2
a.40-10 b.60-30 c.70-40
20. 《千里江山图》是我国传世名画之一,宋代画家王希孟创造性地将炭黑、赭石、孔雀石、蓝铜矿等矿
物颜料用在不同的画层。
(1)画作用水墨打底,保存千年而不变色,说明常温下碳的化学性质______。
(2)画作的青色用到蓝铜矿,其主要成分为Cu (OH) (CO),x=______。
3 2 3 x
(3)画作中所用的矿物颜料也可用于冶炼金属。下图为碳元素的价类转化二维图。利用图中化合物
______(写化学式)的还原性冶炼赭石(主要成分为Fe O),反应过程中碳元素的化合价______(填
2 3
“升高”“降低”或“不变”)。
(4)若反应a~d均属同一种基本反应类型,则该反应类型为______,其中属于吸热反应的是______(填字
母)。
(5)孔雀石(主要成分为Cu (OH) CO 受热分解(反应e)。生成三种氧化物。其中一种为黑色固体。
2 2 3
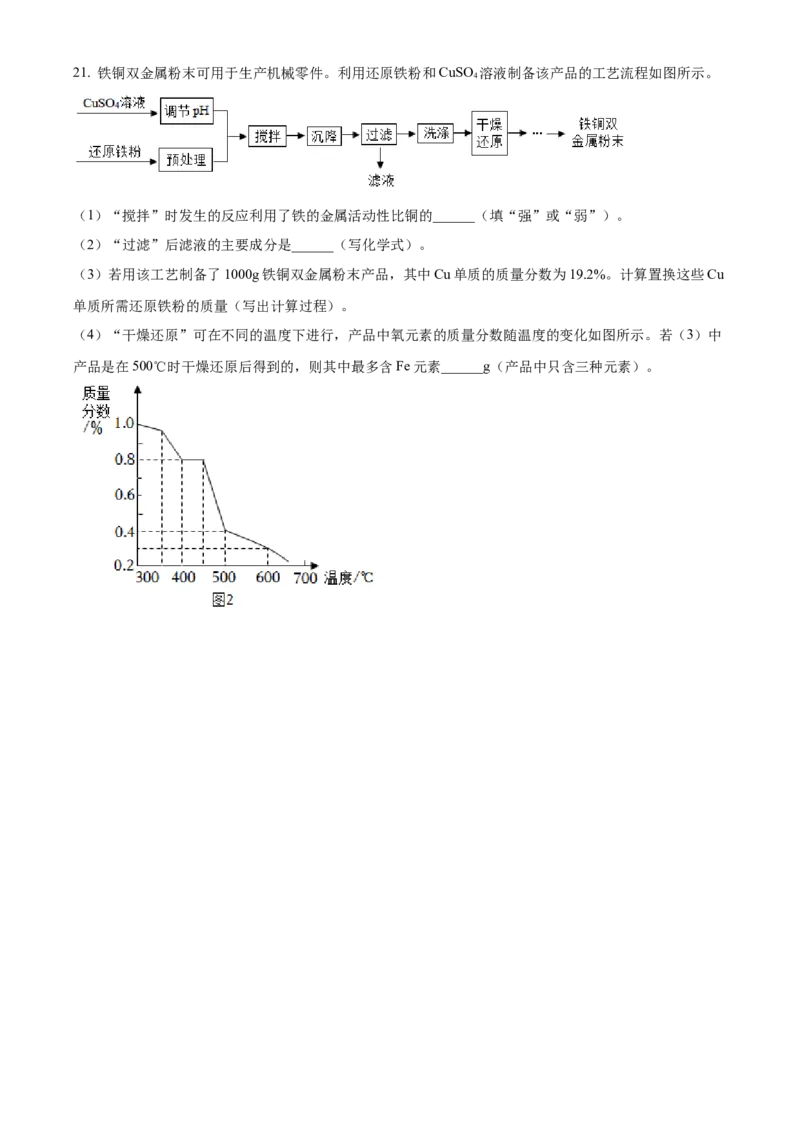
该反应的化学方程式为______。21. 铁铜双金属粉末可用于生产机械零件。利用还原铁粉和CuSO 溶液制备该产品的工艺流程如图所示。
4
(1)“搅拌”时发生的反应利用了铁的金属活动性比铜的______(填“强”或“弱”)。
(2)“过滤”后滤液的主要成分是______(写化学式)。
(3)若用该工艺制备了1000g铁铜双金属粉末产品,其中Cu单质的质量分数为19.2%。计算置换这些Cu
单质所需还原铁粉的质量(写出计算过程)。
(4)“干燥还原”可在不同的温度下进行,产品中氧元素的质量分数随温度的变化如图所示。若(3)中
产品是在500℃时干燥还原后得到的,则其中最多含Fe元素______g(产品中只含三种元素)。