文档内容
1
协同发展共同体第三子共同体2024-2025学年度第一学期期末考试
高一 化学试卷
考试时间:60分钟 分值:100分
可能用到的相对原子质量:H:1 C:12 O:16 Na:23 Mg:24 Cl:35.5
第I卷(54分)
一、选择题:(每小题只有一个选项符合题意,每小题3分,共54分。)
1.2023年6月9日,我省某高校研制的中国首颗平板式新体制低轨宽带通信卫星“龙江三
号”成功发射。该卫星主体材质使用了合金材料。下列所用材料不属于合金的是( )
A.生铁铸造的下 B.硬铝制造的飞 C.聚乙烯制成的食品 D.不锈钢制造的地铁列
水井盖 机外壳 包装袋 车的车体
2.当光束通过鸡蛋清水溶液时,从侧面观察到一条光亮的“通路”,说明鸡蛋清水溶液是(
)
A.溶液 B.胶体 C.悬浊液 D.乳浊液
3.氧化还原反应的本质是( )
A.元素化合价的升降 B.电子的转移
C.有氧元素参加的反应 D.原子的重新组合
4.合成新物质是研究化学的主要目的之一、意大利科学家合成了一种新型的氧分子O ,下列
4
关于O 的说法中,正确的是( )
4
A.O4 是一种新型的化合物 B.O4 和O2 互为同位素
C.O4 和O2 互为同素异形体 D.O4 和O2 可通过物理变化实现转化
5.“东风夜放花千树。更吹落、星如雨”。早在宋代,人们就发现不同的金属化合物在高温灼
烧时,火焰会呈现出不同的颜色,烟花逐渐出现在盛大的典礼或表演中。下列有关说法正确
的是( )
A.焰色试验是一种定性检验金属元素的方法
B.火焰的不同焰色是发生了化学变化
C.某物质在灼烧时焰色为黄色,则该物质中一定不含钾元素
D.将铂丝(或铁丝)用硫酸洗涤后,可蘸取药品灼烧
6.下列物质中,既含有共价键又含有离子键的是( )1
A.HF B.NaCl C.HCl D.KOH
7.在含有大量Ag+、H+、NO —的溶液中,还可能大量共存的离子是( )
3
A. Cl— B. K+ C. Fe2+ D. CO 2—
3
8.下列反应的离子方程式书写正确的是( )
A.碳酸钡和盐酸反应:CO 2— + 2H+= H O + CO ↑
3 2 2
B.FeCl 溶液与Cu反应:Fe3+ + Cu = Fe2+ + Cu2+
3
C.氢氧化铝与氢氧化钠溶液反应:Al(OH) + OH—= [Al(OH) ]—
3 4
D.Na与水反应:Na + H2O = Na++ OH—+ H2↑
9.下列叙述正确的有( )
A.含氧40%的氧化镁、碱石灰、稀硫酸均为混合物
B.Fe(OH)3 、FeCl2 、NaHCO3 均可由化合反应制得
C.氧化还原反应一定有氧元素参加
D.碳纳米管属于胶体分散系,该材料具有超强的吸附能力
10.下列有关物质的性质与用途正确且具有对应关系的是( )
A.FeCl3 具有还原性,可用作铜制线路板的蚀刻剂
B.Fe2O3 能与盐酸反应,可用于制作红色颜料
C.Al2O3 熔点高,可用作耐高温材料
D.NaHCO3 受热易分解,可用于制胃酸中和剂
11.下列说法正确的是( )
A.1 mol 氢的质量为1g
B.等物质的量的O 和O 所含的O原子数目之比为2:3
2 3
C.1L 1mol·L-1CaCl 溶液中含有的Cl-离子数目为N
2 A
D.常温常压下,11.2L O 中含有的原子数目为N
2 A
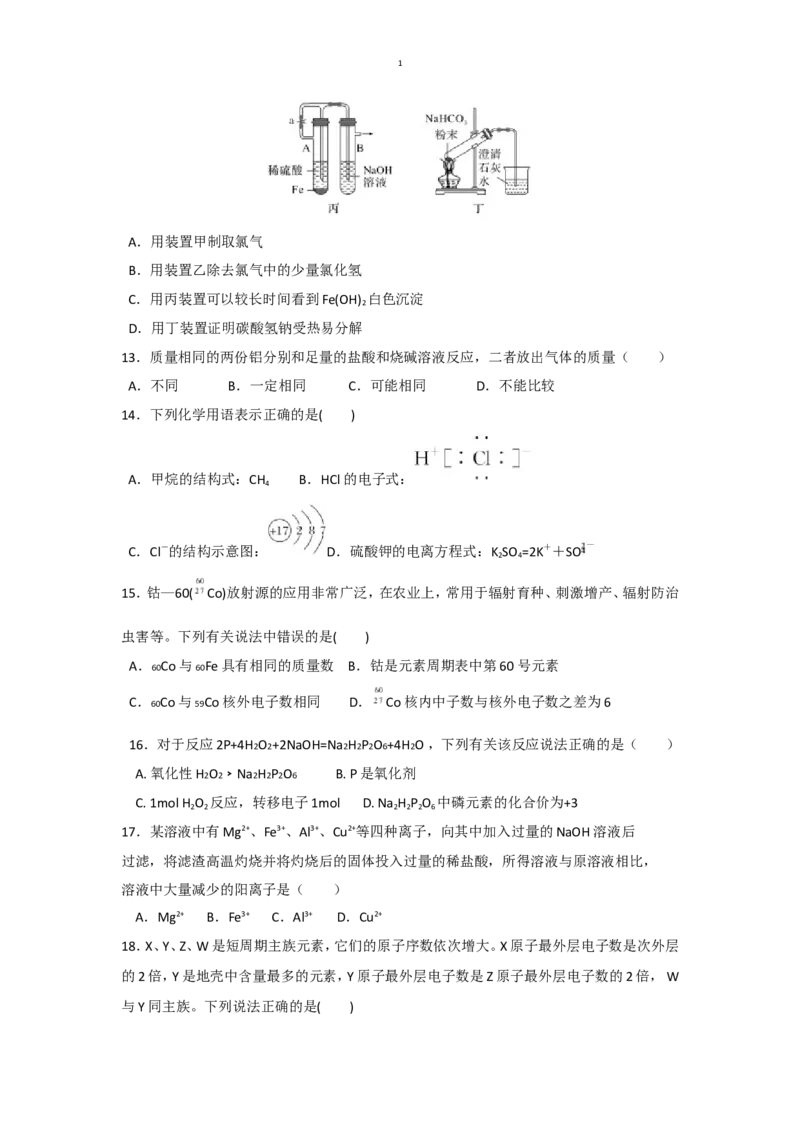
12.关于甲、乙、丙、丁四套装置的说法正确的是( )1
A.用装置甲制取氯气
B.用装置乙除去氯气中的少量氯化氢
C.用丙装置可以较长时间看到Fe(OH) 白色沉淀
2
D.用丁装置证明碳酸氢钠受热易分解
13.质量相同的两份铝分别和足量的盐酸和烧碱溶液反应,二者放出气体的质量( )
A.不同 B.一定相同 C.可能相同 D.不能比较
14.下列化学用语表示正确的是( )
A.甲烷的结构式:CH B.HCl的电子式:
4
C.Cl-的结构示意图: D.硫酸钾的电离方程式:K SO =2K++SO
2 4
15.钴—60( Co)放射源的应用非常广泛,在农业上,常用于辐射育种、刺激增产、辐射防治
虫害等。下列有关说法中错误的是( )
A. 60Co与 60Fe具有相同的质量数 B.钴是元素周期表中第60号元素
C. 60Co与 59Co核外电子数相同 D. Co核内中子数与核外电子数之差为6
16.对于反应2P+4H2O2+2NaOH=Na2H2P2O6+4H2O ,下列有关该反应说法正确的是( )
A. 氧化性H2O2﹥Na2H2P2O6 B. P是氧化剂
C. 1mol H O 反应,转移电子1mol D. Na H P O 中磷元素的化合价为+3
2 2 2 2 2 6
17.某溶液中有Mg2+、Fe3+、Al3+、Cu2+等四种离子,向其中加入过量的NaOH溶液后
过滤,将滤渣高温灼烧并将灼烧后的固体投入过量的稀盐酸,所得溶液与原溶液相比,
溶液中大量减少的阳离子是( )
A.Mg2+ B.Fe3+ C.Al3+ D.Cu2+
18.X、Y、Z、W是短周期主族元素,它们的原子序数依次增大。X原子最外层电子数是次外层
的2倍,Y是地壳中含量最多的元素,Y原子最外层电子数是Z原子最外层电子数的2倍, W
与Y同主族。下列说法正确的是( )1
A.X形成的单质只有一种
B.原子半径:r(W)>r(Z)>r(Y) >r(X )
C.常温下,Z单质及其氧化物均不能溶于KOH溶液中
D.Y简单气态氢化物的热稳定性比W的强
第II卷 (46分)
19.(12分)按要求作答:
Ⅰ、(1)写出小苏打的化学式__________________。
(2) 次氯酸(HClO)属于(填“电解质”或“非电解质”)
(3)Fe(OH)2 在空气中被氧化成红褐色沉淀,写出化学方程式_____________________。
(4)用离子方程式说明Cl2 与Br2 的氧化性相对强弱:______________________。
Ⅱ、欲用Na2CO3 固体配制950mL 0.1mol•L-1 的Na2CO3 溶液。请回答:
(1) 配制该溶液应选用 mL容量瓶。
(2) 用托盘天平称取 g Na2CO3 固体。
(3) 如果将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外,最后配成的溶液中溶质的
浓度将会(填“偏大”或“偏小”)
20. (12分) 元素周期表在学习、研究中有很重要的作用,为纪念元素周期表诞生150周年,
IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期
表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。下表是元素周期表
的一部分。请按要求回答下列问题:
族
ⅠA 0
周期
1 ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
2 (2) (3)
3 (4) (5) (6) (7) ⑦
A. 写出②的元素符号______________。
B. 写出①的最高价氧化物的电子式:______________。
C. 写出③与⑦的单质在加热条件下反应的化学方程式__________________________。
D. ③和④中金属性较强的是_____(填化学式)。
E. ⑤、⑥的原子半径大小是⑤⑥(填“>”或“<”);⑥、⑦的最高价氧化物对应的水化物中,酸1
性较强的物质的化学式是__________。
F. ④和⑦可形成________(填“离子”或“共价”)化合物。
21.(10分)常温下,氯气可用来对自来水进行消毒,
A、B、C、D、E都含氯元素,其转化关系如图所示:
(1)请分别写出下列物质的化学式(如为溶液请填溶
质的化学式):
B________、C________。
(2)写出下列反应的化学方程式或离子方程式(请注明反应条件):
A+H O(离子方程式):___________________________________;
2
A+NaOH(离子方程式): ________________________________________;
D→A(化学方程式):_________________________________________。
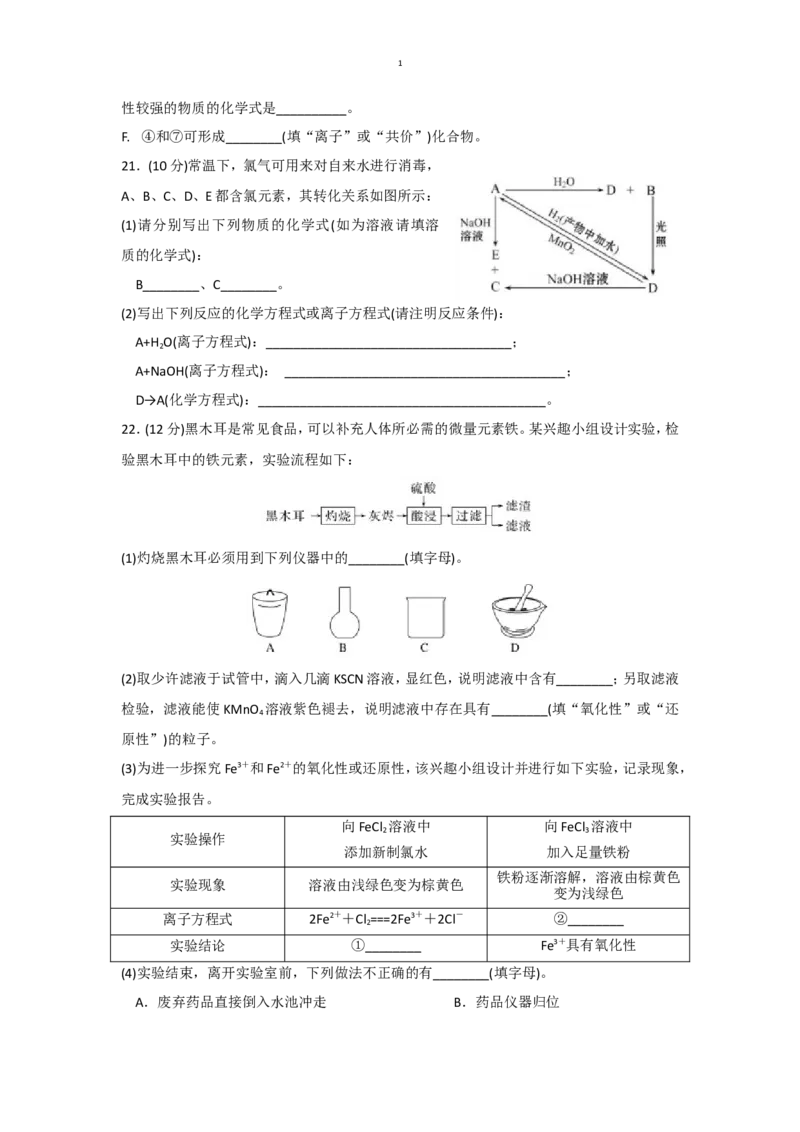
22.(12分)黑木耳是常见食品,可以补充人体所必需的微量元素铁。某兴趣小组设计实验,检
验黑木耳中的铁元素,实验流程如下:
(1)灼烧黑木耳必须用到下列仪器中的________(填字母)。
(2)取少许滤液于试管中,滴入几滴KSCN溶液,显红色,说明滤液中含有________;另取滤液
检验,滤液能使KMnO 溶液紫色褪去,说明滤液中存在具有________(填“氧化性”或“还
4
原性”)的粒子。
(3)为进一步探究Fe3+和Fe2+的氧化性或还原性,该兴趣小组设计并进行如下实验,记录现象,
完成实验报告。
向FeCl 溶液中 向FeCl 溶液中
2 3
实验操作
添加新制氯水 加入足量铁粉
铁粉逐渐溶解,溶液由棕黄色
实验现象 溶液由浅绿色变为棕黄色
变为浅绿色
离子方程式 2Fe2++Cl ===2Fe3++2Cl- ②________
2
实验结论 ①________ Fe3+具有氧化性
(4)实验结束,离开实验室前,下列做法不正确的有________(填字母)。
A.废弃药品直接倒入水池冲走 B.药品仪器归位1
C.清洁实验仪器、打扫实验室卫生 D.关闭水电、门窗
协同发展共同体第三子共同体 2024-2025 学年度第一学期期
末考试化学答案
单选题:
(2) (每小题3分,共54分。每小题只有一个选项符合题意)。
1 2 3 4 5 6 7 8 9
C B B C A D B C B
10 11 12 13 14 15 16 17 18
C B C B D B A C D
(3) 非选择题(共4小题,共计46分)
19. (12分)
Ⅰ、(1)NaHCO3 (1分)
(2) 电解质 (1分)
(3)4F e(OH)2+O2+2H2O=4Fe(OH)3 (2分)
(4) Cl2+2Br—=2Cl—+Br2(2分)
Ⅱ、(1) 1000 (2分) (2) 10.6 (2分) (3)偏小 (2分)
20. (12分)
(1)N (1分) (2) (2分)
(3) (2分) (4) Na (2分) (5) > (2分) HClO4 (2分) (6)离子 (1分)
21. (10分)
(1)HClO (2分) NaCl (2分)
(2)Cl + H O Cl-+HClO +H+ (2分) Cl + 2OH-= Cl-+ClO-+H O (2分)
2 2 2 21
MnO +4HCl(浓) MnCl + Cl ↑+2H O (2分,不写浓或不写反应条件加热不给分)
2 2 2 2
22. (12分)
(1)A (2分)
(2) Fe3+ (2分) 还原性 (2分)
(3)①Fe2+具有还原性 (2分)
②2Fe3++Fe==3Fe2+ (2分)
(4)A (2分)