文档内容
2001 年全国普通高等学校招生统一考试
上海化学试卷
考生注意:
1.本试卷满分l50分,考试时问120分钟·
2.本考试设试卷和答题纸两部分,试卷包括试题与答题要求;所有答题必须涂(选择
题)或写(非选择题)在答题纸上;做在试卷上一律不得分。
3.答题前,考生务必在答题纸上用钢笔或圆珠笔清楚填写姓名、准考证号,并将核对
后的条形码贴在指定位置上。
4.答题纸与试卷在试题编号上是一一对应的,答题时应特别注意,不能错位。
第Ⅰ卷(共75分)
相对原子质量:H—l C—12 N—14 O-16 Mg-24
S—32 K—39 Fe—56 I—127 Cl—35.5
一、选择题(本题共10分),每小题2分,只有一个正确选项,答案涂写在答题纸上。
1.漂粉精的有效成分是
A Ca(OH) B Ca(ClO) C CaCl D CaCO
2 2 2 3
2.美国科学家将两种元素铅和氪的原子核对撞,获得了一种质子数为118、中子数为175
的超重元素,该元素原子核内的中子数与核外电子数之差是
A 57 B 47 C 61 D 293
3.下列物质不属于“城市空气质量日报”报道的是
A 二氧化硫 B 氮氧化物 C 二氧化碳 D 悬浮颗粒
4.下列分子的电子式书写正确的是
A 氨 B 四氯化碳
C 氮 D 二氧化碳
5.下列科学家中,为我国化学工业作出重大贡献的是
A 邓稼先 B 李四光 C 华罗庚 D 侯德榜
二、选择题(本题共36分),每小题3分,只有一个正确选项,答案涂写在答题纸上。
6.下列物质属于分子晶体的化合物是
A 石英 B 硫磺 C 干冰 D 食盐
7.铜片和锌片用导线连接后插入稀硫酸中,锌片是
A 阴极 B 正极 C 阳极 D 负极
第28届国际地质大会提供的资料显示,海底有大量的天然气水合物,可满足人类
1000年的能源需要。天然气水合物是一种晶体,晶体中平均每46个水分子构建成8个笼,每个笼可容纳五个CH 分子或1个游离H O分子。根据上述信息,完成第8、
4 2
9题:
8.下列关于天然气水合物中两种分子极性的描述正确的是
A 两种都是极性分子
B 两种都是非极性分子
C CH 是极性分子,H O是非极性分子
4 2
D H O是极性分子,CH 是非极性分子
2 4
9.若晶体中每8个笼只有6个容纳了CH 分子,另外2个笼被游离H O分子填充,则天
4 2
然气水合物的平均组成可表示为
ACH ·14H O B CH ·8H O C CH ·(23/3)H O D CH ·6H O
4 2 4 2 4 2 4 2
10.标准状况下H S和O 混合气体100mL,经点燃后反应至完全,所得气体经干燥
2 2
后,恢复到原来状况时体积为10mL,该10mL气体可能是
A H S、SO B O C H S D SO
2 2 2 2 3
11.碱金属与卤素所形成的化合物大都具有的性质是
① 高沸点 ② 能溶于水 ② 水溶液能导电 ④ 低熔点 ⑤ 熔融状态不导电
A ①②③ B ③④⑤ C ①④⑤ D ②③⑤
12.下列离子在溶液中因发生氧化还原反应而不能大量共存的是
A H O+、NO -、Fe2+、Na+ B Ag+、NO -、Cl-、K+
3 3 3
C K+、Ba2+、OH-、SO 2- D Cu2+、NH +、Br-、OH-
4 4
13.下列反应的离子方程式错误的是
A 向碳酸氢钙溶液中加人过量氢氧化钠
Ca2++2HCO -+2OH-===CaCO ↓+2H O+CO 2-
3 3 2 3
B 等体积等物质的量浓度的氢氧化钡溶液与碳酸氢按溶液混合
Ba2++2OH-+NH++HCO -===BaCO ↓+NH ·H O+H O
3 3 3 2 2
C 氢氧化铝与足量盐酸反应 Al(OH) +3H+===Al3++3H O
3 2
D 过量CO 通入氢氧化钠溶液中 CO +2OH-===CO 2-+H O
2 2 3 2
14.氯化铁溶液与氢氧化铁胶体具有的共同性质是
A 分散质颗粒直径都在l~100nm之间 B 能透过半透膜
C 加热蒸干、灼烧后都有氧化铁生成 D 呈红褐色
15.下列实验中用错试剂的是
A 用稀盐酸清洗做焰色反应的镍铬丝
B 用酒精萃取碘水中的碘
C 用稀硝酸洗去残留在试管壁上的铜
D 用碱石灰吸收氨气中的水蒸气
16.设N 为阿佛加德罗常数,下列说法不正确的是
AA 标准状况下的22.4L辛烷完全燃烧,生成二氧化碳分子数为8N
A
B 18g水中含有的电子数为10N
A
C 46g 二氧化氮和46g四氧化二氮含有的原子数均为3N
A
D 在1L2mol/L的硝酸镁溶液中含有的硝酸根离子数为4N
A
17.2001年9月1日将执行国家食品卫生标准规定,酱油中3一氯丙醇
(ClCH CH CH OH)含量不得超过1ppm。相对分子质量为94.5的氯丙醇(不含主
2 2 2
结构)共有
A 2种 B 3种 C 4种 D 5种
三、选择题(本题共20分),每小题4分,每小题有一个或两个正确选项。只有一个正
确选项的,多选不给分;有两个正确选项的,选对一个给2分,选错一个该小题不给
分,答案涂写在答题纸上。
18.下列各组物质的稀溶液相互反应,无论是前者滴入后者,还是后者滴入前者,反应现
象都相同的是
A NaHSO 和Ba(OH) B AlCl 和NaOH
4 2 3
C NaAlO 和H SO D Ba(HCO ) 和Ba(OH)
2 2 4 3 2 2
19.将0.1mol/L的醋酸钠溶液20mL与0.1mol/L盐酸10rnL混合后,溶液显酸性,则溶
液中有关微粒的浓度关系正确的是
A c (Ac-)>c (Cl-)>c (H+)>c (HAc)
B c (Ac-)>c (Cl-)>c (HAc)>c(H+)
C c (Ac-)=c (Cl+)>c (H+)>c (HAc)
D c (Na+)+c (H+)=c (Ac-)+c (Cl-)+c (OH-)
20.为更好地表示溶液的酸碱性,科学家提出了酸度(AG)的概念,AG= ,
则下列叙述正确的是
A 中性溶液的AG=0
B 酸性溶液的AG<0
C 常温下0.lmol/L氢氧化钠溶液的AG=12
D 常温下0.lmol/L盐酸溶液的AG=12
21.已知短周期元素的离子。 A2+、 B+、 C3-、 D-都具有相同的电子层结构,则下列叙
a b c d
述正确的是
A 原子半径 A>B>D>C B 原子序数 d>c>b>a
C 离子半径 C>D>B>A D 单质的还原性 A>B>D>C
22.C H 经多步裂化,最后完全转化为C H 、C H 、C H 、C H 、CH 五种气体的混合
8 18 4 8 3 6 2 4 2 6 4
物。该混合物的平均相对分子质量可能是
A 28 B 30 C 38 D 40第Ⅱ卷(共84分)
四、(本题共24分)
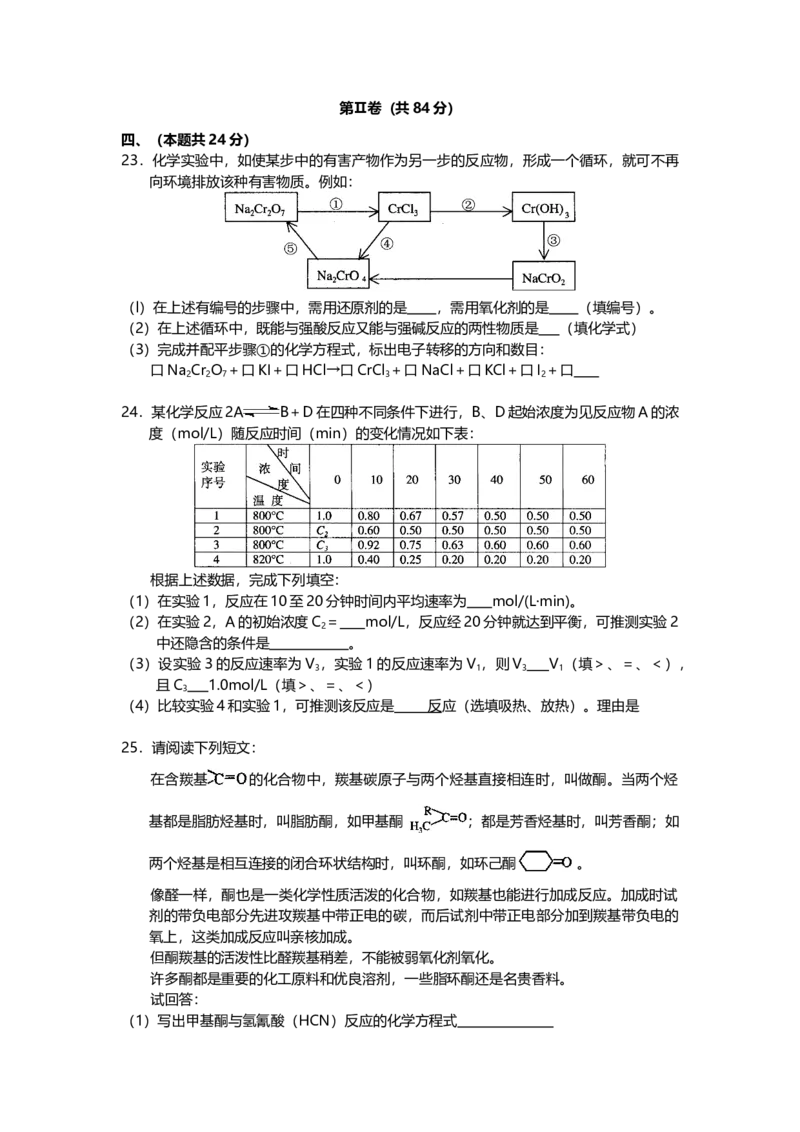
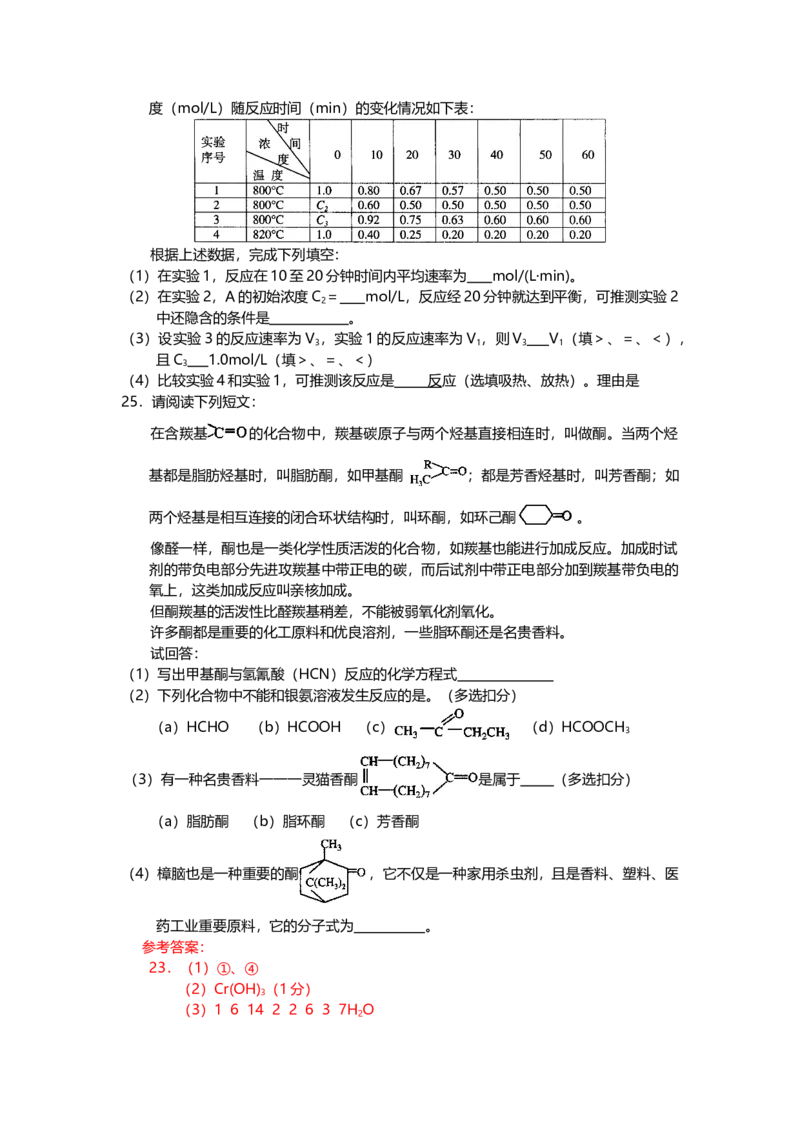
23.化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再
向环境排放该种有害物质。例如:
(l)在上述有编号的步骤中,需用还原剂的是 ,需用氧化剂的是 (填编号)。
(2)在上述循环中,既能与强酸反应又能与强碱反应的两性物质是 (填化学式)
(3)完成并配平步骤①的化学方程式,标出电子转移的方向和数目:
口Na Cr O +口KI+口HCl→口CrCl +口NaCl+口KCl+口I +口
2 2 7 3 2
24.某化学反应2A B+D在四种不同条件下进行,B、D起始浓度为见反应物A的浓
度(mol/L)随反应时间(min)的变化情况如下表:
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内平均速率为 mol/(L·min)。
(2)在实验2,A的初始浓度C = mol/L,反应经20分钟就达到平衡,可推测实验2
2
中还隐含的条件是 。
(3)设实验3的反应速率为V ,实验1的反应速率为V ,则V V (填>、=、<),
3 1 3 1
且C 1.0mol/L(填>、=、<)
3
(4)比较实验4和实验1,可推测该反应是 反应(选填吸热、放热)。理由是
25.请阅读下列短文:
在含羰基 的化合物中,羰基碳原子与两个烃基直接相连时,叫做酮。当两个烃
基都是脂肪烃基时,叫脂肪酮,如甲基酮 ;都是芳香烃基时,叫芳香酮;如
两个烃基是相互连接的闭合环状结构时,叫环酮,如环己酮 。
像醛一样,酮也是一类化学性质活泼的化合物,如羰基也能进行加成反应。加成时试
剂的带负电部分先进攻羰基中带正电的碳,而后试剂中带正电部分加到羰基带负电的
氧上,这类加成反应叫亲核加成。
但酮羰基的活泼性比醛羰基稍差,不能被弱氧化剂氧化。
许多酮都是重要的化工原料和优良溶剂,一些脂环酮还是名贵香料。
试回答:
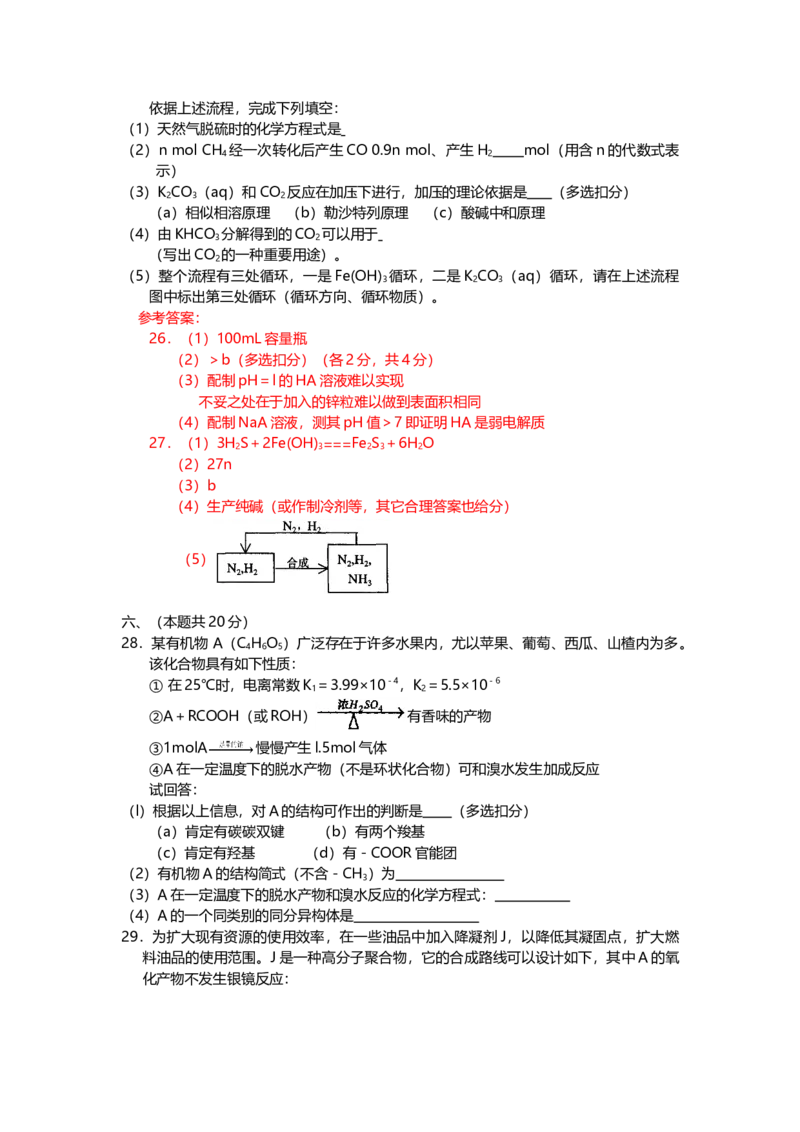
(1)写出甲基酮与氢氰酸(HCN)反应的化学方程式(2)下列化合物中不能和银氨溶液发生反应的是。(多选扣分)
(a)HCHO (b)HCOOH (c) (d)HCOOCH
3
(3)有一种名贵香料一一一灵猫香酮 是属于 (多选扣分)
(a)脂肪酮 (b)脂环酮 (c)芳香酮
(4)樟脑也是一种重要的酮 ,它不仅是一种家用杀虫剂,且是香料、塑料、医
药工业重要原料,它的分子式为 。
五、(本题共24分)
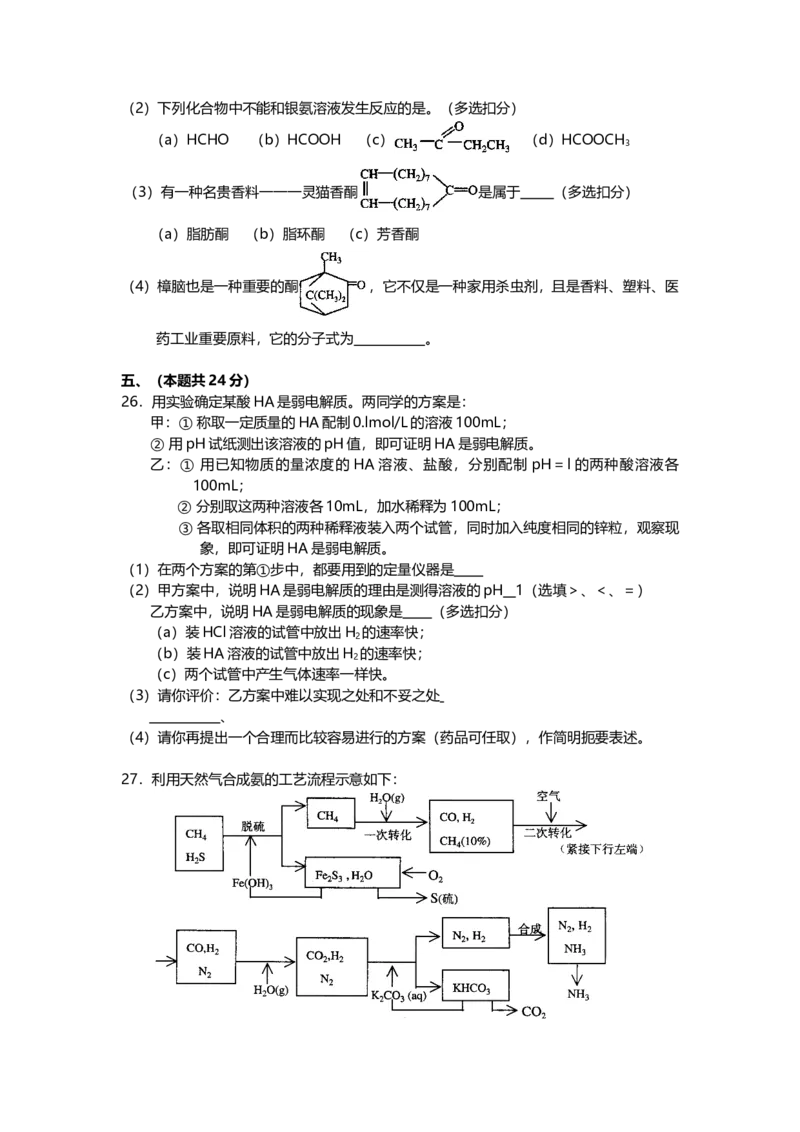
26.用实验确定某酸HA是弱电解质。两同学的方案是:
甲:① 称取一定质量的HA配制0.lmol/L的溶液100mL;
② 用pH试纸测出该溶液的pH值,即可证明HA是弱电解质。
乙:① 用已知物质的量浓度的 HA溶液、盐酸,分别配制 pH=l的两种酸溶液各
100mL;
② 分别取这两种溶液各10mL,加水稀释为100mL;
③ 各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现
象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的pH 1(选填>、<、=)
乙方案中,说明HA是弱电解质的现象是 (多选扣分)
(a)装HCl溶液的试管中放出H 的速率快;
2
(b)装HA溶液的试管中放出H 的速率快;
2
(c)两个试管中产生气体速率一样快。
(3)请你评价:乙方案中难以实现之处和不妥之处
、
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表述。
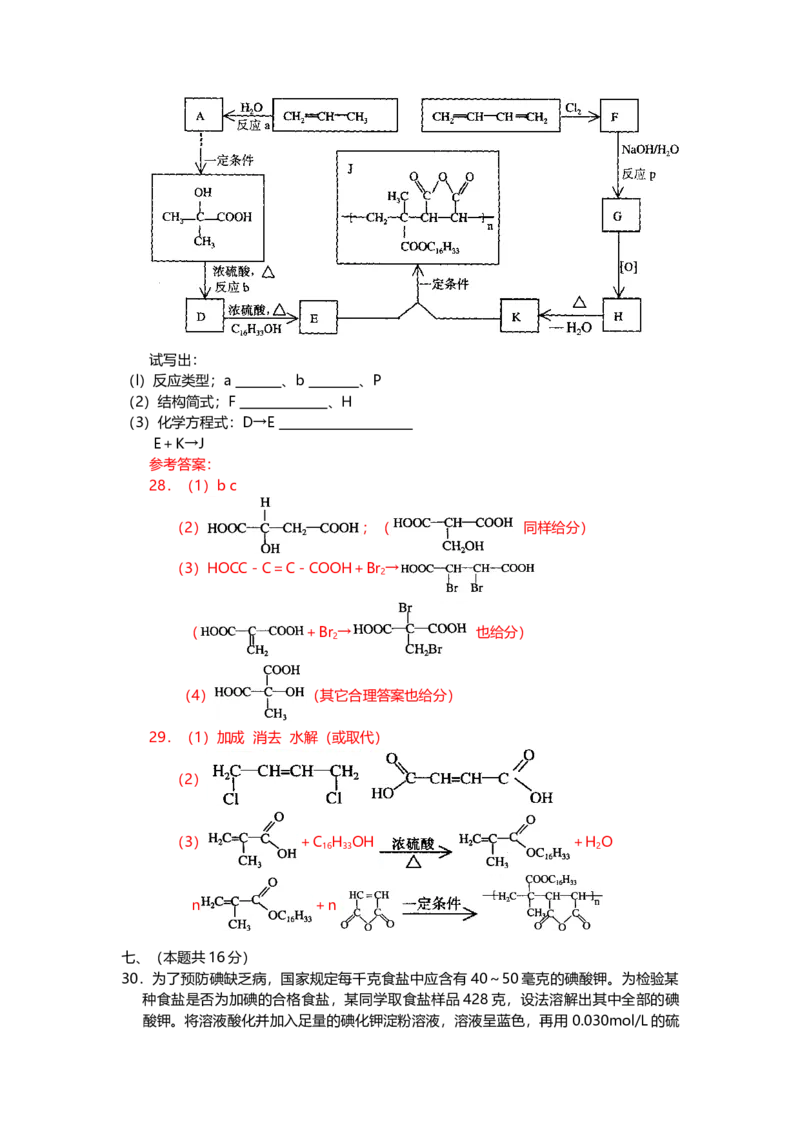
27.利用天然气合成氨的工艺流程示意如下:依据上述流程,完成下列填空:
(1)天然气脱硫时的化学方程式是
(2)n mol CH 经一次转化后产生CO 0.9n mol、产生H mol(用含n的代数式表
4 2
示)
(3)K CO (aq)和 CO 反应在加压下进行,加压的理论依据是 (多选扣分)
2 3 2
(a)相似相溶原理 (b)勒沙特列原理 (c)酸碱中和原理
(4)由KHCO 分解得到的CO 可以用于
3 2
(写出CO 的一种重要用途)。
2
(5)整个流程有三处循环,一是Fe(OH) 循环,二是K CO (aq)循环,请在上述流程
3 2 3
图中标出第三处循环(循环方向、循环物质)。
六、(本题共20分)
28.某有机物 A(C H O )广泛存在于许多水果内,尤以苹果、葡萄、西瓜、山楂内为多。
4 6 5
该化合物具有如下性质:
① 在25℃时,电离常数K =3.99×10-4,K =5.5×10-6
1 2
②A+RCOOH(或ROH) 有香味的产物
③1molA 慢慢产生l.5mol气体
④A在一定温度下的脱水产物(不是环状化合物)可和溴水发生加成反应
试回答:
(l)根据以上信息,对A的结构可作出的判断是 (多选扣分)
(a)肯定有碳碳双键 (b)有两个羧基
(c)肯定有羟基 (d)有-COOR官能团
(2)有机物A的结构简式(不含-CH )为
3
(3)A在一定温度下的脱水产物和溴水反应的化学方程式:
(4)A的一个同类别的同分异构体是
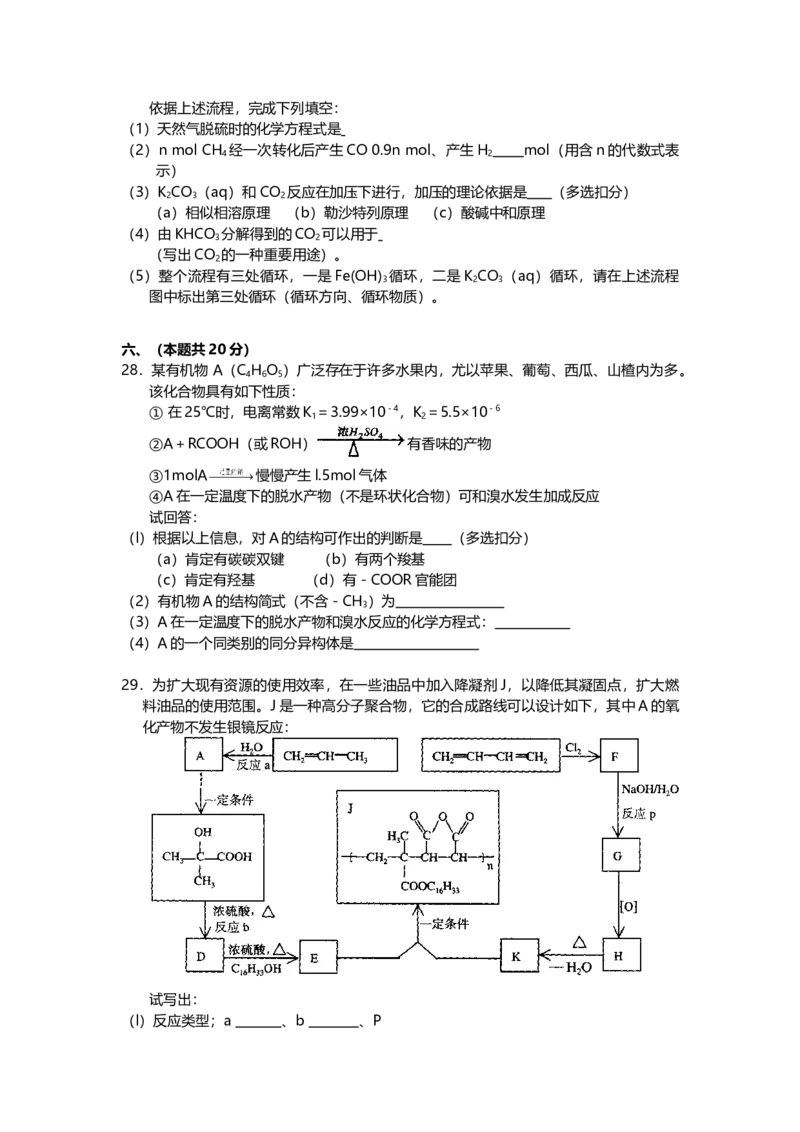
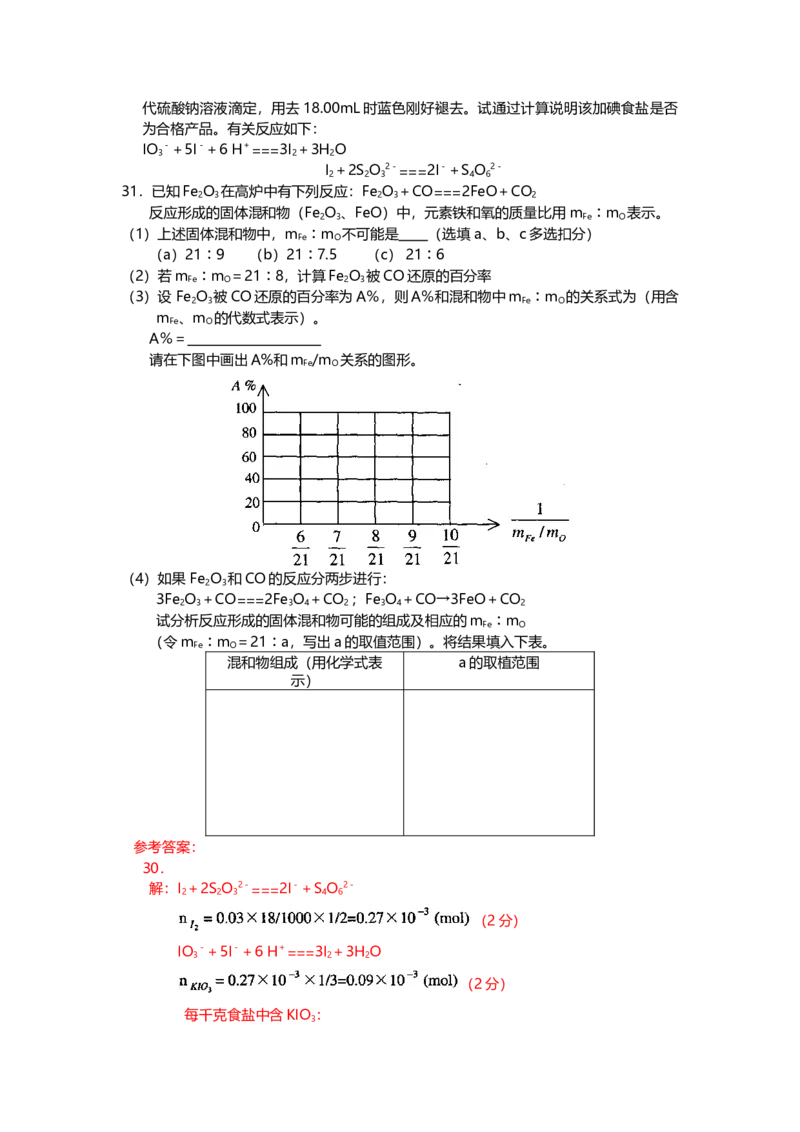
29.为扩大现有资源的使用效率,在一些油品中加入降凝剂J,以降低其凝固点,扩大燃
料油品的使用范围。J是一种高分子聚合物,它的合成路线可以设计如下,其中A的氧
化产物不发生银镜反应:
试写出:
(l)反应类型;a 、b 、P(2)结构简式;F 、H
(3)化学方程式:D→E
E+K→J
七、(本题共16分)
30.为了预防碘缺乏病,国家规定每千克食盐中应含有40~50毫克的碘酸钾。为检验某
种食盐是否为加碘的合格食盐,某同学取食盐样品428克,设法溶解出其中全部的碘
酸钾。将溶液酸化并加入足量的碘化钾淀粉溶液,溶液呈蓝色,再用 0.030mol/L的硫
代硫酸钠溶液滴定,用去18.00mL时蓝色刚好褪去。试通过计算说明该加碘食盐是否
为合格产品。有关反应如下:
IO -+5I-+6 H+===3I +3H O
3 2 2
I +2S O 2-===2I-+S O 2-
2 2 3 4 6
31.已知Fe O 在高炉中有下列反应:Fe O +CO===2FeO+CO
2 3 2 3 2
反应形成的固体混和物(Fe O 、FeO)中,元素铁和氧的质量比用 m ︰m 表示。
2 3 Fe O
(1)上述固体混和物中,m ︰m 不可能是 (选填 a、b、c多选扣分)
Fe O
(a)21︰9 (b)21︰7.5 (c) 21︰6
(2)若m ︰m =21︰8,计算Fe O 被CO还原的百分率
Fe O 2 3
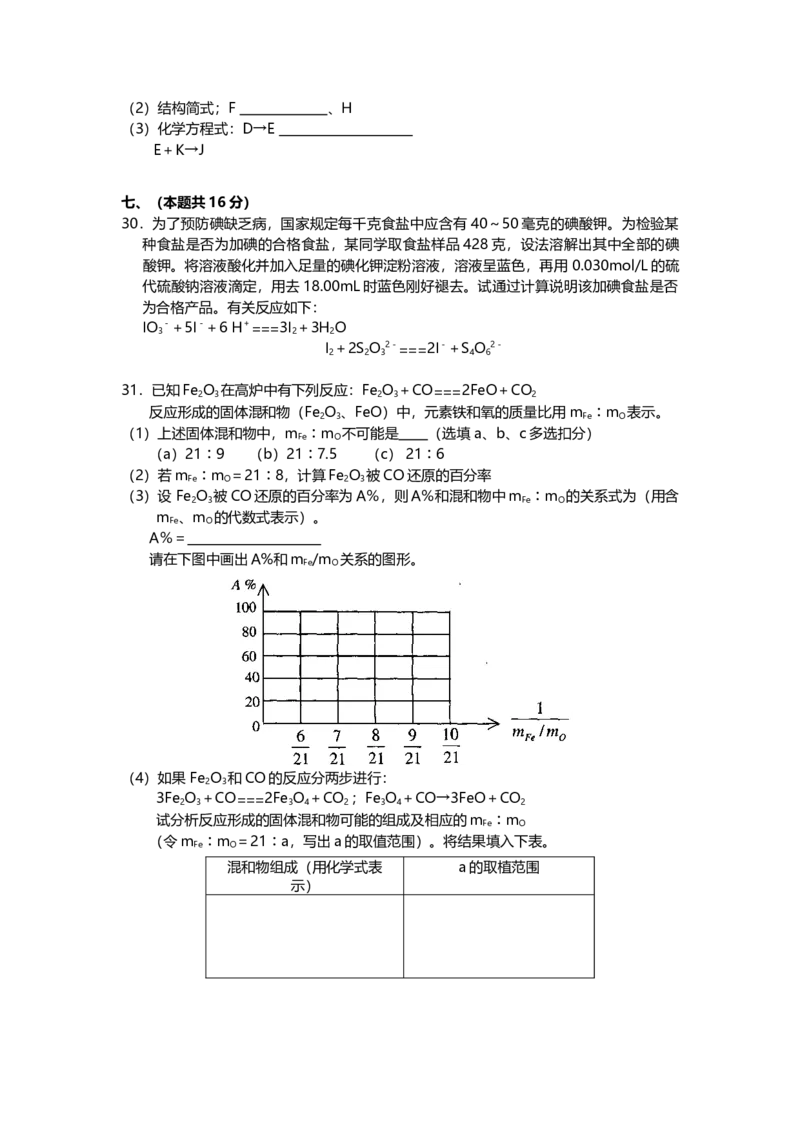
(3)设 Fe O 被CO还原的百分率为A%,则A%和混和物中m ︰m 的关系式为(用含
2 3 Fe O
m 、m 的代数式表示)。
Fe O
A%=
请在下图中画出A%和m /m 关系的图形。
Fe O
(4)如果 Fe O 和CO的反应分两步进行:
2 3
3Fe O +CO===2Fe O +CO ;Fe O +CO→3FeO+CO
2 3 3 4 2 3 4 2
试分析反应形成的固体混和物可能的组成及相应的m ︰m
Fe O
(令m ︰m =21︰a,写出a的取值范围)。将结果填入下表。
Fe O
混和物组成(用化学式表 a的取植范围
示)2001 年全国普通高等学校招生统一考试
上海化学试卷
考生注意:
1.本试卷满分l50分,考试时问120分钟·
2.本考试设试卷和答题纸两部分,试卷包括试题与答题要求;所有答题必须涂(选择
题)或写(非选择题)在答题纸上;做在试卷上一律不得分。
3.答题前,考生务必在答题纸上用钢笔或圆珠笔清楚填写姓名、准考证号,并将核对
后的条形码贴在指定位置上。
4.答题纸与试卷在试题编号上是一一对应的,答题时应特别注意,不能错位。
第Ⅰ卷(共75分)
相对原子质量:H—l C—12 N—14 O-16 Mg-24
S—32 K—39 Fe—56 I—127 Cl—35.5
一、选择题(本题共10分),每小题2分,只有一个正确选项,答案涂写在答题纸上。
1.漂粉精的有效成分是
A Ca(OH) B Ca(ClO) C CaCl D CaCO
2 2 2 3
2.美国科学家将两种元素铅和氪的原子核对撞,获得了一种质子数为118、中子数为175
的超重元素,该元素原子核内的中子数与核外电子数之差是
A 57 B 47 C 61 D 293
3.下列物质不属于“城市空气质量日报”报道的是
A 二氧化硫 B 氮氧化物 C 二氧化碳 D 悬浮颗粒
4.下列分子的电子式书写正确的是
A 氨 B 四氯化碳
C 氮 D 二氧化碳
5.下列科学家中,为我国化学工业作出重大贡献的是
A 邓稼先 B 李四光 C 华罗庚 D 侯德榜
参考答案:
1.B 2.A 3.C 4.C 5.D
二、选择题(本题共36分),每小题3分,只有一个正确选项,答案涂写在答题纸上。
6.下列物质属于分子晶体的化合物是
A 石英 B 硫磺 C 干冰 D 食盐
7.铜片和锌片用导线连接后插入稀硫酸中,锌片是
A 阴极 B 正极 C 阳极 D 负极
第28届国际地质大会提供的资料显示,海底有大量的天然气水合物,可满足人类
1000年的能源需要。天然气水合物是一种晶体,晶体中平均每46个水分子构建成8
个笼,每个笼可容纳五个CH 分子或1个游离H O分子。根据上述信息,完成第8、
4 2
9题:
8.下列关于天然气水合物中两种分子极性的描述正确的是
A 两种都是极性分子B 两种都是非极性分子
C CH 是极性分子,H O是非极性分子
4 2
D H O是极性分子,CH 是非极性分子
2 4
9.若晶体中每8个笼只有6个容纳了CH 分子,另外2个笼被游离H O分子填充,则天
4 2
然气水合物的平均组成可表示为
ACH ·14H O B CH ·8H O C CH ·(23/3)H O D CH ·6H O
4 2 4 2 4 2 4 2
10.标准状况下H S和O 混合气体100mL,经点燃后反应至完全,所得气体经干燥
2 2
后,恢复到原来状况时体积为10mL,该10mL气体可能是
A H S、SO B O C H S D SO
2 2 2 2 3
11.碱金属与卤素所形成的化合物大都具有的性质是
① 高沸点 ② 能溶于水 ② 水溶液能导电 ④ 低熔点 ⑤ 熔融状态不导电
A ①②③ B ③④⑤ C ①④⑤ D ②③⑤
12.下列离子在溶液中因发生氧化还原反应而不能大量共存的是
A H O+、NO -、Fe2+、Na+ B Ag+、NO -、Cl-、K+
3 3 3
C K+、Ba2+、OH-、SO 2- D Cu2+、NH +、Br-、OH-
4 4
13.下列反应的离子方程式错误的是
A 向碳酸氢钙溶液中加人过量氢氧化钠
Ca2++2HCO -+2OH-===CaCO ↓+2H O+CO 2-
3 3 2 3
B 等体积等物质的量浓度的氢氧化钡溶液与碳酸氢按溶液混合
Ba2++2OH-+NH++HCO -===BaCO ↓+NH ·H O+H O
3 3 3 2 2
C 氢氧化铝与足量盐酸反应 Al(OH) +3H+===Al3++3H O
3 2
D 过量CO 通入氢氧化钠溶液中 CO +2OH-===CO 2-+H O
2 2 3 2
14.氯化铁溶液与氢氧化铁胶体具有的共同性质是
A 分散质颗粒直径都在l~100nm之间 B 能透过半透膜
C 加热蒸干、灼烧后都有氧化铁生成 D 呈红褐色
15.下列实验中用错试剂的是
A 用稀盐酸清洗做焰色反应的镍铬丝
B 用酒精萃取碘水中的碘
C 用稀硝酸洗去残留在试管壁上的铜
D 用碱石灰吸收氨气中的水蒸气
16.设N 为阿佛加德罗常数,下列说法不正确的是
A
A 标准状况下的22.4L辛烷完全燃烧,生成二氧化碳分子数为8N
A
B 18g水中含有的电子数为10N
A
C 46g 二氧化氮和46g四氧化二氮含有的原子数均为3N
A
D 在1L2mol/L的硝酸镁溶液中含有的硝酸根离子数为4N
A
17.2001年9月1日将执行国家食品卫生标准规定,酱油中3一氯丙醇
(ClCH CH CH OH)含量不得超过1ppm。相对分子质量为94.5的氯丙醇(不含主
2 2 2
结构)共有
A 2种 B 3种 C 4种 D 5种
参考答案:
6.C 7.D 8.D 9.B 10.C 11.A 12.A
13.D 14.C 15.B 16.A 17.B
三、选择题(本题共20分),每小题4分,每小题有一个或两个正确选项。只有一个正确选项的,多选不给分;有两个正确选项的,选对一个给2分,选错一个该小题不给
分,答案涂写在答题纸上。
18.下列各组物质的稀溶液相互反应,无论是前者滴入后者,还是后者滴入前者,反应现
象都相同的是
A NaHSO 和Ba(OH) B AlCl 和NaOH
4 2 3
C NaAlO 和H SO D Ba(HCO ) 和Ba(OH)
2 2 4 3 2 2
19.将0.1mol/L的醋酸钠溶液20mL与0.1mol/L盐酸10rnL混合后,溶液显酸性,则溶
液中有关微粒的浓度关系正确的是
A c (Ac-)>c (Cl-)>c (H+)>c (HAc)
B c (Ac-)>c (Cl-)>c (HAc)>c(H+)
C c (Ac-)=c (Cl+)>c (H+)>c (HAc)
D c (Na+)+c (H+)=c (Ac-)+c (Cl-)+c (OH-)
20.为更好地表示溶液的酸碱性,科学家提出了酸度(AG)的概念,AG= ,
则下列叙述正确的是
A 中性溶液的AG=0
B 酸性溶液的AG<0
C 常温下0.lmol/L氢氧化钠溶液的AG=12
D 常温下0.lmol/L盐酸溶液的AG=12
21.已知短周期元素的离子。 A2+、 B+、 C3-、 D-都具有相同的电子层结构,则下列叙
a b c d
述正确的是
A 原子半径 A>B>D>C B 原子序数 d>c>b>a
C 离子半径 C>D>B>A D 单质的还原性 A>B>D>C
22.C H 经多步裂化,最后完全转化为C H 、C H 、C H 、C H 、CH 五种气体的混合
8 18 4 8 3 6 2 4 2 6 4
物。该混合物的平均相对分子质量可能是
A 28 B 30 C 38 D 40
参考答案:
18.A、D 19.B、D 20.A、D 21.C 22.B、C
第Ⅱ卷(共84分)
四、(本题共24分)
23.化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再
向环境排放该种有害物质。例如:
(l)在上述有编号的步骤中,需用还原剂的是 ,需用氧化剂的是 (填编号)。
(2)在上述循环中,既能与强酸反应又能与强碱反应的两性物质是 (填化学式)
(3)完成并配平步骤①的化学方程式,标出电子转移的方向和数目:
口Na Cr O +口KI+口HCl→口CrCl +口NaCl+口KCl+口I +口
2 2 7 3 2
24.某化学反应2A B+D在四种不同条件下进行,B、D起始浓度为见反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内平均速率为 mol/(L·min)。
(2)在实验2,A的初始浓度C = mol/L,反应经20分钟就达到平衡,可推测实验2
2
中还隐含的条件是 。
(3)设实验3的反应速率为V ,实验1的反应速率为V ,则V V (填>、=、<),
3 1 3 1
且C 1.0mol/L(填>、=、<)
3
(4)比较实验4和实验1,可推测该反应是 反应(选填吸热、放热)。理由是
25.请阅读下列短文:
在含羰基 的化合物中,羰基碳原子与两个烃基直接相连时,叫做酮。当两个烃
基都是脂肪烃基时,叫脂肪酮,如甲基酮 ;都是芳香烃基时,叫芳香酮;如
两个烃基是相互连接的闭合环状结构时,叫环酮,如环己酮 。
像醛一样,酮也是一类化学性质活泼的化合物,如羰基也能进行加成反应。加成时试
剂的带负电部分先进攻羰基中带正电的碳,而后试剂中带正电部分加到羰基带负电的
氧上,这类加成反应叫亲核加成。
但酮羰基的活泼性比醛羰基稍差,不能被弱氧化剂氧化。
许多酮都是重要的化工原料和优良溶剂,一些脂环酮还是名贵香料。
试回答:
(1)写出甲基酮与氢氰酸(HCN)反应的化学方程式
(2)下列化合物中不能和银氨溶液发生反应的是。(多选扣分)
(a)HCHO (b)HCOOH (c) (d)HCOOCH
3
(3)有一种名贵香料一一一灵猫香酮 是属于 (多选扣分)
(a)脂肪酮 (b)脂环酮 (c)芳香酮
(4)樟脑也是一种重要的酮 ,它不仅是一种家用杀虫剂,且是香料、塑料、医
药工业重要原料,它的分子式为 。
参考答案:
23.(1)①、④
(2)Cr(OH) (1分)
3
(3)1 6 14 2 2 6 3 7H O
224.(1)0.013
(2)1.0 催化剂
(3)> >
(4)由吸热温度升高时,平衡向右移动
25.
(l) +HCN→
(2)c
(3)b
(4)C H O
10 16
五、(本题共24分)
26.用实验确定某酸HA是弱电解质。两同学的方案是:
甲:① 称取一定质量的HA配制0.lmol/L的溶液100mL;
② 用pH试纸测出该溶液的pH值,即可证明HA是弱电解质。
乙:① 用已知物质的量浓度的 HA溶液、盐酸,分别配制 pH=l的两种酸溶液各
100mL;
② 分别取这两种溶液各10mL,加水稀释为100mL;
③ 各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现
象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的pH 1(选填>、<、=)
乙方案中,说明HA是弱电解质的现象是 (多选扣分)
(a)装HCl溶液的试管中放出H 的速率快;
2
(b)装HA溶液的试管中放出H 的速率快;
2
(c)两个试管中产生气体速率一样快。
(3)请你评价:乙方案中难以实现之处和不妥之处
、
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表述。
27.利用天然气合成氨的工艺流程示意如下:依据上述流程,完成下列填空:
(1)天然气脱硫时的化学方程式是
(2)n mol CH 经一次转化后产生CO 0.9n mol、产生H mol(用含n的代数式表
4 2
示)
(3)K CO (aq)和 CO 反应在加压下进行,加压的理论依据是 (多选扣分)
2 3 2
(a)相似相溶原理 (b)勒沙特列原理 (c)酸碱中和原理
(4)由KHCO 分解得到的CO 可以用于
3 2
(写出CO 的一种重要用途)。
2
(5)整个流程有三处循环,一是Fe(OH) 循环,二是K CO (aq)循环,请在上述流程
3 2 3
图中标出第三处循环(循环方向、循环物质)。
参考答案:
26.(1)100mL容量瓶
(2)>b(多选扣分)(各2分,共4分)
(3)配制pH=l的HA溶液难以实现
不妥之处在于加入的锌粒难以做到表面积相同
(4)配制NaA溶液,测其pH值>7即证明HA是弱电解质
27.(1)3H S+2Fe(OH) ===Fe S +6H O
2 3 2 3 2
(2)27n
(3)b
(4)生产纯碱(或作制冷剂等,其它合理答案也给分)
(5)
六、(本题共20分)
28.某有机物 A(C H O )广泛存在于许多水果内,尤以苹果、葡萄、西瓜、山楂内为多。
4 6 5
该化合物具有如下性质:
① 在25℃时,电离常数K =3.99×10-4,K =5.5×10-6
1 2
②A+RCOOH(或ROH) 有香味的产物
③1molA 慢慢产生l.5mol气体
④A在一定温度下的脱水产物(不是环状化合物)可和溴水发生加成反应
试回答:
(l)根据以上信息,对A的结构可作出的判断是 (多选扣分)
(a)肯定有碳碳双键 (b)有两个羧基
(c)肯定有羟基 (d)有-COOR官能团
(2)有机物A的结构简式(不含-CH )为
3
(3)A在一定温度下的脱水产物和溴水反应的化学方程式:
(4)A的一个同类别的同分异构体是
29.为扩大现有资源的使用效率,在一些油品中加入降凝剂J,以降低其凝固点,扩大燃
料油品的使用范围。J是一种高分子聚合物,它的合成路线可以设计如下,其中A的氧
化产物不发生银镜反应:试写出:
(l)反应类型;a 、b 、P
(2)结构简式;F 、H
(3)化学方程式:D→E
E+K→J
参考答案:
28.(1)b c
(2) ;( 同样给分)
(3)HOCC-C=C-COOH+Br →
2
( +Br → 也给分)
2
(4) (其它合理答案也给分)
29.(1)加成 消去 水解(或取代)
(2)
(3) +C H OH +H O
16 33 2
n +n
七、(本题共16分)
30.为了预防碘缺乏病,国家规定每千克食盐中应含有40~50毫克的碘酸钾。为检验某
种食盐是否为加碘的合格食盐,某同学取食盐样品428克,设法溶解出其中全部的碘
酸钾。将溶液酸化并加入足量的碘化钾淀粉溶液,溶液呈蓝色,再用 0.030mol/L的硫代硫酸钠溶液滴定,用去18.00mL时蓝色刚好褪去。试通过计算说明该加碘食盐是否
为合格产品。有关反应如下:
IO -+5I-+6 H+===3I +3H O
3 2 2
I +2S O 2-===2I-+S O 2-
2 2 3 4 6
31.已知Fe O 在高炉中有下列反应:Fe O +CO===2FeO+CO
2 3 2 3 2
反应形成的固体混和物(Fe O 、FeO)中,元素铁和氧的质量比用 m ︰m 表示。
2 3 Fe O
(1)上述固体混和物中,m ︰m 不可能是 (选填 a、b、c多选扣分)
Fe O
(a)21︰9 (b)21︰7.5 (c) 21︰6
(2)若m ︰m =21︰8,计算Fe O 被CO还原的百分率
Fe O 2 3
(3)设 Fe O 被CO还原的百分率为A%,则A%和混和物中m ︰m 的关系式为(用含
2 3 Fe O
m 、m 的代数式表示)。
Fe O
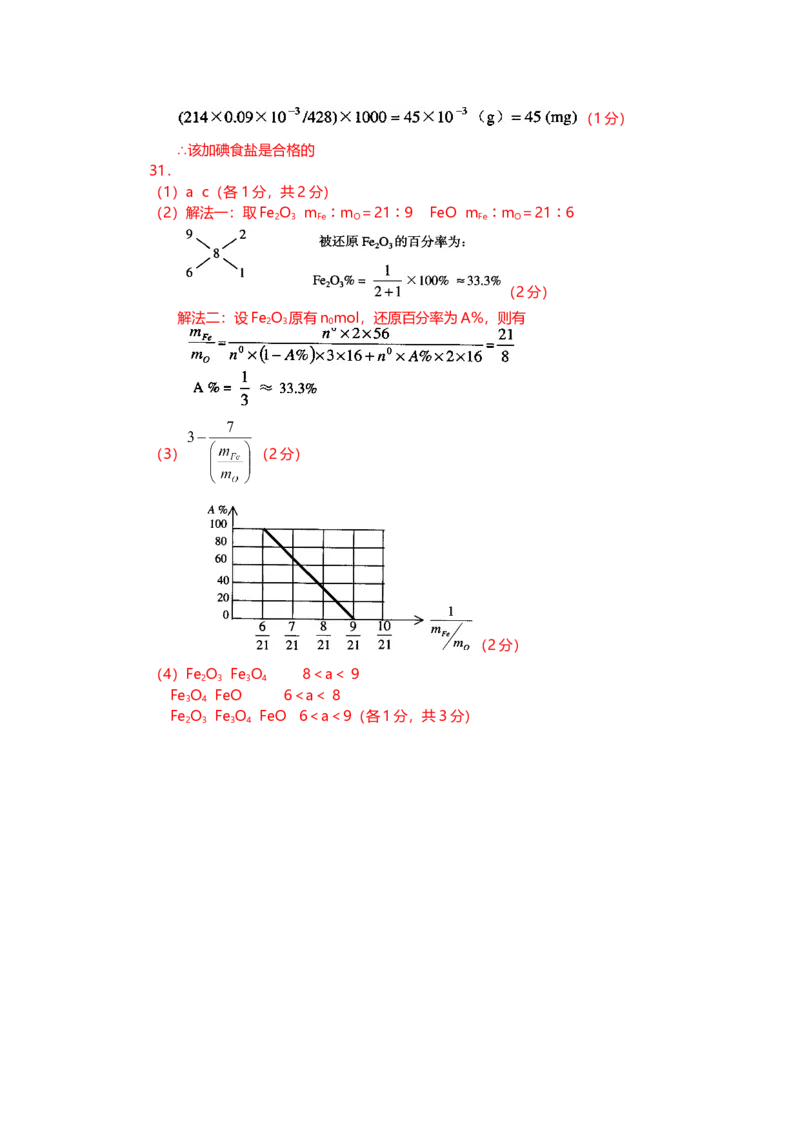
A%=
请在下图中画出A%和m /m 关系的图形。
Fe O
(4)如果 Fe O 和CO的反应分两步进行:
2 3
3Fe O +CO===2Fe O +CO ;Fe O +CO→3FeO+CO
2 3 3 4 2 3 4 2
试分析反应形成的固体混和物可能的组成及相应的m ︰m
Fe O
(令m ︰m =21︰a,写出a的取值范围)。将结果填入下表。
Fe O
混和物组成(用化学式表 a的取植范围
示)
参考答案:
30.
解:I +2S O 2-===2I-+S O 2-
2 2 3 4 6
(2分)
IO -+5I-+6 H+===3I +3H O
3 2 2
(2分)
每千克食盐中含KIO :
3(1分)
∴该加碘食盐是合格的
31.
(1)a c(各 1分,共2分)
(2)解法一:取Fe O m ︰m =21︰9 FeO m ︰m =21︰6
2 3 Fe O Fe O
(2分)
解法二:设Fe O 原有n mol,还原百分率为A%,则有
2 3 0
(3) (2分)
(2分)
(4)Fe O Fe O 8<a< 9
2 3 3 4
Fe O FeO 6<a< 8
3 4
Fe O Fe O FeO 6<a<9(各1分,共3分)
2 3 3 4