文档内容
2011 年福建省高考化学试卷
参考答案与试题解析
一、选择题
1.(3分)(2011•福建)下列关于化学与生产、生活的认识不正确的是( )
A.CO 、CH 、N 等均是造成温室效应的气体
2 4 2
B.使用清洁能源是防止酸雨发生的重要措施之一
C.节能减排符合低碳经济的要求
D.合理开发利用可燃冰(固态甲烷水合物)有助于缓解能源紧缺
【考点】常见的生活环境的污染及治理.
菁优网版权所有
【专题】化学应用.
【分析】A、根据产生温室效应的气体成分判断;
B、根据酸雨的形成原因判断;
C、根据低碳经济的要求判断;
D、根据可燃冰对煤、石油的影响判断;
【解答】解:A CO 、CH 是造成温室效应的主要气体,而N 是空气中的主要气体,不
2 4 2
是温室气体,故A错误;
B、产生酸雨的主要原因是SO 气体,使用清洁能源可以有效防止酸雨发生,故B正确;
2
C、节能减排可以减少CO 的排放,符合低碳经济的要求,故C正确;
2
D、合理开发可燃冰可以减少煤、石油等紧缺能源的使用,故D正确.
故选A.
【点评】本题考查了常见的生活环境的污染和治理,涉及STSE内容,主要与环保、能源
和低碳经济有关,属于常识题.
2.(3分)(2011•福建)依据元素周期表及元素周期律,下列推断正确的是( )
A.H BO 的酸性比H CO 的强
3 3 2 3
B.Mg(OH) 的碱性比Be(OH) 的强
2 2
C.HCl、HBr、HI的热稳定性依次增强
D.若M+和R2﹣的核外电子层结构相同,则原子序数:R>M
【考点】元素周期律和元素周期表的综合应用.
菁优网版权所有
【专题】元素周期律与元素周期表专题.
【分析】A、同周期从左向右元素的非金属性增强,则最高价氧化物对应的水化物的酸性
增强;
B、同主族从上到下元素的金属性增强,则最高价氧化物对应的水化物的碱性增强;
C、同主族从上到下元素的非金属性减弱,则气态氢化物的稳定性减弱;
D、M+和R2﹣的核外电子层结构相同,则阳离子在下一周期的前方,阴离子在上一周期的
后方.
【解答】解:A、非金属性B<C,则最高价氧化物对应的水化物的酸性为H BO <
3 3
H CO ,故A错误;
2 3
B、金属性Mg>Be,则最高价氧化物对应的水化物的碱性为Mg(OH) >Be(OH) ,
2 2
故B正确;
C、非金属性Cl>Br>I,则HCl、HBr、HI的热稳定性依次减弱,故C错误;D、M+和R2﹣的核外电子层结构相同,则M+在下一周期的前方,R2﹣在上一周期的后方,
原子序数M>R,故D错误;
故选B.
【点评】本题考查元素周期律,学生熟悉元素的金属性与非金属性的递变规律是解答本题
的关键,难度不大.
3.(3分)(2011•福建)下列关于有机化合物的认识错误的是( )
A.油脂在空气中完全燃烧转化为水和二氧化碳
B.蔗糖、麦芽糖的分子式都是C H O ,二者互为同分异构体
12 22 11
C.在水溶液里,乙酸分子中的﹣CH 可以电离出H+
3
D.在浓硫酸存在下,苯与浓硝酸共热生成硝基苯的反应属于取代反应
【考点】油脂的性质、组成与结构;苯的性质;乙酸的化学性质;蔗糖、麦芽糖简介.
菁优网版权所有
【专题】有机物的化学性质及推断.
【分析】A、烃的含氧衍生物完全燃烧生成水和二氧化碳;
B、同分异构体指分子式相同结构不同的化合物;
C、在水溶液里,乙酸分子中羧基中的H发生电离;
D、分子中原子或基团被其他原子或原子团所取代的反应称取代反应.
【解答】解:A、油脂含有C、H、O三种元素,完全燃烧生成水和二氧化碳,故A正确;
B、蔗糖、麦芽糖分子式相同,蔗糖是由1分子葡萄糖和1分子果糖脱水形成的,而麦芽糖
是由2分子葡萄糖脱水形成的,结构不同,互为同分异构体,故B正确;
C、在水溶液里,乙酸电离方程式为CH COOH CH COO﹣+H+,发生电离是羧基中的H原
3 3
子,故C错误;
⇌
D、硝基取代苯环上的H原子生成硝基苯,是取代反应,故D正确.
故选C.
【点评】本题涉及同分异构体、有机反应类型、羧酸与油脂的性质等知识,难度不大,重
在考查学生对基础知识的掌握.
4.(3分)(2011•福建)下表各选项中,不能利用置换反应通过Y得到W的一组化合物
是( )
① ② ③ ④
Y CO Fe O C H OH FeCl
2 2 3 2 5 3
W MgO Al O C H ONa CuCl
2 3 2 5 2
A.① B.② C.③ D.④
【考点】常见金属元素的单质及其化合物的综合应用;乙醇的化学性质.
菁优网版权所有
【专题】几种重要的金属及其化合物.
【分析】①二氧化碳和镁反应生成碳和氧化镁,属于置换反应;
②氧化铁和金属铝反应生成氧化铝和铁,发生铝热反应,属于置换反应;
③乙醇和金属钠反应生成乙醇钠和氢气,符合置换反应概念;
④氯化铁和铜反应生成氯化铜和氯化亚铁,不属于置换反应;
【解答】解:①二氧化碳和镁反应生成碳和氧化镁,2Mg+CO =C+2MgO,属于置换反应;
2
故①不符合;
②氧化铁和金属铝反应生成氧化铝和铁,发生铝热反应,2Al+Fe O =2Fe+Al O ,属于置换
2 3 2 3
反应;故②不符合;
③乙醇和金属钠反应生成乙醇钠和氢气,2Na+2CH CH OH=2CH CH ONa+H ↑符合置换反
3 2 3 2 2
应概念;故③不符合;④氯化铁和铜反应生成氯化铜和氯化亚铁,不属于置换反应;
综上所述:④符合;
故答案为:D.
【点评】本题考查了置换反应的分析判断,物质性质的掌握是解题关键,题目较简单.
5.(3分)(2011•福建)常温下0.1mol•L﹣1醋酸溶液的pH=a,下列能使溶液pH=(a+1)
的措施是( )
A.将溶液稀释到原体积的10倍
B.加入适量的醋酸钠固体
C.加入等体积0.2 mol•L﹣1盐酸
D.提高溶液的温度
【考点】弱电解质在水溶液中的电离平衡.
菁优网版权所有
【专题】电离平衡与溶液的pH专题.
【分析】醋酸电离生成醋酸根离子和氢离子,要使溶液的pH增大,则溶液中氢离子浓度
减小,据此分析解答.
【解答】解:A、醋酸是弱电解质,加水稀释能促进水的电离,将溶液稀释到原体积的10
倍,氢离子浓度大于原来的 ,所以pH<(a+1),故A错误;
B、加入适量的醋酸钠固体,醋酸钠中含有醋酸根离子能抑制醋酸的电离,使溶液中氢离
子浓度减小,所以能使溶液pH=(a+1),故B正确;
C、加入等体积的0.2 mol•L﹣1盐酸,氢离子浓度增大,溶液的pH值减小,故C错误;
D、提高温度促进醋酸的电离,使溶液中氢离子浓度增大,溶液的pH值减小,故D错误;
故选B.
【点评】本题考查了弱电解质的电离,根据“加水稀释、提高温度都能促进醋酸的电离,加
入含有相同离子的盐能抑制醋酸的电离”来分析解答,难度不大.
6.(3分)(2011•福建)研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源.
该电池以金属锂和钢板为电极材料,以LiOH为电解质,使用时加入水即可放电.关于该
电池的下列说法不正确的是( )
A.水既是氧化剂又是溶剂
B.放电时正极上有氢气生成
C.放电时OH﹣向正极移动
D.总反应为:2Li+2H O=2LiOH+H ↑
2 2
【考点】原电池和电解池的工作原理.
菁优网版权所有
【专题】压轴题;电化学专题.
【分析】锂水电池中,自发的氧化还原反应是金属锂和水之间反应生成氢氧化锂和氢气的
过程,根据原电池的工作原理以及电极反应特点和规律来回答.
【解答】解:A、金属锂和水之间反应生成氢氧化锂和氢气,该反应中,水是氧化剂,在
电池中还可以担当溶剂,故A正确;
B、放电时正极上是水中的氢离子得电子,所以会有氢气生成,故B正确;
C、原电池中,阴离子移向原电池的负极,即放电时OH﹣向负极移动,故C错误;
D、锂水电池中,自发的氧化还原反应是金属锂和水之间反应生成氢氧化锂和氢气,即总
反应为:2Li+2H O=2LiOH+H ↑,故D正确.
2 2
故选C.【点评】本题考查电化学的热点﹣锂离子电池,根据总反应式判断出正负极和阴阳极的反
应,从化合价变化的角度分析.
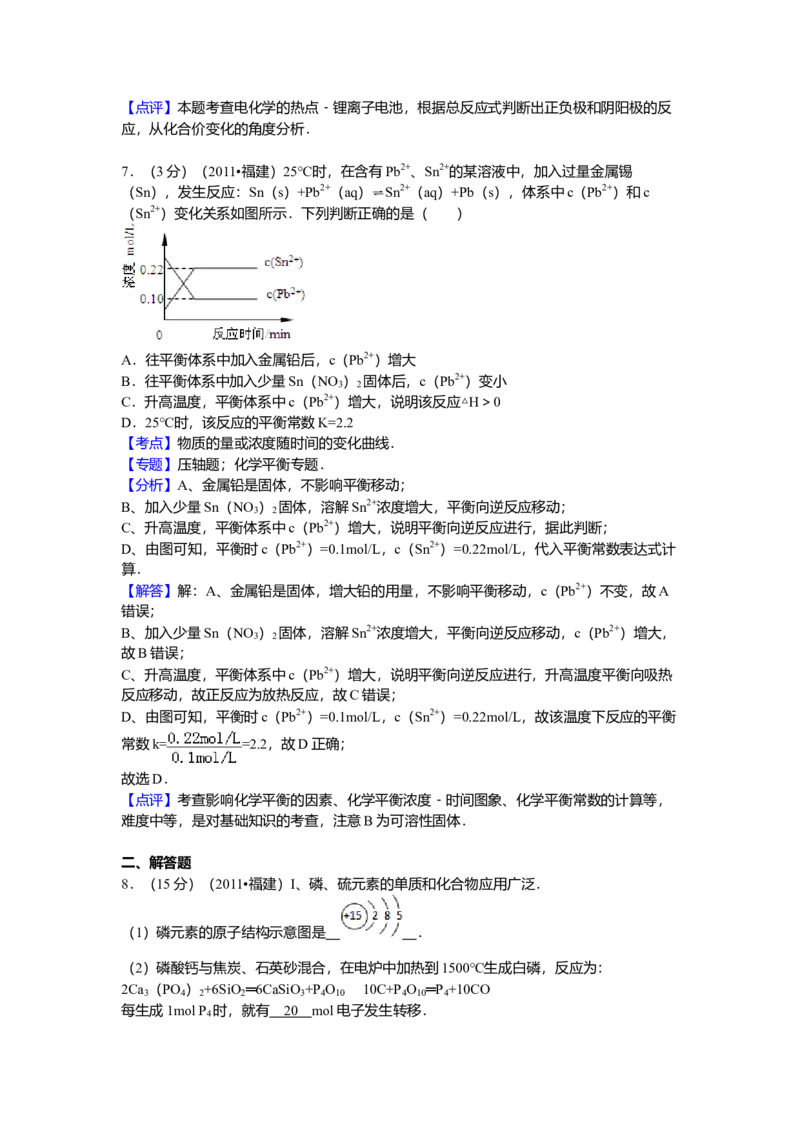
7.(3分)(2011•福建)25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡
(Sn),发生反应:Sn(s)+Pb2+(aq)⇌Sn2+(aq)+Pb(s),体系中c(Pb2+)和c
(Sn2+)变化关系如图所示.下列判断正确的是( )
A.往平衡体系中加入金属铅后,c(Pb2+)增大
B.往平衡体系中加入少量Sn(NO ) 固体后,c(Pb2+)变小
3 2
C.升高温度,平衡体系中c(Pb2+)增大,说明该反应△H>0
D.25℃时,该反应的平衡常数K=2.2
【考点】物质的量或浓度随时间的变化曲线.
菁优网版权所有
【专题】压轴题;化学平衡专题.
【分析】A、金属铅是固体,不影响平衡移动;
B、加入少量Sn(NO ) 固体,溶解Sn2+浓度增大,平衡向逆反应移动;
3 2
C、升高温度,平衡体系中c(Pb2+)增大,说明平衡向逆反应进行,据此判断;
D、由图可知,平衡时c(Pb2+)=0.1mol/L,c(Sn2+)=0.22mol/L,代入平衡常数表达式计
算.
【解答】解:A、金属铅是固体,增大铅的用量,不影响平衡移动,c(Pb2+)不变,故A
错误;
B、加入少量Sn(NO ) 固体,溶解Sn2+浓度增大,平衡向逆反应移动,c(Pb2+)增大,
3 2
故B错误;
C、升高温度,平衡体系中c(Pb2+)增大,说明平衡向逆反应进行,升高温度平衡向吸热
反应移动,故正反应为放热反应,故C错误;
D、由图可知,平衡时c(Pb2+)=0.1mol/L,c(Sn2+)=0.22mol/L,故该温度下反应的平衡
常数k= =2.2,故D正确;
故选D.
【点评】考查影响化学平衡的因素、化学平衡浓度﹣时间图象、化学平衡常数的计算等,
难度中等,是对基础知识的考查,注意B为可溶性固体.
二、解答题
8.(15分)(2011•福建)Ⅰ、磷、硫元素的单质和化合物应用广泛.
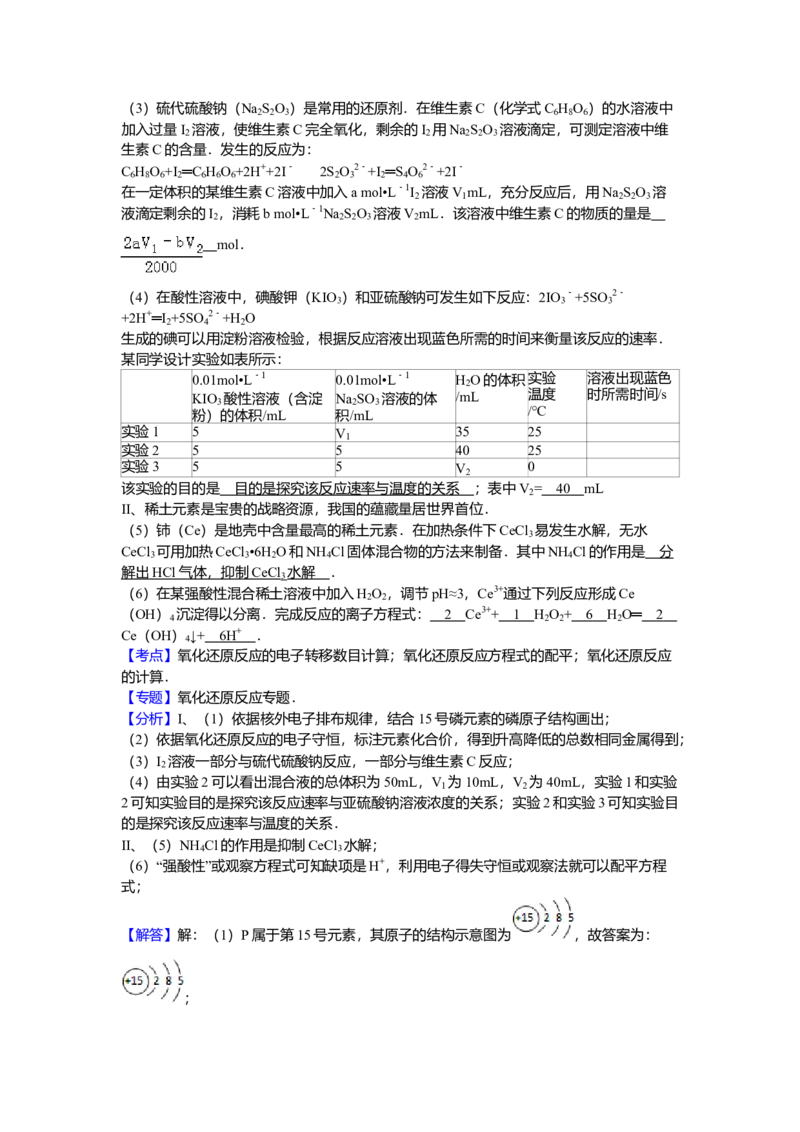
(1)磷元素的原子结构示意图是 .
(2)磷酸钙与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,反应为:
2Ca (PO ) +6SiO ═6CaSiO +P O 10C+P O ═P +10CO
3 4 2 2 3 4 10 4 10 4
每生成1mol P 时,就有 20 mol电子发生转移.
4(3)硫代硫酸钠(Na S O )是常用的还原剂.在维生素C(化学式C H O )的水溶液中
2 2 3 6 8 6
加入过量I 溶液,使维生素C完全氧化,剩余的I 用Na S O 溶液滴定,可测定溶液中维
2 2 2 2 3
生素C的含量.发生的反应为:
C H O +I ═C H O +2H++2I﹣ 2S O 2﹣+I ═S O 2﹣+2I﹣
6 8 6 2 6 6 6 2 3 2 4 6
在一定体积的某维生素C溶液中加入a mol•L﹣1I 溶液V mL,充分反应后,用Na S O 溶
2 1 2 2 3
液滴定剩余的I ,消耗b mol•L﹣1Na S O 溶液V mL.该溶液中维生素C的物质的量是
2 2 2 3 2
mol.
(4)在酸性溶液中,碘酸钾(KIO )和亚硫酸钠可发生如下反应:2IO ﹣+5SO 2﹣
3 3 3
+2H+═I +5SO 2﹣+H O
2 4 2
生成的碘可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率.
某同学设计实验如表所示:
0.01mol•L﹣1 0.01mol•L﹣1 H O的体积实验 溶液出现蓝色
2
KIO 酸性溶液(含淀 Na SO 溶液的体 /mL 温度 时所需时间/s
3 2 3
/℃
粉)的体积/mL 积/mL
实验1 5 V 35 25
1
实验2 5 5 40 25
实验3 5 5 V 0
2
该实验的目的是 目的是探究该反应速率与温度的关系 ;表中V = 40 mL
2
Ⅱ、稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位.
(5)铈(Ce)是地壳中含量最高的稀土元素.在加热条件下CeCl 易发生水解,无水
3
CeCl 可用加热CeCl •6H O和NH Cl固体混合物的方法来制备.其中NH Cl的作用是 分
3 3 2 4 4
解出 HCl 气体,抑制 CeCl 水解 .
3
(6)在某强酸性混合稀土溶液中加入H O ,调节pH≈3,Ce3+通过下列反应形成Ce
2 2
(OH) 沉淀得以分离.完成反应的离子方程式: 2 Ce3++ 1 H O + 6 H O═ 2
4 2 2 2
Ce(OH) ↓+ 6H + .
4
【考点】氧化还原反应的电子转移数目计算;氧化还原反应方程式的配平;氧化还原反应
的计算.
菁优网版权所有
【专题】氧化还原反应专题.
【分析】Ⅰ、(1)依据核外电子排布规律,结合15号磷元素的磷原子结构画出;
(2)依据氧化还原反应的电子守恒,标注元素化合价,得到升高降低的总数相同金属得到;
(3)I 溶液一部分与硫代硫酸钠反应,一部分与维生素C反应;
2
(4)由实验2可以看出混合液的总体积为50mL,V 为10mL,V 为40mL,实验1和实验
1 2
2可知实验目的是探究该反应速率与亚硫酸钠溶液浓度的关系;实验2和实验3可知实验目
的是探究该反应速率与温度的关系.
Ⅱ、(5)NH Cl的作用是抑制CeCl 水解;
4 3
(6)“强酸性”或观察方程式可知缺项是H+,利用电子得失守恒或观察法就可以配平方程
式;
【解答】解:(1)P属于第15号元素,其原子的结构示意图为 ,故答案为:
;(2)每生成1 mol P 时,P由+5价变成0价,电子转移为5×4 mol=20 mol或C化合价由0
4
价变成为+2价,电子转移为2×10 mol=20 mol,故答案为:20;
(3)I 溶液一部分与硫代硫酸钠反应,一部分与维生素C反应,n(Na S O )=
2 2 2 3
mol;
与其反应的碘单质为 mol,与维生素C反应的碘单质为 mol,
即维生素C的物质的量是 = ;
故答案为: ;
(4)由实验2可以看出混合液的总体积为50mL,V 为10mL,V 为40mL,实验1和实验
1 2
2可知实验目的是探究该反应速率与亚硫酸钠溶液浓度的关系;实验2和实验3可知实验目
的是探究该反应速率与温度的关系,
故答案为:目的是探究该反应速率与亚硫酸钠浓度,反应温度的关系;40;
(5)题目中给出:“加热条件下CeCl 易发生水解”,可知NH Cl的作用是肯定是抑制水解
3 4
的,CeCl 水解会生成HCl,可知NH Cl的作用是分解出HCl气体,抑制CeCl 水解,
3 4 3
故答案为:分解出HCl气体,抑制CeCl 的水解;
3
(6)根据题意:“强酸性”或观察方程式可知缺项是H+,利用电子得失守恒或观察法就可
以配平方程式为2Ce3++H O +6H O═2Ce(OH) ↓+6H+,
2 2 2 4
故答案为:2;1;6;2;6H+.
【点评】本题考查化学方程式的配平与计算,滴定实验过程的分析计算应用,盐类水解的
分析判断,难度较大,在氧化还原反应中得失电子总数相等是解题关键,注意审题.
9.(14分)(2011•福建)四氯化钛(TiCl )是制取航天航空工业材料﹣﹣钛合金的重要
4
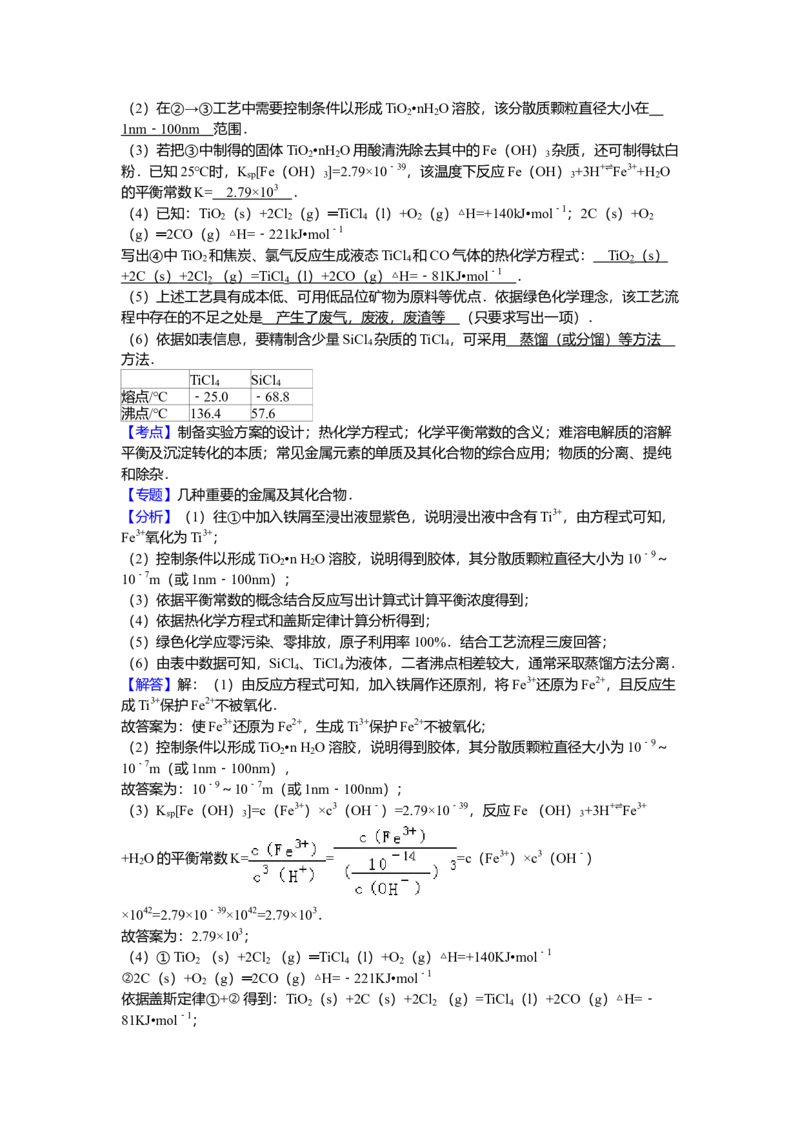
原料,由钛铁矿(主要成分是FeTiO )制备TiCl 等产品的一种工艺流程示意如下:
3 4
回答下列问题:
(1)往①中加入铁屑至浸出液显紫色,此时溶液仍呈强酸性.该过程中有如下反应发生.
2Fe3++Fe═3Fe2+
2TiO2+(无色)+Fe+4H+═2Ti3+(紫色)+Fe2++2H O
2
Ti3+(紫色)+Fe3++H O═TiO2+(无色)+Fe2++2H+
2
加入铁屑的作用是 使 Fe 3+ 还原为 Fe 2+ ,生成 Ti 3+ 保护 Fe 2+ 不被氧化. .(2)在②→③工艺中需要控制条件以形成TiO •nH O溶胶,该分散质颗粒直径大小在
2 2
1nm﹣100nm 范围.
(3)若把③中制得的固体TiO •nH O用酸清洗除去其中的Fe(OH) 杂质,还可制得钛白
2 2 3
粉.已知25℃时,K [Fe(OH) =2.79×10﹣39,该温度下反应Fe(OH) +3H+ Fe3++H O
sp 3 3 2
的平衡常数K= 2.79×10 3 . ⇌
]
(4)已知:TiO (s)+2Cl (g)═TiCl (l)+O (g)△H=+140kJ•mol﹣1;2C(s)+O
2 2 4 2 2
(g)═2CO(g)△H=﹣221kJ•mol﹣1
写出④中TiO 和焦炭、氯气反应生成液态TiCl 和CO气体的热化学方程式: TiO ( s )
2 4 2
+2C ( s ) +2Cl ( g ) =TiCl ( l ) +2CO ( g )△ H=﹣81KJ•mol ﹣1 .
2 4
(5)上述工艺具有成本低、可用低品位矿物为原料等优点.依据绿色化学理念,该工艺流
程中存在的不足之处是 产生了废气,废液,废渣等 (只要求写出一项).
(6)依据如表信息,要精制含少量SiCl 杂质的TiCl ,可采用 蒸馏(或分馏)等方法
4 4
方法.
TiCl SiCl
4 4
熔点/℃ ﹣25.0 ﹣68.8
沸点/℃ 136.4 57.6
【考点】制备实验方案的设计;热化学方程式;化学平衡常数的含义;难溶电解质的溶解
平衡及沉淀转化的本质;常见金属元素的单质及其化合物的综合应用;物质的分离、提纯
和除杂.
菁优网版权所有
【专题】几种重要的金属及其化合物.
【分析】(1)往①中加入铁屑至浸出液显紫色,说明浸出液中含有Ti3+,由方程式可知,
Fe3+氧化为Ti3+;
(2)控制条件以形成TiO •n H O溶胶,说明得到胶体,其分散质颗粒直径大小为10﹣9~
2 2
10﹣7m(或1nm﹣100nm);
(3)依据平衡常数的概念结合反应写出计算式计算平衡浓度得到;
(4)依据热化学方程式和盖斯定律计算分析得到;
(5)绿色化学应零污染、零排放,原子利用率100%.结合工艺流程三废回答;
(6)由表中数据可知,SiCl 、TiCl 为液体,二者沸点相差较大,通常采取蒸馏方法分离.
4 4
【解答】解:(1)由反应方程式可知,加入铁屑作还原剂,将Fe3+还原为Fe2+,且反应生
成Ti3+保护Fe2+不被氧化.
故答案为:使Fe3+还原为Fe2+,生成Ti3+保护Fe2+不被氧化;
(2)控制条件以形成TiO •n H O溶胶,说明得到胶体,其分散质颗粒直径大小为10﹣9~
2 2
10﹣7m(或1nm﹣100nm),
故答案为:10﹣9~10﹣7m(或1nm﹣100nm);
(3)K [Fe(OH) =c(Fe3+)×c3(OH﹣)=2.79×10﹣39,反应Fe (OH) +3H+ Fe3+
sp 3 3
⇌
]
+H O的平衡常数K= = =c(Fe3+)×c3(OH﹣)
2
×1042=2.79×10﹣39×1042=2.79×103.
故答案为:2.79×103;
(4)①TiO (s)+2Cl (g)═TiCl (l)+O (g)△H=+140KJ•mol﹣1
2 2 4 2
②2C(s)+O
2
(g)═2CO(g)△H=﹣221KJ•mol﹣1
依据盖斯定律①+②得到:TiO
2
(s)+2C(s)+2Cl
2
(g)=TiCl
4
(l)+2CO(g)△H=﹣
81KJ•mol﹣1;故答案为:TiO (s)+2C(s)+2Cl (g)=TiCl (l)+2CO(g)△H=﹣81KJ•mol﹣1
2 2 4
(5)由工艺流程可知,生成中产生废气,废液,废渣等,不符合绿色化学理念,
故答案为:产生了废气,废液,废渣等;
(6)由表中数据可知,SiCl 、TiCl 为液体,二者沸点相差较大,要精制含少量SiCl 杂质
4 4 4
的TiCl ,可采用蒸馏(或分馏)方法,
4
故答案为:蒸馏(或分馏).
【点评】本题考查学生阅读题目获取信息能力、氧化还原反应、绿色化学、胶体、物质分
离提纯,平衡常数计算,溶度积常数的计算应用,盖斯定律的计算应用等,难度不大,注
意基础知识的掌握利用.
10.(16分)(2011•福建)化学兴趣小组对某品牌牙膏中摩擦剂成分及其含量进行以下探
究:
查得资料:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体生
成.
Ⅰ.摩擦剂中氢氧化铝的定性检验
取适量牙膏样品,加水成分搅拌、过滤.
(1)往滤渣中加入过量NaOH溶液,过滤.氢氧化铝与NaOH溶液反应的离子方程式是
Al ( OH ) +OH ﹣ ═AlO ﹣ +2H O .
3 2 2
(2)往(1)所得滤液中先通入过量二氧化碳,再加入过量稀盐酸,观察到的现象是 通
入 CO 气体有白色沉淀生成;加入盐酸有气体产生,沉淀溶解 .
2
Ⅱ.牙膏样品中碳酸钙的定量测定
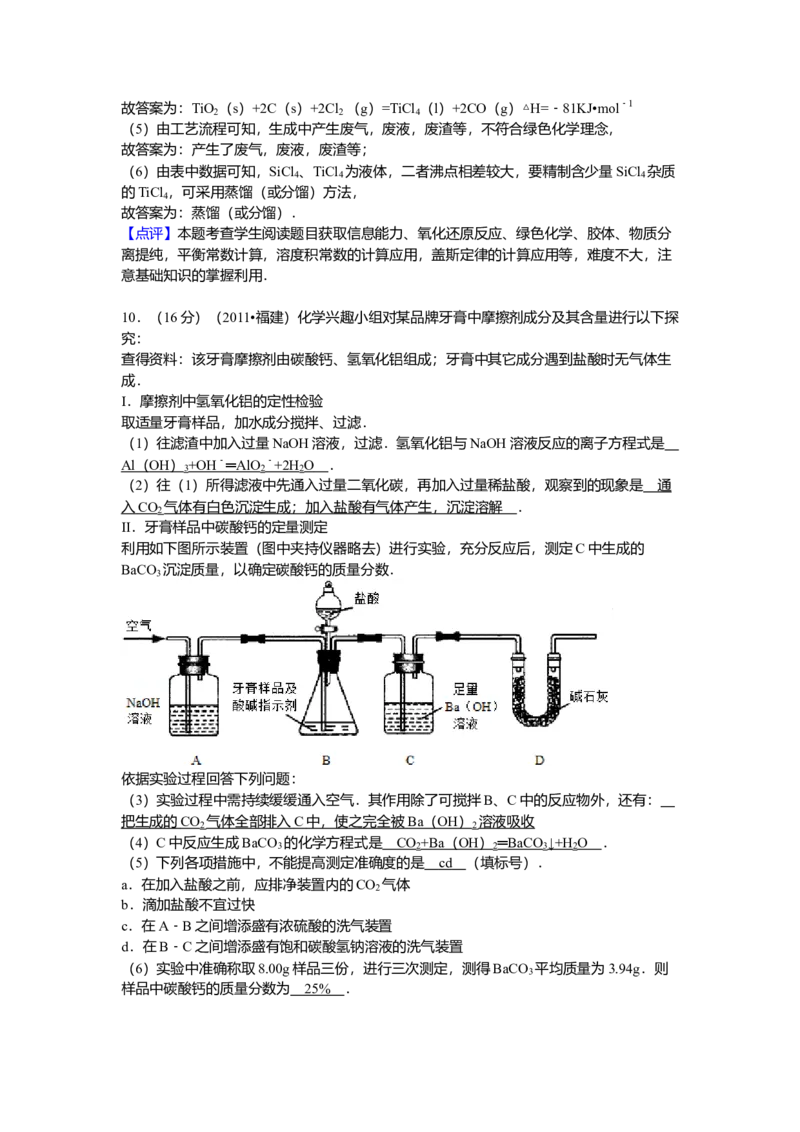
利用如下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的
BaCO 沉淀质量,以确定碳酸钙的质量分数.
3
依据实验过程回答下列问题:
(3)实验过程中需持续缓缓通入空气.其作用除了可搅拌B、C中的反应物外,还有:
把生成的 CO 气体全部排入 C 中,使之完全被 Ba ( OH ) 溶液吸收
2 2
(4)C中反应生成BaCO 的化学方程式是 CO +Ba ( OH ) ═BaCO ↓+H O .
3 2 2 3 2
(5)下列各项措施中,不能提高测定准确度的是 cd (填标号).
a.在加入盐酸之前,应排净装置内的CO 气体
2
b.滴加盐酸不宜过快
c.在A﹣B之间增添盛有浓硫酸的洗气装置
d.在B﹣C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(6)实验中准确称取8.00g样品三份,进行三次测定,测得BaCO 平均质量为3.94g.则
3
样品中碳酸钙的质量分数为 25% .(7)有人认为不必测定C中生成的BaCO 质量,只要测定装置C吸收CO 前后的质量差,
3 2
一样可以确定碳酸钙的质量分数.实验证明按此方法测定的结果明显偏高,原因是 B 中
的水蒸气、氯化氢气体等进入装置 C 中 .
【考点】探究物质的组成或测量物质的含量;镁、铝的重要化合物.
菁优网版权所有
【专题】压轴题;实验探究和数据处理题.
【分析】Ⅰ.(1)氢氧化铝与NaOH溶液反应生成偏铝酸钠与水.
(2)往(1)所得滤液中先通入过量二氧化碳,发生反应AlO ﹣+CO +2H O=Al(OH)
2 2 2
↓+HCO ﹣,再加入过量稀盐酸,Al(OH) +3HCl=AlCl +3H O,HCO ﹣+H+=CO ↑+H O.
3 3 3 3 2 3 2 2
Ⅱ.(3)实验通过C装置生成的碳酸钡的质量测定二氧化碳的质量,进而计算牙膏中碳酸
钙的质量分数.装置中残留部分二氧化碳,不能被完全吸收,导致测定的碳酸钡的质量偏
小.
(4)二氧化碳与氢氧化钡反应生成碳酸钡与水.
(5)a、在加入盐酸之前,应排净装置内的CO 气体,防止影响碳酸钡质量的测定;
2
b、滴加盐酸过快CO ,CO 不能完全被吸收,排出装置C.
2 2
c、在AB之间增添盛有浓硫酸的洗气装置,吸收水分,不影响CO .
2
d、在BC之间增添盛有饱和碳酸氢钠溶液的洗气装置Ba(OH) ,可以吸收CO 中的
2 2
HCl,而不影响CO .
2
(6)BaCO 质量为3.94g n(BaCO )=0.0200mol,则n(CaCO )=0.0200mol,质量为
3 3 3
2.00g.
(7)B中的水蒸气、氯化氢气体等进入装置C中.
【解答】解:Ⅰ.(1)氢氧化铝与NaOH溶液反应生成偏铝酸钠与水,反应离子方程式为
Al(OH) +OH﹣═AlO ﹣+2H O.
3 2 2
故答案为:Al(OH) +OH﹣═AlO ﹣+2H O.
3 2 2
(2)往(1)所得滤液中先通入过量二氧化碳,发生反应AlO ﹣+CO +2H O=Al(OH)
2 2 2
↓+HCO ﹣,再加入过量稀盐酸,Al(OH) +3HCl=AlCl +3H O,HCO ﹣+H+=CO ↑+H O,
3 3 3 3 2 3 2 2
反应现象是通入CO 气体有白色沉淀生成;加入盐酸有气体产生,沉淀溶解.
2
故答案为:通入CO 气体有白色沉淀生成;加入盐酸有气体产生,沉淀溶解.
2
Ⅱ.(3)装置中残留部分二氧化碳,不能被完全吸收,导致测定的碳酸钡的质量偏小,持
续缓缓通入空气的作用为:把生成的CO 气体全部排入C中,使之完全被Ba(OH) 溶液
2 2
吸收.
故答案为:把生成的CO 气体全部排入C中,使之完全被Ba(OH) 溶液吸收.
2 2
(4)二氧化碳与氢氧化钡反应生成碳酸钡与水,反应方程式为CO +Ba(OH)
2
═BaCO ↓+H O.
2 3 2
故答案为:CO +Ba(OH) ═BaCO ↓+H O.
2 2 3 2
(5)a、在加入盐酸之前,应排净装置内的CO 气体,防止影响碳酸钡质量的测定,可以
2
提高测定准确度,故a不符合;
b、滴加盐酸过快CO ,CO 来不及被吸收,就排出装置C,滴加盐酸不宜过快,使二氧化
2 2
碳吸收完全,可以提高测定准确度,故b不符合;
c、在AB之间增添盛有浓硫酸的洗气装置,吸收水分,不影响CO ,不能提高提高测定准
2
确度,故c符合;
d、在BC之间增添盛有饱和碳酸氢钠溶液的洗气装置Ba(OH) ,可以吸收CO 中的
2 2
HCl,影响CO ,不能提高测定准确度,故d符合.
2
故选:cd.(6)BaCO 质量为3.94g,则n(BaCO )= =0.02mol,则n(CaCO )
3 3 3
=0.02mol,质量为0.02mol×100g/mol=2g,所以样品中碳酸钙的质量分数为
×100%=25%.
故答案为:25%.
(7)B中的水蒸气、氯化氢气体等进入装置C中,导致测定二氧化碳的质量偏大,测定的
碳酸钙的质量偏大,碳酸钙的质量分数偏高.
故答案为:B中的水蒸气、氯化氢气体等进入装置C中.
【点评】考查对实验原理与操作步骤的理解及评价、常用化学用语、化学计算、物质组成
的测定等,难度较大,是对所需知识的综合运用,需要学生具有扎实的基础知识与分析问
题、解决问题的能力,理解实验原理是解答的关键.
11.(13分)(2011•福建)氮元素可以形成多种化合物.
回答以下问题:
(1)基态氮原子的价电子排布式是 2s 2 2p 3 .
(2)C、N、O三种元素第一电离能从大到小的顺序是 N > O > C .
(3)肼(N H )分子可视为NH 分子中的一个氢原子被﹣NH (氨基)取代形成的另一种
2 4 3 2
氮的氢化物.
①NH 分子的空间构型是 三角锥型 ;N H 分子中氮原子轨道的杂化类型是 sp 3 .
3 2 4
②肼可用作火箭燃料,燃烧时发生的反应是:
N O (l)+2N H (l)=3N (g)+4H O(g)△H=﹣1038.7kJ•mol﹣1
2 4 2 4 2 2
若该反应中有4mol N﹣H键断裂,则形成的π键有 3 mol.
③肼能与硫酸反应生成N H SO .N H SO 晶体类型与硫酸铵相同,则N H SO 的晶体
2 6 4 2 6 4 2 6 4
内不存在 d (填标号)
a.离子键 b.共价键 c.配位键 d.范德华力
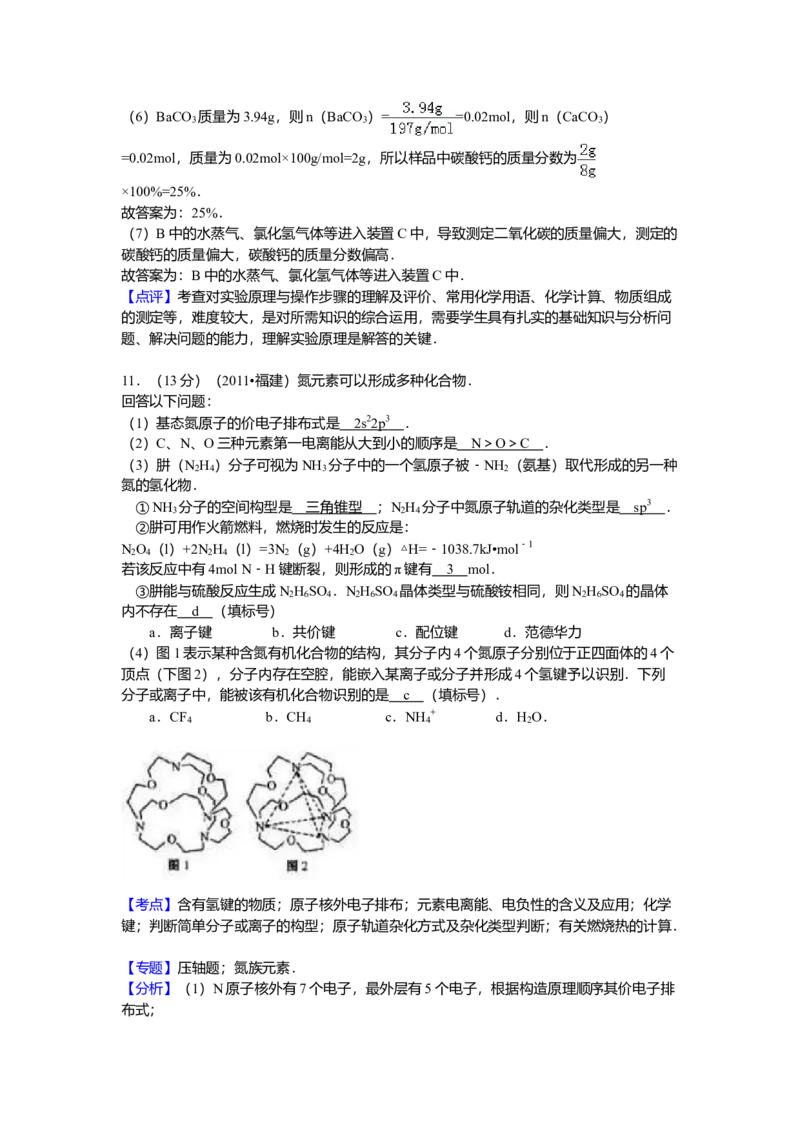
(4)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个
顶点(下图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别.下列
分子或离子中,能被该有机化合物识别的是 c (填标号).
a.CF b.CH c.NH + d.H O.
4 4 4 2
【考点】含有氢键的物质;原子核外电子排布;元素电离能、电负性的含义及应用;化学
键;判断简单分子或离子的构型;原子轨道杂化方式及杂化类型判断;有关燃烧热的计算.
菁优网版权所有
【专题】压轴题;氮族元素.
【分析】(1)N原子核外有7个电子,最外层有5个电子,根据构造原理顺序其价电子排
布式;(2)同一周期元素的第一电离能随着原子序数的增大而呈增大的趋势,但第IIA族和第
VA族元素的第一电离能大于相邻元素;
(3)①根据价层电子对互斥理论确定分子空间构型和原子的杂化方式;
②根据化学方程式计算产生的氮气的物质的量,再根据每个氮分子中含有2个π键计算;
③N
2
H
6
SO
4
晶体类型与硫酸铵相同,含离子键、共价键;
(4)嵌入某微粒分别与4个N原子形成4个氢键.
【解答】解:(1)氮原子的电子排布式1s22s22p3,其价层电子排布式为2s22p3,故答案为:
2s22p3;
(2)C、N、O属于同一周期元素且原子序数依次减小,同一周期元素的第一电离能随着
原子序数的增大而增大,但第ⅤA族的大于第ⅥA族的,所以其第一电离能大小顺序是N
>O>C,故答案为:N>O>C;
(3)①NH 分子中氮原子含有3个共价键和一个孤电子对,所以空间构型是三角锥型;
3
N H 分子中氮原子的加成电子对=3+1=4,含有一个孤电子对,N原子轨道的杂化类型是
2 4
sp3,故答案为:三角锥型;sp3;
②反应中有4mol N﹣H键断裂,即有1molN H 参加反应,根据化学方程式可知产生的氮
2 4
气的物质的量为1.5mol,而每个氮分子中含有2个π键,所以形成3molπ键,故答案为:
3;
③肼与硫酸反应的离子方程式为N H +2H+═N H 2+,N H SO 晶体类型与硫酸铵相同,
2 4 2 6 2 6 4
N H 2+中的化学键是共价键与配位键,N H 2+与SO 2﹣之间是离子键,不存在范德华力,故
2 6 2 6 4
答案为:d;
(4)注意氢键的形成条件及成键元素(N、O、F、H),本题中嵌入某微粒分别与4个N
原子形成4个氢键,由成键元素及数目可知为NH +,故答案为:c.
4
【点评】本题考查考查原子结构与性质,涉及核外电子排布、电离能的大小比较、杂化类
型、配位键等知识,综合考查学生的分析能力和基本概念的综合运用能力,为高考常见题
型和高频考点,注意相关基础知识的学习,题目难度中等.
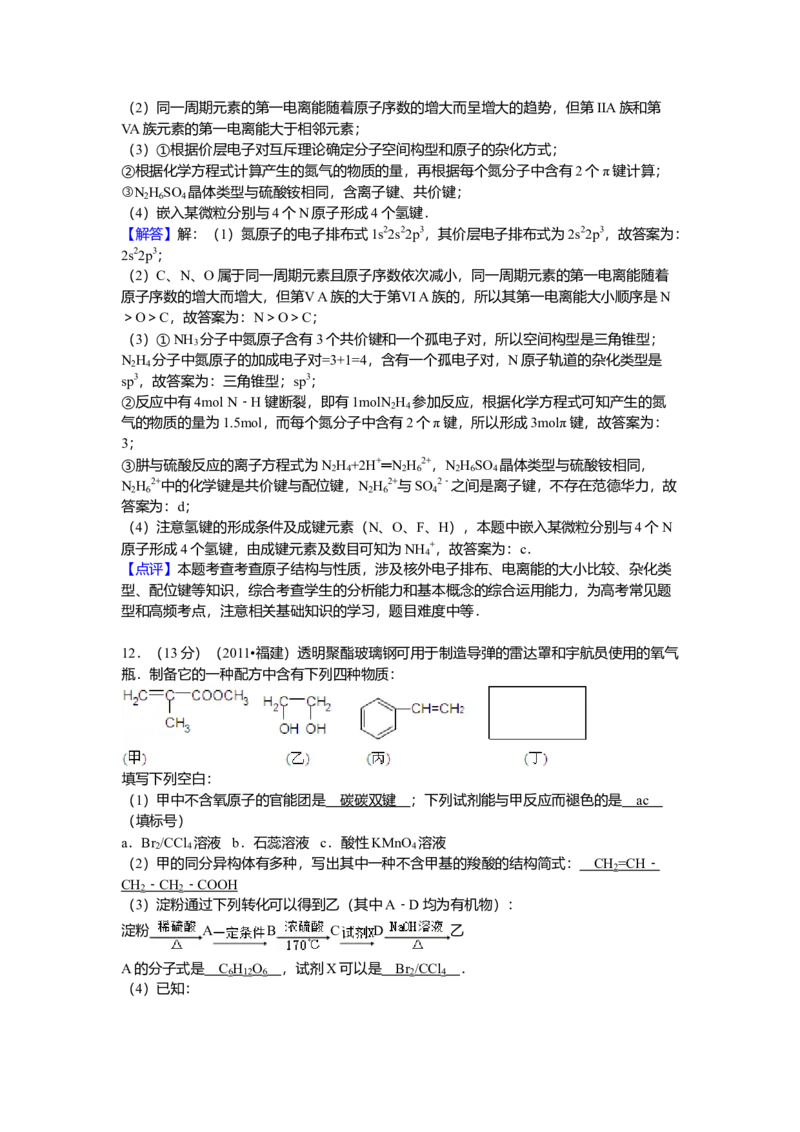
12.(13分)(2011•福建)透明聚酯玻璃钢可用于制造导弹的雷达罩和宇航员使用的氧气
瓶.制备它的一种配方中含有下列四种物质:
填写下列空白:
(1)甲中不含氧原子的官能团是 碳碳双键 ;下列试剂能与甲反应而褪色的是 ac
(填标号)
a.Br /CCl 溶液 b.石蕊溶液 c.酸性KMnO 溶液
2 4 4
(2)甲的同分异构体有多种,写出其中一种不含甲基的羧酸的结构简式: CH =CH﹣
2
CH ﹣CH ﹣COOH
2 2
(3)淀粉通过下列转化可以得到乙(其中A﹣D均为有机物):
淀粉 A B C D 乙
A的分子式是 C H O ,试剂X可以是 Br /CCl .
6 12 6 2 4
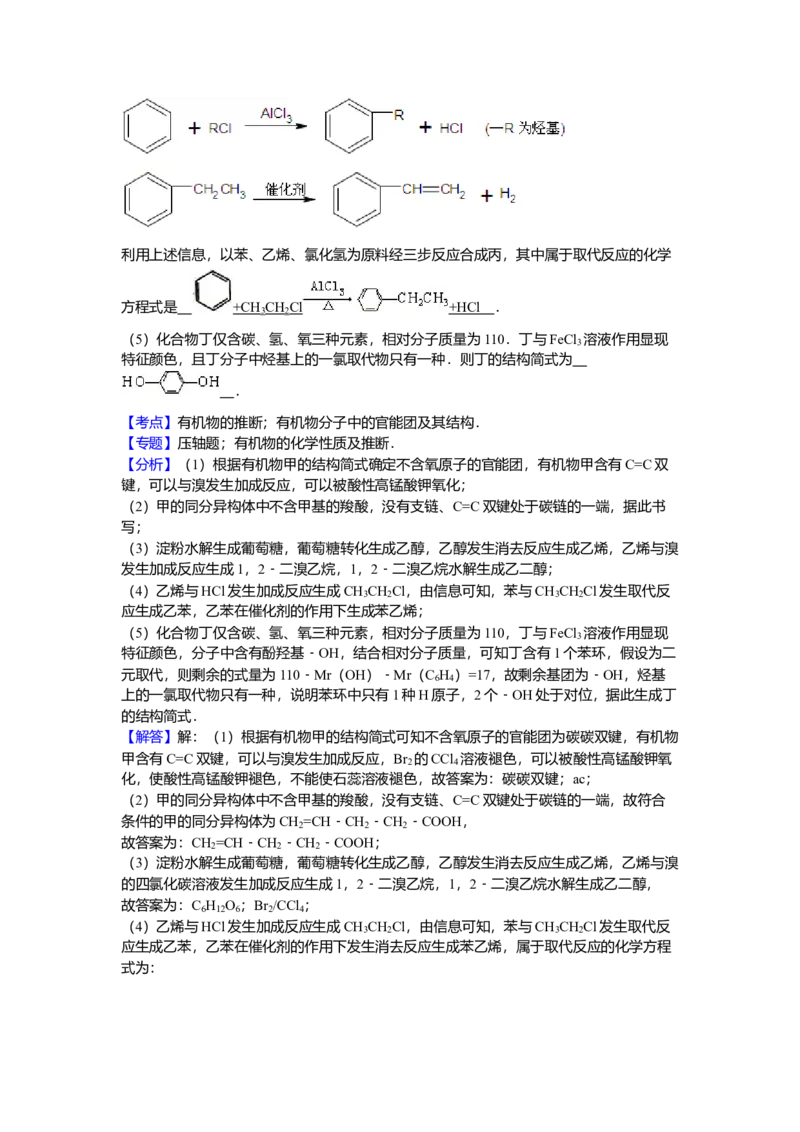
(4)已知:利用上述信息,以苯、乙烯、氯化氢为原料经三步反应合成丙,其中属于取代反应的化学
方程式是 +CH CH Cl +HCl .
3 2
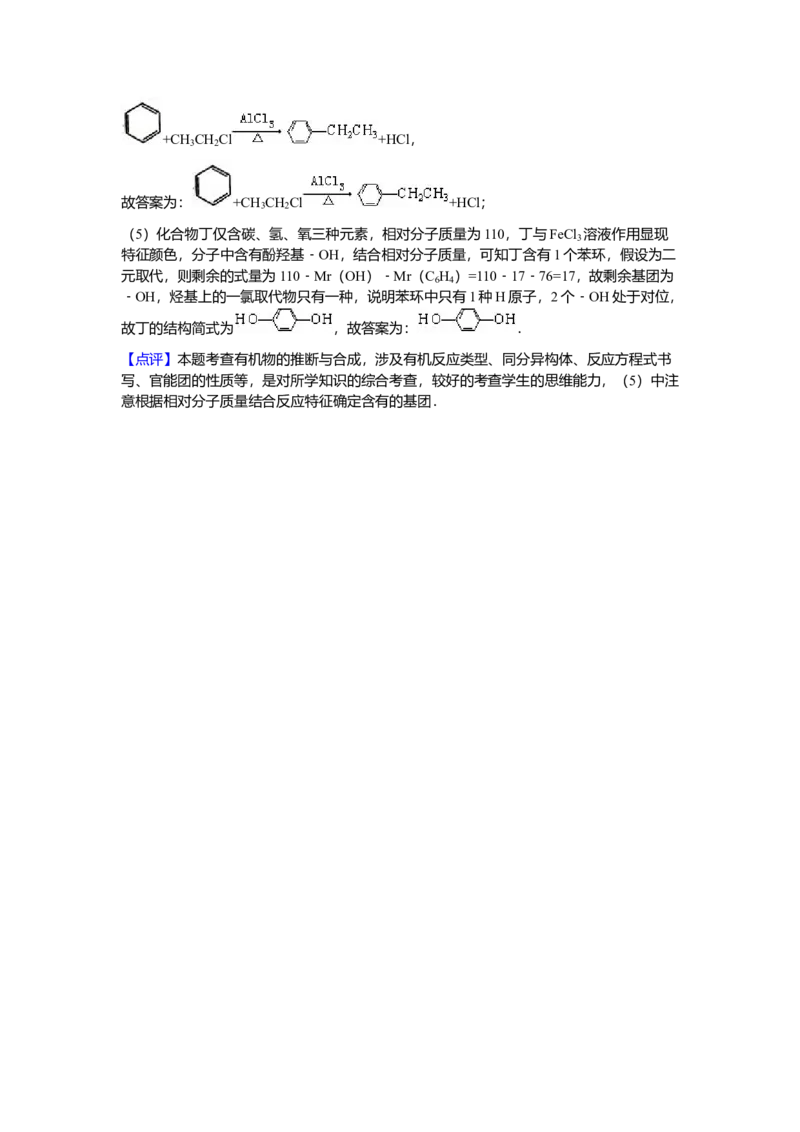
(5)化合物丁仅含碳、氢、氧三种元素,相对分子质量为110.丁与FeCl 溶液作用显现
3
特征颜色,且丁分子中烃基上的一氯取代物只有一种.则丁的结构简式为
.
【考点】有机物的推断;有机物分子中的官能团及其结构.
菁优网版权所有
【专题】压轴题;有机物的化学性质及推断.
【分析】(1)根据有机物甲的结构简式确定不含氧原子的官能团,有机物甲含有C=C双
键,可以与溴发生加成反应,可以被酸性高锰酸钾氧化;
(2)甲的同分异构体中不含甲基的羧酸,没有支链、C=C双键处于碳链的一端,据此书
写;
(3)淀粉水解生成葡萄糖,葡萄糖转化生成乙醇,乙醇发生消去反应生成乙烯,乙烯与溴
发生加成反应生成1,2﹣二溴乙烷,1,2﹣二溴乙烷水解生成乙二醇;
(4)乙烯与HCl发生加成反应生成CH CH Cl,由信息可知,苯与CH CH Cl发生取代反
3 2 3 2
应生成乙苯,乙苯在催化剂的作用下生成苯乙烯;
(5)化合物丁仅含碳、氢、氧三种元素,相对分子质量为110,丁与FeCl 溶液作用显现
3
特征颜色,分子中含有酚羟基﹣OH,结合相对分子质量,可知丁含有1个苯环,假设为二
元取代,则剩余的式量为110﹣Mr(OH)﹣Mr(C H )=17,故剩余基团为﹣OH,烃基
6 4
上的一氯取代物只有一种,说明苯环中只有1种H原子,2个﹣OH处于对位,据此生成丁
的结构简式.
【解答】解:(1)根据有机物甲的结构简式可知不含氧原子的官能团为碳碳双键,有机物
甲含有C=C双键,可以与溴发生加成反应,Br 的CCl 溶液褪色,可以被酸性高锰酸钾氧
2 4
化,使酸性高锰酸钾褪色,不能使石蕊溶液褪色,故答案为:碳碳双键;ac;
(2)甲的同分异构体中不含甲基的羧酸,没有支链、C=C双键处于碳链的一端,故符合
条件的甲的同分异构体为CH =CH﹣CH ﹣CH ﹣COOH,
2 2 2
故答案为:CH =CH﹣CH ﹣CH ﹣COOH;
2 2 2
(3)淀粉水解生成葡萄糖,葡萄糖转化生成乙醇,乙醇发生消去反应生成乙烯,乙烯与溴
的四氯化碳溶液发生加成反应生成1,2﹣二溴乙烷,1,2﹣二溴乙烷水解生成乙二醇,
故答案为:C H O ;Br /CCl ;
6 12 6 2 4
(4)乙烯与HCl发生加成反应生成CH CH Cl,由信息可知,苯与CH CH Cl发生取代反
3 2 3 2
应生成乙苯,乙苯在催化剂的作用下发生消去反应生成苯乙烯,属于取代反应的化学方程
式为:+CH CH Cl +HCl,
3 2
故答案为: +CH CH Cl +HCl;
3 2
(5)化合物丁仅含碳、氢、氧三种元素,相对分子质量为110,丁与FeCl 溶液作用显现
3
特征颜色,分子中含有酚羟基﹣OH,结合相对分子质量,可知丁含有1个苯环,假设为二
元取代,则剩余的式量为110﹣Mr(OH)﹣Mr(C H )=110﹣17﹣76=17,故剩余基团为
6 4
﹣OH,烃基上的一氯取代物只有一种,说明苯环中只有1种H原子,2个﹣OH处于对位,
故丁的结构简式为 ,故答案为: .
【点评】本题考查有机物的推断与合成,涉及有机反应类型、同分异构体、反应方程式书
写、官能团的性质等,是对所学知识的综合考查,较好的考查学生的思维能力,(5)中注
意根据相对分子质量结合反应特征确定含有的基团.