文档内容
2014 年全国统一高考化学试卷(新课标Ⅱ) C.pH=2 的 H 2 C 2 O 4 溶液与pH=12 的NaOH 溶液任意比例混合:c(Na+)+c(H+)=c(OH﹣)
+c(HC O ﹣)
一、选择题:本题共 7小题,每小题 6分,在每小题给出的四个选项中,只有一项是符合题目要 2 4
D.pH 相同的①CH COONa②NaHCO ③NaClO 三种溶液的c(Na+):①>②>③
求的. 3 3
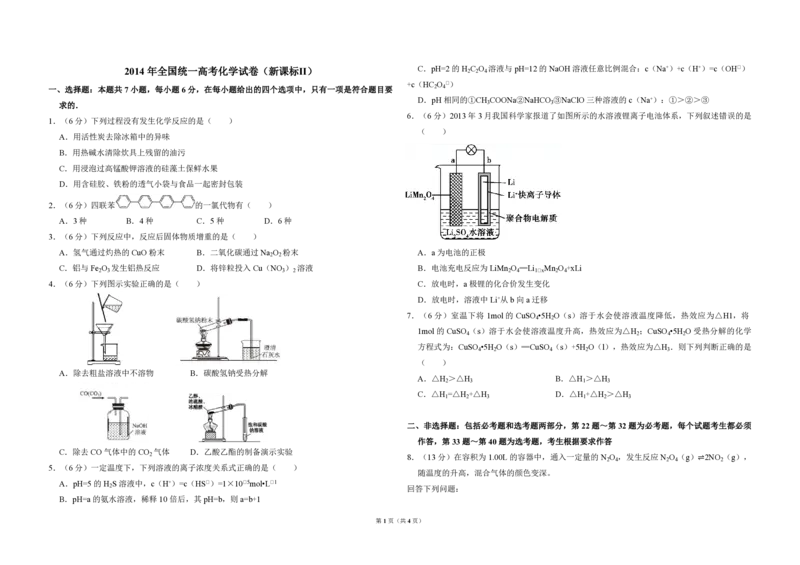
6.(6分)2013年 3月我国科学家报道了如图所示的水溶液锂离子电池体系,下列叙述错误的是
1.(6分)下列过程没有发生化学反应的是( )
( )
A.用活性炭去除冰箱中的异味
B.用热碱水清除炊具上残留的油污
C.用浸泡过高锰酸钾溶液的硅藻土保鲜水果
D.用含硅胶、铁粉的透气小袋与食品一起密封包装
2.(6分)四联苯 的一氯代物有( )
A.3种 B.4 种 C.5种 D.6种
3.(6分)下列反应中,反应后固体物质增重的是( )
A.氢气通过灼热的CuO 粉末 B.二氧化碳通过Na O 粉末 A.a为电池的正极
2 2
C.铝与 Fe O 发生铝热反应 D.将锌粒投入 Cu(NO ) 溶液 B.电池充电反应为LiMn O ═Li Mn O +xLi
2 3 3 2 2 4 1﹣x 2 4
4.(6分)下列图示实验正确的是( ) C.放电时,a极锂的化合价发生变化
D.放电时,溶液中Li+从b向a迁移
7.(6分)室温下将 1mol的 CuSO •5H O(s)溶于水会使溶液温度降低,热效应为△H1,将
4 2
1mol的 CuSO (s)溶于水会使溶液温度升高,热效应为△H ;CuSO •5H O 受热分解的化学
4 2 4 2
方程式为:CuSO •5H O(s)═CuSO (s)+5H O(l),热效应为△H .则下列判断正确的是
4 2 4 2 3
( )
A.除去粗盐溶液中不溶物 B.碳酸氢钠受热分解
A.△H >△H B.△H >△H
2 3 1 3
C.△H =△H +△H D.△H +△H >△H
1 2 3 1 2 3
二、非选择题:包括必考题和选考题两部分,第 22题~第 32题为必考题,每个试题考生都必须
作答,第 33题~第 40 题为选考题,考生根据要求作答
C.除去 CO 气体中的CO 气体 D.乙酸乙酯的制备演示实验
2 8.(13分)在容积为 1.00L的容器中,通入一定量的 N O ,发生反应 N O (g)⇌2NO (g),
2 4 2 4 2
5.(6分)一定温度下,下列溶液的离子浓度关系式正确的是( )
随温度的升高,混合气体的颜色变深。
A.pH=5 的H S 溶液中,c(H+)=c(HS﹣)=1×10﹣5mol•L﹣1
2 回答下列问题:
B.pH=a 的氨水溶液,稀释 10倍后,其pH=b,则a=b+1
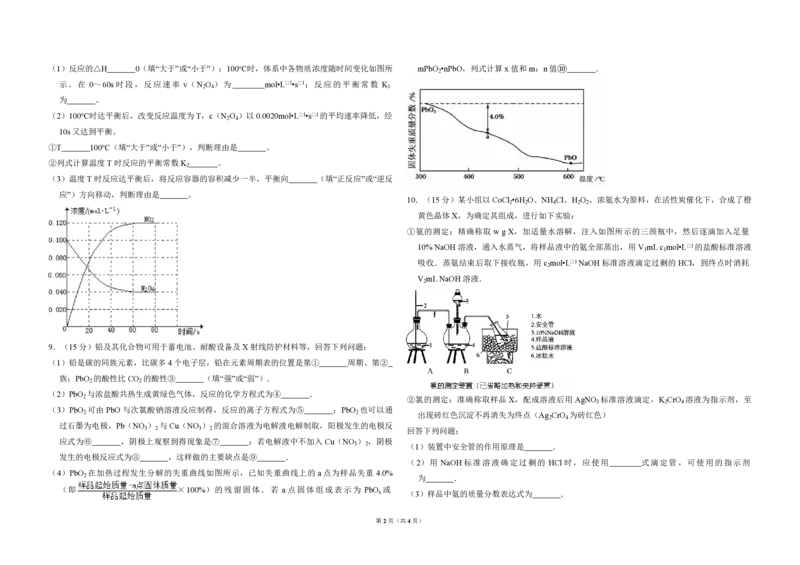
第1页(共4页)(1)反应的△H 0(填“大于”或“小于”);100℃时,体系中各物质浓度随时间变化如图所 mPbO •nPbO,列式计算x值和m:n值⑩ .
2
示。在 0~60s 时段,反应速率 v(N O )为 mol•L﹣1•s﹣1;反应的平衡常数 K
2 4 1
为 。
(2)100℃时达平衡后,改变反应温度为 T,c(N O )以0.0020mol•L﹣1•s﹣1的平均速率降低,经
2 4
10s 又达到平衡。
①T 100℃(填“大于”或“小于”),判断理由是 。
②列式计算温度T时反应的平衡常数K 。
2
(3)温度 T时反应达平衡后,将反应容器的容积减少一半,平衡向 (填“正反应”或“逆反
应”)方向移动,判断理由是 。
10.(15分)某小组以 CoCl •6H O、NH Cl、H O 、浓氨水为原料,在活性炭催化下,合成了橙
2 2 4 2 2
黄色晶体X,为确定其组成,进行如下实验:
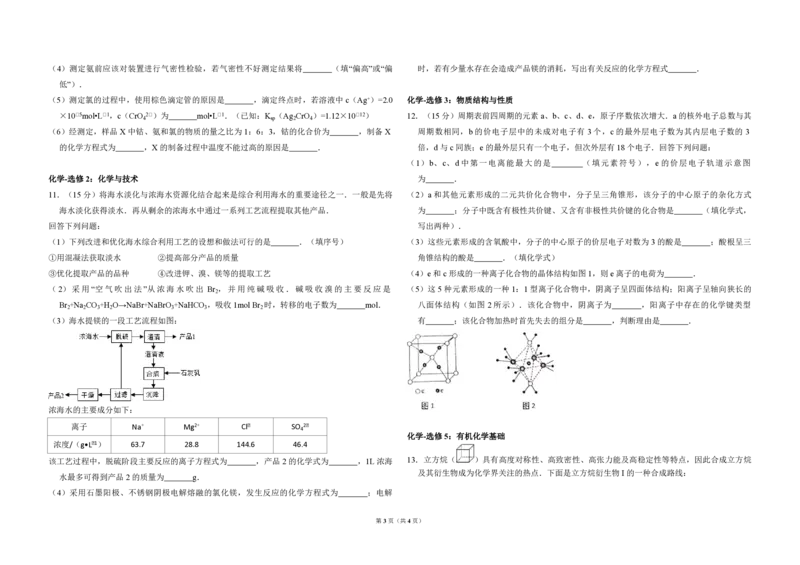
①氨的测定:精确称取 w g X,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量
10% NaOH 溶液,通入水蒸气,将样品液中的氨全部蒸出,用 V mL c mol•L﹣1的盐酸标准溶液
1 1
吸收.蒸氨结束后取下接收瓶,用 c mol•L﹣1 NaOH 标准溶液滴定过剩的 HCl,到终点时消耗
2
V mL NaOH 溶液.
2
9.(15分)铅及其化合物可用于蓄电池、耐酸设备及X 射线防护材料等,回答下列问题:
(1)铅是碳的同族元素,比碳多 4个电子层,铅在元素周期表的位置是第① 周期、第②
族;PbO 的酸性比CO 的酸性③ (填“强”或“弱”).
2 2
(2)PbO 与浓盐酸共热生成黄绿色气体,反应的化学方程式为④ .
2 ②氯的测定:准确称取样品 X,配成溶液后用 AgNO 标准溶液滴定,K CrO 溶液为指示剂,至
3 2 4
(3)PbO 可由 PbO 与次氯酸钠溶液反应制得,反应的离子方程式为⑤ ;PbO 也可以通
2 2 出现砖红色沉淀不再消失为终点(Ag CrO 为砖红色)
2 4
过石墨为电极,Pb(NO ) 与 Cu(NO ) 的混合溶液为电解液电解制取,阳极发生的电极反
3 2 3 2 回答下列问题:
应式为⑥ ,阴极上观察到得现象是⑦ ;若电解液中不加入 Cu(NO ) ,阴极
3 2 (1)装置中安全管的作用原理是 .
发生的电极反应式为⑧ ,这样做的主要缺点是⑨ .
(2)用 NaOH 标准溶液确定过剩的 HCl时,应使用 式滴定管,可使用的指示剂
(4)PbO 在加热过程发生分解的失重曲线如图所示,已知失重曲线上的 a点为样品失重 4.0%
2 为 .
(即 ×100%)的残留固体.若 a点固体组成表示为 PbO 或
x (3)样品中氨的质量分数表达式为 .
第2页(共4页)(4)测定氨前应该对装置进行气密性检验,若气密性不好测定结果将 (填“偏高”或“偏 时,若有少量水存在会造成产品镁的消耗,写出有关反应的化学方程式 .
低”).
(5)测定氯的过程中,使用棕色滴定管的原因是 ,滴定终点时,若溶液中 c(Ag+)=2.0 化学-选修 3:物质结构与性质
×10﹣5mol•L﹣1,c(CrO 2﹣)为 mol•L﹣1.(已知:K (Ag CrO )=1.12×10﹣12) 12.(15分)周期表前四周期的元素 a、b、c、d、e,原子序数依次增大.a的核外电子总数与其
4 sp 2 4
(6)经测定,样品 X 中钴、氨和氯的物质的量之比为 1:6:3,钴的化合价为 ,制备 X 周期数相同,b的价电子层中的未成对电子有 3 个,c的最外层电子数为其内层电子数的 3
的化学方程式为 ,X 的制备过程中温度不能过高的原因是 . 倍,d与c同族;e的最外层只有一个电子,但次外层有 18个电子.回答下列问题:
(1)b、c、d中第一电离能最大的是 (填元素符号),e的价层电子轨道示意图
化学-选修 2:化学与技术 为 .
11.(15分)将海水淡化与浓海水资源化结合起来是综合利用海水的重要途径之一.一般是先将 (2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式
海水淡化获得淡水.再从剩余的浓海水中通过一系列工艺流程提取其他产品. 为 ;分子中既含有极性共价键、又含有非极性共价键的化合物是 (填化学式,
回答下列问题: 写出两种).
(1)下列改进和优化海水综合利用工艺的设想和做法可行的是 .(填序号) (3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为 3的酸是 ;酸根呈三
①用混凝法获取淡水 ②提高部分产品的质量 角锥结构的酸是 .(填化学式)
③优化提取产品的品种 ④改进钾、溴、镁等的提取工艺 (4)e和c形成的一种离子化合物的晶体结构如图 1,则e离子的电荷为 .
(2)采用“空气吹出法”从浓海水吹出 Br ,并用纯碱吸收.碱吸收溴的主要反应是 (5)这 5种元素形成的一种 1:1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的
2
Br +Na CO +H O→NaBr+NaBrO +NaHCO ,吸收1mol Br 时,转移的电子数为 mol. 八面体结构(如图 2所示).该化合物中,阴离子为 ,阳离子中存在的化学键类型
2 2 3 2 3 3 2
(3)海水提镁的一段工艺流程如图: 有 ;该化合物加热时首先失去的组分是 ,判断理由是 .
浓海水的主要成分如下:
离子 Na+ Mg2+ Cl﹣ SO 2﹣
4
化学-选修 5:有机化学基础
浓度/(g•L﹣1) 63.7 28.8 144.6 46.4
该工艺过程中,脱硫阶段主要反应的离子方程式为 ,产品 2的化学式为 ,1L浓海 13.立方烷( )具有高度对称性、高致密性、高张力能及高稳定性等特点,因此合成立方烷
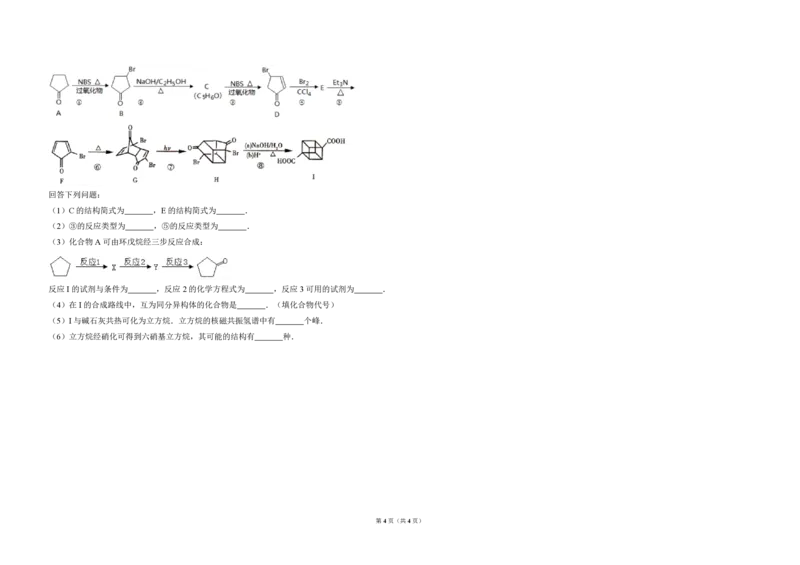
及其衍生物成为化学界关注的热点.下面是立方烷衍生物 I 的一种合成路线:
水最多可得到产品2的质量为 g.
(4)采用石墨阳极、不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为 ;电解
第3页(共4页)回答下列问题:
(1)C 的结构简式为 ,E的结构简式为 .
(2)③的反应类型为 ,⑤的反应类型为 .
(3)化合物A 可由环戊烷经三步反应合成:
反应I的试剂与条件为 ,反应2的化学方程式为 ,反应3可用的试剂为 .
(4)在I的合成路线中,互为同分异构体的化合物是 .(填化合物代号)
(5)I与碱石灰共热可化为立方烷.立方烷的核磁共振氢谱中有 个峰.
(6)立方烷经硝化可得到六硝基立方烷,其可能的结构有 种.
第4页(共4页)