文档内容
2014年全国统一高考化学试卷(新课标Ⅱ)
一、选择题:本题共 7小题,每小题6分,在每小题给出的四个选项中,只有
一项是符合题目要求的.
1.(6分)下列过程没有发生化学反应的是( )
A.用活性炭去除冰箱中的异味
B.用热碱水清除炊具上残留的油污
C.用浸泡过高锰酸钾溶液的硅藻土保鲜水果
D.用含硅胶、铁粉的透气小袋与食品一起密封包装
2.(6分)四联苯 的一氯代物有( )
A.3种 B.4种 C.5种 D.6种
3.(6分)下列反应中,反应后固体物质增重的是( )
A.氢气通过灼热的CuO粉末 B.二氧化碳通过Na O 粉末
2 2
C.铝与Fe O 发生铝热反应 D.将锌粒投入Cu(NO ) 溶液
2 3 3 2
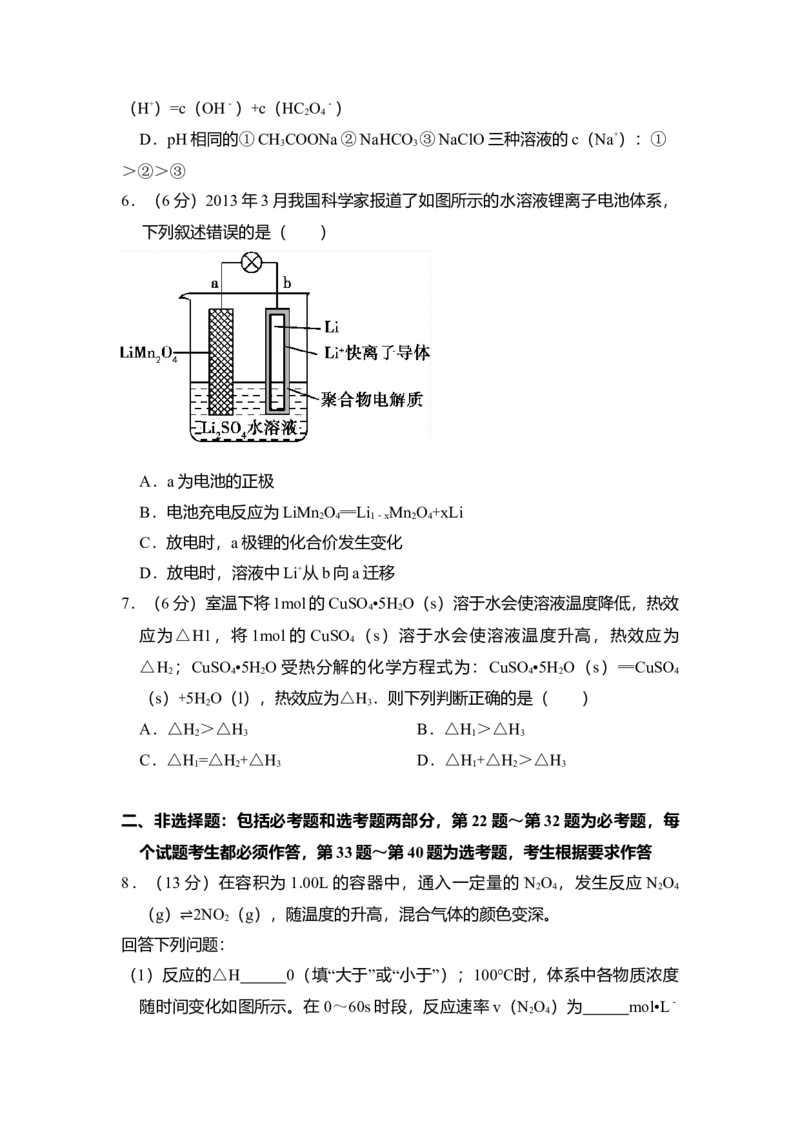
4.(6分)下列图示实验正确的是( )
A.除去粗盐溶液中不溶物 B.碳酸氢钠受热分解
C.除去CO气体中的CO 气体 D.乙酸乙酯的制备演示实验
2
5.(6分)一定温度下,下列溶液的离子浓度关系式正确的是( )
A.pH=5的H S溶液中,c(H+)=c(HS﹣)=1×10﹣5mol•L﹣1
2
B.pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C.pH=2的H C O 溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+c
2 2 4(H+)=c(OH﹣)+c(HC O ﹣)
2 4
D.pH相同的①CH COONa②NaHCO ③NaClO三种溶液的c(Na+):①
3 3
>②>③
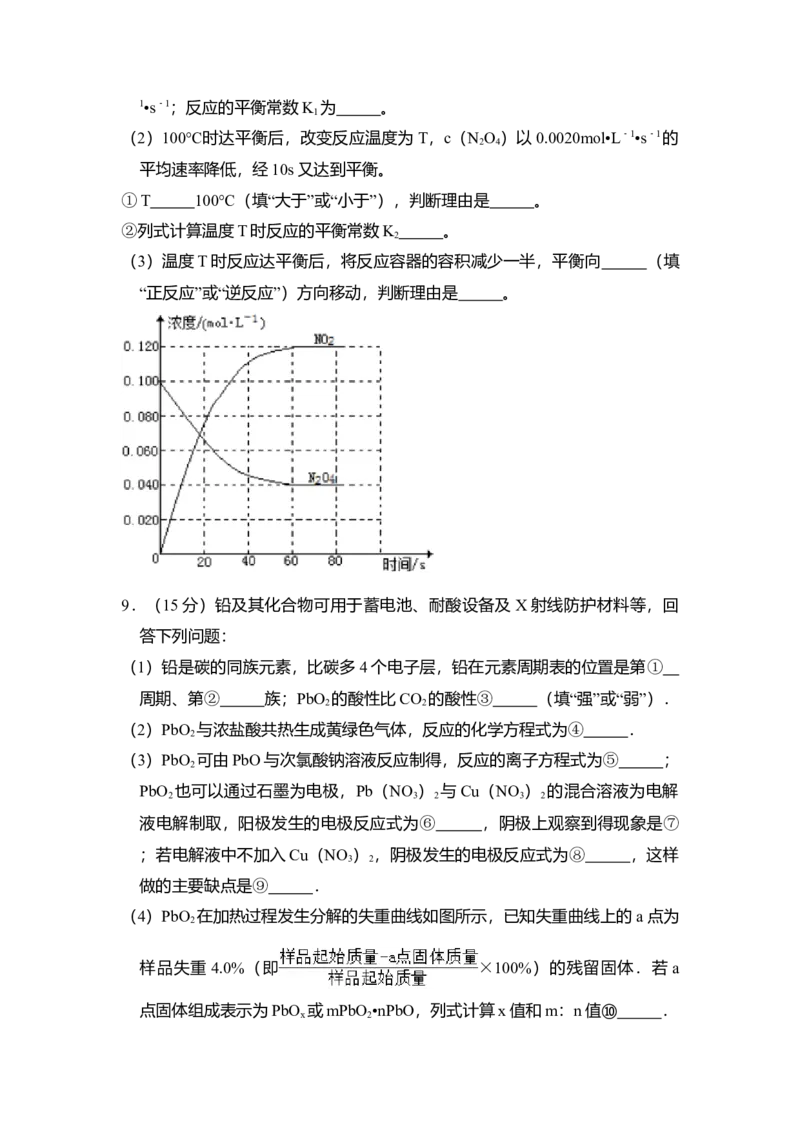
6.(6分)2013年3月我国科学家报道了如图所示的水溶液锂离子电池体系,
下列叙述错误的是( )
A.a为电池的正极
B.电池充电反应为LiMn O ═Li Mn O +xLi
2 4 1﹣x 2 4
C.放电时,a极锂的化合价发生变化
D.放电时,溶液中Li+从b向a迁移
7.(6分)室温下将1mol的CuSO •5H O(s)溶于水会使溶液温度降低,热效
4 2
应为△H1,将 1mol 的 CuSO (s)溶于水会使溶液温度升高,热效应为
4
△H ;CuSO •5H O 受热分解的化学方程式为:CuSO •5H O(s)═CuSO
2 4 2 4 2 4
(s)+5H O(l),热效应为△H .则下列判断正确的是( )
2 3
A.△H >△H B.△H >△H
2 3 1 3
C.△H =△H +△H D.△H +△H >△H
1 2 3 1 2 3
二、非选择题:包括必考题和选考题两部分,第22题~第32题为必考题,每
个试题考生都必须作答,第33题~第40题为选考题,考生根据要求作答
8.(13 分)在容积为 1.00L 的容器中,通入一定量的 N O ,发生反应 N O
2 4 2 4
(g) 2NO (g),随温度的升高,混合气体的颜色变深。
2
回答下列问题:
⇌
(1)反应的△H 0(填“大于”或“小于”);100℃时,体系中各物质浓度
随时间变化如图所示。在 0~60s时段,反应速率v(N O )为 mol•L﹣
2 41•s﹣1;反应的平衡常数K 为 。
1
(2)100℃时达平衡后,改变反应温度为 T,c(N O )以0.0020mol•L﹣1•s﹣1的
2 4
平均速率降低,经10s又达到平衡。
①T 100℃(填“大于”或“小于”),判断理由是 。
②列式计算温度T时反应的平衡常数K 。
2
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向 (填
“正反应”或“逆反应”)方向移动,判断理由是 。
9.(15分)铅及其化合物可用于蓄电池、耐酸设备及 X射线防护材料等,回
答下列问题:
(1)铅是碳的同族元素,比碳多4个电子层,铅在元素周期表的位置是第①
周期、第② 族;PbO 的酸性比CO 的酸性③ (填“强”或“弱”).
2 2
(2)PbO 与浓盐酸共热生成黄绿色气体,反应的化学方程式为④ .
2
(3)PbO 可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为⑤ ;
2
PbO 也可以通过石墨为电极,Pb(NO ) 与Cu(NO ) 的混合溶液为电解
2 3 2 3 2
液电解制取,阳极发生的电极反应式为⑥ ,阴极上观察到得现象是⑦
;若电解液中不加入Cu(NO ) ,阴极发生的电极反应式为⑧ ,这样
3 2
做的主要缺点是⑨ .
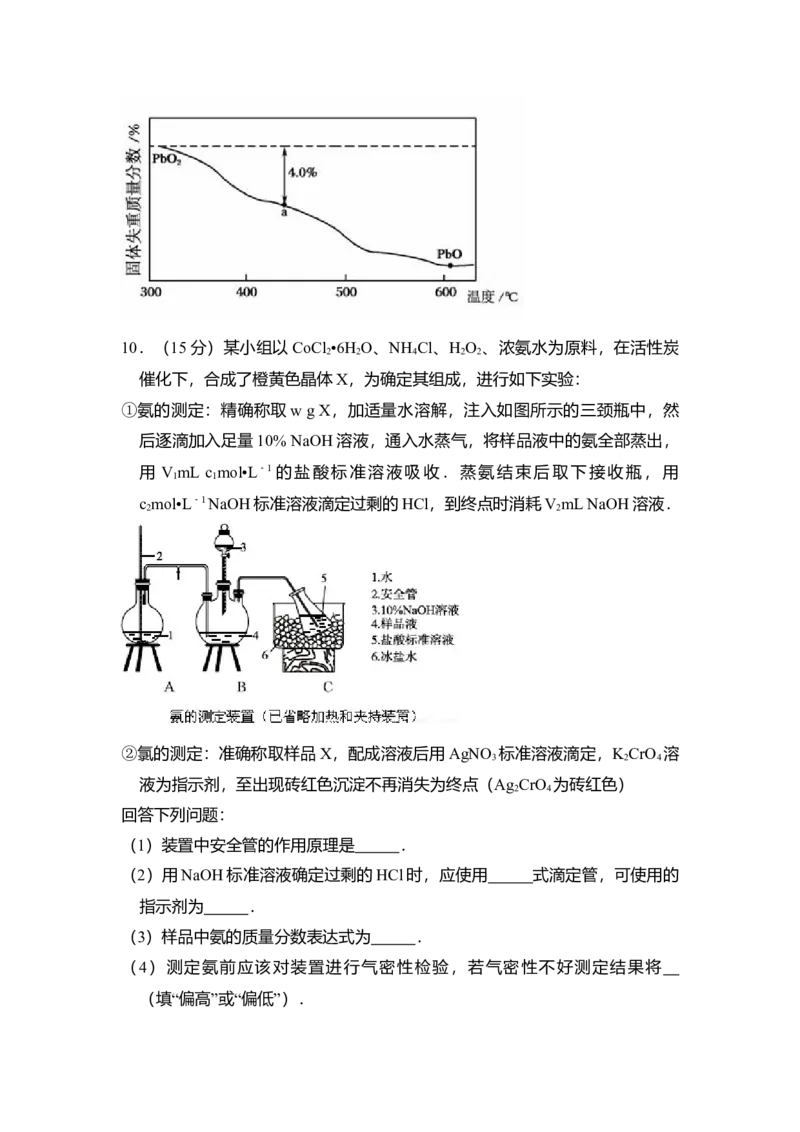
(4)PbO 在加热过程发生分解的失重曲线如图所示,已知失重曲线上的 a点为
2
样品失重 4.0%(即 ×100%)的残留固体.若 a
点固体组成表示为PbO 或mPbO •nPbO,列式计算x值和m:n值⑩ .
x 210.(15分)某小组以CoCl •6H O、NH Cl、H O 、浓氨水为原料,在活性炭
2 2 4 2 2
催化下,合成了橙黄色晶体X,为确定其组成,进行如下实验:
①氨的测定:精确称取w g X,加适量水溶解,注入如图所示的三颈瓶中,然
后逐滴加入足量10% NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,
用 V mL c mol•L﹣1的盐酸标准溶液吸收.蒸氨结束后取下接收瓶,用
1 1
c mol•L﹣1 NaOH标准溶液滴定过剩的HCl,到终点时消耗V mL NaOH溶液.
2 2
②氯的测定:准确称取样品X,配成溶液后用AgNO 标准溶液滴定,K CrO 溶
3 2 4
液为指示剂,至出现砖红色沉淀不再消失为终点(Ag CrO 为砖红色)
2 4
回答下列问题:
(1)装置中安全管的作用原理是 .
(2)用NaOH标准溶液确定过剩的HCl时,应使用 式滴定管,可使用的
指示剂为 .
(3)样品中氨的质量分数表达式为 .
(4)测定氨前应该对装置进行气密性检验,若气密性不好测定结果将
(填“偏高”或“偏低”).(5)测定氯的过程中,使用棕色滴定管的原因是 ,滴定终点时,若溶液
中c(Ag+)=2.0×10﹣5mol•L﹣1,c(CrO 2﹣)为 mol•L﹣1.(已知:K
4 sp
(Ag CrO )=1.12×10﹣12)
2 4
(6)经测定,样品X中钴、氨和氯的物质的量之比为1:6:3,钴的化合价为
,制备X的化学方程式为 ,X的制备过程中温度不能过高的原因是
.
化学-选修2:化学与技术
11.(15分)将海水淡化与浓海水资源化结合起来是综合利用海水的重要途径
之一.一般是先将海水淡化获得淡水.再从剩余的浓海水中通过一系列工艺
流程提取其他产品.
回答下列问题:
(1)下列改进和优化海水综合利用工艺的设想和做法可行的是 .(填序
号)
①用混凝法获取淡水 ②提高部分产品的质量
③优化提取产品的品种 ④改进钾、溴、镁等的提取工艺
(2)采用“空气吹出法”从浓海水吹出Br ,并用纯碱吸收.碱吸收溴的主要反
2
应是Br +Na CO +H O→NaBr+NaBrO +NaHCO ,吸收1mol Br 时,转移的电
2 2 3 2 3 3 2
子数为 mol.
(3)海水提镁的一段工艺流程如图:
浓海水的主要成分如下:
离子 Na+ Mg2+ Cl﹣ SO 2﹣
4
浓度/(g•L﹣1) 63.7 28.8 144.6 46.4
该工艺过程中,脱硫阶段主要反应的离子方程式为 ,产品2的化学式为
,1L浓海水最多可得到产品2的质量为 g.(4)采用石墨阳极、不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为
;电解时,若有少量水存在会造成产品镁的消耗,写出有关反应的化学方程
式 .
化学-选修3:物质结构与性质
12.(15分)周期表前四周期的元素a、b、c、d、e,原子序数依次增大.a的
核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最
外层电子数为其内层电子数的 3倍,d与c同族;e的最外层只有一个电子,
但次外层有18个电子.回答下列问题:
(1)b、c、d中第一电离能最大的是 (填元素符号),e的价层电子轨道
示意图为 .
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心
原子的杂化方式为 ;分子中既含有极性共价键、又含有非极性共价键
的化合物是 (填化学式,写出两种).
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为 3的酸是
;酸根呈三角锥结构的酸是 .(填化学式)
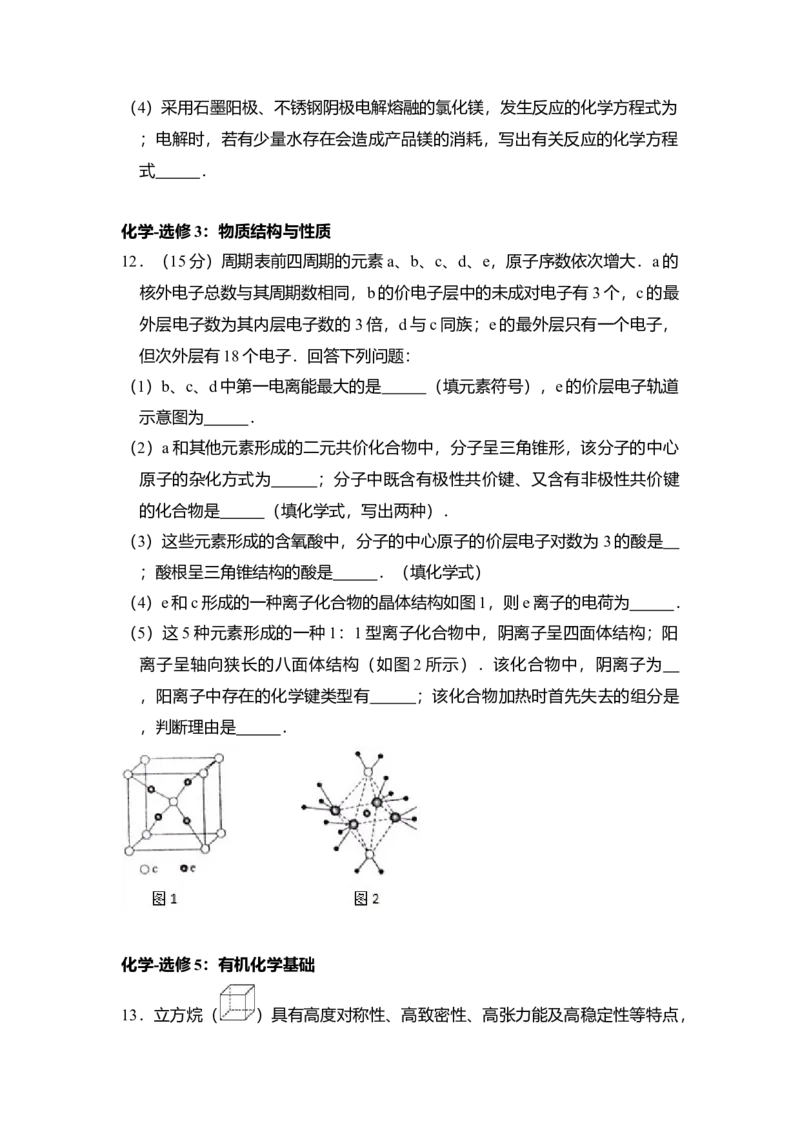
(4)e和c形成的一种离子化合物的晶体结构如图1,则e离子的电荷为 .
(5)这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构;阳
离子呈轴向狭长的八面体结构(如图 2所示).该化合物中,阴离子为
,阳离子中存在的化学键类型有 ;该化合物加热时首先失去的组分是
,判断理由是 .
化学-选修5:有机化学基础
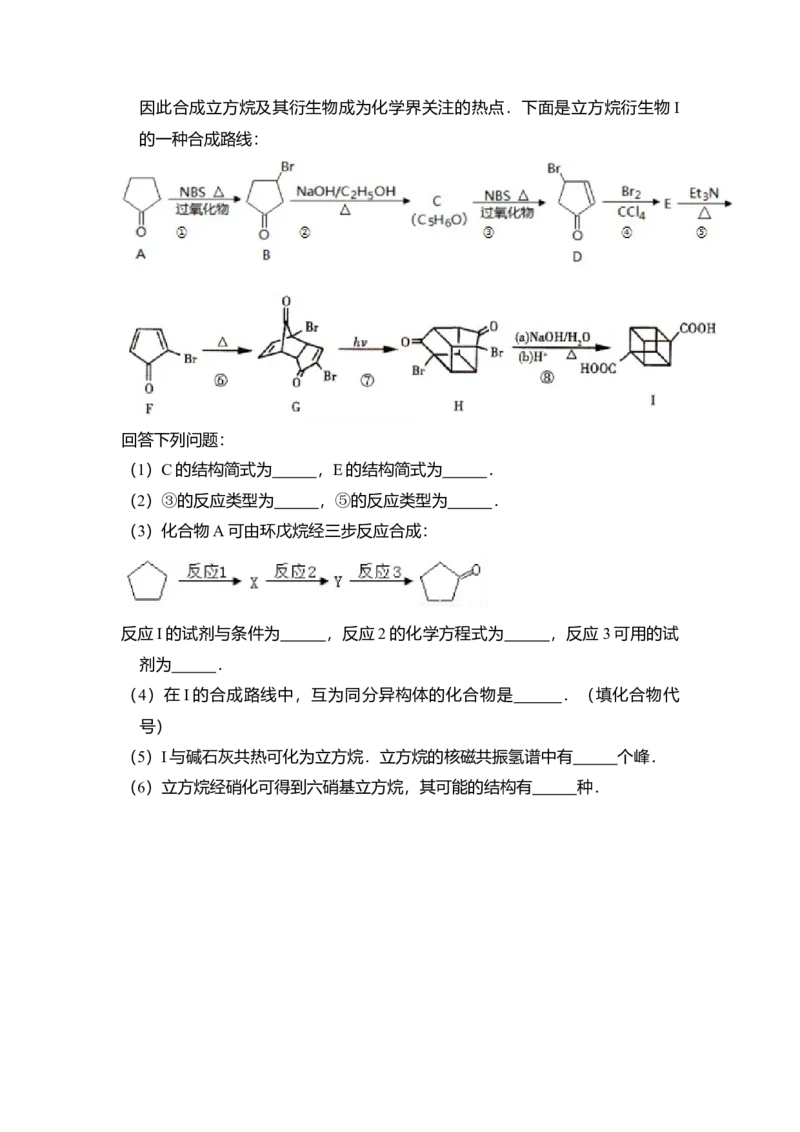
13.立方烷( )具有高度对称性、高致密性、高张力能及高稳定性等特点,因此合成立方烷及其衍生物成为化学界关注的热点.下面是立方烷衍生物I
的一种合成路线:
回答下列问题:
(1)C的结构简式为 ,E的结构简式为 .
(2)③的反应类型为 ,⑤的反应类型为 .
(3)化合物A可由环戊烷经三步反应合成:
反应I的试剂与条件为 ,反应2的化学方程式为 ,反应3可用的试
剂为 .
(4)在I的合成路线中,互为同分异构体的化合物是 .(填化合物代
号)
(5)I与碱石灰共热可化为立方烷.立方烷的核磁共振氢谱中有 个峰.
(6)立方烷经硝化可得到六硝基立方烷,其可能的结构有 种.