文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
主题二 物质的性质与应用
专题 09 常见的酸和碱
01考情透视·目标导航 题型二 常见的酸
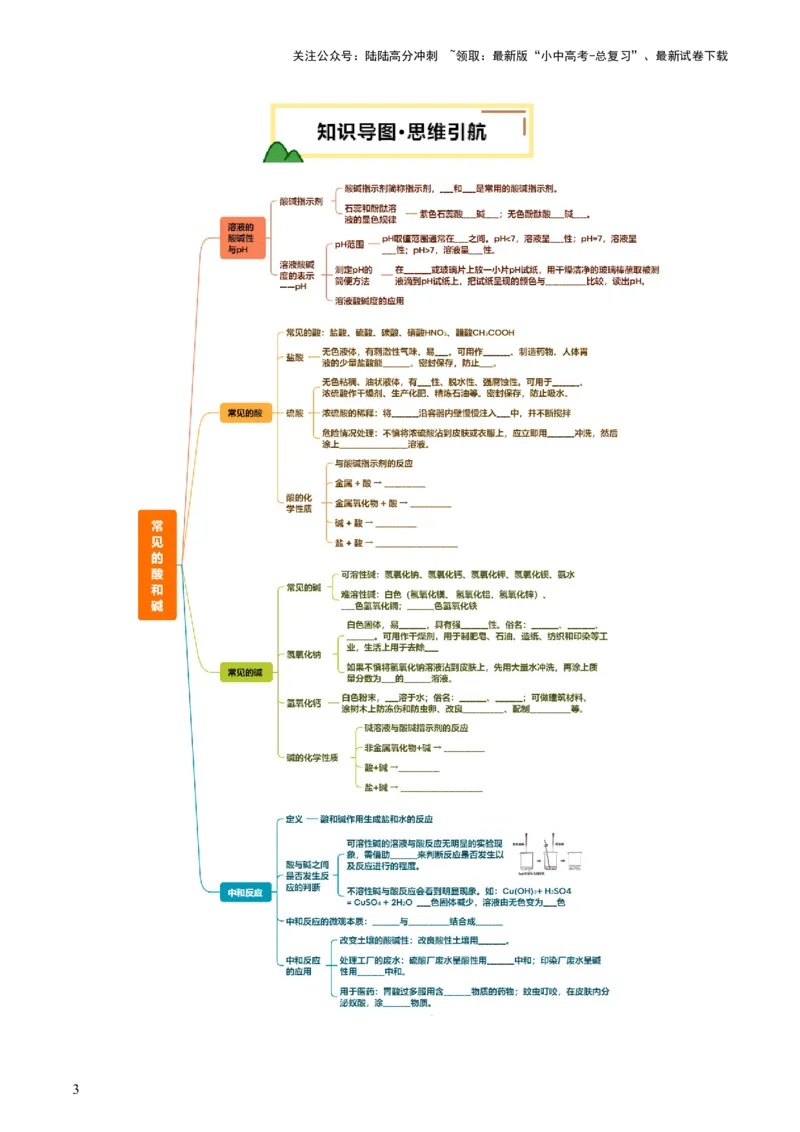
02知识导图·思维引航
►考向01 盐酸、硫酸的性质
►考向02 浓硫酸的稀释
03考点突破·考法探究
►考向03 性质与用途的对应关系
考点一 溶液的酸碱性与pH
►考向04 酸的化学性质
考点二 常见的酸
►考向05 实验探究酸的化学性质
考点三 常见的碱
题型三 常见的碱
考点四 中和反应
►考向01 氢氧化钠、氢氧化钙的性质
04题型精研·考向洞悉
►考向02性质与用途的对应关系
题型一 溶液的酸碱性与pH
►考向03 碱的化学性质
►考向01 常见酸碱指示剂及变色情况
►考向04 实验探究碱的化学性质
►考向02 自制酸碱指示剂
题型四 中和反应
►考向03 溶液pH的测定
►考向01无明显现象中和反应的判断
►考向04 溶液pH 的应用
►考向02 中和反应的应用
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考点要求 课标要求 命题预测
了解检验溶液酸碱性的基本方法, 溶液的酸碱性与 pH 考查常结合生产生活、
溶液的酸碱性
知道酸碱性对人体健康和农作物生长的 化学实验等考查;考查题型以选择题为
与pH
影响。 主,也可穿插于填空、实验探究等题型
中。常见的酸和碱可直接考查,也可结合
以盐酸和硫酸为例,通过实验探究
常见的酸
生产生活等情境。考查题型有选择题、实
认识酸的主要性质和用途。
验探究题和流程题等题型中。中和反应的
以氢氧化钠和氢氧化钙为例,通过
常见的碱 考查可单独进行,也可与其他知识点结合
实验探究认识碱的主要性质和用途。
考查。在实验探究题和选择题中呈现。常
见的考点有:指示剂的显色规律;溶液酸
依据中和反应,初步预测常见的酸
碱性的判断;盐酸、硫酸、氢氧化钠和氢
和碱的主要性质,设计实验方案,分
中和反应
氧化钙的性质和用途;酸的化学性质;碱
析、解释有关实验现象,进行证据推
的化学性质;无明显现象的中和反应的判
理,得出合理结论。
断;中和反应的应用等。
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考点一 溶液的酸碱性与pH
1.酸碱指示剂
(1) 酸碱指示剂简称 ,遇酸性或碱性溶液能显示不同颜色的物质。 和 是常用的酸碱指示
剂。
(2)石蕊和酚酞溶液的显色规律
酸碱指示剂 酸性溶液 中性溶液 碱性溶液
紫色石蕊溶液 色 紫色 色
无色酚酞溶液 色 无色 色
归纳:紫色石蕊酸红碱蓝;无色酚酞酸无碱红。
【特别提醒】
1 . 酸碱指示剂遇酸性或碱性溶液时,变色的是指示剂。
2 . 酸碱指示剂只能对酸、碱溶液作出定性判断,而不能对酸碱性的强弱程度作出判断。
3 . 水和氯化钠溶液是中性液体。
(3)用指示剂鉴别酸碱性不同的溶液
典例:实验室有3瓶失去标签的液体,分别为蒸馏水、稀硫酸、氢氧化钠溶液,如何鉴别?
分别取三种液体样品于试管中, ,若液体变为 色,则为稀硫酸;若液体变为 色,则为
氢氧化钠溶液;若仍为 色,则为蒸馏水。
2.溶液酸碱度的表示——pH
(1)溶液酸碱性强弱的程度即溶液的酸碱度,常用 来表示。
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
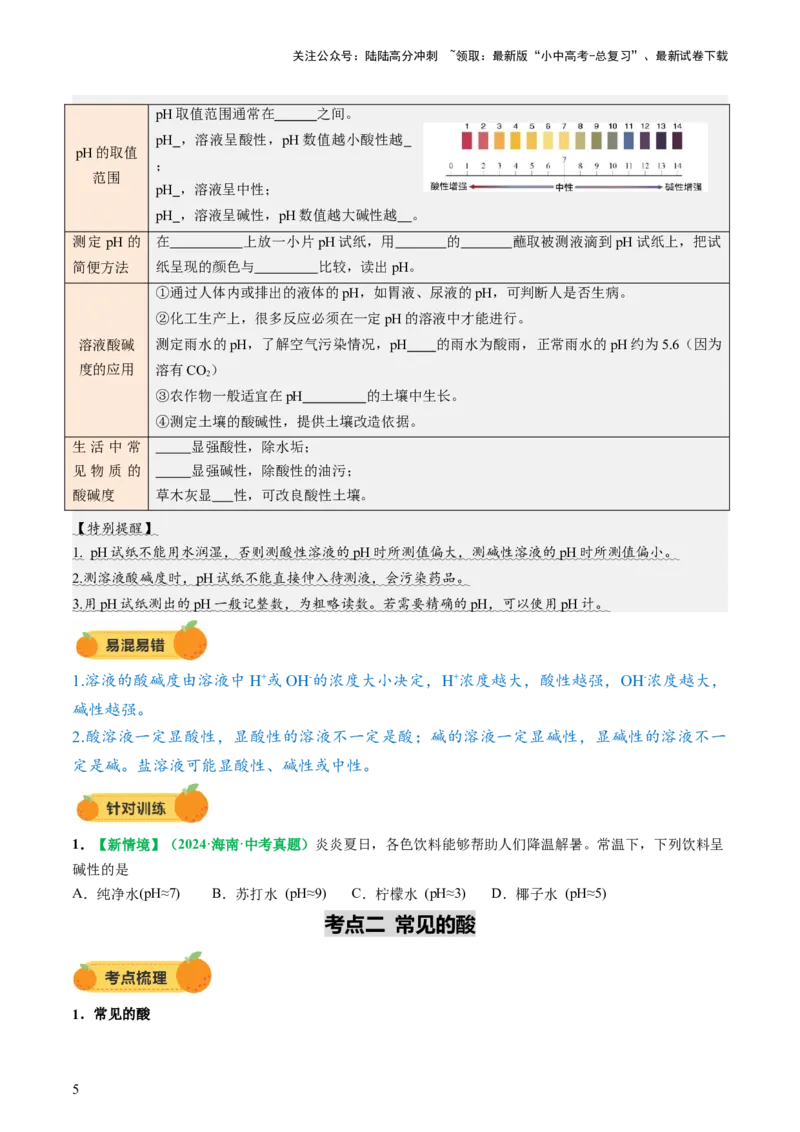
pH取值范围通常在 之间。
pH ,溶液呈酸性,pH数值越小酸性越
pH的取值
;
范围
pH ,溶液呈中性;
pH ,溶液呈碱性,pH数值越大碱性越 。
测定 pH 的 在 上放一小片pH试纸,用 的 蘸取被测液滴到pH试纸上,把试
简便方法 纸呈现的颜色与 比较,读出pH。
①通过人体内或排出的液体的pH,如胃液、尿液的pH,可判断人是否生病。
②化工生产上,很多反应必须在一定pH的溶液中才能进行。
溶液酸碱 测定雨水的pH,了解空气污染情况,pH 的雨水为酸雨,正常雨水的pH约为5.6(因为
度的应用 溶有CO)
2
③农作物一般适宜在pH 的土壤中生长。
④测定土壤的酸碱性,提供土壤改造依据。
生 活 中 常 显强酸性,除水垢;
见 物 质 的 显强碱性,除酸性的油污;
酸碱度 草木灰显 性,可改良酸性土壤。
【特别提醒】
1. pH 试纸不能用水润湿,否则测酸性溶液的 pH 时所测值偏大,测碱性溶液的 pH 时所测值偏小。
2 . 测溶液酸碱度时, pH 试纸不能直接伸入待测液,会污染药品。
3 . 用 pH 试纸测出的 pH 一般记整数,为粗略读数。若需要精确的 pH ,可以使用 pH 计。
1.溶液的酸碱度由溶液中H+或OH-的浓度大小决定,H+浓度越大,酸性越强,OH-浓度越大,
碱性越强。
2.酸溶液一定显酸性,显酸性的溶液不一定是酸;碱的溶液一定显碱性,显碱性的溶液不一
定是碱。盐溶液可能显酸性、碱性或中性。
1.【新情境】(2024·海南·中考真题)炎炎夏日,各色饮料能够帮助人们降温解暑。常温下,下列饮料呈
碱性的是
A.纯净水(pH≈7) B.苏打水 (pH≈9) C.柠檬水 (pH≈3) D.椰子水 (pH≈5)
考点二 常见的酸
1.常见的酸
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
盐酸 、硫酸 、碳酸HCO、硝酸 、 CHCOOH
2 3 3
2.盐酸、硫酸的性质和用途
(1)盐酸、硫酸的性质、用途及保存方法
盐酸 硫酸
颜色、状态 液体 无色粘稠、油状液体
气味 有 气味 无
浓盐酸易 ,打开瓶盖,瓶口有 浓硫酸的特性:
特性 (浓盐酸挥发出的 气体与空气 吸水性( 性质,可做 )
中的水蒸气结合形成盐酸小液滴) 脱水性、腐蚀性、强氧化性( 性质)
** 错误的表达式 ** 用于生产化肥、农
** 错误的表达式 **金属 药、火药、染料
** 错误的表达式 **制造 ** 错误的表达式 **冶炼金属、精炼石
用途
** 错误的表达式 **人体胃液含有 油、
少量盐酸, ** 错误的表达式 **在实验室中,浓硫酸
常用作
保存方法及原理 保存,防 保存,防
(2)浓盐酸与浓硫酸敞口放置在空气中的变化
性质 溶质质量 溶剂质量 溶液质量 溶质质量分数
浓盐酸 挥发性 不变 减小
浓硫酸 吸水性 不变 增大
【特别提醒】
1. 浓盐酸和浓硫酸敞口放置一段时间后,浓度都变小,但原因不同。浓盐酸是因为挥发后溶质质量减小导
致浓度变小,浓硫酸是因为其有吸水性,能吸收空气中的水蒸气,使溶剂质量增大导致浓度变小。
(3)浓硫酸的稀释
正确操作 操作要领 错误操作 注意事项及原因
。 切不可把 注入 !因为若将水
(酸入水,沿器壁,慢倾 倒入浓硫酸中,
倒,及时搅) ,非
常危险!
手触碰烧杯外壁的感觉 。说明 。
不慎将浓硫酸沾到皮肤或衣服上,应立即用 ,然后涂上
危险情况处理
。
【特别提醒】
稀硫酸沾在衣服上,水分蒸发后会变成浓硫酸,也要进行处理。
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
3.酸的化学性质
(1)酸溶液有相似的化学性质,原因是:不同的酸溶液中都有相同的阳离子: 。
(2)酸的化学性质
酸的化学性质 实验现象 化学方程式
酸能使紫色石蕊试液变 色,不
1.与酸碱指示剂的反应
能使无色酚酞试液变色
Mg + 2HCl = MgCl +H ↑
2 2
快速产生大量 ,固体逐渐
Mg + HSO = MgSO +H ↑
2 4 4 2
Zn + 2HCl = ZnCl+H ↑
2 2
产生 较快,固体逐渐 。
Zn + H SO = ZnSO +H ↑
2 4 4 2
2.金属 + 酸 → 盐 + 氢气
产生 很慢,固体逐渐 ,溶液 Fe + 2HCl = FeCl +H ↑
2 2
由 色逐渐变为 色。 Fe + H SO = FeSO +H ↑
2 4 4 2
2Al + 6HCl = 2AlCl + 3H↑
3 2
迅速产生大量气泡,固体逐渐
2Al + 3H SO = Al (SO ) +3H↑
2 4 2 4 3 2
固体逐渐减少,溶液由无色变 CuO + 2HCl = CuCl +H O;
2 2
3.金属氧化物 + 酸 → 盐 为 CuO + H SO = CuSO +H O
2 4 4 2
+ 水 固体逐渐减少,溶液由无色 Fe O +6 HCl =2FeCl + 3HO ;
2 3 3 2
变为 Fe O +3H SO = Fe (SO ) + 3HO
2 3 2 4 2 4 3 2
无明显现象,需借助 来判读 Ca(OH) + 2HCl = CaCl + 2H O;
2 2 2
4.碱 + 酸 → 盐 + 水
反应是否发生 2NaOH + H SO = Na SO + H O
2 4 2 4 2
CaCO + 2HCl = CaCl + H O+CO↑
3 2 2 2
产生大量 ,固体逐渐 NaHCO +HCl = NaCl + H O+CO↑
3 2 2
5.盐 + 酸 → 另一种盐 +
NaCO+2HCl = 2NaCl + H O+CO↑
2 3 2 2
另一种酸
AgNO + HCl = AgCl↓+ HNO
3 3
产生
BaCl + H SO =BaSO ↓+2HCl
2 2 4 4
【特别提醒】
用盐酸或稀硫酸除去铁表面的铁锈时不宜长时间浸泡在酸中。
判断对错:
1.用pH试纸测定浓硫酸的pH值为1。( )
2.浓硫酸具有脱水性,在实验室可用作某些气体的干燥剂。( )
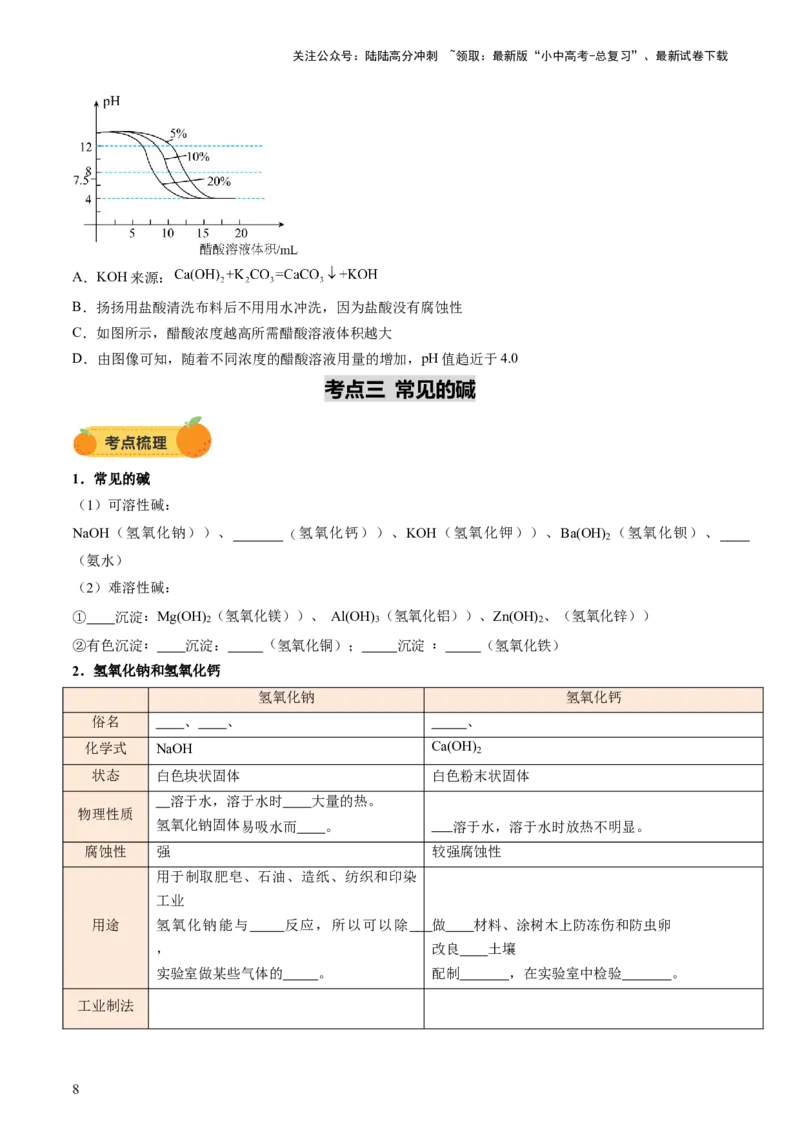
1.【新考向】(2024·广东深圳·中考真题)扬扬同学发现染布前可以用盐酸洗去布料表面部分碱性物质
(如KOH),染色后用5%,10%,20%的醋酸溶液与等浓度等质量的KOH溶液反应,pH值变化如下
图。下列选项正确的是
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.KOH来源:
B.扬扬用盐酸清洗布料后不用用水冲洗,因为盐酸没有腐蚀性
C.如图所示,醋酸浓度越高所需醋酸溶液体积越大
D.由图像可知,随着不同浓度的醋酸溶液用量的增加,pH值趋近于4.0
考点三 常见的碱
1.常见的碱
(1)可溶性碱:
NaOH(氢氧化钠))、 (氢氧化钙))、KOH(氢氧化钾))、Ba(OH) (氢氧化钡)、
2
(氨水)
(2)难溶性碱:
① 沉淀:Mg(OH) (氢氧化镁))、 Al(OH) (氢氧化铝))、Zn(OH) 、(氢氧化锌))
2 3 2
②有色沉淀: 沉淀: (氢氧化铜); 沉淀 : (氢氧化铁)
2.氢氧化钠和氢氧化钙
氢氧化钠 氢氧化钙
俗名 、 、 、
化学式 NaOH Ca(OH) 2
状态 白色块状固体 白色粉末状固体
溶于水,溶于水时 大量的热。
物理性质
氢氧化钠固体易吸水而 。 溶于水,溶于水时放热不明显。
腐蚀性 强 较强腐蚀性
用于制取肥皂、石油、造纸、纺织和印染
工业
用途 氢氧化钠能与 反应,所以可以除 做 材料、涂树木上防冻伤和防虫卵
, 改良 土壤
实验室做某些气体的 。 配制 ,在实验室中检验 。
工业制法
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
保存方法
,防 ,防吸收 变质 ,防吸收 变质
意外事故处
如果不慎将氢氧化钠溶液沾到皮肤上,先用大量水冲洗,再涂上质量分数为 的 溶液。
理
鉴别 通入CO,产生白色沉淀的为
2
【特别提醒】
1 .氢氧化钠不能干燥: CO 、 SO 、 SO 、 HCl 气体
2 2 3
氧化钙不能干燥: CO 、 SO 、 SO 、 HCl 气体
2 2 3
2.碱的化学性质
(1)碱溶液有相似化学性质的原因:可溶性碱在水中解离时所生成的阴离子全部是
(2)碱的化学性质
碱溶液与酸碱指示
使紫色石蕊试液变 色,使无色酚酞试液变 色
剂的反应
2NaOH + CO = NaCO + H O 常用于 某气体中的CO
2 2 3 2 2
非金属氧化物+碱 2NaOH + SO = + H O
2 2
→ 盐+水 2NaOH + SO = + H O
3 2
Ca(OH) + CO = CaCO↓+ H O 常用于 CO
2 2 3 2 2
2HNO + Mg(OH) = Mg(NO) + 2H O
3 2 3 2 2
酸+碱 → 盐+水
Al(OH) +3HCl = AlCl +3H O
3 3 2
条件:反应物均可溶,产物有气体或沉淀或水
盐+碱 → 另一种 3NaOH+FeCl = +3NaCl生成 色沉淀,溶液由 逐渐变成无色
3
盐+另一种碱 2NaOH+CuSO = +2Na SO 生成 沉淀,溶液由 逐渐变成无色
4 2 4
NaCO+Ca(OH) = + 2NaOH有白色生成
2 3 2
氢氧化钠、氢氧化钙都能使无色酚酞变红,氢氧化铜也能使酚酞变红。( )
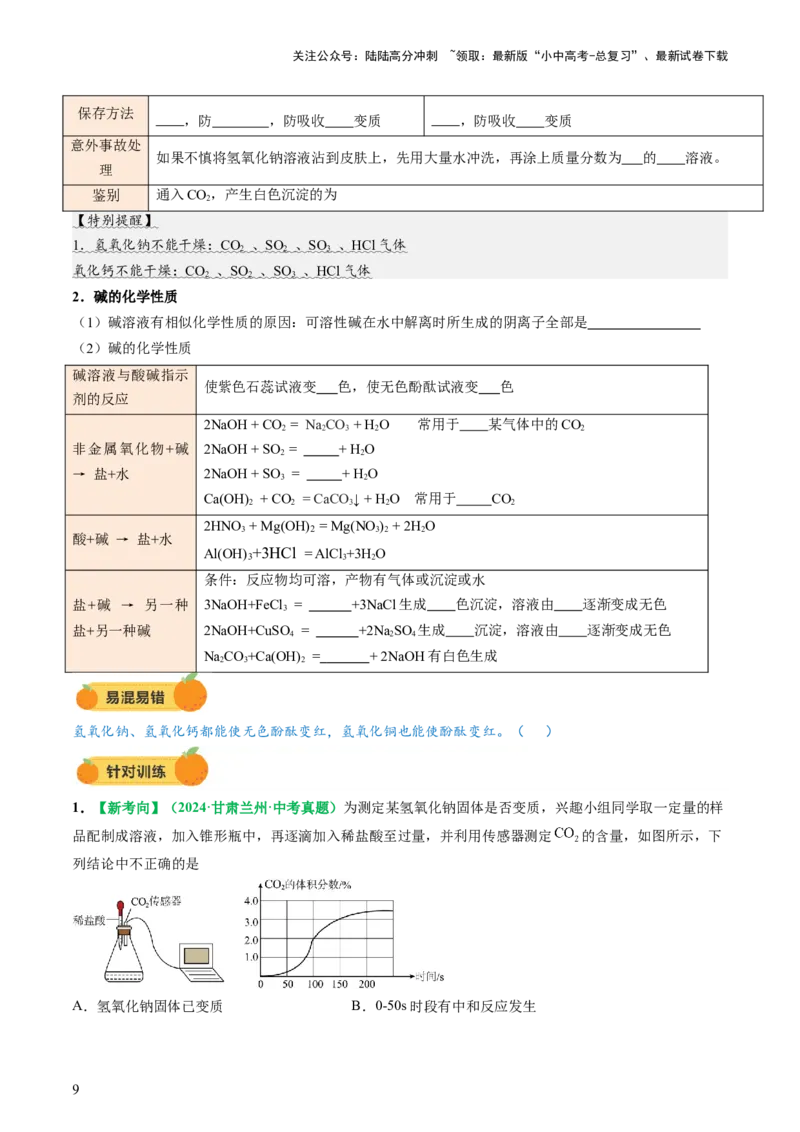
1.【新考向】(2024·甘肃兰州·中考真题)为测定某氢氧化钠固体是否变质,兴趣小组同学取一定量的样
品配制成溶液,加入锥形瓶中,再逐滴加入稀盐酸至过量,并利用传感器测定 的含量,如图所示,下
列结论中不正确的是
A.氢氧化钠固体已变质 B.0-50s时段有中和反应发生
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C.100s时溶液的pH>7 D.200s时溶液中的溶质只有一种
考点四 中和反应
1.中和反应
酸和碱作用生成盐和水的反应,叫做中和反应。
2.酸与碱之间是否发生反应的判断
碱的溶液与酸反应无明显的实验现象,
需借助 来判断反应是否发生以及反应进行的程度。
通常是向碱溶液中滴加 ,溶液 ,再滴加酸至溶液
反应的 ,此时恰好完全反应。
判断 若用氢氧化钠或氢氧化钙固体与酸反应,则会看到固体减少。
碱与酸反应会看到明显现象。如:
Cu(OH) + H SO = CuSO + 2H O 固体减少,溶液由 色变为 色
2 2 4 4 2
Fe(OH) + 3HCl = FeCl + 2H O 固体减少,溶液由 色变为 色
3 3 2
3.中和反应的微观本质
酸中的 与碱中的 结合成 : 。
4.中和反应的应用
(1)改变土壤的酸碱性:改良酸性土壤用 。
(2)处理工厂的废水:硫酸厂废水呈酸性用 中和;印染厂废水呈碱性用 中和。
(3)用于医药:胃酸过多服用 的药物,如 、 等,中和过多的胃酸;
蚊虫叮咬,在皮肤内分泌蚁酸,涂 物质如 、 等,可减轻症状。
氢氧化钙和氢氧化钠都具有碱性,故都能改良酸性土壤。( )
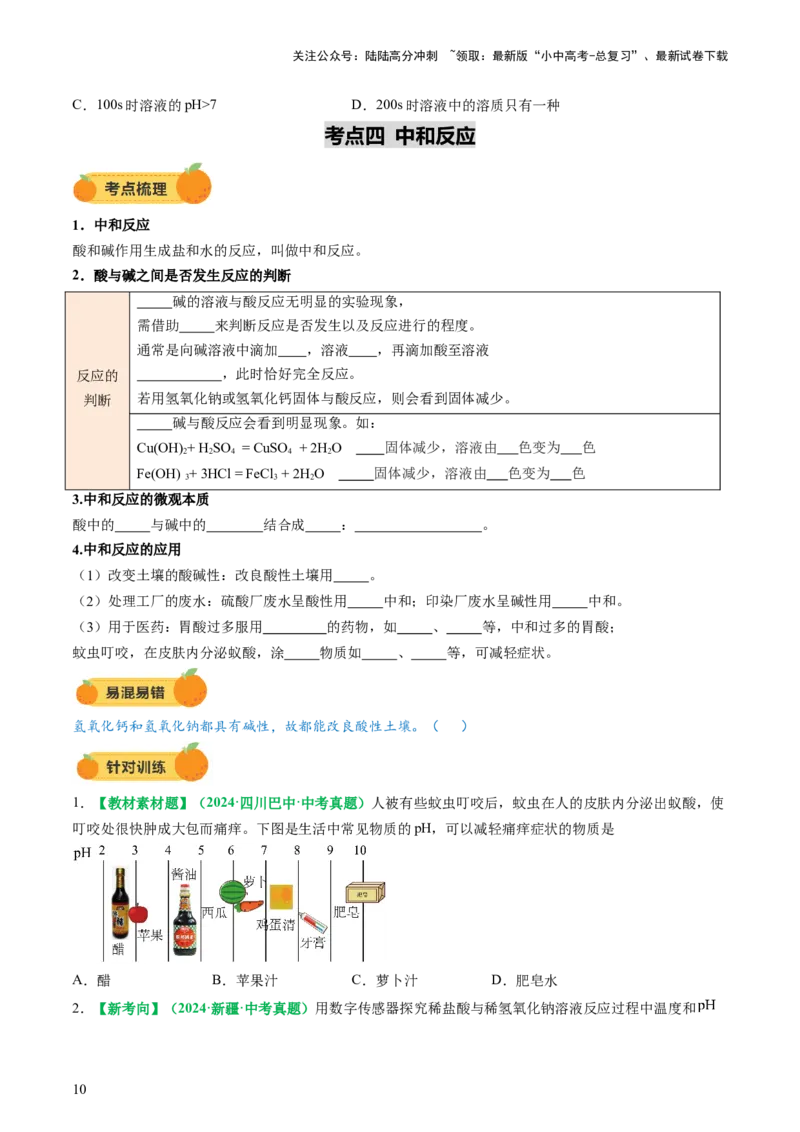
1.【教材素材题】(2024·四川巴中·中考真题)人被有些蚊虫叮咬后,蚊虫在人的皮肤内分泌出蚁酸,使
叮咬处很快肿成大包而痛痒。下图是生活中常见物质的pH,可以减轻痛痒症状的物质是
A.醋 B.苹果汁 C.萝卜汁 D.肥皂水
2.【新考向】(2024·新疆·中考真题)用数字传感器探究稀盐酸与稀氢氧化钠溶液反应过程中温度和
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
的变化,测定结果如图所示。下列说法正确的是
A.该反应为吸热反应
B.反应过程中,溶液的酸性逐渐增强
C.该实验是向稀氢氧化钠溶液中加入稀盐酸
D. 时,稀盐酸与稀氢氧化钠溶液恰好完全反应
题型一 溶液的酸碱性与pH
►考向01常见酸碱指示剂及变色情况
1.(2024·上海·中考真题)下列物质中能使石蕊试液变红的是
A.石灰水 B.食盐水 C.白醋 D.酒精
2.【新素材】(2024·江苏扬州·中考真题)室温下,维生素C的水溶液能使紫色石蕊试液变红。其水溶液
的酸碱性是
A.酸性 B.中性 C.碱性 D.无法判断
►考向02自制酸碱指示剂
3.【新素材】(2023·江苏常州·中考真题)唐代流行服饰石榴裙因其颜色类似石榴花的红色而得名,古法
染色工艺记载:“取石榴之花,入白细杵之,得厚汁,加之以醋或乌梅汁,以之染布,不可加热,尽赤,
可为石榴裙也。”下列说法不正确的是
A.石榴花捣碎出汁后可提取红色染料
B.加酸性物质有利于红色素浸染布料
C.石榴花中红色染料受热有利于上色
D.古法制石榴裙不宜与碱性物质接触
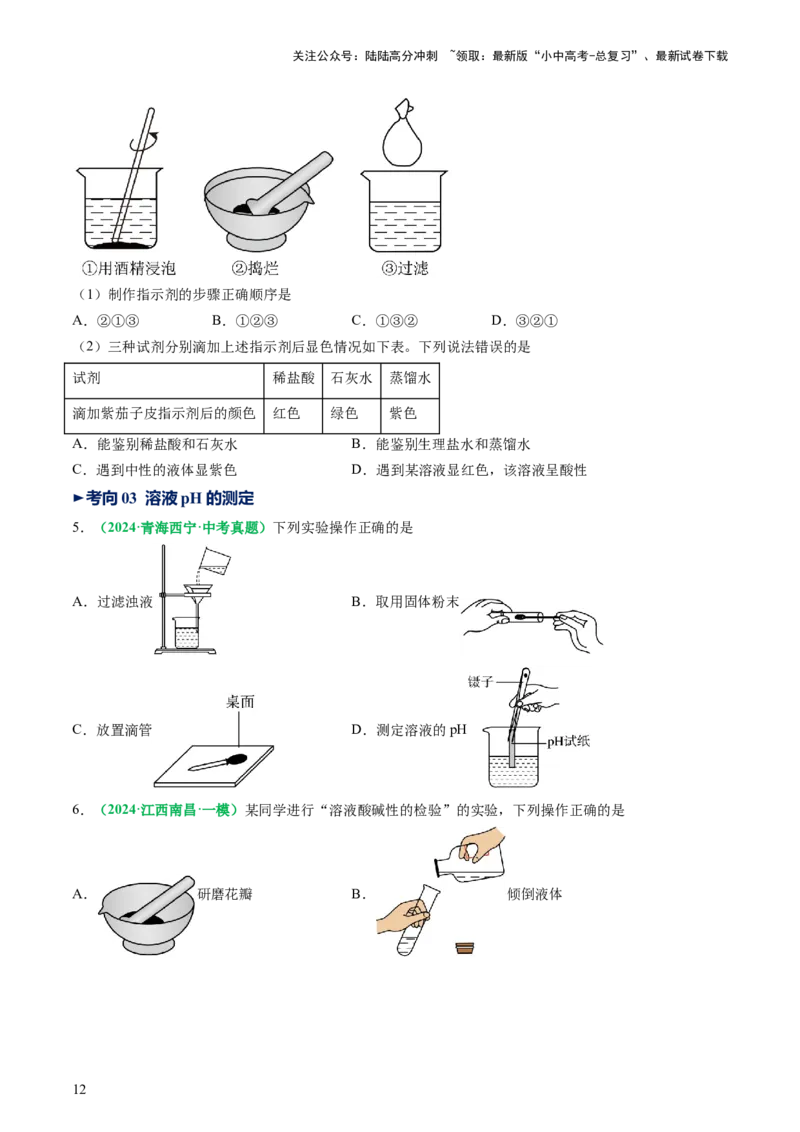
4.【新素材】(2024·内蒙古赤峰·二模)某校研究性学习小组用茄子皮在实验室制作酸碱指示剂,相关步
骤如下,完成下面小题。
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)制作指示剂的步骤正确顺序是
A.②①③ B.①②③ C.①③② D.③②①
(2)三种试剂分别滴加上述指示剂后显色情况如下表。下列说法错误的是
试剂 稀盐酸 石灰水 蒸馏水
滴加紫茄子皮指示剂后的颜色 红色 绿色 紫色
A.能鉴别稀盐酸和石灰水 B.能鉴别生理盐水和蒸馏水
C.遇到中性的液体显紫色 D.遇到某溶液显红色,该溶液呈酸性
►考向03 溶液pH的测定
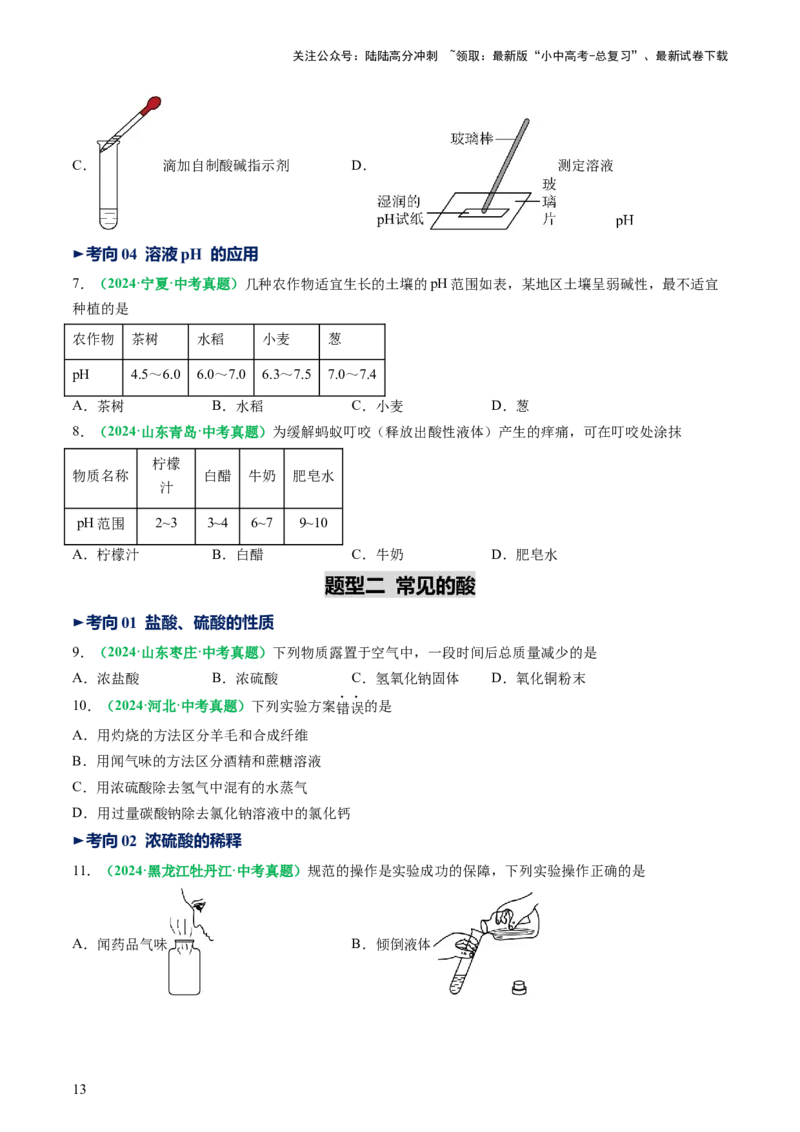
5.(2024·青海西宁·中考真题)下列实验操作正确的是
A.过滤浊液 B.取用固体粉末
C.放置滴管 D.测定溶液的pH
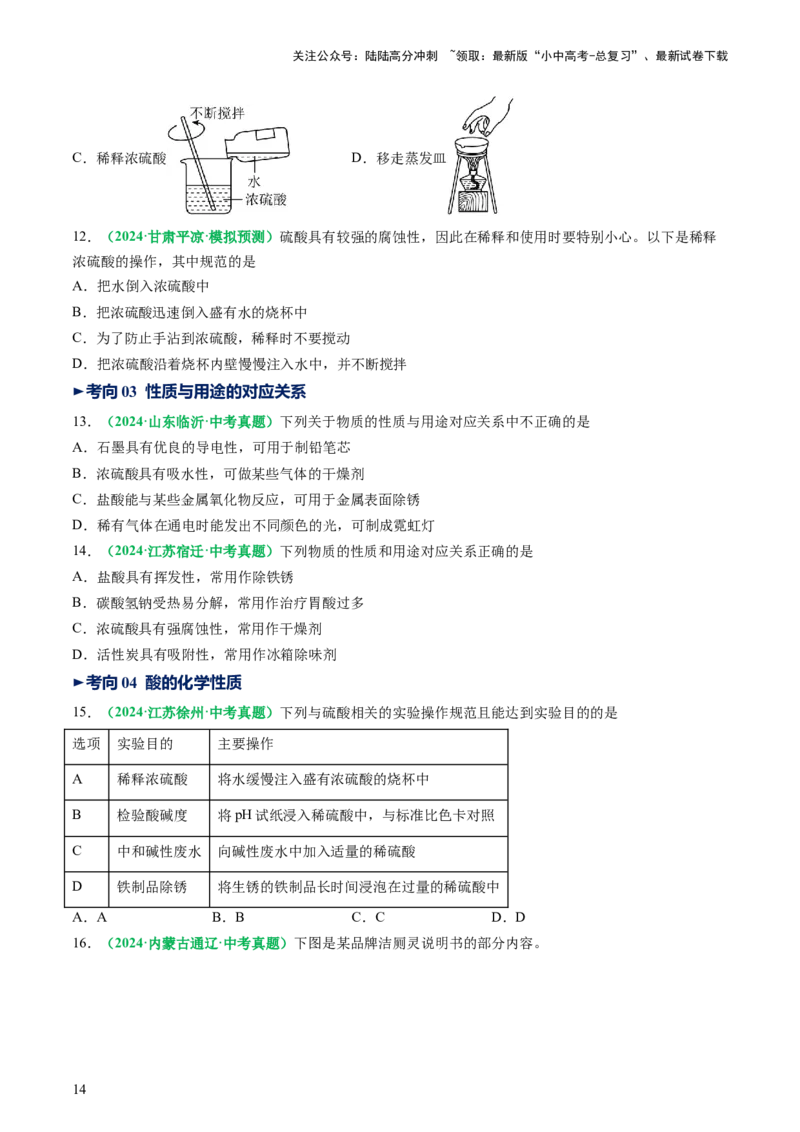
6.(2024·江西南昌·一模)某同学进行“溶液酸碱性的检验”的实验,下列操作正确的是
A. 研磨花瓣 B. 倾倒液体
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C. 滴加自制酸碱指示剂 D. 测定溶液
►考向04 溶液pH 的应用
7.(2024·宁夏·中考真题)几种农作物适宜生长的土壤的pH范围如表,某地区土壤呈弱碱性,最不适宜
种植的是
农作物 茶树 水稻 小麦 葱
pH 4.5~6.0 6.0~7.0 6.3~7.5 7.0~7.4
A.茶树 B.水稻 C.小麦 D.葱
8.(2024·山东青岛·中考真题)为缓解蚂蚁叮咬(释放出酸性液体)产生的痒痛,可在叮咬处涂抹
柠檬
物质名称 白醋 牛奶 肥皂水
汁
pH范围 2~3 3~4 6~7 9~10
A.柠檬汁 B.白醋 C.牛奶 D.肥皂水
题型二 常见的酸
►考向01 盐酸、硫酸的性质
9.(2024·山东枣庄·中考真题)下列物质露置于空气中,一段时间后总质量减少的是
A.浓盐酸 B.浓硫酸 C.氢氧化钠固体 D.氧化铜粉末
10.(2024·河北·中考真题)下列实验方案错误的是
A.用灼烧的方法区分羊毛和合成纤维
B.用闻气味的方法区分酒精和蔗糖溶液
C.用浓硫酸除去氢气中混有的水蒸气
D.用过量碳酸钠除去氯化钠溶液中的氯化钙
►考向02 浓硫酸的稀释
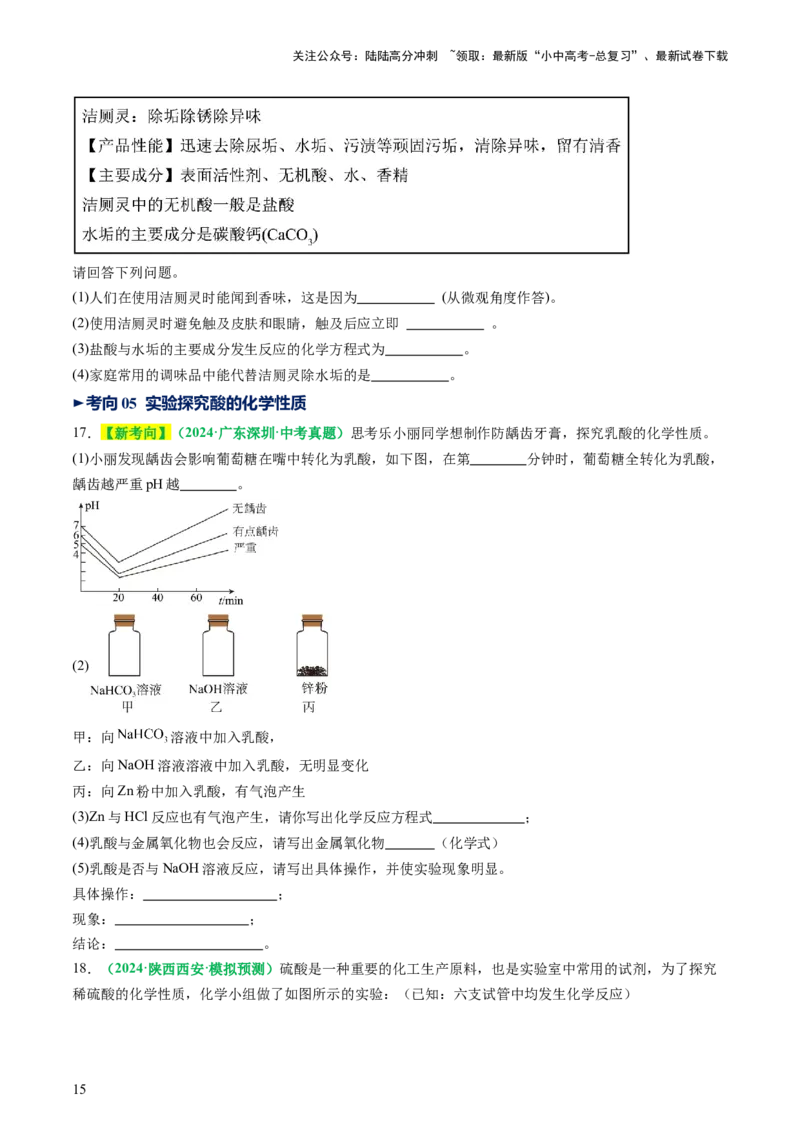
11.(2024·黑龙江牡丹江·中考真题)规范的操作是实验成功的保障,下列实验操作正确的是
A.闻药品气味 B.倾倒液体
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C.稀释浓硫酸 D.移走蒸发皿
12.(2024·甘肃平凉·模拟预测)硫酸具有较强的腐蚀性,因此在稀释和使用时要特别小心。以下是稀释
浓硫酸的操作,其中规范的是
A.把水倒入浓硫酸中
B.把浓硫酸迅速倒入盛有水的烧杯中
C.为了防止手沾到浓硫酸,稀释时不要搅动
D.把浓硫酸沿着烧杯内壁慢慢注入水中,并不断搅拌
►考向03 性质与用途的对应关系
13.(2024·山东临沂·中考真题)下列关于物质的性质与用途对应关系中不正确的是
A.石墨具有优良的导电性,可用于制铅笔芯
B.浓硫酸具有吸水性,可做某些气体的干燥剂
C.盐酸能与某些金属氧化物反应,可用于金属表面除锈
D.稀有气体在通电时能发出不同颜色的光,可制成霓虹灯
14.(2024·江苏宿迁·中考真题)下列物质的性质和用途对应关系正确的是
A.盐酸具有挥发性,常用作除铁锈
B.碳酸氢钠受热易分解,常用作治疗胃酸过多
C.浓硫酸具有强腐蚀性,常用作干燥剂
D.活性炭具有吸附性,常用作冰箱除味剂
►考向04 酸的化学性质
15.(2024·江苏徐州·中考真题)下列与硫酸相关的实验操作规范且能达到实验目的的是
选项 实验目的 主要操作
A 稀释浓硫酸 将水缓慢注入盛有浓硫酸的烧杯中
B 检验酸碱度 将pH试纸浸入稀硫酸中,与标准比色卡对照
C 中和碱性废水 向碱性废水中加入适量的稀硫酸
D 铁制品除锈 将生锈的铁制品长时间浸泡在过量的稀硫酸中
A.A B.B C.C D.D
16.(2024·内蒙古通辽·中考真题)下图是某品牌洁厕灵说明书的部分内容。
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
请回答下列问题。
(1)人们在使用洁厕灵时能闻到香味,这是因为 (从微观角度作答)。
(2)使用洁厕灵时避免触及皮肤和眼睛,触及后应立即 。
(3)盐酸与水垢的主要成分发生反应的化学方程式为 。
(4)家庭常用的调味品中能代替洁厕灵除水垢的是 。
►考向05 实验探究酸的化学性质
17.【新考向】(2024·广东深圳·中考真题)思考乐小丽同学想制作防龋齿牙膏,探究乳酸的化学性质。
(1)小丽发现龋齿会影响葡萄糖在嘴中转化为乳酸,如下图,在第 分钟时,葡萄糖全转化为乳酸,
龋齿越严重pH越 。
(2)
甲:向 溶液中加入乳酸,
乙:向NaOH溶液溶液中加入乳酸,无明显变化
丙:向Zn粉中加入乳酸,有气泡产生
(3)Zn与HCl反应也有气泡产生,请你写出化学反应方程式 ;
(4)乳酸与金属氧化物也会反应,请写出金属氧化物 (化学式)
(5)乳酸是否与NaOH溶液反应,请写出具体操作,并使实验现象明显。
具体操作: ;
现象: ;
结论: 。
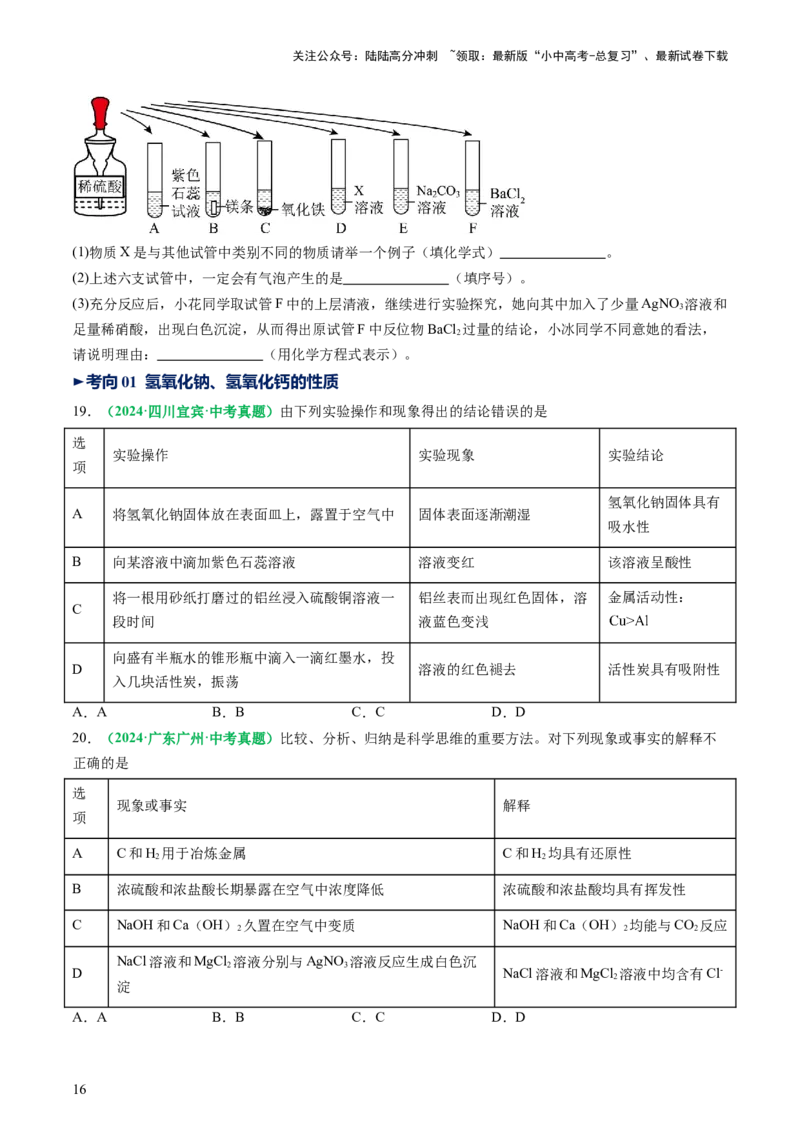
18.(2024·陕西西安·模拟预测)硫酸是一种重要的化工生产原料,也是实验室中常用的试剂,为了探究
稀硫酸的化学性质,化学小组做了如图所示的实验:(已知:六支试管中均发生化学反应)
15关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)物质X是与其他试管中类别不同的物质请举一个例子(填化学式) 。
(2)上述六支试管中,一定会有气泡产生的是 (填序号)。
(3)充分反应后,小花同学取试管F中的上层清液,继续进行实验探究,她向其中加入了少量AgNO 溶液和
3
足量稀硝酸,出现白色沉淀,从而得出原试管F中反位物BaCl 过量的结论,小冰同学不同意她的看法,
2
请说明理由: (用化学方程式表示)。
►考向01 氢氧化钠、氢氧化钙的性质
19.(2024·四川宜宾·中考真题)由下列实验操作和现象得出的结论错误的是
选
实验操作 实验现象 实验结论
项
氢氧化钠固体具有
A 将氢氧化钠固体放在表面皿上,露置于空气中 固体表面逐渐潮湿
吸水性
B 向某溶液中滴加紫色石蕊溶液 溶液变红 该溶液呈酸性
将一根用砂纸打磨过的铝丝浸入硫酸铜溶液一 铝丝表而出现红色固体,溶 金属活动性:
C
段时间 液蓝色变浅
向盛有半瓶水的锥形瓶中滴入一滴红墨水,投
D 溶液的红色褪去 活性炭具有吸附性
入几块活性炭,振荡
A.A B.B C.C D.D
20.(2024·广东广州·中考真题)比较、分析、归纳是科学思维的重要方法。对下列现象或事实的解释不
正确的是
选
现象或事实 解释
项
A C和H 用于冶炼金属 C和H 均具有还原性
2 2
B 浓硫酸和浓盐酸长期暴露在空气中浓度降低 浓硫酸和浓盐酸均具有挥发性
C NaOH和Ca(OH) 久置在空气中变质 NaOH和Ca(OH) 均能与CO 反应
2 2 2
NaCl溶液和MgCl 溶液分别与AgNO 溶液反应生成白色沉
2 3
D NaCl溶液和MgCl 溶液中均含有Cl-
2
淀
A.A B.B C.C D.D
16关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
►考向02性质与用途的对应关系
21.(2024·江苏无锡·中考真题)下列物质的性质和用途对应关系正确的是
A.氧气具有氧化性,用作燃料 B.干冰升华吸热,用于人工降雨
C.浓盐酸具有挥发性,用作除锈剂 D.氢氧化钠具有碱性,用于治疗胃酸过多
22.(2024·山东菏泽·中考真题)物质的性质决定用途,下列物质的性质与用途对应关系表述合理的是
A.熟石灰能与酸反应——改良酸性土壤
B.一氧化碳有可燃性——冶炼金属
C.氧气能助燃——用作燃料
D.碳酸氢铵受热易分解——用作氮肥
►考向03 碱的化学性质
23.【新考向】(2024·内蒙古通辽·中考真题)物质的结构决定性质。氢氧化锂(LiOH)与氢氧化钠(NaOH)
结构相似,性质相似。关于 LiOH,下列说法不正确的是
A.能使紫色石蕊溶液变红 B.能与硫酸发生化学反应
C.能与硫酸铜发生化学反应 D.水溶液中含有氢氧根离子
24.【跨学科】(2024·江苏镇江·中考真题)NaOH是重要的化工原料,对其性质作如下探究。
实验①:将适量NaOH固体溶于水,搅拌、测量温度。
实验②:取适量实验①中的溶液加入如图烧杯中,闭合开关。
实验③:向试管中加入适量实验①中的溶液,滴加2~3滴酚酞试液,再加入稀盐酸,振荡。
实验④:取少量硫酸铵放在试管中,加入适量实验①中的溶液,微热。
下列说法不正确的是
A.实验①中温度升高,说明NaOH固体溶解放热
B.实验②中小灯泡发光,说明NaOH溶解时生成自由移动的离子
C.实验③中溶液由红色变成无色,说明溶液恰好呈中性
D.实验④中产生氨臭气味,该反应为2NaOH+(NH )SO NaSO +2NH↑+2H O
4 2 4 2 4 3 2
►考向05 实验探究碱的化学性质
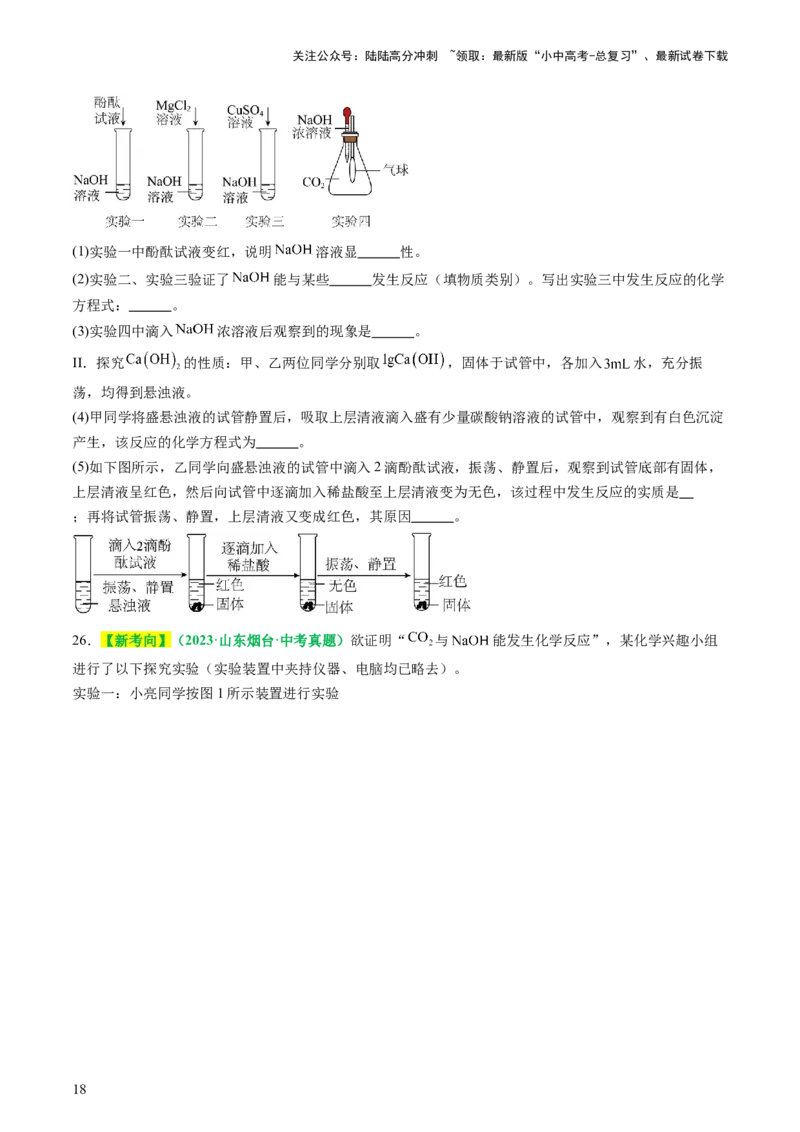
25.【新考向】(2023·江苏宿迁·中考真题)学习小组在老师的指导下对氢氧化钠、氧氧化钙的性质进行
探究。
I.探究 的性质:同学们设计如图所示实验。
17关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)实验一中酚酞试液变红,说明 溶液显 性。
(2)实验二、实验三验证了 能与某些 发生反应(填物质类别)。写出实验三中发生反应的化学
方程式: 。
(3)实验四中滴入 浓溶液后观察到的现象是 。
II.探究 的性质:甲、乙两位同学分别取 ,固体于试管中,各加入 水,充分振
荡,均得到悬浊液。
(4)甲同学将盛悬浊液的试管静置后,吸取上层清液滴入盛有少量碳酸钠溶液的试管中,观察到有白色沉淀
产生,该反应的化学方程式为 。
(5)如下图所示,乙同学向盛悬浊液的试管中滴入2滴酚酞试液,振荡、静置后,观察到试管底部有固体,
上层清液呈红色,然后向试管中逐滴加入稀盐酸至上层清液变为无色,该过程中发生反应的实质是
;再将试管振荡、静置,上层清液又变成红色,其原因 。
26.【新考向】(2023·山东烟台·中考真题)欲证明“ 与 能发生化学反应”,某化学兴趣小组
进行了以下探究实验(实验装置中夹持仪器、电脑均已略去)。
实验一:小亮同学按图1所示装置进行实验
18关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
实验前 型管两端液面相平,将 溶液滴入试管中,待反应后恢复到室温, 型管中的液面左高右
低。
(1)小亮同学根据 型管中液面高度变化得出结论: 与 发生了化学反应,该反应的化学方程式是
。
(2)小明认为仅凭 型管中液面高度变化,不足以得出” 与 发生了化学反应”的结论,理由是
。
实验二:为获得充足的证据,兴趣小组设计了图2所示装置进行实验探究,并利用压强传感器测定实验过
程中三颈瓶内压强的变化。
按图2所示,打开压强传感器,观察到三颈瓶内初始压强为 ,将滴有酚酞试液的适量氢氧化钠溶液
快速推入瓶内,振荡充分反应。待压强不再减小后,再将适量的稀盐酸快速推入瓶内,振荡充分反应。待
压强不再增大后,将两个注射器活塞先后拉回原位(不进行活塞操作时,活塞不能自主移动)。瓶内压强
变化如图3所示。
(3)滴有酚酞试液的 溶液呈 色。
(4)向瓶内推入适量稀盐酸后,能证明 与 已发生了反应的现象是 ,产生此现象的反应的
化学方程式是 。
(5)图3中, (填序号)段的压强比初始压强低,说明瓶内的水能吸收 。
① 段 ② 段 ③ 段
19关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(6)图3中, 段压强远低于 段压强,能够说明 。
题型四 中和反应
►考向01 无明显现象中和反应的判断
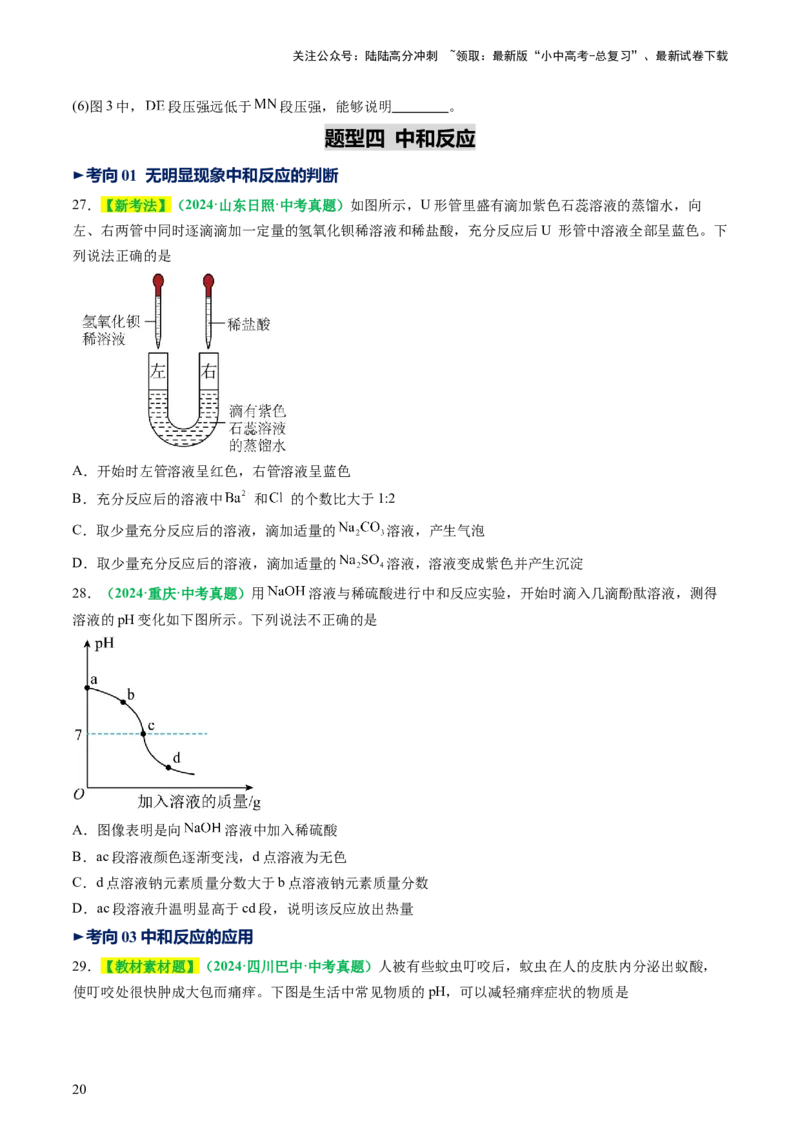
27.【新考法】(2024·山东日照·中考真题)如图所示,U形管里盛有滴加紫色石蕊溶液的蒸馏水,向
左、右两管中同时逐滴滴加一定量的氢氧化钡稀溶液和稀盐酸,充分反应后U 形管中溶液全部呈蓝色。下
列说法正确的是
A.开始时左管溶液呈红色,右管溶液呈蓝色
B.充分反应后的溶液中 和 的个数比大于1:2
C.取少量充分反应后的溶液,滴加适量的 溶液,产生气泡
D.取少量充分反应后的溶液,滴加适量的 溶液,溶液变成紫色并产生沉淀
28.(2024·重庆·中考真题)用 溶液与稀硫酸进行中和反应实验,开始时滴入几滴酚酞溶液,测得
溶液的pH变化如下图所示。下列说法不正确的是
A.图像表明是向 溶液中加入稀硫酸
B.ac段溶液颜色逐渐变浅,d点溶液为无色
C.d点溶液钠元素质量分数大于b点溶液钠元素质量分数
D.ac段溶液升温明显高于cd段,说明该反应放出热量
►考向03中和反应的应用
29.【教材素材题】(2024·四川巴中·中考真题)人被有些蚊虫叮咬后,蚊虫在人的皮肤内分泌出蚁酸,
使叮咬处很快肿成大包而痛痒。下图是生活中常见物质的pH,可以减轻痛痒症状的物质是
20关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.醋 B.苹果汁 C.萝卜汁 D.肥皂水
30.(2024·山东日照·中考真题)下列物质的性质与用途对应关系错误的是
选项 物质 性质 用途
A 甲烷 可燃性 作燃料
B 石墨 质软且滑 制作电极
C 氮气 化学性质不活泼 焊接金属时作保护气
D 熟石灰 碱性 处理含有硫酸的污水
A.A B.B C.C D.D
21