文档内容
D. 鉴别NaBr和KI溶液 分别加新制氯水后,用CCl 萃取
2017年天津市高考化学试卷 4
A.A B.B C.C D.D
一、本卷共6题,每题6分,共36分.在每题给出的四个选项中,只有一项是最符合题目要求的.
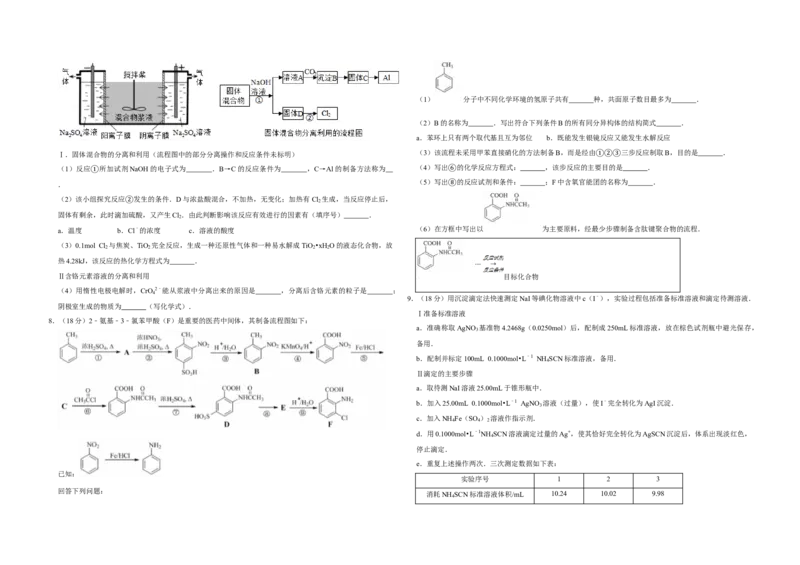
5.(6分)根据元素周期表和元素周期律,判断下列叙述不正确的是( )
1.(6分)下列有关水处理方法不正确的是( )
A.气态氢化物的稳定性:H O>NH >SiH
2 3 4
A.用石灰、碳酸钠等碱性物质处理废水中的酸
B.氢元素与其他元素可形成共价化合物或离子化合物
B.用可溶性的铝盐和铁盐处理水中的悬浮物
C.用氯气处理水中的Cu2+、Hg2+等重金属离子
D.用烧碱处理含高浓度NH +的废水并回收利用氨
4
2.(6分)汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用.下列有关汉黄芩素的
叙述正确的是( )
C. 如图所示实验可证明元素的非金属性:Cl>C>Si
D.用中文“ ”(ào)命名的第118号元素在周期表中位于第七周期0族
6.(6分)常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g) Ni(CO) (g).230℃时,该反应的平衡
4
A.汉黄芩素的分子式为C 16 H 13 O 5 常数K=2×10﹣5.已知:Ni(CO) 的沸点为42.2℃,固体杂质⇌不参与反应。
4
B.该物质遇FeCl
3
溶液显色
第一阶段:将粗镍与CO反应转化成气态Ni(CO) ;
4
C.1 mol该物质与溴水反应,最多消耗1mol Br 2 第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
D.与足量H 2 发生加成反应后,该分子中官能团的种类减少1种 下列判断正确的是( )
3.(6分)下列能量转化过程与氧化还原反应无关的是( ) A.增加c(CO),平衡向正向移动,反应的平衡常数增大
A.硅太阳能电池工作时,光能转化成电能 B.第一阶段,在30℃和50℃两者之间选择反应温度,选50℃
B.锂离子电池放电时,化学能转化成电能 C.第二阶段,Ni(CO) 分解率较低
4
C.电解质溶液导电时,电能转化成化学能 D.该反应达到平衡时,v生成[Ni(CO)
4
]=4v生成 (CO)
D.葡萄糖为人类生命活动提供能量时,化学能转化成热能
二、本卷共4题,共64分.
4.(6分)以下实验设计能达到实验目的是( )
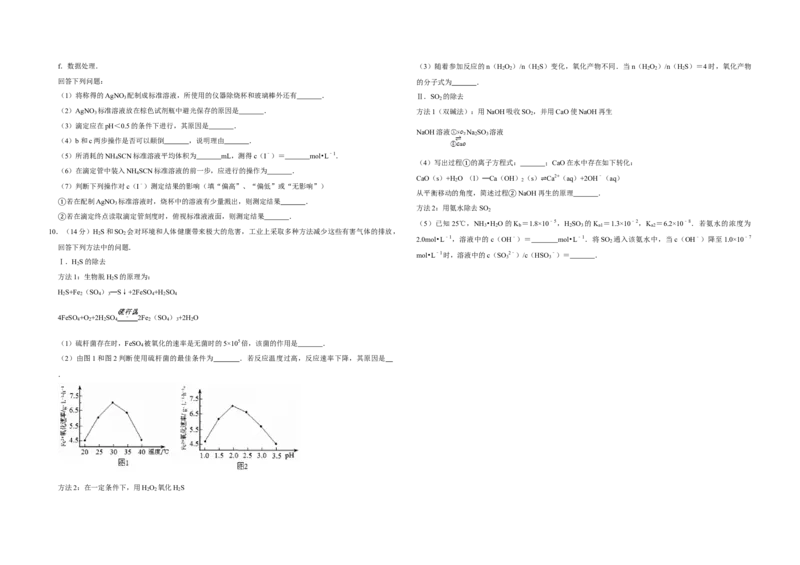
7.(14分)某混合物浆液含有Al(OH) 、MnO 和少量Na CrO .考虑到胶体的吸附作用使Na CrO 不易完
3 2 2 4 2 4
实验目的 实验设计
全被水浸出,某研究小组利用设计的电解分离装置(见图),使浆液分离成固体混合物和含铬元素溶液,并
A. 除去NaHCO 固体中的Na CO 将固体加热至恒重
3 2 3 回收利用.回答Ⅰ和Ⅱ中的问题.
B. 制备无水AlCl
3
蒸发Al与稀盐酸反应后的溶液
C. 重结晶提纯苯甲酸 将粗品水溶、过滤、蒸发、结晶(1) 分子中不同化学环境的氢原子共有 种,共面原子数目最多为 .
(2)B的名称为 .写出符合下列条件B的所有同分异构体的结构简式 .
a.苯环上只有两个取代基且互为邻位 b.既能发生银镜反应又能发生水解反应
Ⅰ.固体混合物的分离和利用(流程图中的部分分离操作和反应条件未标明) (3)该流程未采用甲苯直接硝化的方法制备B,而是经由 三步反应制取B,目的是 .
(1)反应 所加试剂NaOH的电子式为 .B→C的反应条件为 ,C→Al的制备方法称为 (4)写出 的化学反应方程式: ,该步反应的主要①目②的③是 .
. ①
(5)写出⑥的反应试剂和条件: ;F中含氧官能团的名称为 .
(2)该小组探究反应 发生的条件.D与浓盐酸混合,不加热,无变化;加热有Cl 生成,当反应停止后, ⑧
2
固体有剩余,此时滴加②硫酸,又产生Cl .由此判断影响该反应有效进行的因素有(填序号) .
2
a.温度 b.Cl﹣的浓度 c.溶液的酸度 (6)在方框中写出以 为主要原料,经最少步骤制备含肽键聚合物的流程.
(3)0.1mol Cl 与焦炭、TiO 完全反应,生成一种还原性气体和一种易水解成TiO •xH O的液态化合物,放
2 2 2 2
热4.28kJ,该反应的热化学方程式为 .
Ⅱ含铬元素溶液的分离和利用 目标化合物
(4)用惰性电极电解时,CrO 2﹣能从浆液中分离出来的原因是 ,分离后含铬元素的粒子是 ;
4
9.(18分)用沉淀滴定法快速测定NaI等碘化物溶液中c(I﹣),实验过程包括准备标准溶液和滴定待测溶液.
阴极室生成的物质为 (写化学式).
Ⅰ准备标准溶液
8.(18分)2﹣氨基﹣3﹣氯苯甲酸(F)是重要的医药中间体,其制备流程图如下:
a.准确称取AgNO 基准物4.2468g(0.0250mol)后,配制成250mL标准溶液,放在棕色试剂瓶中避光保存,
3
备用.
b.配制并标定100mL 0.1000mol•L﹣1 NH SCN标准溶液,备用.
4
Ⅱ滴定的主要步骤
a.取待测NaI溶液25.00mL于锥形瓶中.
b.加入25.00mL 0.1000mol•L﹣1 AgNO 溶液(过量),使I﹣完全转化为AgI沉淀.
3
c.加入NH Fe(SO ) 溶液作指示剂.
4 4 2
d.用0.1000mol•L﹣1NH SCN溶液滴定过量的Ag+,使其恰好完全转化为AgSCN沉淀后,体系出现淡红色,
4
停止滴定.
e.重复上述操作两次.三次测定数据如下表:
已知:
实验序号 1 2 3
回答下列问题:
消耗NH SCN标准溶液体积/mL 10.24 10.02 9.98
4f.数据处理. (3)随着参加反应的n(H O )/n(H S)变化,氧化产物不同.当n(H O )/n(H S)=4时,氧化产物
2 2 2 2 2 2
回答下列问题: 的分子式为 .
(1)将称得的AgNO
3
配制成标准溶液,所使用的仪器除烧杯和玻璃棒外还有 . Ⅱ.SO
2
的除去
(2)AgNO
3
标准溶液放在棕色试剂瓶中避光保存的原因是 . 方法1(双碱法):用NaOH吸收SO
2
,并用CaO使NaOH再生
(3)滴定应在pH<0.5的条件下进行,其原因是 .
NaOH溶液 Na SO 溶液
2 3
(4)b和c两步操作是否可以颠倒 ,说明理由 .
(5)所消耗的NH SCN标准溶液平均体积为 mL,测得c(I﹣)= mol•L﹣1.
4
(4)写出过程 的离子方程式: ;CaO在水中存在如下转化:
(6)在滴定管中装入NH SCN标准溶液的前一步,应进行的操作为 .
4
CaO(s)+H
2
O① (l)═Ca(OH)
2
(s) Ca2+(aq)+2OH﹣(aq)
(7)判断下列操作对c(I﹣)测定结果的影响(填“偏高”、“偏低”或“无影响”)
从平衡移动的角度,简述过程 NaOH再⇌生的原理 .
若在配制AgNO 标准溶液时,烧杯中的溶液有少量溅出,则测定结果 .
3
方法2:用氨水除去SO 2 ②
①若在滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果 .
(5)已知25℃,NH •H O的K =1.8×10﹣5,H SO 的K =1.3×10﹣2,K =6.2×10﹣8.若氨水的浓度为
3 2 b 2 3 a1 a2
10.②(14分)H
2
S和SO
2
会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放,
2.0mol•L﹣1,溶液中的c(OH﹣)= mol•L﹣1.将SO 通入该氨水中,当c(OH﹣)降至1.0×10﹣7
2
回答下列方法中的问题.
mol•L﹣1时,溶液中的c(SO 2﹣)/c(HSO ﹣)= .
3 3
Ⅰ.H S的除去
2
方法1:生物脱H S的原理为:
2
H S+Fe (SO ) ═S↓+2FeSO +H SO
2 2 4 3 4 2 4
4FeSO +O +2H SO 2Fe (SO ) +2H O
4 2 2 4 2 4 3 2
(1)硫杆菌存在时,FeSO 被氧化的速率是无菌时的5×105倍,该菌的作用是 .
4
(2)由图1和图2判断使用硫杆菌的最佳条件为 .若反应温度过高,反应速率下降,其原因是
.
方法2:在一定条件下,用H O 氧化H S
2 2 2