文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
主题五 常见的酸碱盐
专题 10 常见的盐
01模拟基础练
【题型一】常见的盐
【题型二】复分解反应
【题型三】化肥
02重难创新练
03真题实战练
题型一 常见的盐
1.【新考向】(2024·安徽池州·三模)“灵璧一石天下奇,声如青铜色如玉”,这是宋代诗人方岩对灵璧
石发出的由衷赞叹。灵璧石产自于安徽省宿州市灵璧县,矿石中含较多碳酸钙。下列说法错误的是
A.碳酸钙可用作补钙剂
B.碳酸钙高温分解可得到CaO和CO
2
C.碳酸钙能溶于水并放出热量
D.碳酸钙可与盐酸发生复分解反应
【新情境】(2024·广东佛山·二模)碳酸钠和碳酸氢钠都是常见的盐,在生活生产中均有广泛用途。某品
牌苏打水的标签部分内容如图,完成下面小题。
2.有关该瓶“苏打水”,说法不正确的是
A.“苏打水”呈弱碱性 B.“配料”碳酸氢钠俗称“苏打”
C.氯化钾在饮料中以 存在 D.“苏打水”瓶属于可回收垃圾
3.有关 和 说法不正确的是
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A. 广泛用于玻璃、洗涤剂等 B. 用于焙制糕点、治疗胃酸过多
C.加入足量稀盐酸能区分 和 D.侯德榜为制备 作出了杰出的贡献
4.【新考法】(2024·山东菏泽·二模)低钠盐是用氯化钠和氯化钾等为原料经科学合理配比加工而成的食
盐。它不但能降低钠盐摄入过量的问题,还可以帮助膳食中的钠、钾元素达到更好的平衡.下列说法正确
的是
A.日常生活中选择食用低钠盐能实现减钠补钾,可以大量食用
B.低钠盐中的钠指的是钠元素
C.若该盐含氯化钠70%,则摄入6g低钠盐,补充的钠元素质量为
D.氯化钾可以替代氯化钠使用
题型二 复分解反应
5.【新考向】(2024·贵州黔东南·一模)下列离子能在pH=3 的溶液中大量共存的是
A.Ba2+ 、 Na+ 、OH-、 B.Ba2+、 、Cl-、Mg2+
C.K+、Na+、 、 D. 、Ca2+、Na+、Cl-
6.(2024•广东湛江•模拟预测)下列各组物质在溶液中能大量共存,且溶液无色、透明的是
A.NaCO、CaCl 、KNO B.NaOH、KCO、NaCl
2 3 2 3 2 3
C.HCl、NaSO 、NaHCO D.CaCl 、KNO、FeCl
2 4 3 2 3 3
7.(2023·江苏镇江·中考真题)下列实验操作能达到实验目的的是
选 目
物质 主要实验操作
项 的
鉴
A H、CH 点燃,在火焰上方罩一个干冷的烧杯,观察现象
2 4
别
NaOH溶液中混有 除
B 加入适量的CaCl 溶液,振荡、静置、过滤
2
NaCO 杂
2 3
NaCO 溶液中是否含有 检
2 3
C 取样,滴加BaCl 溶液,观察现象
2
NaSO 验
2 4
KNO 和Ba(NO ) 的 分 先加入过量的KCO 溶液,搅拌、静置、过滤、洗涤,再分别向滤
3 3 2 2 3
D
混合溶液 离 液、滤渣中加入适量的稀硝酸,搅拌
A.A B.B C.C D.D
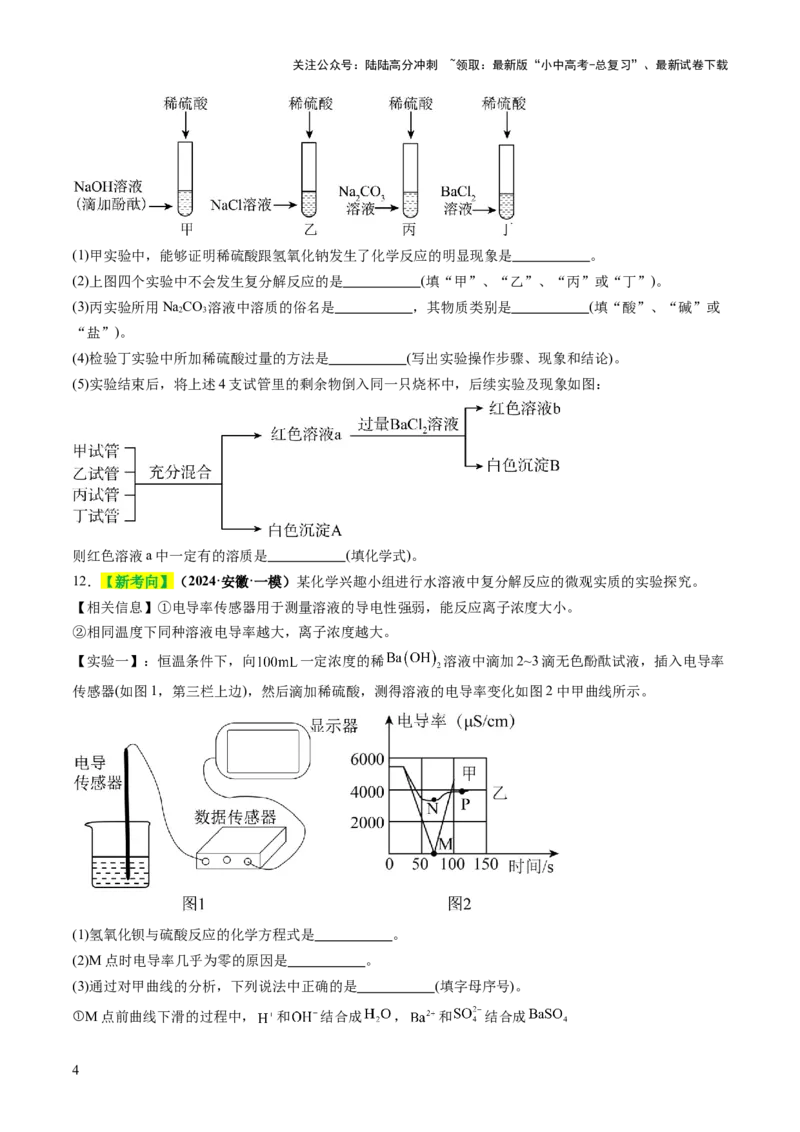
8.【新考向】(2024·江苏宿迁·二模)复分解反应的实质是离子之间通过生成水、沉淀或气体发生反应。
如图稀盐酸和氢氧化钠溶液反应的实质是 ,则图中氯化钠溶液和硝酸银溶液反应,实际参
加反应的离子是
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.Ag+、Cl- B.Ag+、 C.Na+、Cl- D.Na+、
9.(2023·江苏无锡·中考真题)某固体粉末可能由氢氧化钠、氢氧化钙、碳酸钠和碳酸钙中的一种或几种
组成,进行如下实验:①取少量固体加入足量的水,搅拌,有白色沉淀;②过滤,向滤液中加入盐酸,有
气泡产生。下列对固体粉末成分的判断中正确的是
A.一定有碳酸钙 B.一定有氢氧化钠 C.一定有碳酸钠 D.一定有氢氧化钙
10.(2024·广西南宁·一模)在学习复分解反应发生的条件后,同学们利用已学知识,对稀硫酸与下表中
四种化合物的溶液之间能否发生反应作出判断。
进行实验验证:
实验① 实验② 实验③ 实验④
物质 氢氧化钠溶液 氯化钠溶液 碳酸钾溶液 硝酸钡溶液
能否反
能 不能 能 能
应
实验现
无明显现象 无明显现象 产生气泡 _______
象
(1)根据复分解反应发生的条件,实验①中反应能发生的依据是有 生成。
(2)实验③中不发生变化的离子是 (填离子符号)。
(3)实验④中可观察到的现象是 。
(4)向装有稀硫酸的试管中先滴加少量酚酞溶液,然后滴入1-2滴氢氧化钠溶液,若观察到 的现象,
说明实验①的反应确实发生。
(5)为证明稀硫酸和氯化钠溶液不发生反应,取实验②中混合后的溶液于试管中,滴加足量硝酸钡 (将
方案补充完整,要求写出具体的方法、现象和结论)。
11.(23-24九年级下·湖南长沙·期中)某初三化学兴趣小组的同学为验证“复分解反应的条件”进行了如
图所示的甲、乙、丙、丁四个实验:
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)甲实验中,能够证明稀硫酸跟氢氧化钠发生了化学反应的明显现象是 。
(2)上图四个实验中不会发生复分解反应的是 (填“甲”、“乙”、“丙”或“丁”)。
(3)丙实验所用NaCO 溶液中溶质的俗名是 ,其物质类别是 (填“酸”、“碱”或
2 3
“盐”)。
(4)检验丁实验中所加稀硫酸过量的方法是 (写出实验操作步骤、现象和结论)。
(5)实验结束后,将上述4支试管里的剩余物倒入同一只烧杯中,后续实验及现象如图:
则红色溶液a中一定有的溶质是 (填化学式)。
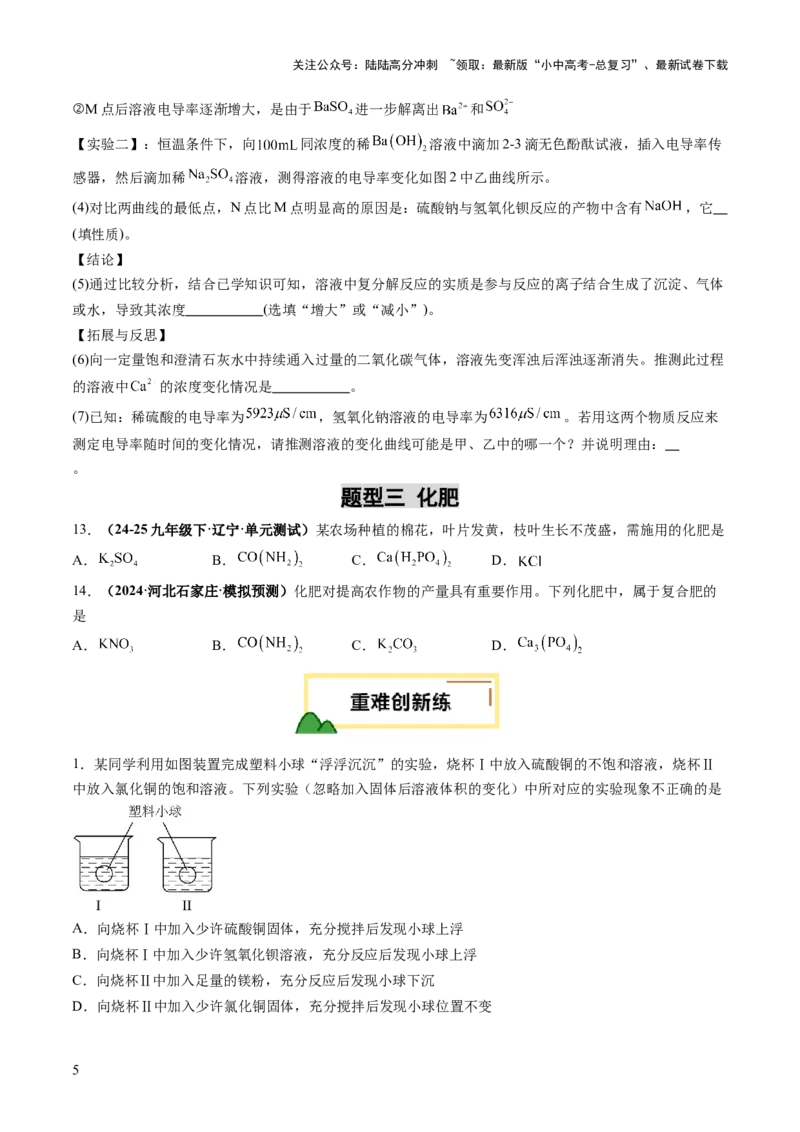
12.【新考向】(2024·安徽·一模)某化学兴趣小组进行水溶液中复分解反应的微观实质的实验探究。
【相关信息】①电导率传感器用于测量溶液的导电性强弱,能反应离子浓度大小。
②相同温度下同种溶液电导率越大,离子浓度越大。
【实验一】:恒温条件下,向 一定浓度的稀 溶液中滴加2~3滴无色酚酞试液,插入电导率
传感器(如图1,第三栏上边),然后滴加稀硫酸,测得溶液的电导率变化如图2中甲曲线所示。
(1)氢氧化钡与硫酸反应的化学方程式是 。
(2)M点时电导率几乎为零的原因是 。
(3)通过对甲曲线的分析,下列说法中正确的是 (填字母序号)。
①M点前曲线下滑的过程中, 和 结合成 , 和 结合成
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
②M点后溶液电导率逐渐增大,是由于 进一步解离出 和
【实验二】:恒温条件下,向 同浓度的稀 溶液中滴加2-3滴无色酚酞试液,插入电导率传
感器,然后滴加稀 溶液,测得溶液的电导率变化如图2中乙曲线所示。
(4)对比两曲线的最低点,N点比M点明显高的原因是:硫酸钠与氢氧化钡反应的产物中含有 ,它
(填性质)。
【结论】
(5)通过比较分析,结合已学知识可知,溶液中复分解反应的实质是参与反应的离子结合生成了沉淀、气体
或水,导致其浓度 (选填“增大”或“减小”)。
【拓展与反思】
(6)向一定量饱和澄清石灰水中持续通入过量的二氧化碳气体,溶液先变浑浊后浑浊逐渐消失。推测此过程
的溶液中 的浓度变化情况是 。
(7)已知:稀硫酸的电导率为 ,氢氧化钠溶液的电导率为 。若用这两个物质反应来
测定电导率随时间的变化情况,请推测溶液的变化曲线可能是甲、乙中的哪一个?并说明理由:
。
题型三 化肥
13.(24-25九年级下·辽宁·单元测试)某农场种植的棉花,叶片发黄,枝叶生长不茂盛,需施用的化肥是
A. B. C. D.
14.(2024·河北石家庄·模拟预测)化肥对提高农作物的产量具有重要作用。下列化肥中,属于复合肥的
是
A. B. C. D.
1.某同学利用如图装置完成塑料小球“浮浮沉沉”的实验,烧杯Ⅰ中放入硫酸铜的不饱和溶液,烧杯Ⅱ
中放入氯化铜的饱和溶液。下列实验(忽略加入固体后溶液体积的变化)中所对应的实验现象不正确的是
A.向烧杯Ⅰ中加入少许硫酸铜固体,充分搅拌后发现小球上浮
B.向烧杯Ⅰ中加入少许氢氧化钡溶液,充分反应后发现小球上浮
C.向烧杯Ⅱ中加入足量的镁粉,充分反应后发现小球下沉
D.向烧杯Ⅱ中加入少许氯化铜固体,充分搅拌后发现小球位置不变
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
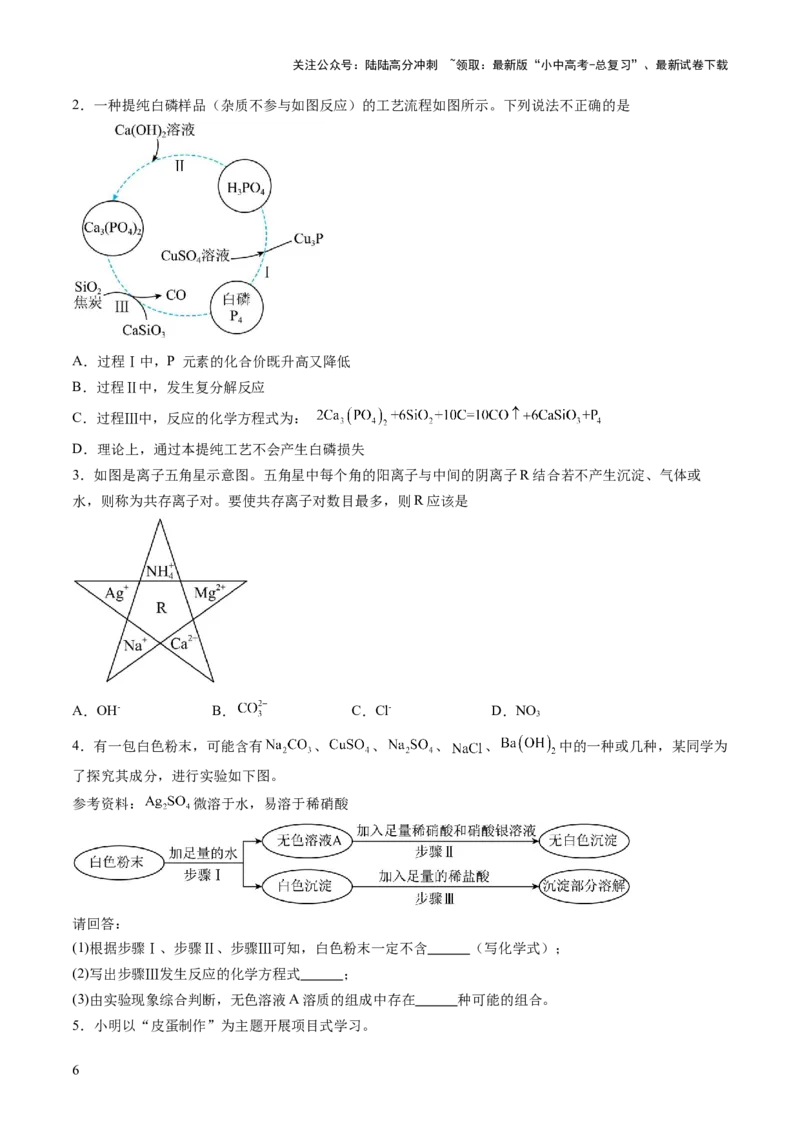
2.一种提纯白磷样品(杂质不参与如图反应)的工艺流程如图所示。下列说法不正确的是
A.过程Ⅰ中,P 元素的化合价既升高又降低
B.过程Ⅱ中,发生复分解反应
C.过程Ⅲ中,反应的化学方程式为:
D.理论上,通过本提纯工艺不会产生白磷损失
3.如图是离子五角星示意图。五角星中每个角的阳离子与中间的阴离子R结合若不产生沉淀、气体或
水,则称为共存离子对。要使共存离子对数目最多,则R应该是
A.OH- B. C.Cl- D.NO
3
4.有一包白色粉末,可能含有 、 、 、 、 中的一种或几种,某同学为
了探究其成分,进行实验如下图。
参考资料: 微溶于水,易溶于稀硝酸
请回答:
(1)根据步骤Ⅰ、步骤Ⅱ、步骤Ⅲ可知,白色粉末一定不含 (写化学式);
(2)写出步骤Ⅲ发生反应的化学方程式 ;
(3)由实验现象综合判断,无色溶液A溶质的组成中存在 种可能的组合。
5.小明以“皮蛋制作”为主题开展项目式学习。
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
一、配制皮蛋粉:将生石灰、纯碱和食盐按照一定比例混合,制成皮蛋粉。
(1)二、浸鲜蛋:向配制的皮蛋粉中加入一定量的水,将新鲜鸭蛋放入浸泡即可。向皮蛋粉中加水时,发生
反应的化学方程式有CaO+H O=Ca(OH) ;Ca(OH) +Na CO=CaCO ↓+2NaOH。充分反应后过滤,所得滤液
2 2 2 2 3 3
称为浸出液。制作时应带橡胶手套,分析浸出液中一定含有的腐蚀性物质是 。
【提出问题】浸出液中还含有哪些溶质?
【猜想与假设】
(2)猜想1:NaCl、NaOH 猜想2:NaCl、NaOH和Ca(OH) 猜想3:NaCl、NaOH和 。
2
【实验探究】
(3)为验证猜想,小明进行了如下探究。
实验方案 实验现象 实验结论
操作1:取浸出液加入试管,然后滴加足量稀盐酸 没有气泡产生 猜想 不成立
操作2:取浸出液加入试管,加入适量碳酸钠溶液 猜想2成立
【讨论交流】
(4)据复分解反应发生的条件,操作1中除可用稀盐酸外,还可选用 (填字母序号)也能达到同样
的实验目的。
a.氯化钾溶液 b.氢氧化钾溶液 c.氯化钡溶液 d.稀硫酸
(5)操作2中换作通入二氧化碳气体也可得到相同的结论,请写出相关反应的化学方程式 。
【反思拓展】
(6)制作皮蛋后的废水滴入无色酚酞溶液后,酚酞溶液显 色,直接排放会对环境造成很大的伤
害,应进行中和后再排放。
(7)制作过程中,碱液会渗入皮蛋使之略带涩味。食用时可以蘸少量 去除涩味。
1.(2024·四川南充·中考真题)下列物质的俗名、化学式、分类完全正确的是
A.水银、Hg、单质 B.熟石灰、CaO、氧化物
C.苛性钠、NaOH、盐 D.纯碱、NaCO、碱
2 3
2.(2024·广西·中考真题)我国著名化工专家侯德榜发明了联合制碱法,为纯碱工业的发展做出了杰出的
贡献。纯碱是指
A.NaOH B.Ca(OH) C.NaCO D.CaCO
2 2 3 3
3.(2024·山东滨州·中考真题)下列各组离子在 的溶液中能大量共存的是
A. B.
C. D.
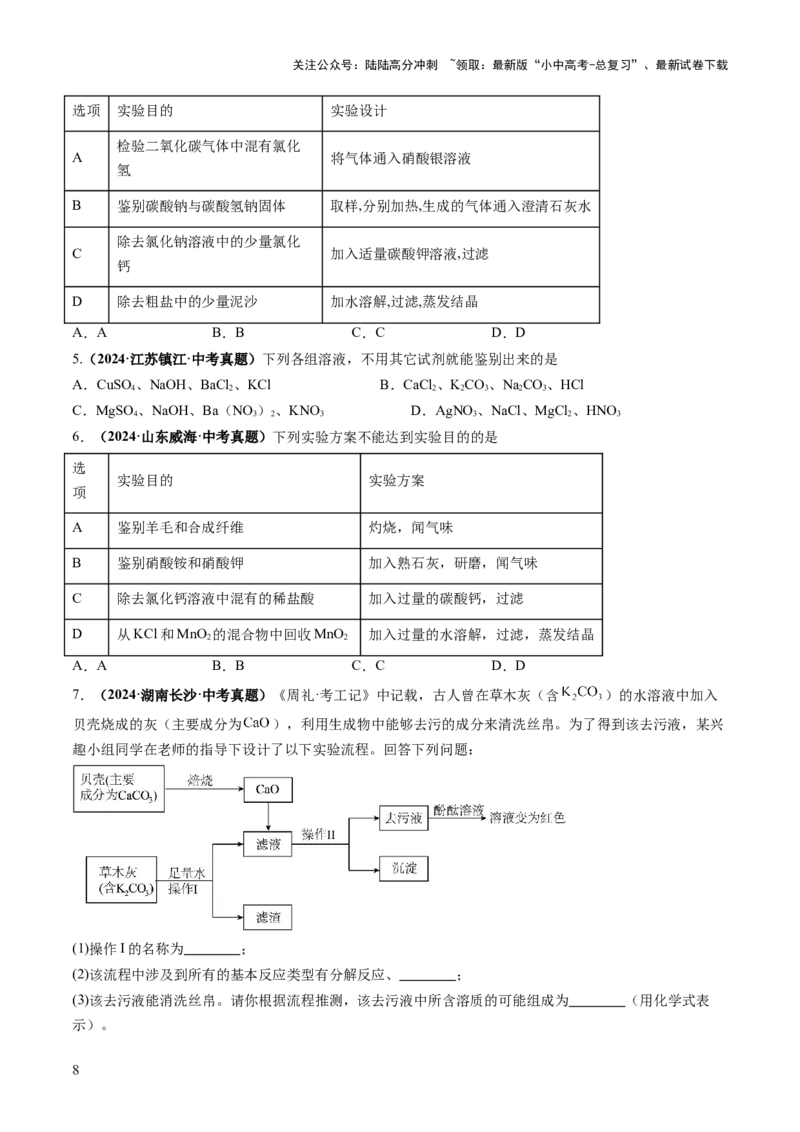
4.(2024·山东淄博·中考真题)下列有关物质检验、鉴别和除杂的实验设计,错误的是
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
选项 实验目的 实验设计
检验二氧化碳气体中混有氯化
A 将气体通入硝酸银溶液
氢
B 鉴别碳酸钠与碳酸氢钠固体 取样,分别加热,生成的气体通入澄清石灰水
除去氯化钠溶液中的少量氯化
C 加入适量碳酸钾溶液,过滤
钙
D 除去粗盐中的少量泥沙 加水溶解,过滤,蒸发结晶
A.A B.B C.C D.D
5.(2024·江苏镇江·中考真题)下列各组溶液,不用其它试剂就能鉴别出来的是
A.CuSO 、NaOH、BaCl 、KCl B.CaCl 、KCO、NaCO、HCl
4 2 2 2 3 2 3
C.MgSO 、NaOH、Ba(NO )、KNO D.AgNO、NaCl、MgCl 、HNO
4 3 2 3 3 2 3
6.(2024·山东威海·中考真题)下列实验方案不能达到实验目的的是
选
实验目的 实验方案
项
A 鉴别羊毛和合成纤维 灼烧,闻气味
B 鉴别硝酸铵和硝酸钾 加入熟石灰,研磨,闻气味
C 除去氯化钙溶液中混有的稀盐酸 加入过量的碳酸钙,过滤
D 从KCl和MnO 的混合物中回收MnO 加入过量的水溶解,过滤,蒸发结晶
2 2
A.A B.B C.C D.D
7.(2024·湖南长沙·中考真题)《周礼·考工记》中记载,古人曾在草木灰(含 )的水溶液中加入
贝壳烧成的灰(主要成分为 ),利用生成物中能够去污的成分来清洗丝帛。为了得到该去污液,某兴
趣小组同学在老师的指导下设计了以下实验流程。回答下列问题:
(1)操作I的名称为 ;
(2)该流程中涉及到所有的基本反应类型有分解反应、 ;
(3)该去污液能消洗丝帛。请你根据流程推测,该去污液中所含溶质的可能组成为 (用化学式表
示)。
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
8.(2024·湖北·中考真题) 是治疗胃酸过多症的一种抗酸药。某学习小组在室温下,对
是否适合作为抗酸药进行了如下探究。
【查阅资料】
(1)① 俗称小苏打, 俗称 。
②人体胃液(含有盐酸)通常约100mL,pH约1.5.体温约37℃。
③抗酸药的标准之一:药物发生疗效时,胃液的pH保持在3~5之间最宜,pH过高会导致胃痛等不适症
状。
【提出猜想】
(2)猜想甲: 适合作为抗酸药。其理由是 (用化学方程式表示)。
猜想乙: 不适合作为抗酸药。其原因可能是碱性较强。
【实验探究1】探究 与 碱性的强弱
(3)依次测量等浓度的 溶液和 溶液的pH,结果分别为11和9。 溶液的碱性比
溶液 (填“强”或“弱”)。
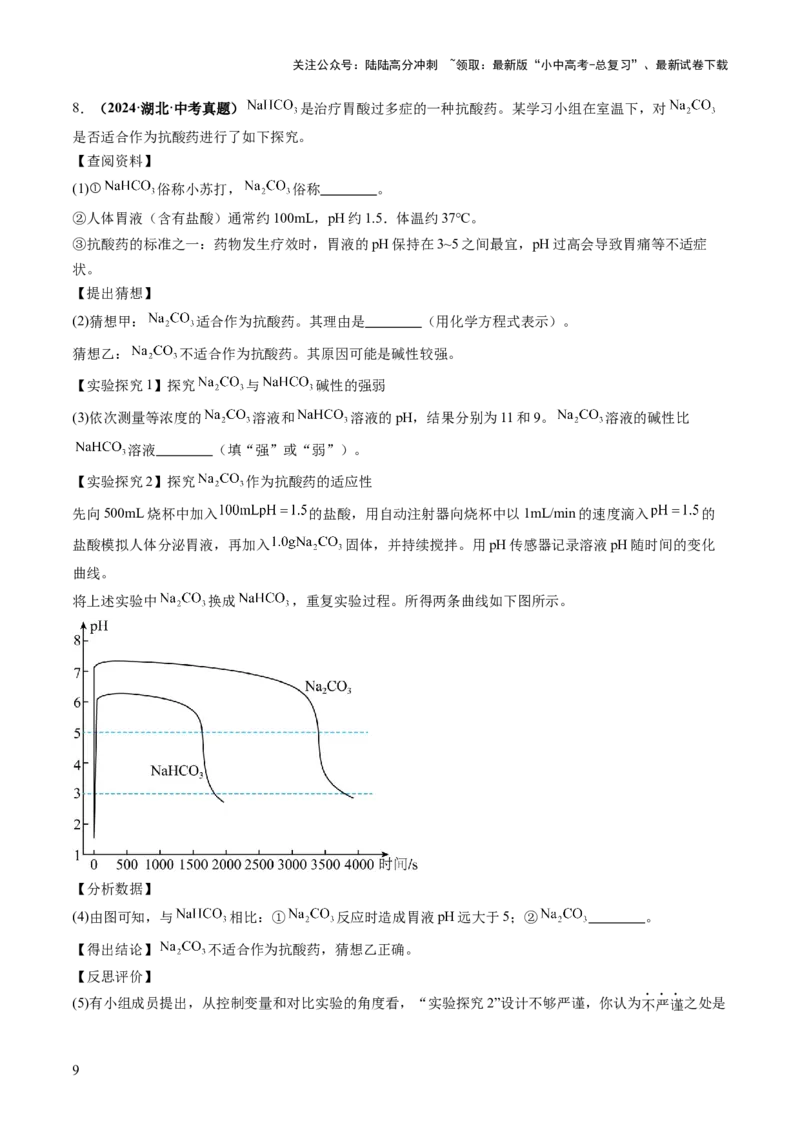
【实验探究2】探究 作为抗酸药的适应性
先向500mL烧杯中加入 的盐酸,用自动注射器向烧杯中以1mL/min的速度滴入 的
盐酸模拟人体分泌胃液,再加入 固体,并持续搅拌。用pH传感器记录溶液pH随时间的变化
曲线。
将上述实验中 换成 ,重复实验过程。所得两条曲线如下图所示。
【分析数据】
(4)由图可知,与 相比:① 反应时造成胃液pH远大于5;② 。
【得出结论】 不适合作为抗酸药,猜想乙正确。
【反思评价】
(5)有小组成员提出,从控制变量和对比实验的角度看,“实验探究2”设计不够严谨,你认为不严谨之处是
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
。
【拓展延伸】
(6) 也是一种常用的抗酸药。相比 ,从与胃酸反应的产物分析, 抗酸药存在的不
足是 。
9.(2024·四川宜宾·中考真题)某实验小组将稀盐酸逐滴加入 溶液中,观察到先无气泡,过一段
时间后产生气泡。
[问题提出]为什么滴入稀盐酸没有立即产生气泡?
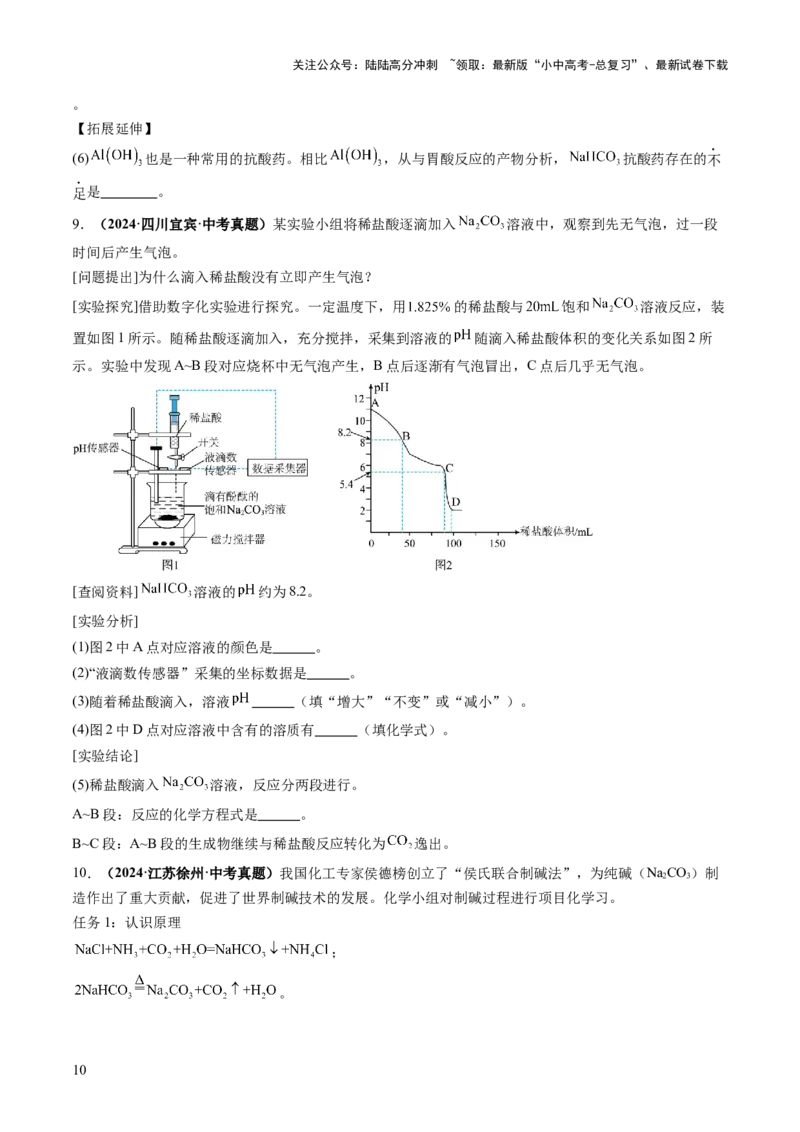
[实验探究]借助数字化实验进行探究。一定温度下,用 的稀盐酸与 饱和 溶液反应,装
置如图1所示。随稀盐酸逐滴加入,充分搅拌,采集到溶液的 随滴入稀盐酸体积的变化关系如图2所
示。实验中发现A~B段对应烧杯中无气泡产生,B点后逐渐有气泡冒出,C点后几乎无气泡。
[查阅资料] 溶液的 约为8.2。
[实验分析]
(1)图2中A点对应溶液的颜色是 。
(2)“液滴数传感器”采集的坐标数据是 。
(3)随着稀盐酸滴入,溶液 (填“增大”“不变”或“减小”)。
(4)图2中D点对应溶液中含有的溶质有 (填化学式)。
[实验结论]
(5)稀盐酸滴入 溶液,反应分两段进行。
A~B段:反应的化学方程式是 。
B~C段:A~B段的生成物继续与稀盐酸反应转化为 逸出。
10.(2024·江苏徐州·中考真题)我国化工专家侯德榜创立了“侯氏联合制碱法”,为纯碱(NaCO)制
2 3
造作出了重大贡献,促进了世界制碱技术的发展。化学小组对制碱过程进行项目化学习。
任务1:认识原理
;
。
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
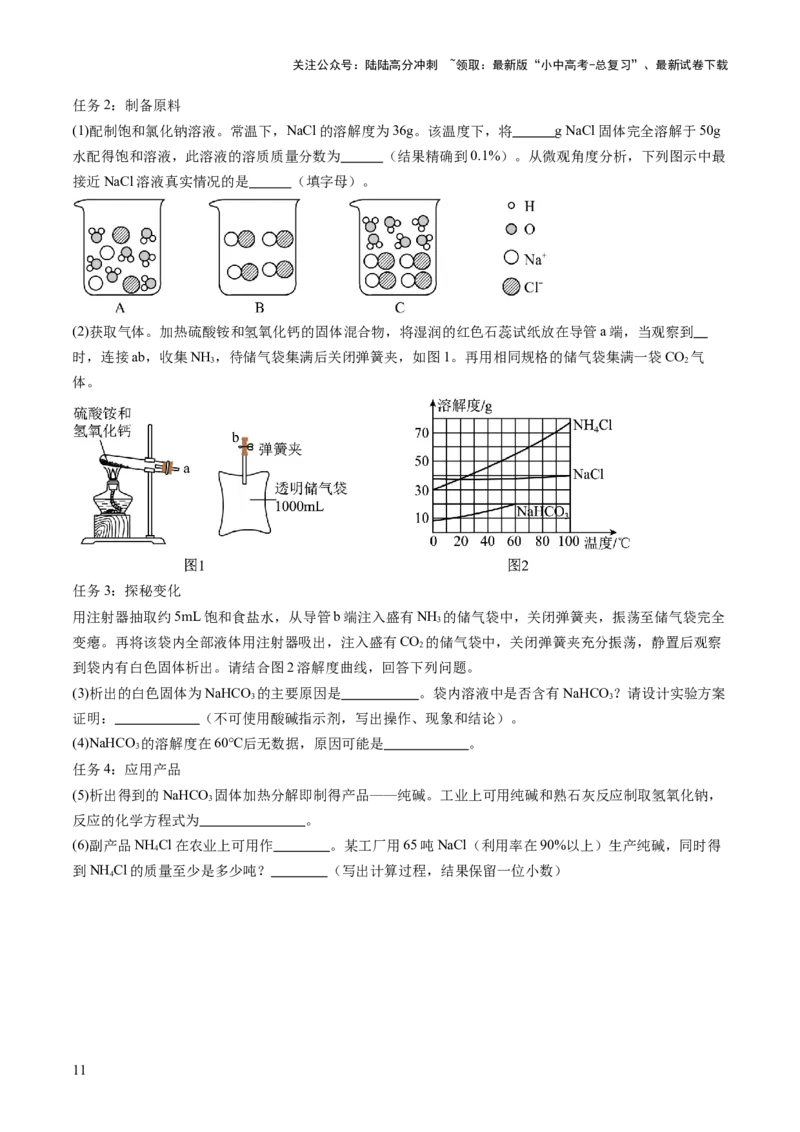
任务2:制备原料
(1)配制饱和氯化钠溶液。常温下,NaCl的溶解度为36g。该温度下,将 g NaCl固体完全溶解于50g
水配得饱和溶液,此溶液的溶质质量分数为 (结果精确到0.1%)。从微观角度分析,下列图示中最
接近NaCl溶液真实情况的是 (填字母)。
(2)获取气体。加热硫酸铵和氢氧化钙的固体混合物,将湿润的红色石蕊试纸放在导管a端,当观察到
时,连接ab,收集NH ,待储气袋集满后关闭弹簧夹,如图1。再用相同规格的储气袋集满一袋CO 气
3 2
体。
任务3:探秘变化
用注射器抽取约5mL饱和食盐水,从导管b端注入盛有NH 的储气袋中,关闭弹簧夹,振荡至储气袋完全
3
变瘪。再将该袋内全部液体用注射器吸出,注入盛有CO 的储气袋中,关闭弹簧夹充分振荡,静置后观察
2
到袋内有白色固体析出。请结合图2溶解度曲线,回答下列问题。
(3)析出的白色固体为NaHCO 的主要原因是 。袋内溶液中是否含有NaHCO ?请设计实验方案
3 3
证明: (不可使用酸碱指示剂,写出操作、现象和结论)。
(4)NaHCO 的溶解度在60℃后无数据,原因可能是 。
3
任务4:应用产品
(5)析出得到的NaHCO 固体加热分解即制得产品——纯碱。工业上可用纯碱和熟石灰反应制取氢氧化钠,
3
反应的化学方程式为 。
(6)副产品NH Cl在农业上可用作 。某工厂用65吨NaCl(利用率在90%以上)生产纯碱,同时得
4
到NH Cl的质量至少是多少吨? (写出计算过程,结果保留一位小数)
4
11