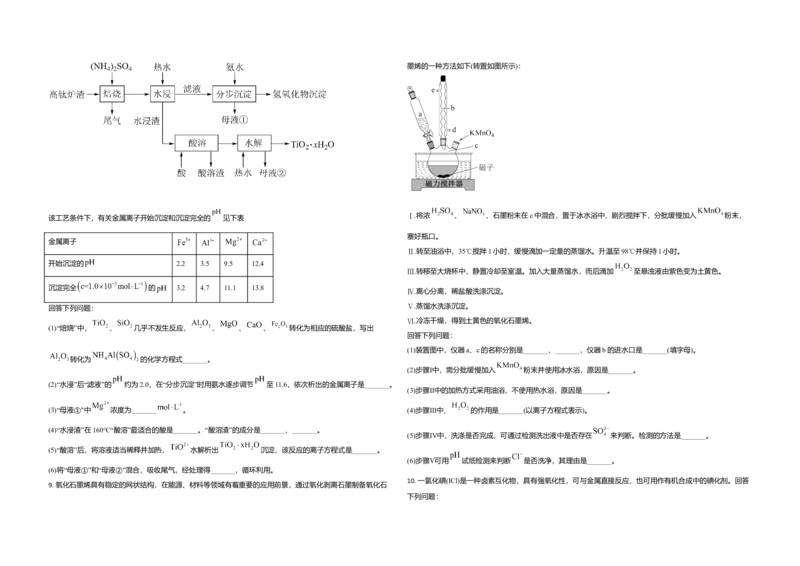文档内容
2021 年普通高等学校招生全国统一考试(全国乙卷)
化学试剂 制备的气体
化 学
A
注意事项: B (浓)
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上,并将自己的姓名、准考证号、座
C
位号填写在本试卷上。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;如需改动, D (浓)
用橡皮擦干净后,再选涂其他答案标号,涂写在本试卷上无效。
A. A B. B C. C D. D
3.作答非选择题时,将答案书写在答题卡上,书写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
3. 下列过程中的化学反应,相应的离子方程式正确的是
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Al 27 Cl35.5 Fe 56
A. 用碳酸钠溶液处理水垢中的硫酸钙:
一、选择题
1. 我国提出争取在2030年前实现碳达峰,2060年实现碳中和,这对于改善环境,实现绿色发展至关重要。碳中
B. 过量铁粉加入稀硝酸中:
.
和是指 的排放总量和减少总量相当。下列措施中能促进碳中和最直接有效的是 C 硫酸铝溶液中滴加少量氢氧化钾溶液:
A. 将重质油裂解为轻质油作为燃料
D. 氯化铜溶液中通入硫化氢:
B. 大规模开采可燃冰作为清洁燃料
C. 通过清洁煤技术减少煤燃烧污染
4. 一种活性物质的结构简式为 ,下列有关该物质的叙述正
D. 研发催化剂将 还原为甲醇
2. 在实验室采用如图装置制备气体,合理的是
确的是
A. 能发生取代反应,不能发生加成反应
B. 既是乙醇的同系物也是乙酸的同系物
C. 与 互为同分异构体
D. 该物质与碳酸钠反应得5. 我国嫦娥五号探测器带回 的月球土壤,经分析发现其构成与地球士壤类似土壤中含有的短周期元素
W、X、Y、Z,原子序数依次增大,最外层电子数之和为15,X、Y、Z为同周期相邻元素,且均不与W同族,
下列结论正确的是
A. 原子半径大小顺序为
B. 化合物XW中的化学键为离子键
C. Y单质的导电性能弱于Z单质的
D. Z的氧化物的水化物的酸性强于碳酸
6. 沿海电厂采用海水为冷却水,但在排水管中生物的附着和滋生会阻碍冷却水排放并降低冷却效率,为解决这
一问题,通常在管道口设置一对惰性电极(如图所示),通入一定的电流。
下列叙述错误的是
A. 溶液 时,
B. MA的溶度积度积
C. 溶液 时,
下列叙述错误的是
A. 阳极发生将海水中的 氧化生成 的反应
D. HA的电离常数
B. 管道中可以生成氧化灭杀附着生物的
三、非选择题:共174分。第22~32为必考题,每个试题考生都必须作答。第33~38题为选考题,
考生根据要求作答。
C. 阴极生成的 应及时通风稀释安全地排入大气
8. 磁选后的炼铁高钛炉渣,主要成分有 、 、 、 、 以及少量的 。为节约和充
D. 阳极表面形成的 等积垢需要定期清理
分利用资源,通过如下工艺流程回收钛、铝、镁等。
7. HA是一元弱酸,难溶盐MA的饱和溶液中 随c(H+)而变化, 不发生水解。实验发现, 时
为线性关系,如下图中实线所示。墨烯的一种方法如下(转置如图所示):
Ⅰ.将浓 、 、石墨粉末在c中混合,置于冰水浴中,剧烈搅拌下,分批缓慢加入 粉末,
该工艺条件下,有关金属离子开始沉淀和沉淀完全的 见下表
塞好瓶口。
金属离子
Ⅱ.转至油浴中,35℃搅拌1小时,缓慢滴加一定量的蒸馏水。升温至98℃并保持1小时。
开始沉淀的 2.2 3.5 9.5 12.4
Ⅲ.转移至大烧杯中,静置冷却至室温。加入大量蒸馏水,而后滴加 至悬浊液由紫色变为土黄色。
沉淀完全 的 3.2 4.7 11.1 13.8
Ⅳ.离心分离,稀盐酸洗涤沉淀。
Ⅴ.蒸馏水洗涤沉淀。
回答下列问题:
Ⅵ.冷冻干燥,得到土黄色的氧化石墨烯。
(1)“焙烧”中, 、 几乎不发生反应, 、 、 、 转化为相应的硫酸盐,写出
回答下列问题:
(1)装置图中,仪器a、c的名称分别是_______、_______,仪器b的进水口是_______(填字母)。
转化为 的化学方程式_______。
(2)步骤Ⅰ中,需分批缓慢加入 粉末并使用冰水浴,原因是_______。
(2)“水浸”后“滤液”的 约为2.0,在“分步沉淀”时用氨水逐步调节 至11.6,依次析出的金属离子是_______。
(3)步骤Ⅱ中的加热方式采用油浴,不使用热水浴,原因是_______。
(3)“母液①"中 浓度为_______ 。 (4)步骤Ⅲ中, 的作用是_______(以离子方程式表示)。
(4)“水浸渣”在160℃“酸溶”最适合的酸是_______。“酸溶渣”的成分是_______、_______。
(5)步骤Ⅳ中,洗涤是否完成,可通过检测洗出液中是否存在 来判断。检测的方法是_______。
(5)“酸溶”后,将溶液适当稀释并加热, 水解析出 沉淀,该反应的离子方程式是_______。
(6)步骤Ⅴ可用 试纸检测来判断 是否洗净,其理由是_______。
(6)将“母液①”和“母液②”混合,吸收尾气,经处理得_______,循环利用。
10. 一氯化碘(ICl)是一种卤素互化物,具有强氧化性,可与金属直接反应,也可用作有机合成中的碘化剂。回答
9. 氧化石墨烯具有稳定的网状结构,在能源、材料等领域有着重要的应用前景,通过氧化剥离石墨制备氧化石
下列问题:(1)历史上海藻提碘中得到一种红棕色液体,由于性质相似,Liebig误认为是ICl,从而错过了一种新元素的发现,
①由图可知,NOCl分解为NO和 反应的 _______0(填“大于”或“小于”)
该元素是_______。
②反应 的K=_______(用 、 表示):该反应的 _______0(填“大于”或“小于”),
(2)氯铂酸钡( )固体加热时部分分解为 、 和 ,376.8℃时平衡常数 ,在一
写出推理过程_______。
硬质玻璃烧瓶中加入过量 ,抽真空后,通过一支管通入碘蒸气(然后将支管封闭),在376.8℃,碘蒸气 (4)Kistiakowsky曾研究了NOCl光化学分解反应,在一定频率(v)光的照射下机理为:
初始压强为 。376.8℃平衡时,测得烧瓶中压强为 ,则 _______ ,反应
的平衡常数K=_______(列出计算式即可)。
其中 表示一个光子能量, 表示NOCl的激发态。可知,分解1mol的NOCl需要吸收_______mol光子。
(3)McMorris测定和计算了在136~180℃范围内下列反应的平衡常数 。
11. 过渡金属元素铬 是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
(1)对于基态Cr原子,下列叙述正确的是_______(填标号)。
为
A.轨道处于半充满时体系总能量低,核外电子排布应
B.4s电子能量较高,总是在比3s电子离核更远的地方运动
得到 和 均为线性关系,如下图所示: C.电负性比钾高,原子对键合电子的吸引力比钾大
(2)三价铬离子能形成多种配位化合物。 中提供电子对形成配位键的原子是_______,
中心离子的配位数为_______。
(3) 中配体分子 、 以及分子 的空间结构和相应的键角如图所示。
中P的杂化类型是_______。 的沸点比 的_______,原因是_______, 的键角小于 的,
分析原因_______。回答下列问题:
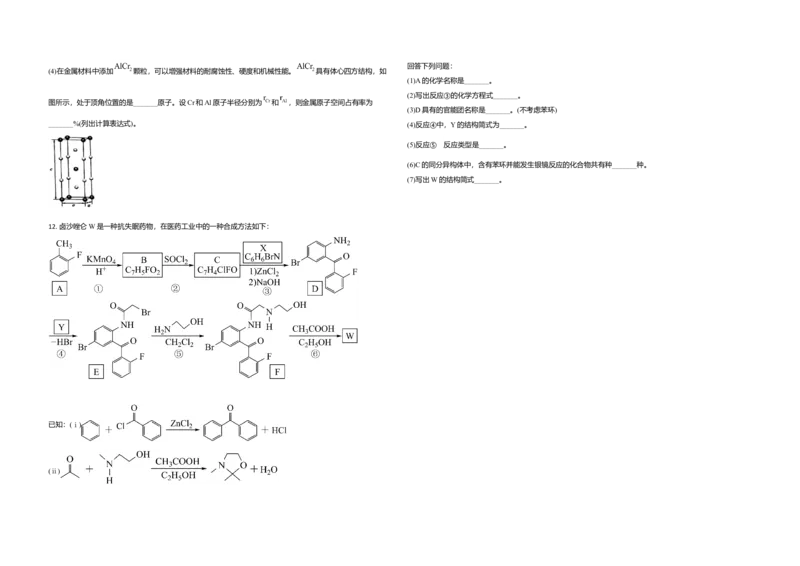
(4)在金属材料中添加 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。 具有体心四方结构,如
(1)A的化学名称是_______。
(2)写出反应③的化学方程式_______。
图所示,处于顶角位置的是_______原子。设Cr和Al原子半径分别为 和 ,则金属原子空间占有率为
(3)D具有的官能团名称是_______。(不考虑苯环)
_______%(列出计算表达式)。 (4)反应④中,Y的结构简式为_______。
的
(5)反应⑤ 反应类型是_______。
(6)C的同分异构体中,含有苯环并能发生银镜反应的化合物共有种_______种。
(7)写出W的结构简式_______。
12. 卤沙唑仑W是一种抗失眠药物,在医药工业中的一种合成方法如下:
已知:(ⅰ)
(ⅱ)