文档内容
2021 年天津市高考化学试卷
化学试题
本试卷分为第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共 100分,考试用时
60分钟。第Ⅰ卷 1至 4页,第Ⅱ卷 5至 8页。
答卷前,考生务必将自己的姓名、考生号、考场号和座位号填写在答题卡上,
并在规定位置粘贴考试用条形码。答卷时,考生务必将答案涂写在答题卡上,
答在试卷上的无效。考试结束后,将本试卷和答题卡一并交回。
祝各位考生考试顺利!
第Ⅰ卷
注意事项:
1.每题选出答案后,用铅笔将答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。
2.本卷共 12题,每题 3分,共 36分。在每题给出的四个选项中,只有一项是
最符合题目要求的。
以下数据可供解题时参考:
相对原子质量:H 1 C 12 N 14 O 16 Fe 56
1. 近年我国在科学技术领域取得了举世瞩目的成就。对下列成就所涉及的化学知识的判断
错误的是
A. 北斗三号卫星搭载了精密计时的铷原子钟,铷(Rb)是金属元素
B. 奋斗者号潜水器载人舱外壳使用了钛合金,钛合金属于无机非金属材料
C. 长征五号B遥二火箭把天和核心舱送入太空,火箭动力源于氧化还原反应
D. 天问一号探测器着陆火星过程中使用了芳纶制作的降落伞,芳纶是高分材料用
【答案】B
【解析】
【分析】
【详解】A.铷位于周期表第六周期第ⅠA族,属于碱金属,属于铷(Rb)是金属元素,故
A正确;
B.钛合金为合金,属于金属材料,故B错误;
C.火箭动力源于火箭燃料的燃烧,属于氧化还原反应,故C正确;
D.芳纶属于合成纤维,是高分子材料,故D正确;
故选B。2. 下列各组物质的晶体类型相同的是
A. SiO 和SO B. I 和NaCl C. Cu和Ag D. SiC和
2 3 2
MgO
【答案】C
【解析】
【分析】
【详解】A.SiO 为原子晶体,SO 为分子晶体,晶体类型不同,故A错误;
2 3
B.I 为分子晶体,NaCl为离子晶体,晶体类型不同,故B错误;
2
C.Cu和Ag都为金属晶体,晶体类型相同,故C正确;
D.SiC为原子晶体,MgO为离子晶体,晶体类型不同,故D错误;
故选C。
3. 核聚变发电有望成为解决人类能源问题的重要手段之一、氘(2H)是核聚变反应的主要
1
原料,下列有关叙述正确的是
A. 2H 的中子数为2 B. 2H的核电荷数为1
1 1
C. 2H是自然界中最轻的原子 D. 2H是氢元素的一种同素异形体
1 1
【答案】B
【解析】
【分析】
【详解】A.2H的中子数为2-1=1,故A错误;
1
B.2H的质子数为1,则核电荷数为1,故B正确;
1
C.自然界中最轻的原子是1H,不是2H,故C错误;
1 1
D.2H是氢元素的一种同位素,故D错误;
1
故选B。
4. 关于反应H SO +Na SO =Na SO +SO +H O所涉及的物质,下列说法错误的是
2 4 2 3 2 4 2 2
A. H SO 在该反应中为氧化剂 B. Na SO 容易被空气中的O 氧化变
2 4 2 3 2
质
C. Na SO 是含有共价键的离子化合物 D. SO 是导致酸雨的主要有害污染物
2 4 2
【答案】A
【解析】
【分析】
【详解】A.H SO +Na SO =Na SO +SO +H O中无化合价的变化,不属于氧化还原反
2 4 2 3 2 4 2 2
应,所以该反应中无氧化剂,故A错误;B.Na SO 不稳定,容易被空气中的O 氧化成硫酸钠变质,故B正确;
2 3 2
C.Na SO 含有阴阳离子,存在离子键,硫酸根中含有共价键,故C正确;
2 4
D.SO 在空去中会转化成硫酸,形成酸雨,所以二氧化硫是导致酸雨的主要有害污染物,
2
故D正确;
故选A。
5. 下列化学用语表达正确的是
A. F-的离子结构示意图:
B. 基态碳原子的轨道表示式:
C. 丙炔的键线式:
D. H O分子的球棍模型:
2
【答案】D
【解析】
【分析】
【详解】A.F-最外层有8个电子,离子结构示意图: ,故A错误;
B.基态碳原子的轨道表示式: ,故B错误;
C.丙炔的三个碳原子在一条线上,故C错误;
D.H O分子的空间构型为V型,所以球棍模型为: ,故D正确;
2
故选D。
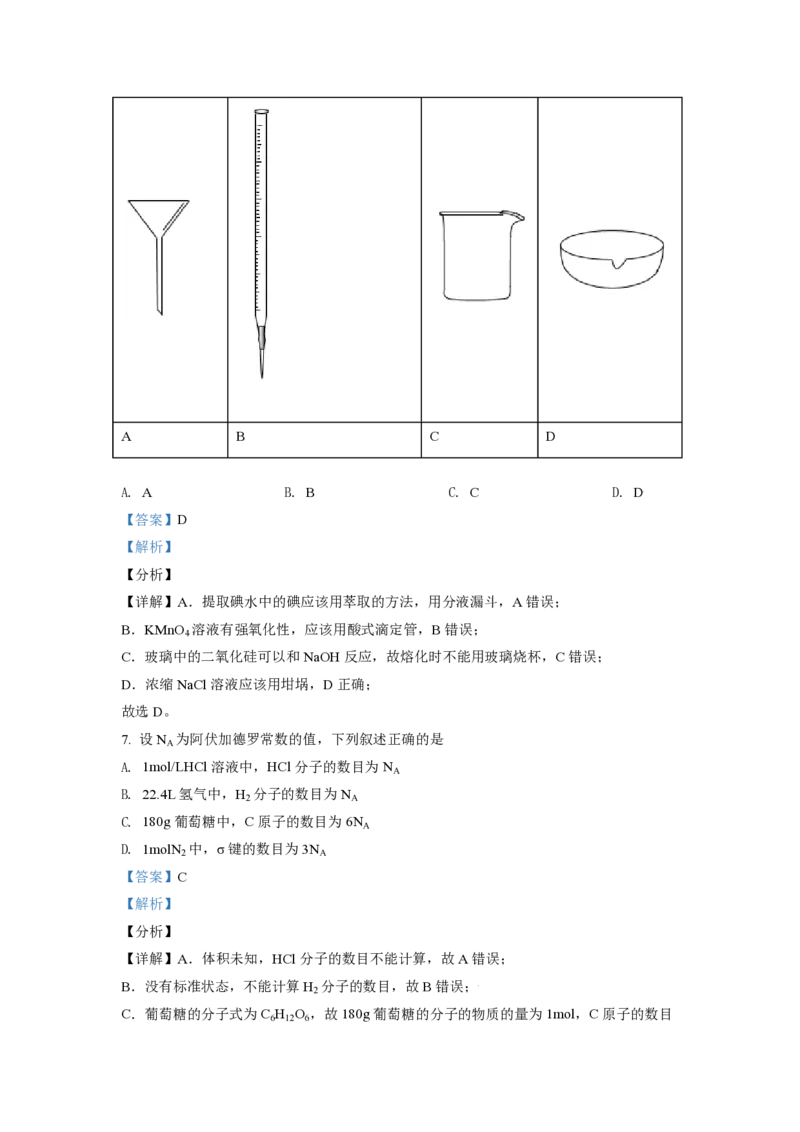
6. 进行下列实验操作时,选用仪器正确的是
量取一定体积的KMnO 溶
4
提取碘水中的碘 熔化NaOH固体 浓缩NaCl溶液
液A B C D
A. A B. B C. C D. D
【答案】D
【解析】
【分析】
【详解】A.提取碘水中的碘应该用萃取的方法,用分液漏斗,A错误;
B.KMnO 溶液有强氧化性,应该用酸式滴定管,B错误;
4
C.玻璃中的二氧化硅可以和NaOH反应,故熔化时不能用玻璃烧杯,C错误;
D.浓缩NaCl溶液应该用坩埚,D正确;
故选D。
7. 设N 为阿伏加德罗常数的值,下列叙述正确的是
A
A. 1mol/LHCl溶液中,HCl分子的数目为N
A
B. 22.4L氢气中,H 分子的数目为N
2 A
C. 180g葡萄糖中,C原子的数目为6N
A
D. 1molN 中,σ键的数目为3N
2 A
【答案】C
【解析】
【分析】
【详解】A.体积未知,HCl分子的数目不能计算,故A错误;
B.没有标准状态,不能计算H 分子的数目,故B错误;
2
C.葡萄糖的分子式为C H O ,故180g葡萄糖的分子的物质的量为1mol,C原子的数目
6 12 6为6N ,故C正确;
A
D.1molN 中有2molσ键,故σ键的数目为2N ,故D错误;
2 A
故选C。
8. 最理想的“原子经济性反应”是指反应物的原子全部转化为期望的最终产物的反应。下
列属于最理想的“原子经济性反应”的是
A. 用电石与水制备乙炔的反应
B. 用溴乙烷与NaOH的乙醇溶液共热制备乙烯的反应
C. 用苯酚稀溶液与饱和溴水制备2,4,6-三溴苯酚的反应
D. 用乙烯与氧气在Ag催化下制备环氧乙烷( )的反应
【答案】D
【解析】
【分析】
【详解】A.用电石与水制备乙炔,还生成了氢氧化钙,原子没有全部转化为期望的最终
产物,不属于最理想的“原子经济性反应”,故A错误;
B.用溴乙烷与NaOH的乙醇溶液共热制备乙烯,还生成了水和溴化钠,原子没有全部转
化为期望的最终产物,不属于最理想的“原子经济性反应”,故B错误;
C.用苯酚稀溶液与饱和溴水制备2,4,6-三溴苯酚,还生成了溴化氢,原子没有全部转
化为期望的最终产物,不属于最理想的“原子经济性反应”,故C错误;
D.用乙烯与氧气在Ag催化下制备环氧乙烷( ),原子全部转化为期望的最终产
物,属于最理想的“原子经济性反应”,故D正确;
故选D。
9. 常温下,下列各组离子在给定溶液中能大量共存的是
A. pH=1的溶液:Fe2+、Mg2+、SO2-、NO-
4 3
B. pH=12的溶液:K+、Na+、NO-、CO2-
3 3
C. pH=7的溶液:Na+、Cu2+、S2-、Cl-
D. pH=7的溶液:Al3+、K+、Cl-、HCO-
3
【答案】B
【解析】
【分析】
【详解】A.pH=1的溶液中,NO-在酸性条件下与Fe2+会发生氧化还原反应,不能大量
3
共存,故A错误;B.pH=12的溶液中,K+、Na+、NO-、CO2-均不能发生反应,能大量共存,故B正确;
3 3
C.pH=7的溶液中,Cu2+、S2-会发生反应生成沉淀,不能大量共存,故C错误;
D.pH=7的溶液中,Al3+、HCO- 会发生双水解,不能大量共存,故D错误;
3
故选B。
10. 常温下,下列有关电解质溶液的叙述正确的是
A. 在0.1molL-1 H PO 溶液中c(H PO )>c(H PO-)>c(HPO2-)>c(PO3-)
3 4 3 4 2 4 4 4
B. 在0.1molL-1 Na C O 溶液中c(Na+)+c(H+)=c(OH-)+c(HC O-)+c(C O2-)
2 2 4 2 4 2 4
C. 在0.1molL-1 NaHCO 溶液中c(H CO )+c(HCO-)=0.1molL-1
3 2 3 3
D. 氨水和NH Cl溶液混合,形成pH=9的溶液中c(Cl-)>c(NH+)>c(OH-)>c(H+)
4 4
【答案】A
【解析】
【分析】
【详解】A.由于磷酸为多元酸,第一步电离大于第二步电离大于第三步电离,所以在
0.1molL-1H PO 溶液中,离子浓度大小为:c(H PO )>c(H PO-)>c(HPO2-)>c(PO3-)
3 4 3 4 2 4 4 4
,故A正确;
B.在0.1molL-1Na C O 溶液中,根据电荷守恒得到
2 2 4
c(Na+)+c(H+)=c(OH-)+c(HC O-)+2c(C O2-),故B错误;
2 4 2 4
C.在0.1molL-1NaHCO 溶液中,根据物料守恒得到
3
c(H CO )+c(HCO-)+c(H CO )=0.1molL-1,故C错误;
2 3 3 2 3
D.氨水和NH Cl溶液混合,形成pH=9的溶液,则c(OH-)>c(H+),根据电荷守恒
4
c(Cl-)+c(OH-)=c(NH+)+c(H+),则c(Cl-)