文档内容
2023年上海市高考化学试卷
一、选择题
1.(3分)2022年,科学家们已经证实“四中子态”的存在,该物质只由四个中子组成,
则其质量数是( )
A.1 B.2 C.4 D.8
2.(3分)海底五彩斑斓的珊瑚是由珊瑚虫吸收海水中的钙和CO ,然后分泌出石灰石,
2
变为自己生存的外壳。植物有光合作用会吸收CO 、释放O ,但随着全球变暖,CO 含
2 2 2
量增加,海底珊瑚含量减少,下列说法错误的是( )
A.光合作用吸收CO
2
B.植物呼吸作用放出CO
2
C.海水吸收过多CO 使pH增大
2
D.珊瑚礁溶解是因为生成Ca(HCO )
3 2
3.(3分)战国用青铜浇铸塑形成各样的青铜器,青铜器比纯铜更便于制成形态各异的容
器的原因( )
A.熔点低 B.密度大 C.硬度大 D.不易被腐蚀
4.(3分)下列物质中,能通过化学氧化法去除石油开采过程中伴生的H S的是( )
2
A.氨水 B.双氧水 C.FeSO 溶液 D.NaOH溶液
4
5.(3分)对于反应8NH +3Cl ═6NH Cl+N ,以下说法正确的是( )
3 2 4 2
A.HCl的电子式为
B.NH 的空间构型为三角锥形
3
C.NH Cl中只含有离子键
4
D.氯离子最外层电子排布式是3s33p5
6.(3分)向饱和氯水中加入少量Na SO 固体,下列说法正确的是( )
2 3
A.溶液pH减小 B.溶液颜色变深
C.溶液漂白性增强 D.溶液导电性减弱
7.(3分)已知稠油是黏度超过50mPa•s的原油,数据显示,在世界剩余石油资源中,约
有70%都是稠油。下列关于稠油的说法错误的是( )
A.稠油易溶于水 B.稠油主要是C、H元素
C.稠油属于混合物 D.稠油可以裂化8.(3分)最简式相同的有机物( )
A.一定是同系物 B.一定是同分异构体
C.碳的质量分数一定相等 D.燃烧时耗氧量一定相等
9.(3分)我国科学家研发的高效稳定的单原子催化剂,能够实现临氢条件下丙烷高效脱
氢制丙烯,下列选项正确的是( )
A.丙烷脱氢生成丙烯的反应是加成反应
B.丙烷可以使酸性高锰酸钾溶液褪色
C.丙烯分子中所有原子可能共面
D.丙烯可以发生加聚反应
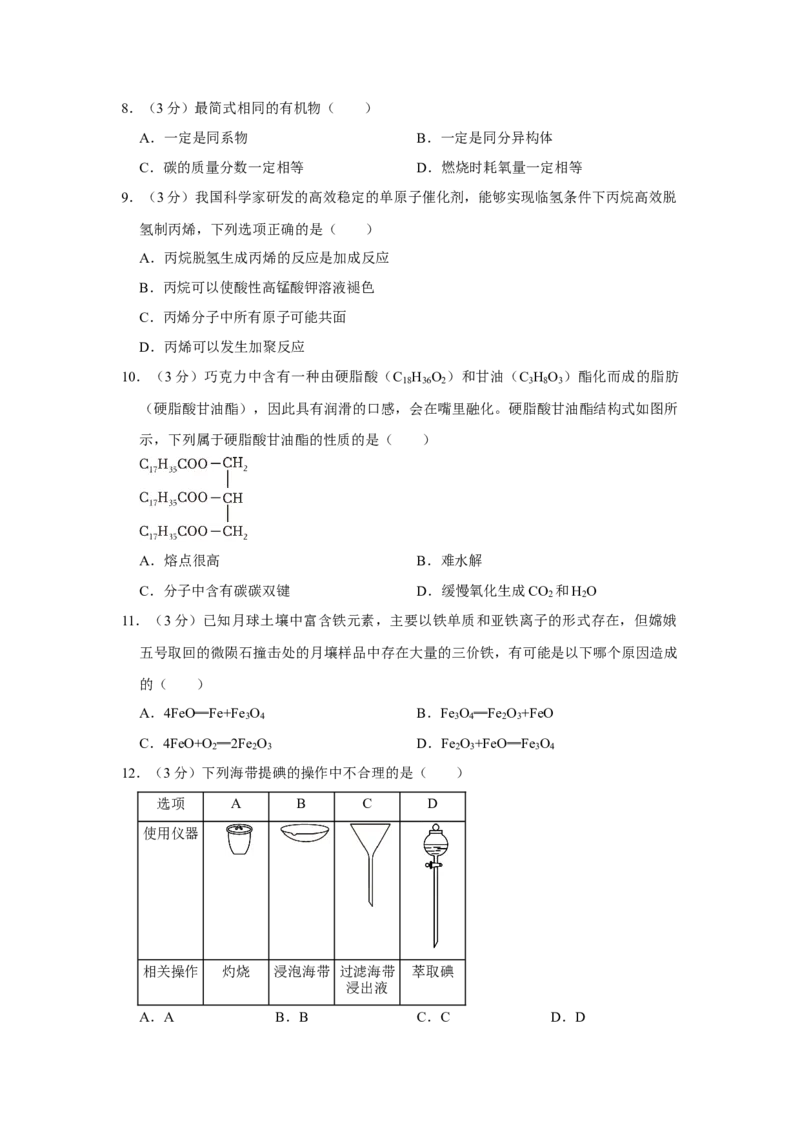
10.(3分)巧克力中含有一种由硬脂酸(C H O )和甘油(C H O )酯化而成的脂肪
18 36 2 3 8 3
(硬脂酸甘油酯),因此具有润滑的口感,会在嘴里融化。硬脂酸甘油酯结构式如图所
示,下列属于硬脂酸甘油酯的性质的是( )
A.熔点很高 B.难水解
C.分子中含有碳碳双键 D.缓慢氧化生成CO 和H O
2 2
11.(3分)已知月球土壤中富含铁元素,主要以铁单质和亚铁离子的形式存在,但嫦娥
五号取回的微陨石撞击处的月壤样品中存在大量的三价铁,有可能是以下哪个原因造成
的( )
A.4FeO═Fe+Fe O B.Fe O ═Fe O +FeO
3 4 3 4 2 3
C.4FeO+O ═2Fe O D.Fe O +FeO═Fe O
2 2 3 2 3 3 4
12.(3分)下列海带提碘的操作中不合理的是( )
选项 A B C D
使用仪器
相关操作 灼烧 浸泡海带 过滤海带 萃取碘
浸出液
A.A B.B C.C D.D13.(3分)现有3种不同颜色的橡皮泥代表着不同元素,还有4根火柴棒代表化学键,可
以搭建的有机分子是( )
A.甲醇 B.甲醛 C.甲酸 D.CH ClF
2
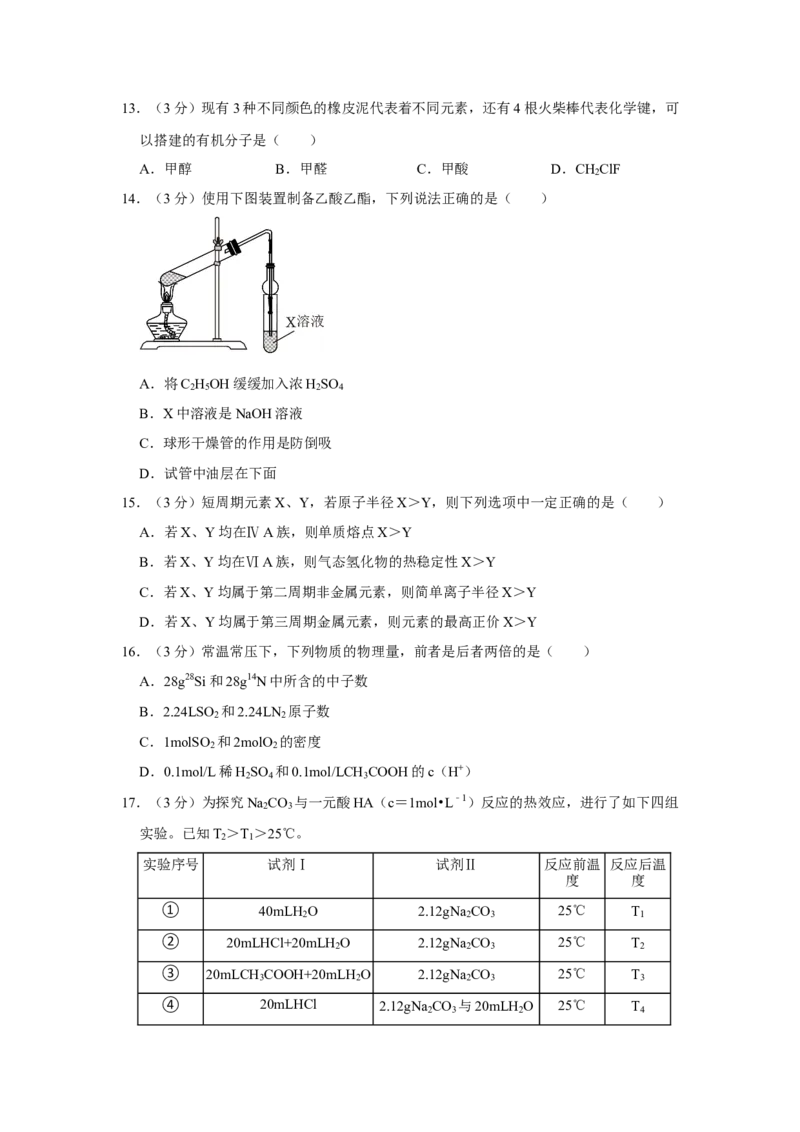
14.(3分)使用下图装置制备乙酸乙酯,下列说法正确的是( )
A.将C H OH缓缓加入浓H SO
2 5 2 4
B.X中溶液是NaOH溶液
C.球形干燥管的作用是防倒吸
D.试管中油层在下面
15.(3分)短周期元素X、Y,若原子半径X>Y,则下列选项中一定正确的是( )
A.若X、Y均在ⅣA族,则单质熔点X>Y
B.若X、Y均在ⅥA族,则气态氢化物的热稳定性X>Y
C.若X、Y均属于第二周期非金属元素,则简单离子半径X>Y
D.若X、Y均属于第三周期金属元素,则元素的最高正价X>Y
16.(3分)常温常压下,下列物质的物理量,前者是后者两倍的是( )
A.28g28Si和28g14N中所含的中子数
B.2.24LSO 和2.24LN 原子数
2 2
C.1molSO 和2molO 的密度
2 2
D.0.1mol/L稀H SO 和0.1mol/LCH COOH的c(H+)
2 4 3
17.(3分)为探究Na CO 与一元酸HA(c=1mol•L﹣1)反应的热效应,进行了如下四组
2 3
实验。已知T >T >25℃。
2 1
实验序号 试剂Ⅰ 试剂Ⅱ 反应前温 反应后温
度 度
① 40mLH O 2.12gNa CO 25℃ T
2 2 3 1
② 20mLHCl+20mLH O 2.12gNa CO 25℃ T
2 2 3 2
③ 20mLCH COOH+20mLH O 2.12gNa CO 25℃ T
3 2 2 3 3
④ 20mLHCl 2.12gNa CO 与20mLH O 25℃ T
2 3 2 4形成的溶液
下列说法错误的是( )
A.Na CO 溶于水放热 B.Na CO 与HCl反应放热
2 3 2 3
C.T >T D.T >T
2 3 4 2
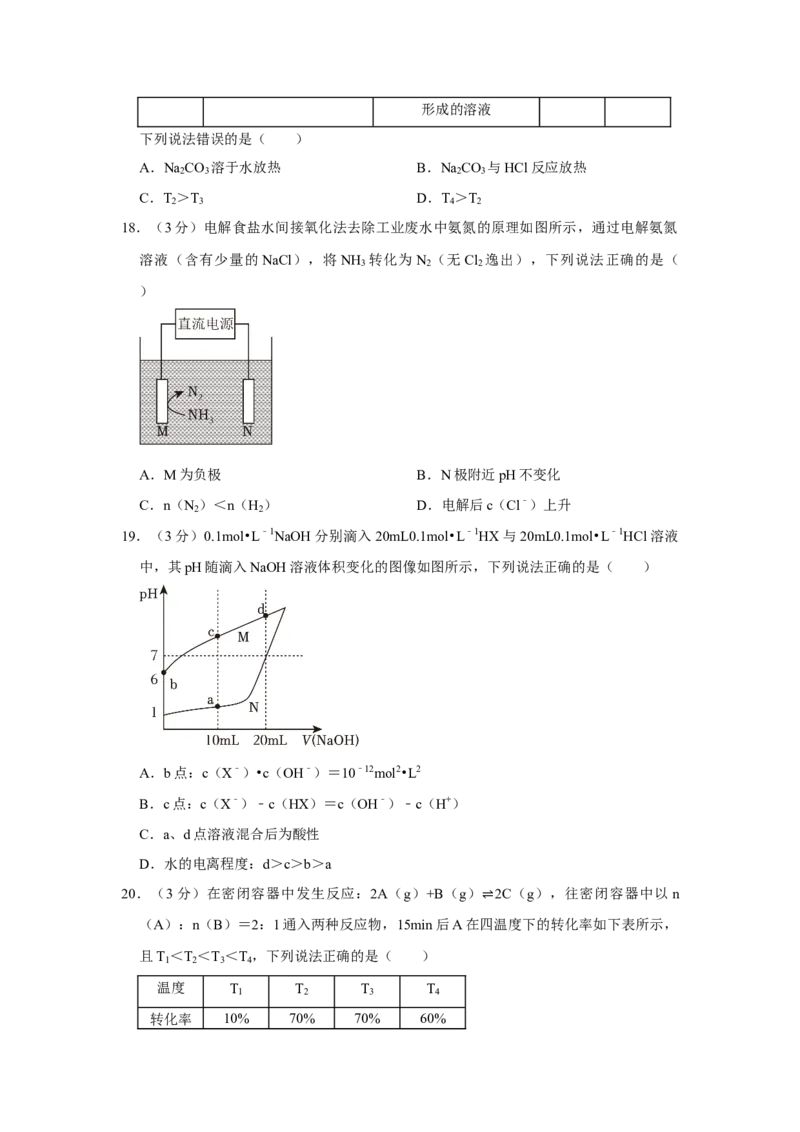
18.(3分)电解食盐水间接氧化法去除工业废水中氨氮的原理如图所示,通过电解氨氮
溶液(含有少量的NaCl),将NH 转化为N (无Cl 逸出),下列说法正确的是(
3 2 2
)
A.M为负极 B.N极附近pH不变化
C.n(N )<n(H ) D.电解后c(Cl﹣)上升
2 2
19.(3分)0.1mol•L﹣1NaOH分别滴入20mL0.1mol•L﹣1HX与20mL0.1mol•L﹣1HCl溶液
中,其pH随滴入NaOH溶液体积变化的图像如图所示,下列说法正确的是( )
A.b点:c(X﹣)•c(OH﹣)=10﹣12mol2•L2
B.c点:c(X﹣)﹣c(HX)=c(OH﹣)﹣c(H+)
C.a、d点溶液混合后为酸性
D.水的电离程度:d>c>b>a
20.(3分)在密闭容器中发生反应:2A(g)+B(g) 2C(g),往密闭容器中以n
(A):n(B)=2:1通入两种反应物,15min后A在四⇌温度下的转化率如下表所示,
且T <T <T <T ,下列说法正确的是( )
1 2 3 4
温度 T T T T
1 2 3 4
转化率 10% 70% 70% 60%A.该反应是吸热反应
B.T温度时(T <T<T ),A的转化率是70%
2 3
C.T 温度下,若反应在15min后继续进行,则A的转化率变大
3
D.T 温度反应15min后,若c(B)=0.5mol•L﹣1,则T 温度时的平衡常数是4.5
4 4
二、综合题
21.在某温度下,在体积为5L的密闭容器内发生如下反应:CH (g)+H O(g) CO
4 2
(g)+3H (g)﹣Q ⇌
2
(1)在上述反应的反应物与生成物中,非极性分子为: 。
(2)若反应 20min后气体总物质的量增加了 10mol,则甲烷的平均反应速率为
。
(3)下列选项中的物理量不变时,一定可以判断反应达到平衡的是 。
A.容器中氢元素的质量分数
B.容器内的压强
C.反应的平衡常数
D.容器内气体的平均相对分子质量
(4)在某一时刻,v正 =v逆 =v
0
,反应若改变一条件,可使得v正 <v逆 <v
0
,指出可以
改变的条件,并说明理由: 。
已知CO与H 合成CH OH是可逆反应:CO+2H CH OH。
2 3 2 3
(5)若上述反应达到平衡时CO与H
2
的转化率相⇌同,则投料比n(CO):n(H
2
)=
。
22.聚合氯化铝用于城市给排水净化。氧化铝法制取无水三氯化铝的反应如下:Al O
2 3
(s)+3C(s)+3Cl (g) 2AlCl (g)+3CO(g)。
2 3
(1)标出上述反应的电子转移方向和数目 。
(2)写出该反应的平衡常数表达式:K= 。
(3)Al原子核外有 种不同能量的电子。
聚合氯化铝(PAC)是一种介于AlCl 和Al(OH) 之间的水溶性无机高分子聚合物,
3 3
PAC的水解过程中会有一种聚合稳定态物质[AlO Al (OH) (H O) ]7+称为Al ,
4 12 24 2 12 13
Al 对水中胶体和颗粒物具有高度电中和桥联作用,是净水过程中的重要物质。
13
(4)Al 在水解过程中会产生[Al(OH) ]+、[Al(OH)]2+等产物,请写出Al3+水解产
13 2生[Al(OH)]2+的离子方程式: 。
(5)AlCl 溶液与NaOH溶液反应,若参加反应的铝离子最终转化生成Al ,则理论上
3 13
参与反应的Al3+与OH﹣的物质的量之比是 。
(6)使用Al3+净水时应控制pH在6.8~8.02之间,否则净水效果不佳。请结合使用
Al3+水解净化水时铝元素存在的形态,分析在强酸性和强碱性环境时净水效果差的原因
。
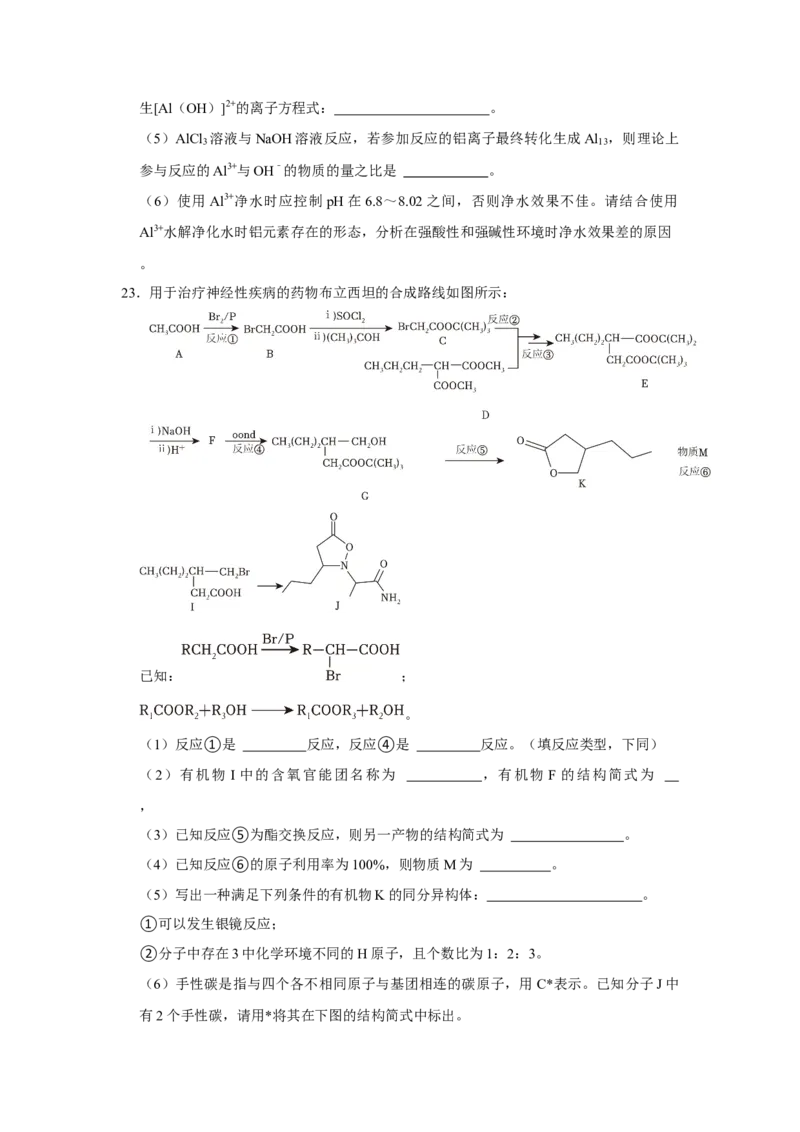
23.用于治疗神经性疾病的药物布立西坦的合成路线如图所示:
已知: ;
。
(1)反应①是 反应,反应④是 反应。(填反应类型,下同)
(2)有机物 I 中的含氧官能团名称为 ,有机物 F 的结构简式为
,
(3)已知反应⑤为酯交换反应,则另一产物的结构简式为 。
(4)已知反应⑥的原子利用率为100%,则物质M为 。
(5)写出一种满足下列条件的有机物K的同分异构体: 。
①可以发生银镜反应;
②分子中存在3中化学环境不同的H原子,且个数比为1:2:3。
(6)手性碳是指与四个各不相同原子与基团相连的碳原子,用C*表示。已知分子J中
有2个手性碳,请用*将其在下图的结构简式中标出。(7)请写出以CH (CH ) COOH和CH OH为原料制备CH CH CH=CHCOOCH 的
3 2 3 3 3 2 3
路线(合成路线的表示方式为 •••••• 目标产物)
。
24.Ⅰ.过氧化氢和盐酸的混合溶液可以刻蚀含铜的电路板。
(1)请写出用过氧化氢和盐酸刻蚀电路板时发生的离子反应方程式:
。
(2)当反应一段时间后,随着溶液变蓝,气泡产生的速率加快,可能的原因是
。
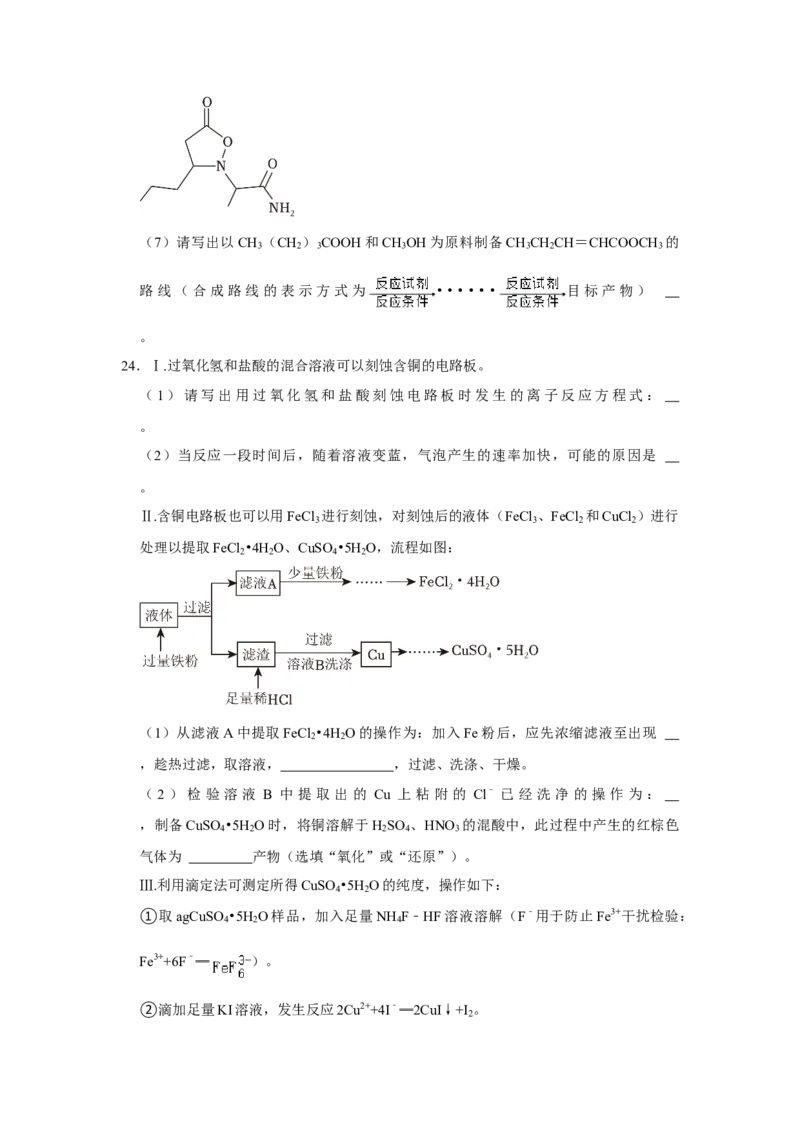
Ⅱ.含铜电路板也可以用FeCl 进行刻蚀,对刻蚀后的液体(FeCl 、FeCl 和CuCl )进行
3 3 2 2
处理以提取FeCl •4H O、CuSO •5H O,流程如图:
2 2 4 2
(1)从滤液A中提取FeCl •4H O的操作为:加入Fe粉后,应先浓缩滤液至出现
2 2
,趁热过滤,取溶液, ,过滤、洗涤、干燥。
( 2 ) 检 验 溶 液 B 中 提 取 出 的 Cu 上 粘 附 的 Cl﹣ 已 经 洗 净 的 操 作 为 :
,制备CuSO •5H O时,将铜溶解于H SO 、HNO 的混酸中,此过程中产生的红棕色
4 2 2 4 3
气体为 产物(选填“氧化”或“还原”)。
Ⅲ.利用滴定法可测定所得CuSO •5H O的纯度,操作如下:
4 2
①取agCuSO •5H O样品,加入足量NH F﹣HF溶液溶解(F﹣用于防止Fe3+干扰检验:
4 2 4
Fe3++6F﹣═ )。
②滴加足量KI溶液,发生反应2Cu2++4I﹣═2CuI↓+I 。
2③再用cmol/LNa S O 标准溶液滴定,以淀粉溶液作指示剂,到达滴定终点时消耗亚硫
2 2 3
酸钠标准溶液VmL,发生的反应为:I +2S ═S +2I﹣。
2 2 4
(1)已知 NH F 溶液呈酸性,则水解程度 F﹣(填“>”、“<”或
4
“=”),稀释后消耗 的值 (选填“增大”、“减小”或
“不变”)。
(2)接近滴定终点时,向溶液中滴加KSCN,会发现CuI沉淀转化为CuSCN,其沉淀
转化的原因是 。已知CuI能够吸附大量I ,若不加KSCN,则
2
测得CuSO •5H O的纯度 (选填“偏高”、“偏低”或“不变”)。
4 2
(3)计算CuSO •5H O的纯度: (用a、c、V的代数式表
4 2
示)。