文档内容
2025 年湖南省普通高中学业水平选择性考试
化学
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在本试题卷和答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改
动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在
本试题卷上无效。
3.考试结束后,将本试题卷和答题卡一并交回。
可能用到的相对原子质量:
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 材料是人类赖以生存和发展的物质基础。下列材料属于金属材料的是
A. 高强韧无磁不锈钢——聚变能实验装置中的低温结构部件
B. 金刚石薄膜——“梦想”号大洋钻探船使用的钻头表面涂层
C. 超细玄武岩纤维——嫦娥六号携带的月面国旗的纺织材料
D. 超细玻璃纤维——国产大飞机中隔音隔热的“飞机棉”
2. 化学实验充满着五颜六色的变化。下列描述错误的是
B.产生红色沉 D.试纸变为蓝
A.溶液褪色 C.溶液呈紫色
淀 色
A. A B. B C. C D. D
3. 加热时,浓硫酸与木炭发生反应: (浓) 。设 为阿伏加德罗
常数的值。下列说法正确的是
A. 含质子数为B. 常温常压下, 含σ键数目为
C. 的稀硫酸中含 数目为
D. 与 充分反应得到 的分子数为
4. 只用一种试剂,将 四种物质的溶液区分开,这种试剂是
A. 溶液 B. 溶液 C. 溶液 D. 溶液
5. 下列有关物质性质的解释错误的是
性质 解释
A 酸性: 是推电子基团
B 熔点: 的体积大于
C 熔点: 比 的金属性弱
D 沸点: 分子间存在氢键
A. A B. B C. C D. D
6. 浓溶液中含有的 具有酸性,能溶解金属氧化物。元素X、Y、Z、M的原子序数依
次增大,分别位于不同的前四周期。Y的最外层电子数是内层的3倍,X和Y的最外层电子数之和等于Z
的最外层电子数,M的价层电子排布是 。下列说法正确的是
A. 电负性:
B. Y形成的两种单质均为非极性分子
C. 由X、Y、Z形成的化合物均为强电解质
D. 铁管上镶嵌M,铁管不易被腐蚀
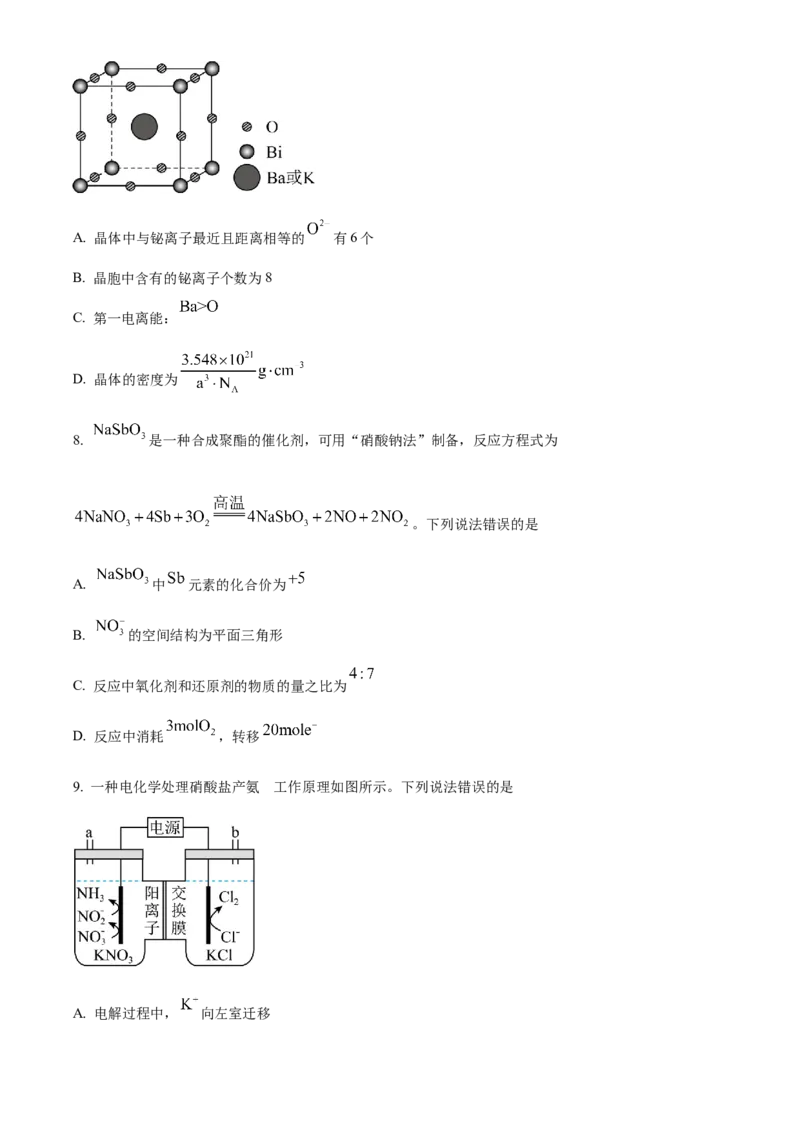
7. 掺杂的铋酸钡具有超导性。 替代部分 形成 (摩尔质量为 ),其
晶胞结构如图所示。该立方晶胞的参数为 ,设 为阿伏加德罗常数的值。下列说法正确的是A. 晶体中与铋离子最近且距离相等的 有6个
B. 晶胞中含有的铋离子个数为8
C. 第一电离能:
D. 晶体的密度为
8. 是一种合成聚酯的催化剂,可用“硝酸钠法”制备,反应方程式为
。下列说法错误的是
A. 中 元素的化合价为
B. 的空间结构为平面三角形
C. 反应中氧化剂和还原剂的物质的量之比为
D. 反应中消耗 ,转移
的
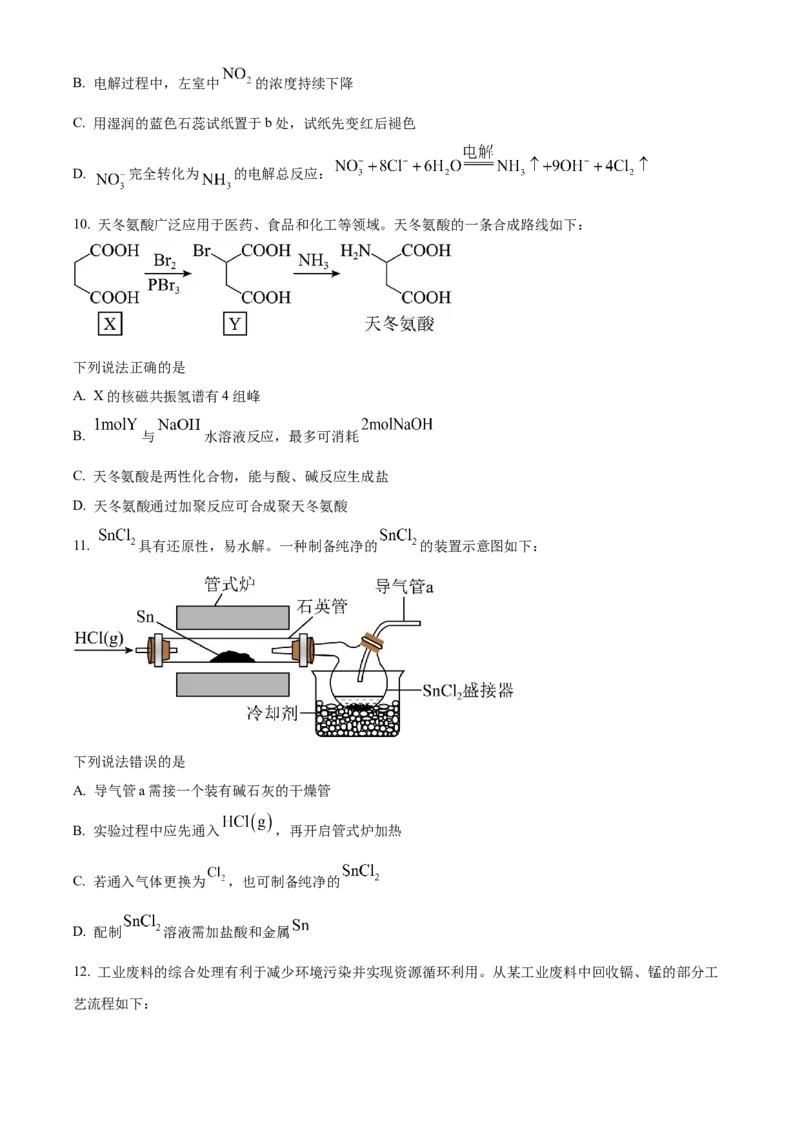
9. 一种电化学处理硝酸盐产氨 工作原理如图所示。下列说法错误的是
A. 电解过程中, 向左室迁移B. 电解过程中,左室中 的浓度持续下降
C. 用湿润的蓝色石蕊试纸置于b处,试纸先变红后褪色
D. 完全转化为 的电解总反应:
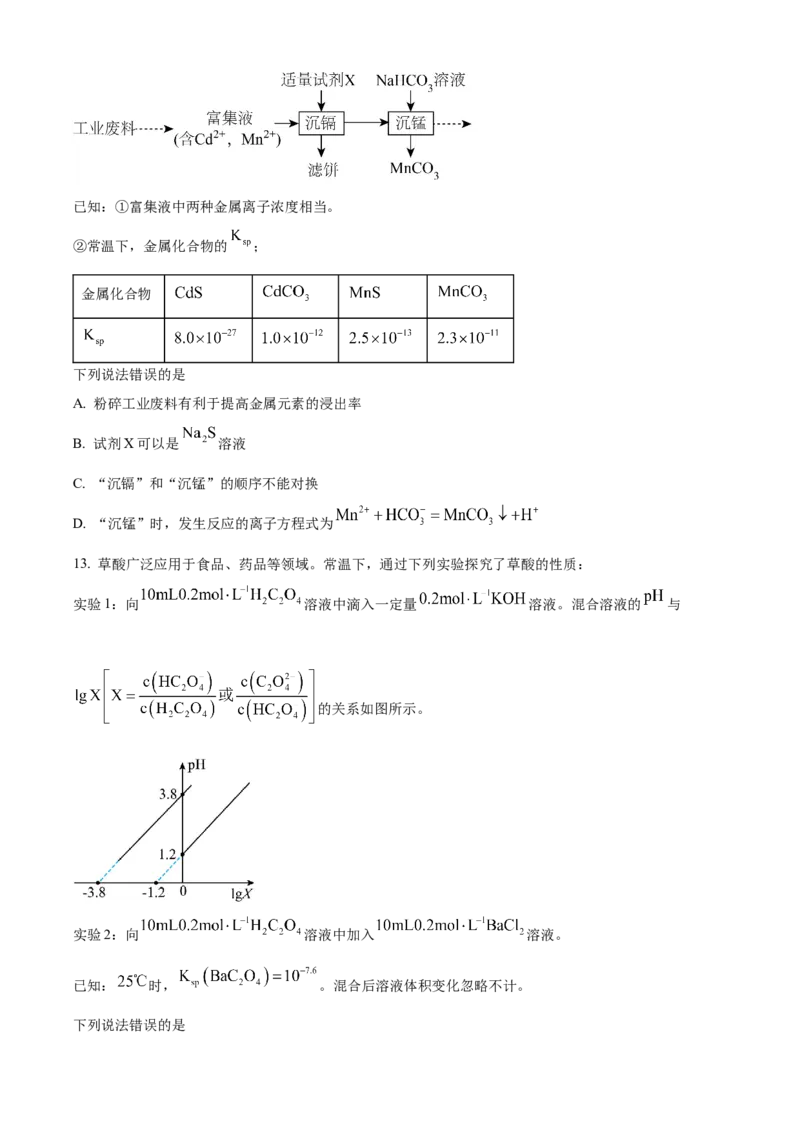
10. 天冬氨酸广泛应用于医药、食品和化工等领域。天冬氨酸的一条合成路线如下:
下列说法正确的是
A. X的核磁共振氢谱有4组峰
B. 与 水溶液反应,最多可消耗
C. 天冬氨酸是两性化合物,能与酸、碱反应生成盐
D. 天冬氨酸通过加聚反应可合成聚天冬氨酸
11. 具有还原性,易水解。一种制备纯净的 的装置示意图如下:
下列说法错误的是
A. 导气管a需接一个装有碱石灰的干燥管
B. 实验过程中应先通入 ,再开启管式炉加热
C. 若通入气体更换为 ,也可制备纯净的
D. 配制 溶液需加盐酸和金属
12. 工业废料的综合处理有利于减少环境污染并实现资源循环利用。从某工业废料中回收镉、锰的部分工
艺流程如下:已知:①富集液中两种金属离子浓度相当。
②常温下,金属化合物的 ;
金属化合物
下列说法错误的是
A. 粉碎工业废料有利于提高金属元素的浸出率
B. 试剂X可以是 溶液
C. “沉镉”和“沉锰”的顺序不能对换
D. “沉锰”时,发生反应的离子方程式为
13. 草酸广泛应用于食品、药品等领域。常温下,通过下列实验探究了草酸的性质:
实验1:向 溶液中滴入一定量 溶液。混合溶液的 与
的关系如图所示。
实验2:向 溶液中加入 溶液。
已知: 时, 。混合后溶液体积变化忽略不计。
下列说法错误的是.
A 实验1,当溶液中 时,
B. 实验1,当溶液呈中性时:
.
C 实验2,溶液中有沉淀生成
D. 实验2,溶液中存在:
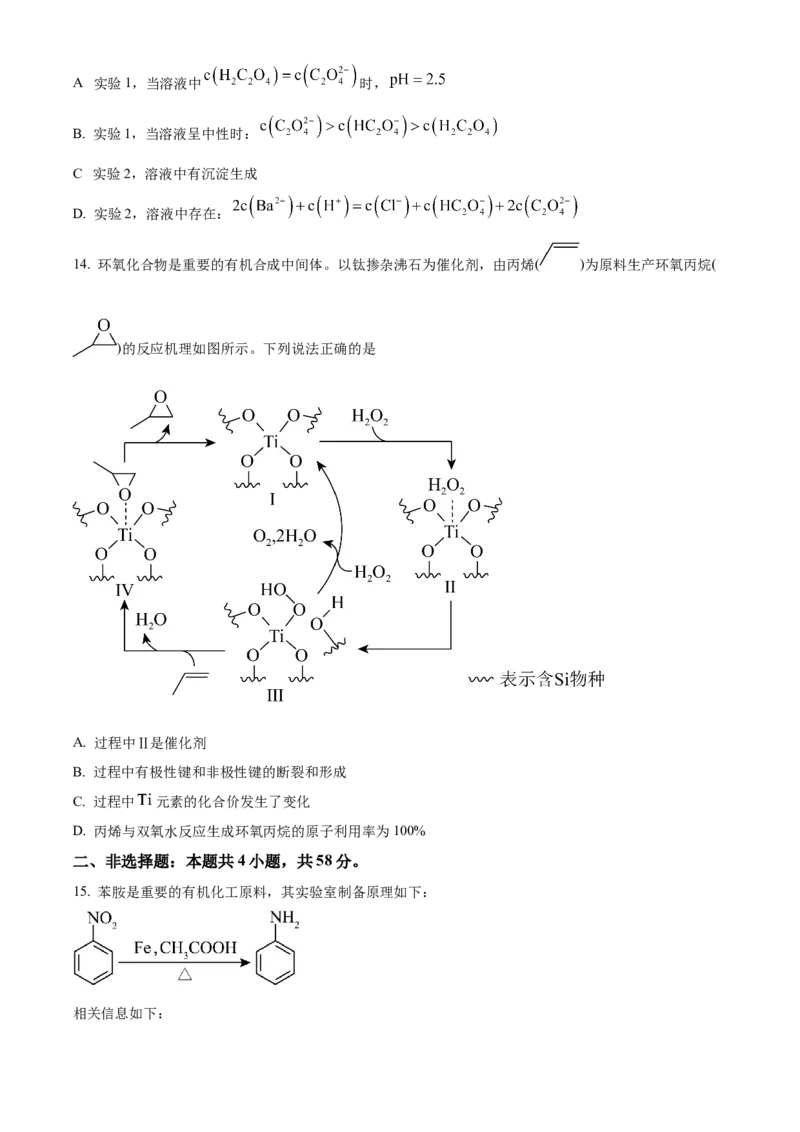
14. 环氧化合物是重要的有机合成中间体。以钛掺杂沸石为催化剂,由丙烯( )为原料生产环氧丙烷(
)的反应机理如图所示。下列说法正确的是
A. 过程中Ⅱ是催化剂
B. 过程中有极性键和非极性键的断裂和形成
C. 过程中 元素的化合价发生了变化
D. 丙烯与双氧水反应生成环氧丙烷的原子利用率为100%
二、非选择题:本题共4小题,共58分。
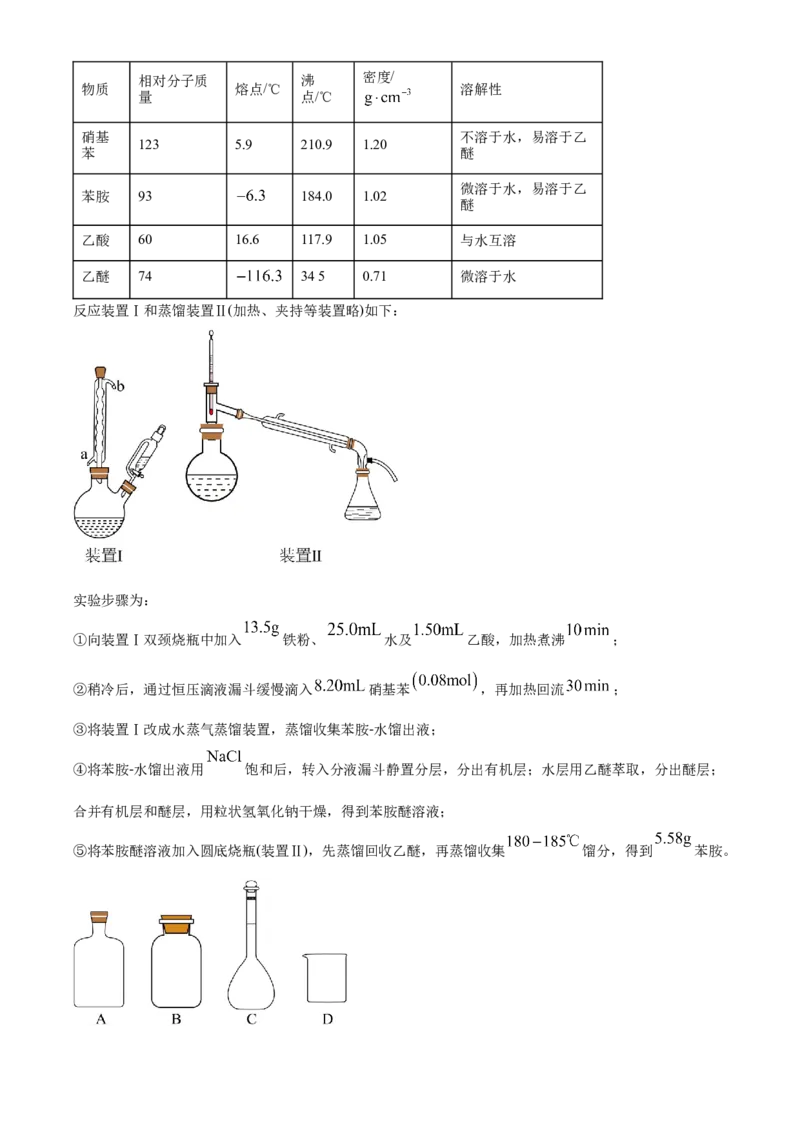
15. 苯胺是重要的有机化工原料,其实验室制备原理如下:
相关信息如下:相对分子质 沸 密度/
物质 熔点/℃ 溶解性
量 点/℃
硝基 不溶于水,易溶于乙
123 5.9 210.9 1.20
苯 醚
微溶于水,易溶于乙
苯胺 93 184.0 1.02
醚
乙酸 60 16.6 117.9 1.05 与水互溶
.
乙醚 74 345 0.71 微溶于水
反应装置Ⅰ和蒸馏装置Ⅱ(加热、夹持等装置略)如下:
实验步骤为:
①向装置Ⅰ双颈烧瓶中加入 铁粉、 水及 乙酸,加热煮沸 ;
②稍冷后,通过恒压滴液漏斗缓慢滴入 硝基苯 ,再加热回流 ;
③将装置Ⅰ改成水蒸气蒸馏装置,蒸馏收集苯胺-水馏出液;
④将苯胺-水馏出液用 饱和后,转入分液漏斗静置分层,分出有机层;水层用乙醚萃取,分出醚层;
合并有机层和醚层,用粒状氢氧化钠干燥,得到苯胺醚溶液;
⑤将苯胺醚溶液加入圆底烧瓶(装置Ⅱ),先蒸馏回收乙醚,再蒸馏收集 馏分,得到 苯胺。回答下列问题:
(1)实验室保存硝基苯的玻璃容器是_______(填标号)。
(2)装置Ⅰ中冷凝管的进水口为_______(填“a”或“b”)。
(3)步骤④中将苯胺-水馏出液用 饱和的原因是_______。
(4)步骤④中第二次分液,醚层位于_______层(填“上”或“下”)。
(5)蒸馏回收乙醚时,锥形瓶需冰水浴的原因是_______;回收乙醚后,需要放出冷凝管中的冷凝水再蒸
馏,这样操作的原因是_______。
(6)下列说法正确的是_______(填标号)。
A. 缓慢滴加硝基苯是为了减小反应速率
B. 蒸馏时需加沸石,防止暴沸
C. 用红外光谱不能判断苯胺中是否含有硝基苯
D. 蒸馏回收乙醚,无需尾气处理
(7)苯胺的产率为_______。
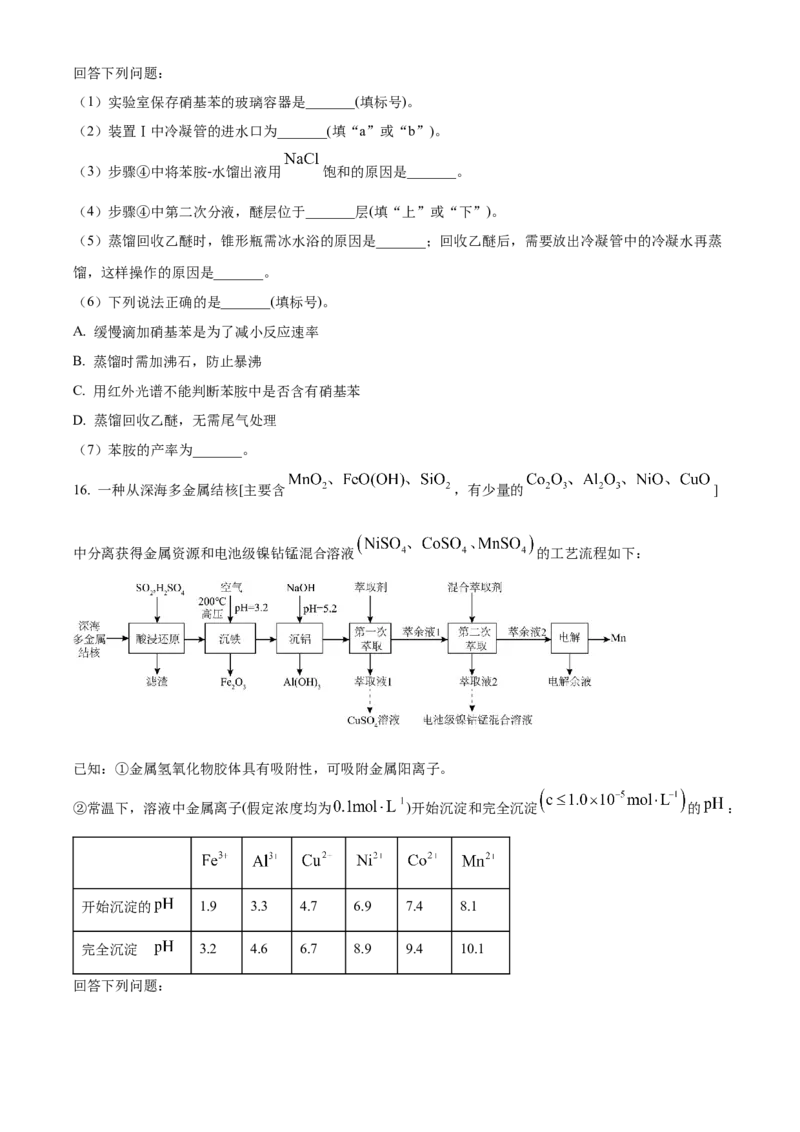
16. 一种从深海多金属结核[主要含 ,有少量的 ]
中分离获得金属资源和电池级镍钻锰混合溶液 的工艺流程如下:
已知:①金属氢氧化物胶体具有吸附性,可吸附金属阳离子。
②常温下,溶液中金属离子(假定浓度均为 )开始沉淀和完全沉淀 的 :
开始沉淀的 1.9 3.3 4.7 6.9 7.4 8.1
完全沉淀 的3.2 4.6 6.7 8.9 9.4 10.1
回答下列问题:(1)基态 的价层电子排布式为_______。
(2)“酸浸还原”时,“滤渣”的主要成分是_______(写化学式); 还原 的化学方程式为
_______。
(3)“沉铁”时, 转化为 的离子方程式为_______,加热至 的主要原因是_______。
(4)“沉铝”时,未产生 沉淀,该溶液中 不超过_______ 。
(5)“第二次萃取”时,_______、_______(填离子符号)与混合萃取剂形成的配合物(其结构如图所示,M
表示金属元素)更稳定,这些配合物中氮原子的杂化类型为_______。
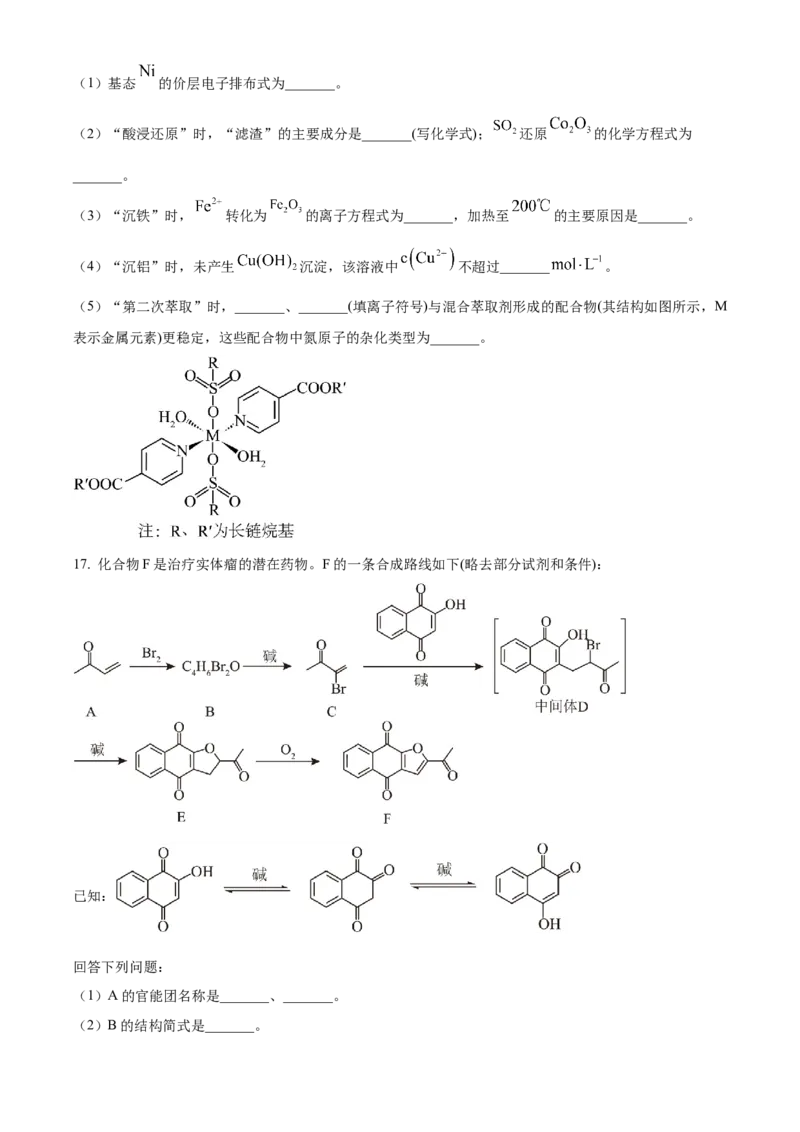
17. 化合物F是治疗实体瘤的潜在药物。F的一条合成路线如下(略去部分试剂和条件):
已知:
回答下列问题:
(1)A的官能团名称是_______、_______。
(2)B的结构简式是_______。(3)E生成F的反应类型是_______。
(4)F所有的碳原子_______共面(填“可能”或“不可能”)。
(5)B在生成C的同时,有副产物G生成。已知G是C的同分异构体,且与C的官能团相同。G的结构
简式是_______、_______(考虑立体异构)。
(6)C与 生成E的同时,有少量产物I生成,此时中间体H的结构简式是_______。
(7)依据以上流程信息,结合所学知识,设计以 和 为原料合成
的路线_______(无机试剂和溶剂任选)。
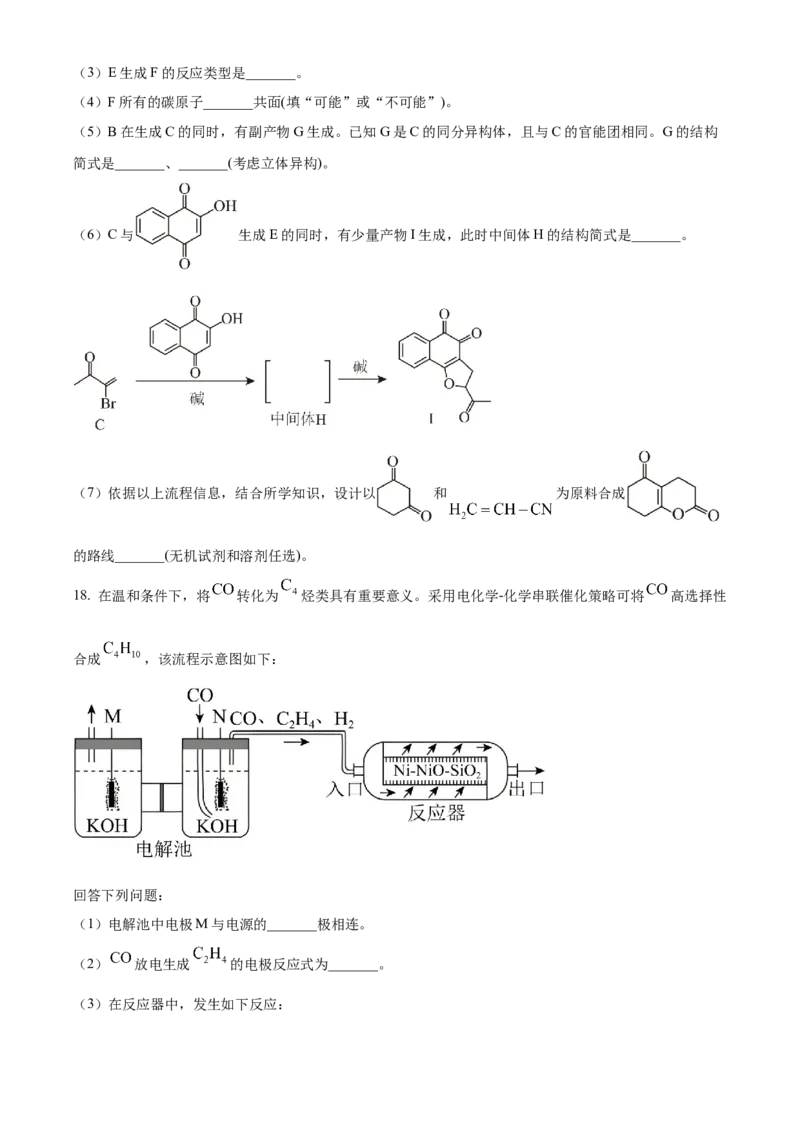
18. 在温和条件下,将 转化为 烃类具有重要意义。采用电化学-化学串联催化策略可将 高选择性
合成 ,该流程示意图如下:
回答下列问题:
(1)电解池中电极M与电源的_______极相连。
(2) 放电生成 的电极反应式为_______。
(3)在反应器中,发生如下反应:反应i:
反应ii:
计算反应 的 _______ ,该反应_______(填标号)。
A.高温自发 B.低温自发 C.高温低温均自发 D.高温低温均不自发
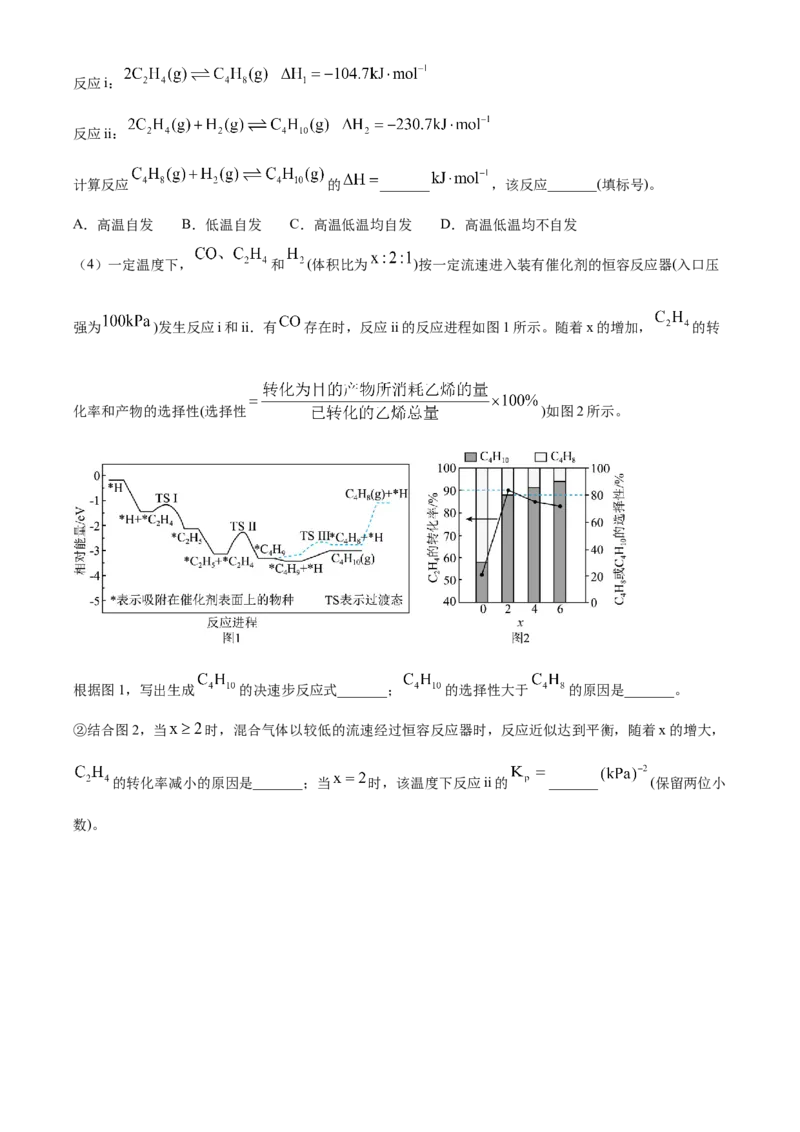
(4)一定温度下, 和 (体积比为 )按一定流速进入装有催化剂的恒容反应器(入口压
强为 )发生反应i和ii.有 存在时,反应ii的反应进程如图1所示。随着x的增加, 的转
化率和产物的选择性(选择性 )如图2所示。
根据图1,写出生成 的决速步反应式_______; 的选择性大于 的原因是_______。
②结合图2,当 时,混合气体以较低的流速经过恒容反应器时,反应近似达到平衡,随着x的增大,
的转化率减小的原因是_______;当 时,该温度下反应ii的 _______ (保留两位小
数)。