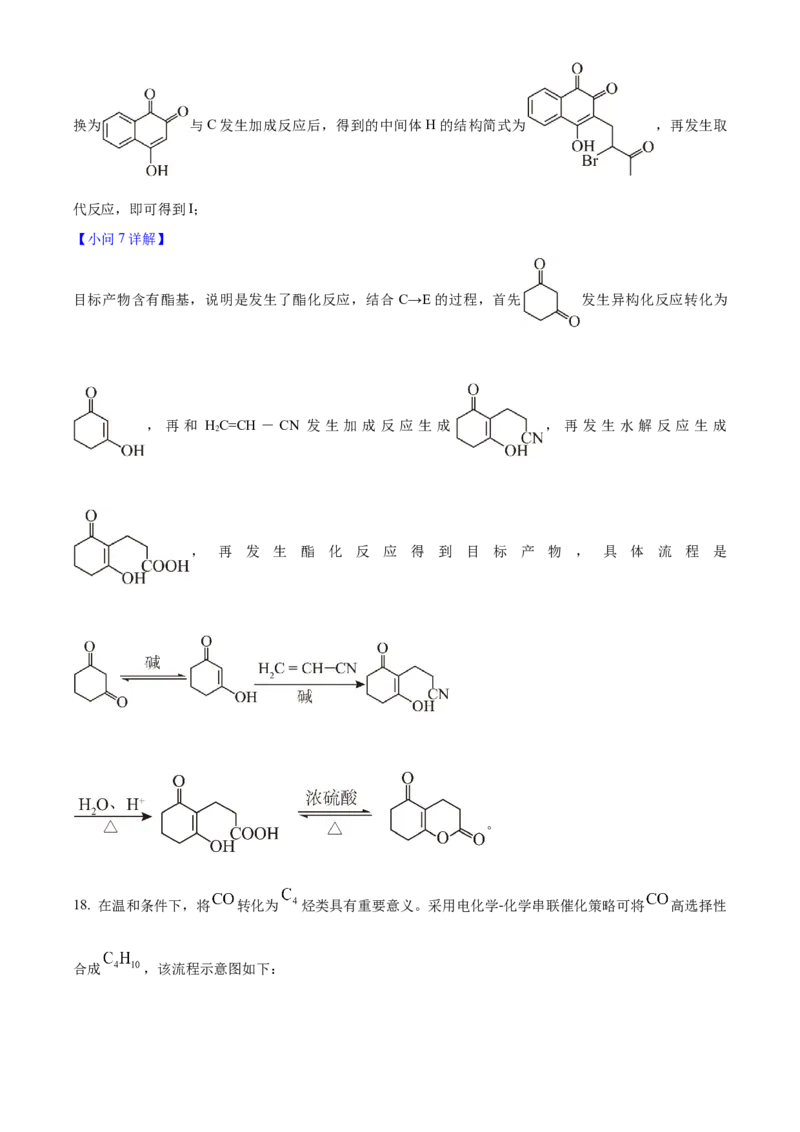
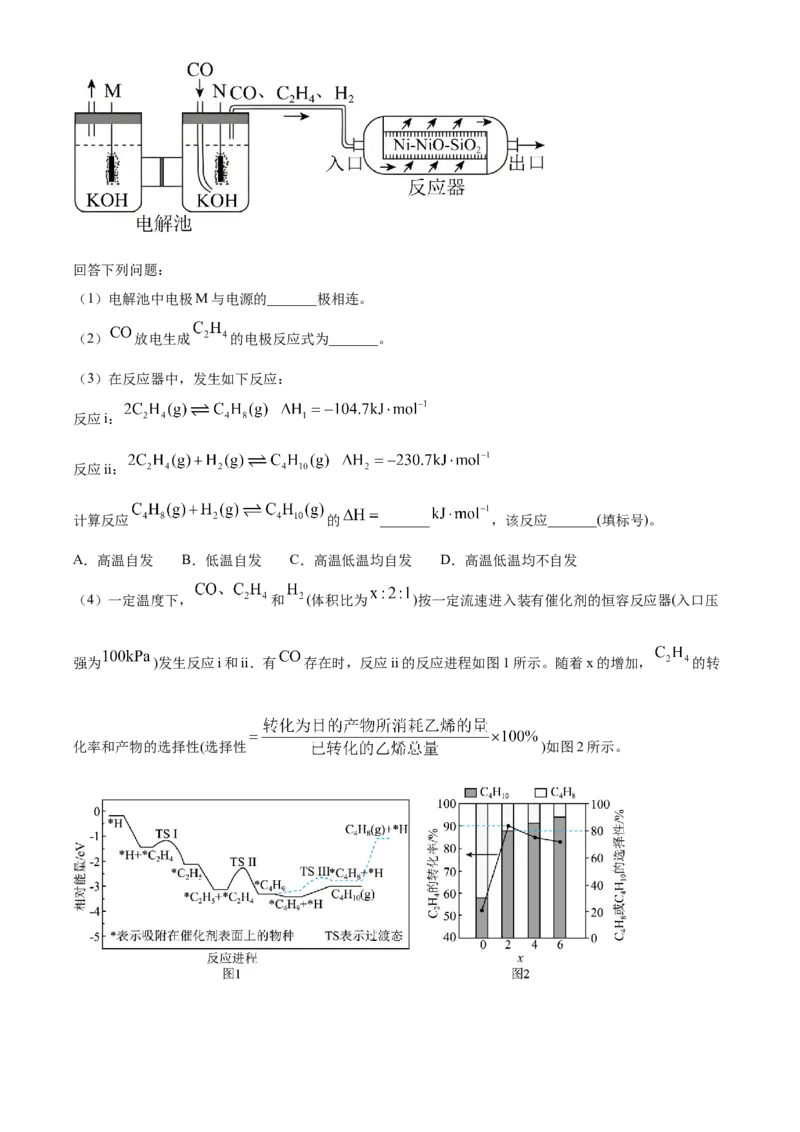
文档内容
2025 年湖南省普通高中学业水平选择性考试
化学
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在本试题卷和答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改
动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在
本试题卷上无效。
3.考试结束后,将本试题卷和答题卡一并交回。
可能用到的相对原子质量:
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 材料是人类赖以生存和发展的物质基础。下列材料属于金属材料的是
A. 高强韧无磁不锈钢——聚变能实验装置中的低温结构部件
B. 金刚石薄膜——“梦想”号大洋钻探船使用的钻头表面涂层
C. 超细玄武岩纤维——嫦娥六号携带的月面国旗的纺织材料
D. 超细玻璃纤维——国产大飞机中隔音隔热的“飞机棉”
【答案】A
【解析】
A.金属材料包括纯金属及其合金,选项中的不锈钢是铁基合金,属于金属材料,A正确;
B.金刚石是碳的非金属形态,是无机非金属材料,B错误;
C.玄武岩纤维是由火山岩(主要成分为硅酸盐矿物)熔融制成的无机非金属材料,类似于玻璃纤维,不
属于金属材料,C错误;
D.玻璃纤维的主要成分是二氧化硅等非金属氧化物,属于无机非金属材料,因此不属于金属材料,D错
误;
故选A。
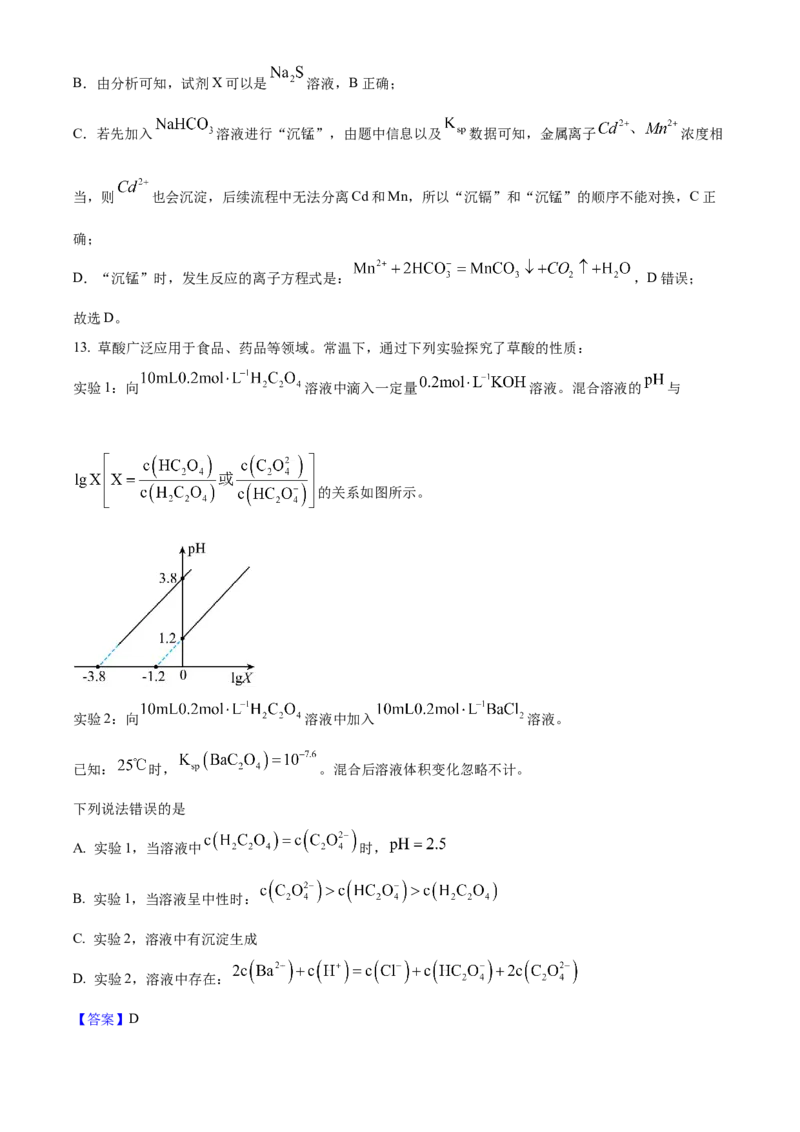
2. 化学实验充满着五颜六色的变化。下列描述错误的是B.产生红色沉 D.试纸变为蓝
A.溶液褪色 C.溶液呈紫色
淀 色
.
A A B. B C. C D. D
【答案】B
【解析】
A. 乙烯与酸性KMnO 溶液反应,溶液褪色,故A正确;
4
B. KOH溶液与CuSO 溶液反应生成Cu(OH) 蓝色沉淀,故B错误;
4 2
C. FeCl 溶液与苯酚发生显色反应生成紫色络合物,故C正确;
3
D. 浓氨水挥发出的氨气遇到湿润的红色石蕊试纸,发生反应: ,
试纸变为蓝色,故D正确。
故选B。
3. 加热时,浓硫酸与木炭发生反应: (浓) 。设 为阿伏加德罗
常数的值。下列说法正确的是
A. 含质子数为
B. 常温常压下, 含σ键数目为
C. 的稀硫酸中含 数目为
D. 与 充分反应得到 的分子数为
【答案】A
【解析】
A.12g的12C的物质的量为1mol,每个12C原子含有6个质子,因此总质子数为6N ,A正确;
A
B.常温常压下,6.72L CO 的物质的量小于0.3mol,每个CO 分子含2个σ键,总σ键数小于0.6N ,B错
2 2 A
误;C.pH=1的稀硫酸中, 浓度为0.1mol/L,1L溶液中 数目为0.1N ,而非0.2N ,C错误;
A A
D.SO 与O 生成SO 的反应为可逆反应,无法完全转化,实际生成的SO 分子数小于N ,D错误;
2 2 3 3 A
故选A。
4. 只用一种试剂,将 四种物质的溶液区分开,这种试剂是
A. 溶液 B. 溶液 C. 溶液 D. 溶液
【答案】D
【解析】
A.NaOH溶液分别和Na SO 、KNO 溶液混合时都没有明显现象,无法鉴别Na SO 、KNO ,故
2 4 3 2 4 3
A错误;
B.AgNO 溶液和Na SO 、(N H ) CO 、AlCl 溶液都能生成白色沉淀,无法鉴别
3 2 4 4 2 3 3
Na SO 、(N H ) CO
2 4 4 2 3
、AlCl ,故B错误;
3
C.稀硫酸分别和Na SO 、AlCl 、KNO 溶液混合,都没有明显现象,无法鉴别
2 4 3 3
Na SO 、AlCl 、KNO ,故C错误;
2 4 3 3
D.Ba(OH) 溶液分别和Na SO 、(N H ) CO 、AlCl 、KNO 溶液混合时,现象分别为:生成白
2 2 4 4 2 3 3 3
色沉淀、生成气体、先生成白色沉淀后沉淀溶解、无明显现象,现象不同,可以鉴别,故D正确。
故选D。
5. 下列有关物质性质的解释错误的是
性质 解释
A 酸性: 是推电子基团
熔点:
B 的体积大于
C 熔点: 比 的金属性弱
D 沸点: 分子间存在氢键
A. A B. B C. C D. D
【答案】C
【解析】
A.羧酸酸性强弱与烃基的电子效应有关,−CH 是推电子基团,会使CH COOH中羧基的电子云密度相
3 3对
HCOOH更大,H+更难电离,所以酸性CH COOHH S,解释合
2 2 2 2
理,D项正确;
故选C。
6. 浓溶液中含有的 具有酸性,能溶解金属氧化物。元素X、Y、Z、M的原子序数依
次增大,分别位于不同的前四周期。Y的最外层电子数是内层的3倍,X和Y的最外层电子数之和等于Z
的最外层电子数,M的价层电子排布是 。下列说法正确的是
A. 电负性:
B. Y形成的两种单质均为非极性分子
C. 由X、Y、Z形成的化合物均为强电解质
D. 铁管上镶嵌M,铁管不易被腐蚀
【答案】D
【解析】
【分析】Y的最外层电子数是内层的3倍,则Y的最外层电子数为6,Y为O,X和Y的最外层电子数之
和等于Z的最外层电子数,则X的最外层电子数应为1,原子序数小于氧元素,则X为H,Z的最外层电
子数为7,则Z为Cl,M的价层电子排布是 ,M是Zn,综上所述:X为H、Y为O、Z为Cl、M
是Zn,据此解答;
A.非金属性越强,电负性越大, 中O为负化合价,因此X(H)的电负性小于Y(O),A错误;B.Y(O)的单质O 是非极性分子,但O 是极性分子(V形结构导致偶极矩不为零),B错误;
2 3
C.X(H)、Y(O)、Z(Cl)形成的化合物如HClO,属于弱电解质,并非全部为强电解质,C错误;
D.M为Zn,比Fe活泼,镶嵌Zn会通过牺牲阳极保护铁管,使其不易被腐蚀,D正确;
故选D。
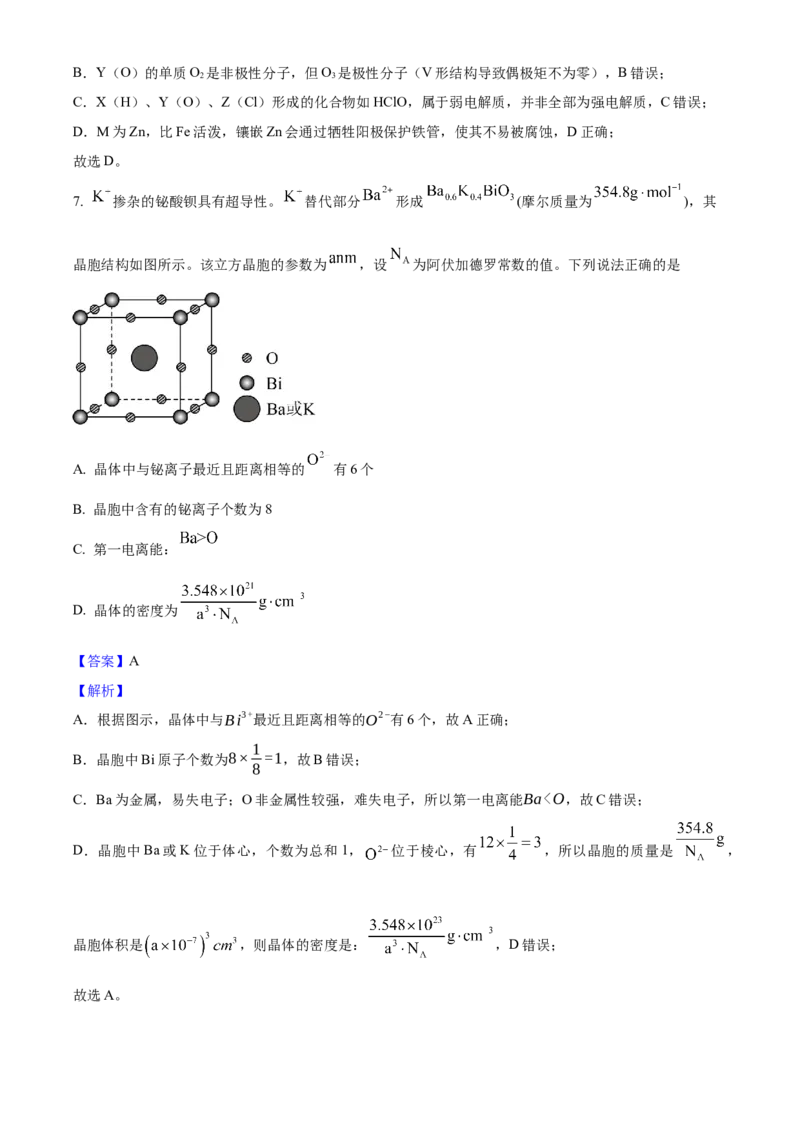
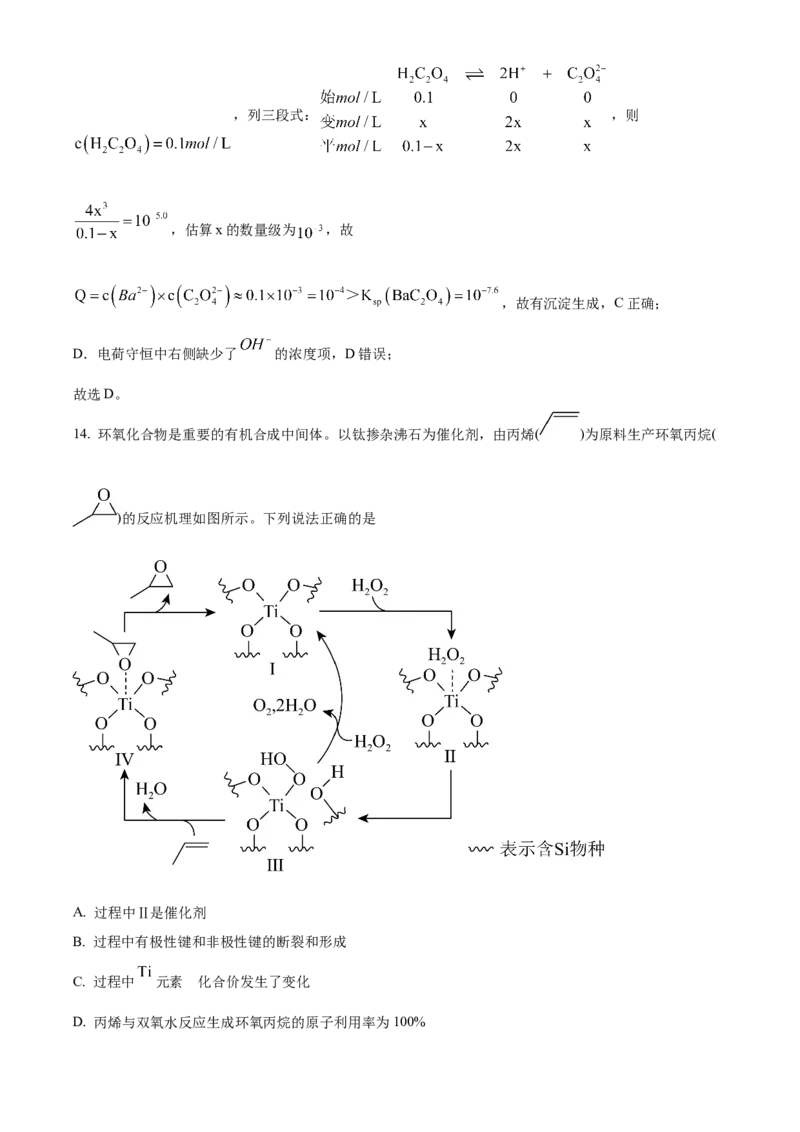
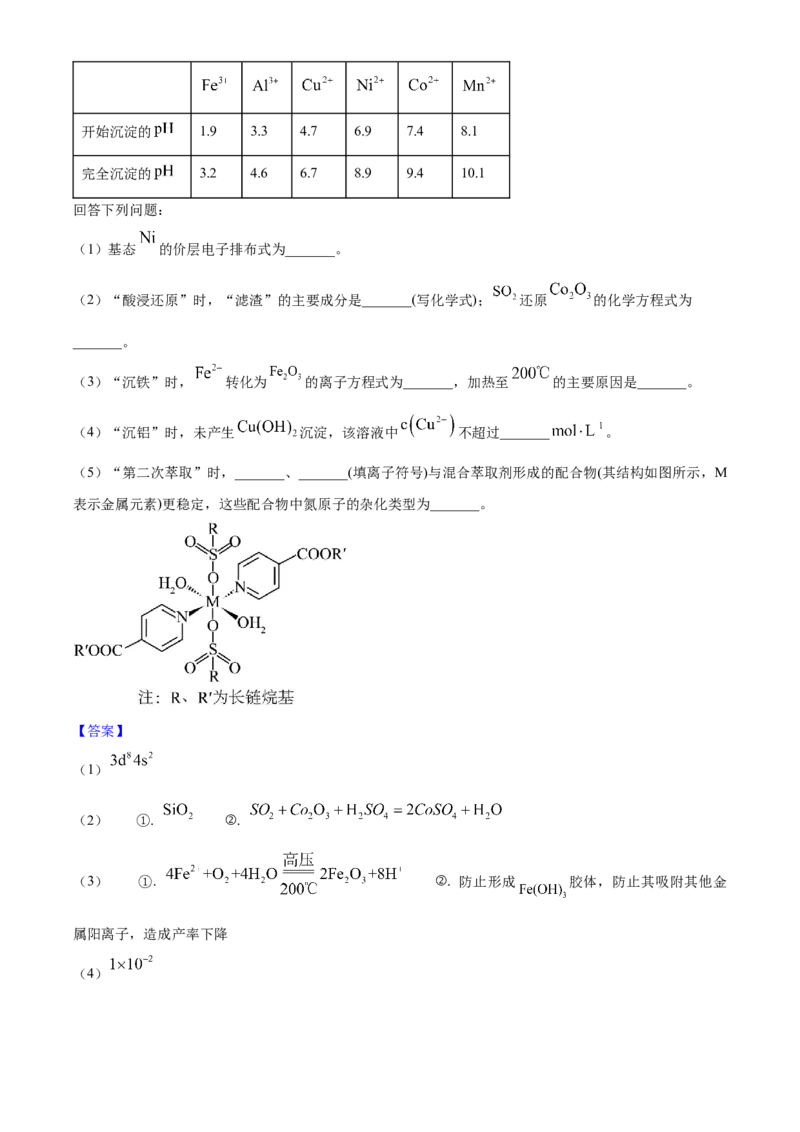
7. 掺杂的铋酸钡具有超导性。 替代部分 形成 (摩尔质量为 ),其
晶胞结构如图所示。该立方晶胞的参数为 ,设 为阿伏加德罗常数的值。下列说法正确的是
A. 晶体中与铋离子最近且距离相等的 有6个
B. 晶胞中含有的铋离子个数为8
C. 第一电离能:
D. 晶体的密度为
【答案】A
【解析】
A.根据图示,晶体中与Bi3+最近且距离相等的O2−有6个,故A正确;
1
B.晶胞中Bi原子个数为8× =1,故B错误;
8
C.Ba为金属,易失电子;O非金属性较强,难失电子,所以第一电离能Ba