文档内容
相对原子质量(原子量):H-1 N-14 O-16 Al-27
一、选择题(本大题共7个小题,每小题6分,共42分,在每小题给出的4个选项中,
只有一项符合题目要求)
1.在水溶液中能量共存的一组离子是( )
A.Na+、Ba2+、Cl-、NO - B. Pb2+、Hg2+、S2-、SO 2-
3 4
C.NH +、H+、SO2-、PO 3- D.ClO-、Al3+、Br-、CO2-
4 2 3 4 3
3.下列排序正确的是( )
A.酸性:HCO<C HOH<HCOOH
2 3 6 5 3
B.碱性:Ba(OH) <Ca(OH) <KOH
2 2
C.熔点:MgBr <SiCl <BN
2 4
D.沸点:PH <NH <HO
3 3 2
4.按以下实验方案可以从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物。
水层溶液 析出固体(粗产品)
⑶
NaNO 溶液
滤渣 3
甲苯+甲醇 ⑵
样品粉末
⑴ 有机层溶液 甲苯
⑷
不溶性物质
下列说法错误的是( )
A.步骤(1)需要过滤装置 B.步骤(2)需要用到分流漏斗
C.步骤(3)需要用到坩埚 D.步骤(4)需要蒸馏装置
5.有机物X和Y可作为“分子伞”给药物载体的伞面和中心支撑架(未表示出原子或原子团的空
间排列)
第1页 | 共5页COOH
OH
H NCHCHCHNHCHCHCHCHNH
2 2 2 2 2 2 2 2 2
HO OH
X(C H O ) Y
24 40 5
下列叙述错误的是( )
A.1molX在浓硫酸作用下发生消去反应,最多生成3molH O
2
B.1molY发生类似酯化的反应,最多消耗2molX
C.X与足量HBr反应,所得有机物的分子式为C H OBr
24 37 2 3
D.Y与癸烷的分子链均呈锯齿形,但Y的极性较强
7.将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s) 2G(g)。忽略固体体积,
平衡时G的体积分数(%)随温度和压强的变化如下表所示。
压强/MPa
体积分数/%
1.0 2.0 3.0
温度/℃
810 54.0 a b
915 c 75.0 d
1000 e f 83.0
① b<f ② 915℃、2.0MPa 时 E 的转化率为 60% ③该反应的 ΔS>0 ④ K(1000℃)>
K(810℃)
上述①~④中正确的有( )
A.4个 B.3个 C.2个 D.1个
二、非选择题(本大题共4小题,共58分)
第2页 | 共5页8.(14分)合金是建筑航空母舰的主体材料。
(1)航母升降机可由铝合金制造。
①铝元素在周期表中的位置是 。工业炼铝的原料由铝土矿提
取而得,提取过程中通入的气体为 。
② Al—Mg 合 金 焊 接 前 用 NaOH 溶 液 处 理 Al O 膜 , 其 化 学 方 程 式 为
2 3
。焊接过程中使用的保护气为 (填化学式)。
(2)航母舰体材料为合金钢。
①舰体在海水中发生的电化学腐蚀主要为 。
②航母用钢可由低硅生铁冶炼而成,则在炼铁过程中为降低硅含量需加入的物质为
(3)航母螺旋浆主要用铜合金制造。
开始 1 2 3 4 5 7 8 9 10 11 12
①80.0gCu-Al合金用酸完全溶解后,加入过量 沉淀 6
氨水,过滤得到白色沉淀 39.0,则合金中Cu的质量
Fe3+ Al3+ Cu2+ Fe2+ Ni2+ Mg2+
分数为
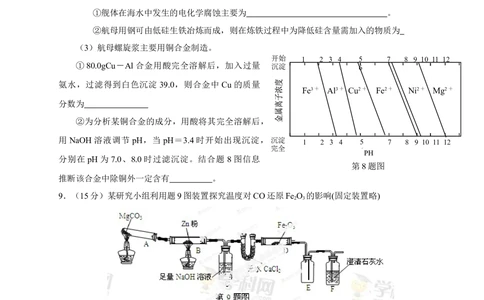
②为分析某铜合金的成分,用酸将其完全溶解后,
用NaOH溶液调节pH,当pH=3.4时开始出现沉淀,沉淀
1 2 3 4 5 7 8 9 10 11 12
完全 6
PH
分别在pH为7.0、8.0时过滤沉淀。结合题 8图信息
第8题图
推断该合金中除铜外一定含有 。
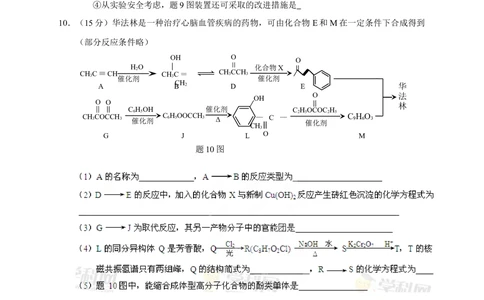
9.(15分)某研究小组利用题9图装置探究温度对CO还原Fe O 的影响(固定装置略)
2 3
(1)MgCO 的分解产物为
3
(2)装置C的作用是 ,处理尾气的方法为
(3)将研究小组分为两组,按题9图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对
装置D加热,反应产物均为黑色粉末(纯净物),两组分别用产物进行以下实验。
步骤 操作 甲组现象 乙组现象
1 取黑色粉末加入稀盐酸 溶解,无气泡 溶解,有气泡
第3页 | 共5页2 取步骤1中溶液,滴加K[Fe(CN) ]溶液 蓝色沉淀 蓝色沉淀
3 6
3 取步骤1中溶液,滴加KSCN溶液 变红 无现象
4 向步骤3溶液中滴加新制氯水 红色褪去 先变红,后褪色
①乙组得到的黑色粉末是
②甲组步骤1中反应的离子方程式为
③乙组步骤4中,溶液变红的原因为 ;
溶液褪色可能的原因及其验证方法为
④从实验安全考虑,题9图装置还可采取的改进措施是
10.(15分)华法林是一种治疗心脑血管疾病的药物,可由化合物E和M在一定条件下合成得到
(部分反应条件略)
OH O
O
CH 3 C≡CH 催 化 H 剂 2 O CH 3 C= CH 3 CCH 3 化 催 合 化 物 剂 X
CH
A B 2 D E 华
O 法
OH
O O
林
CH 3 COCCH 3 C 催 6 H 化 5 O 剂 H C 6 H 5 OOCCH 3 催化 Δ 剂 — C — C 2 H 5 催 OC 化 O 剂 C 2 H 5 C 9 H 6 O 3
CH
3
G J L O M
题10图
O O
(6)已知:LM的原理为:①C H OH+C H OCR
催 化
C
剂
H OCR +C H OH和
6 5 2 5 6 5 2 5
O O O O
催化剂
②R CCH +C H OCR R CCH CR +C H OH,M的结构简式为
1 3 2 5 2 1 2 2 2 5
第4页 | 共5页11. (14分)化学在环境保护中起着十分重要的作用,催化反硝化法和电化学降解法可用于治理水
中硝酸盐的污染。
(1)催化反硝化法中,H 能将NO -还原为N 。25℃时,反应进行10min,溶液的pH由7变
2 3 2
为12。
①N 的结构式为 。
2
②上述反应的离子方程式为 ,其平
均反应速率υ(NO -)为 mol·L-1min-1。
3
③ 还 原 过 程 中 可 生 成 中 间 产 物 NO - , 写 出 3 种 促 进 NO - 水 解 的 方 法
2 2
。
(2)电化学降解NO -的原理如题11图所示。
3
①电源正极为 (填A或B),阴极反应式为 。
②若电解过程中转移了 2mol 电子,则膜两侧电解液的质量变化差(Δm -Δm )为
左 右
g。
第5页 | 共5页