文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
专题 16 物质的检验与鉴别
知识点一、常见气体的检验与鉴别
常见气体的检验与鉴别
气体 检验方法 现象
氧气 带火星的木条伸入集气瓶 木条复燃
二氧化 通入澄清的石灰水 石灰水变浑浊
碳
氢气 点燃,在火焰上方罩干冷的烧杯 纯净气体能安静燃烧,有淡蓝色火焰,烧
杯内壁有水珠
依次通过灼热的氧化铜和白色的无水硫酸铜 黑色氧化铜变红,白色无水硫酸铜粉末
粉末 变蓝
一氧化 点燃,在火焰上方罩涂有澄清石灰水的烧杯 燃烧产生蓝色火焰,烧杯内壁石灰水变
碳 浑浊
依次通过灼热的氧化铜和澄清石灰水 黑色氧化铜变红,澄清石灰水变浑浊
甲烷 点燃,在火焰上方罩干冷的烧杯,迅速倒转后, 烧杯内壁有水珠,澄清石灰水变浑浊
注入少量澄清石灰水
氨气 用湿润的红色石蕊试纸放在试管口 红色石蕊试纸变蓝
水蒸气 用燃着的木条伸入,再加入澄清石灰水,振荡 木条的火焰熄灭,澄清石灰水不变浑浊
氮气 通入酸化的AgNO 溶液 产生白色沉淀
3
【1 淘宝店铺:向阳百分百】关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
知识点二、物质的检验与鉴别综合运用
(一)常见离子的检验与鉴别
离子 试剂、方法 实验现象
酸(H+) ①滴加紫色石蕊试液;②pH试纸;③加入 ①变红;②pH<7;③产生气泡
Zn粒
碱(OH-) ①滴加紫色石蕊试液;②滴加无色酚酞试 ①变蓝;②变红;③pH>7
液;③pH试纸
Cl- 加入AgNO 溶液和稀硝酸 产生白色沉淀,且白色沉淀不溶解
3
SO2
4
− 加入稀盐酸酸化后再加入BaCl
2
溶液 酸化后无现象,加入BaCl
2
后产生白色沉淀
CO2− 加入稀盐酸,将产生的气体通入澄清的石 有无色无味气体产生,石灰水变浑浊
3
灰水中
NH+ 加入强碱,加热,将产生的气体用湿润红色 产生有刺激性气味的气体,试纸变蓝
4
石蕊试纸检验
Fe3+ 加入强碱溶液 产生红褐色沉淀
Cu2+ 插入铁丝(或加入强碱溶液) 铁丝附有红色物质(或产生蓝色沉淀)
(二)日常生活中一些常见物质的检验与鉴别
1. 化肥的鉴别
(1)铵态氮肥:白色,易溶于水,与熟石灰研磨会产生有刺激性气味的气体。
(2)磷肥:多呈灰白色,不溶于水。
(3)钾肥:白色,易溶于水,与熟石灰研磨没有刺激性气味的气体产生。
2. 硬水和软水的鉴别:用肥皂水,有浮渣产生或泡沫较少的是硬水,泡沫较多的是软水。
3. 羊毛织品、合成纤维和棉织品的鉴别(灼烧法):灼烧,产生烧焦羽毛气味且不易结球的为羊毛织品;
有特殊气味,易结球的为合成纤维;产生烧纸味,不结球的是棉织品。
考点一.常见气体的检验与除杂方法
1.(2023•自贡)下列方法能区分氮气和二氧化碳两瓶气体的是( )
A.观察颜色
B.闻气味
C.将燃着的木条伸入集气瓶中
D.倒入适量澄清石灰水
【解答】解:A、氮气和二氧化碳两瓶气体均没有颜色,用观察颜色的方法不能鉴别,故选项错
【2 淘宝店铺:向阳百分百】关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
误。
B、氮气和二氧化碳两瓶气体均没有气味,用闻气味的方法不能鉴别,故选项错误。
C、氮气和二氧化碳均不能燃烧、不能支持燃烧,均能使燃着的木条熄灭,不能鉴别,故选项错
误。
D、二氧化碳能使澄清的石灰水变浑浊,氮气不能,倒入适量澄清石灰水,能使澄清石灰水变浑
浊的是二氧化碳,无明显现象的是氮气,可以鉴别,故选项正确。
故选:D。
2.(2023•东城区校级模拟)下列方法能鉴别空气、氧气和二氧化碳3瓶气体的是( )
A.闻气味
B.向集气瓶中倒入澄清的石灰水
C.观察颜色
D.将燃着的木条伸入集气瓶中
【解答】解:A、空气、氧气和二氧化碳3瓶气体均没有气味,用闻气味的方法不能鉴别,故选
项错误。
B、二氧化碳能使澄清的石灰水变浑浊,用澄清的石灰水只能鉴别出二氧化碳,无法鉴别空气、
氧气,故选项错误。
C、空气、氧气和二氧化碳3瓶气体均没有颜色,用观察颜色的方法不能鉴别,故选项错误。
D、把燃着的木条分别伸入三个集气瓶中,若木条熄灭,则是二氧化碳;若木条燃烧更旺,则是
氧气;若木条正常燃烧,则是空气;现象明显,能一次鉴别出这三瓶气体,故选项正确。
故选:D。
3.(2023•肇东市校级模拟)下列方法能区分二氧化碳和空气两瓶气体的是( )
A.闻气味
B.观察颜色
C.将燃着的木条伸入瓶中
D.倒入相同体积的水
【解答】解:A、二氧化碳和空气均没有气味,用闻气味的方法不能鉴别,故选项错误。
B、二氧化碳和空气均没有颜色,用观察颜色的方法不能鉴别,故选项错误。
C、把燃着的木条分别伸入两个集气瓶中,若木条熄灭,则是二氧化碳;若木条正常燃烧,则是
空气;现象明显,可以鉴别,故选项正确。
【3 淘宝店铺:向阳百分百】关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
D、二氧化碳能溶于水,能与水反应,但无明显变化,空气不易溶于水,不能鉴别,故选项错误。
故选:C。
4.(2023•衡阳县模拟)某无色气体可能含有 CO 、CO、H 中的一种或几种,依次进行以下实验:
2 2
①通过澄清石灰水后,石灰水变浑浊;②通过灼热的氧化铜时,固体变成红色;③通过澄清
石灰水,石灰水变浑浊;④通过白色硫酸铜粉末,粉末变成蓝色。(提示:白色硫酸铜粉末遇
水变蓝)。则下列判断正确的是( )
A.原混合气体中一定有CO 、CO、H
2 2
B.原混合气体中一定有CO ,可能有CO、H
2 2
C.原混合气体中一定有CO 、H 、可能有CO
2 2
D.原混合气体中一定有CO 、CO,可能有H
2 2
【解答】解:①通过澄清石灰水后,石灰水变浑浊,说明气体中含有二氧化碳;
②通过灼热的氧化铜时,固体变成红色,说明氧化铜被还原成铜,CO、H 都能还原氧化铜,无
2
法确定是含有一种,还是两种都有;
③通过澄清石灰水,石灰水变浑浊,说明上一步反应后生成了二氧化碳,能判断出气体中含有
CO,CO还原氧化铜生成铜和二氧化碳;
④通过白色硫酸铜粉末变成蓝色,说明硫酸铜遇到了水,此时的水有可能是生成的水,也可能
是从澄清石灰水中带出来的水蒸气;
故原混合气体中一定含有CO 、CO,可能含有氢气;
2
故选:D。
5.(2023•黄冈模拟)某无色气体可能含有 H 、CO、CH 中的一种或几种,依次进行下列实验
2 4
(假设每一步反应或吸收均完全):①无色气体在氧气中充分燃烧;②燃烧生成的气体先通过
盛浓硫酸的洗气瓶,装置质量增加10.8g;③再将剩余气体通过盛NaOH溶液的洗气瓶,装置质
量增加13.2g。下列推断正确的是( )
A.该气体一定含有H 、CO、CH
2 4
B.该气体可能含有H 和CO
2
C.该气体可能含有CO和CH
4
D.该气体只可能含有CH
4
【解答】解:由生成的气体通过浓硫酸,装置质量增加 10.8g,可判断燃烧生成了10.8g水,说
2
明混合气体中含氢元素,且氢元素质量=10.8g× ×100%=1.2g;
18
由气体通过氢氧化钠溶液,装置质量增加13.2g,可判断燃烧生成了13.2g二氧化碳,说明混合
【4 淘宝店铺:向阳百分百】关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
12
气体中含碳元素,且碳元素质量=13.2g× ×100%=3.6g;
44
甲烷气体中C、H元素质量比=12:(1×4)=3:1,则混合气体中C、H元素质量比=3.6g:
1.2g=3:1,因此可判断混合气体可能只有甲烷;也可能只含有CO和H ;也可能是甲烷、氢气、
2
一氧化碳同时存在,但不可能含有甲烷和另外任何一种气体。
故选:B。
6.(2023•正安县模拟)为证明某气体中是否含有 CO 、H 、CO、H O这四种成分,兴趣小组同
2 2 2
学设计了如图装置进行验证(实验开始前先向装置内通一段时间的 N )。则下列判断错误的是
2
( )
A.B中浓硫酸的作用是除去水蒸气
B.若C处CuO由黑变红,D处无水硫酸铜变蓝,则证明该气体中含有H
2
C.若A、E处澄清石灰水变浑浊,则证明该气体中含有CO和CO
2
D.若要证明气体中是否含有H O,则还需在A装置前加一个盛有无水硫酸铜的U形管
2
【解答】解:A.浓硫酸具有吸水性,不和CO 、H 、CO反应,B中浓硫酸的作用是除去水蒸气,
2 2
故A正确;
B.B中的浓硫酸具有吸水性,进入C中的气体中不会含有水蒸气,若C处CuO由黑变红,D处
无水硫酸铜变蓝,则证明水是混合气体中含有的氢气和氧化铜反应生成,故B正确;
C.氢氧化钙微溶于水,不能证明A的澄清石灰水把混合气体中的二氧化碳吸收完全,所以使 E
处澄清石灰水变浑浊的二氧化碳可能是反应生成,也可能是原先含有的,故C错误;
D.若要证明气体中是否含有H O,则还需在A装置前加一个盛有无水硫酸铜的 U型管,如果硫
2
酸铜变蓝色,说明含有H O,否则没有,故D正确。
2
故选:C。
7.(2023•江岸区校级模拟)某气体由H 、N 、CO、CO 中的若干种组成,为了探究其成分,化
2 2 2
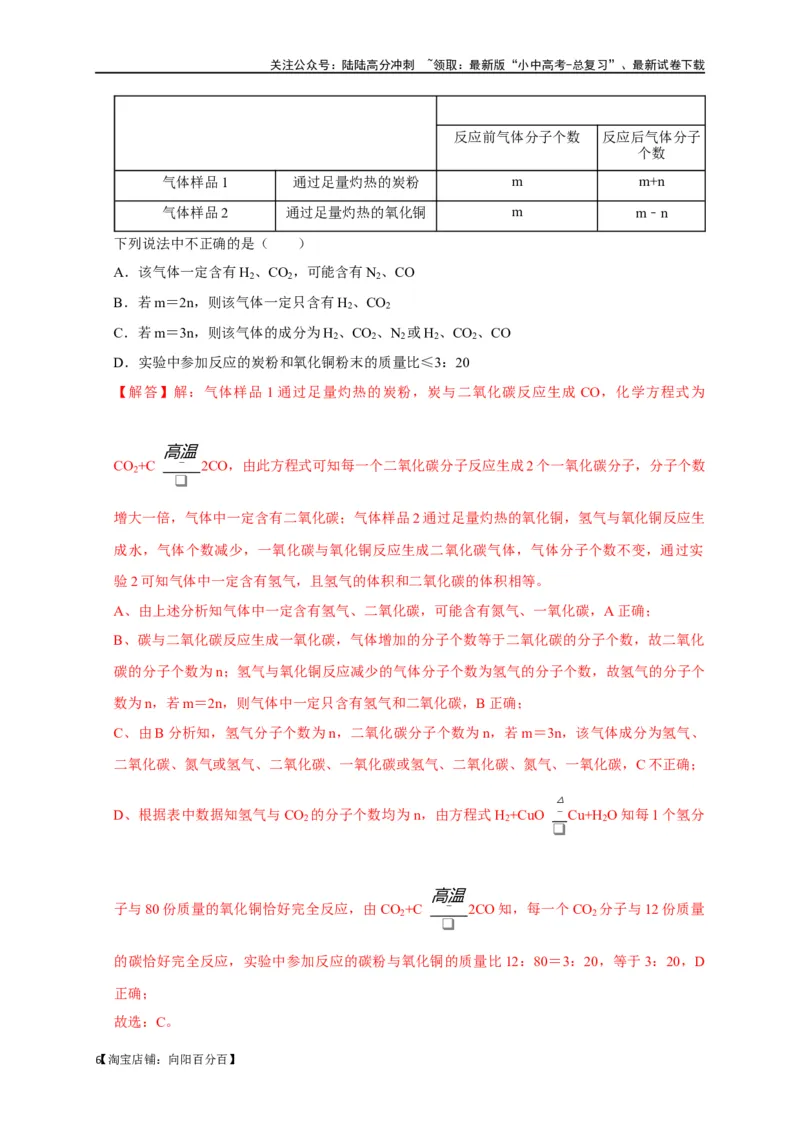
学兴趣小组取两份相同体积的该气体样品分别进行实验,测得气体分子个数的变化如下表所示:
实验操作(充分反应后冷却至室温) 实验结果
【5 淘宝店铺:向阳百分百】关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
反应前气体分子个数 反应后气体分子
个数
气体样品1 通过足量灼热的炭粉 m m+n
气体样品2 通过足量灼热的氧化铜 m m﹣n
下列说法中不正确的是( )
A.该气体一定含有H 、CO ,可能含有N 、CO
2 2 2
B.若m=2n,则该气体一定只含有H 、CO
2 2
C.若m=3n,则该气体的成分为H 、CO 、N 或H 、CO 、CO
2 2 2 2 2
D.实验中参加反应的炭粉和氧化铜粉末的质量比≤3:20
【解答】解:气体样品1通过足量灼热的炭粉,炭与二氧化碳反应生成 CO,化学方程式为
高温
CO 2 +C ¯ 2CO,由此方程式可知每一个二氧化碳分子反应生成2个一氧化碳分子,分子个数
❑
增大一倍,气体中一定含有二氧化碳;气体样品2通过足量灼热的氧化铜,氢气与氧化铜反应生
成水,气体个数减少,一氧化碳与氧化铜反应生成二氧化碳气体,气体分子个数不变,通过实
验2可知气体中一定含有氢气,且氢气的体积和二氧化碳的体积相等。
A、由上述分析知气体中一定含有氢气、二氧化碳,可能含有氮气、一氧化碳,A正确;
B、碳与二氧化碳反应生成一氧化碳,气体增加的分子个数等于二氧化碳的分子个数,故二氧化
碳的分子个数为n;氢气与氧化铜反应减少的气体分子个数为氢气的分子个数,故氢气的分子个
数为n,若m=2n,则气体中一定只含有氢气和二氧化碳,B正确;
C、由B分析知,氢气分子个数为n,二氧化碳分子个数为n,若m=3n,该气体成分为氢气、
二氧化碳、氮气或氢气、二氧化碳、一氧化碳或氢气、二氧化碳、氮气、一氧化碳,C不正确;
△
D、根据表中数据知氢气与CO 2 的分子个数均为n,由方程式H 2 +CuO ¯ Cu+H 2 O知每1个氢分
❑
高温
子与80份质量的氧化铜恰好完全反应,由CO 2 +C ¯ 2CO知,每一个CO 2 分子与12份质量
❑
的碳恰好完全反应,实验中参加反应的碳粉与氧化铜的质量比12:80=3:20,等于3:20,D
正确;
故选:C。
【6 淘宝店铺:向阳百分百】关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
8.(2023•大庆)化学实验设计中经常涉及到“一器多用”和“多器一用”的情况。请根据下列装
置回答问题:
(1)图1为气体的收集装置:
①若用排空气法收集H ,气体的进气口为 b (填“a”或“b”)。
2
②若用排水法收集O ,气体的进气口为 b (填“a”或“b”)。
2
③图1也可用于除去CO中的CO 气体,则瓶内所盛装试剂为 氢氧化钠溶液 。
2
(2)图2为某同学设计的几种防倒吸装置,其中合理的是 CD 。
【解答】解:(1)①氢气的密度比空气的小,若用排空气法收集H ,气体的进气口为b,将空
2
气从长导管排出。
②若用排水法收集O ,长导管是出水管,气体的进气口为b。
2
③图1用于除去CO中的CO 气体,则瓶内所盛装试剂为氢氧化钠溶液,CO 能与氢氧化钠溶液
2 2
反应生成碳酸钠和水,CO不与氢氧化钠溶液反应,能除去杂质且没有引入新的杂质,符合除杂
原则。
(2)防止倒吸,可以增加气体和液体的接触面积,减小压强差,但漏斗被完全浸没在液面下,
无法起到防倒吸的作用;C中球形管可以起到缓冲作用,能防止倒吸;D中左侧导管刚刚露出塞
子,由装置的特点可知,可防止液体倒吸,则BCD防倒吸装置设计合理,E起不到放倒吸的作
用。
故答案为:
(1)①b;②b;③氢氧化钠溶液;
(2)CD。
9.(2023•深圳)已知H 与菱铁矿(主要成分FeCO ,其它成分不参与反应)反应制成纳米铁粉。
2 3
某小组进行探究并完成如下实验:
查阅资料:①H 能与CuO反应生成H O,H O能使无水硫酸铜变蓝
2 2 2
②CO 与无水硫酸铜不反应
2
(1)某同学探究反应后气体成分,先将反应后气体通入无水硫酸铜,无水硫酸铜变蓝,证明气
体中含有 水 ,再通入足量的澄清石灰水,澄清石灰水变浑浊,反应方程式为 CO +Ca
2
【7 淘宝店铺:向阳百分百】关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
( OH ) = CaCO ↓ +H O 。
2 3 2
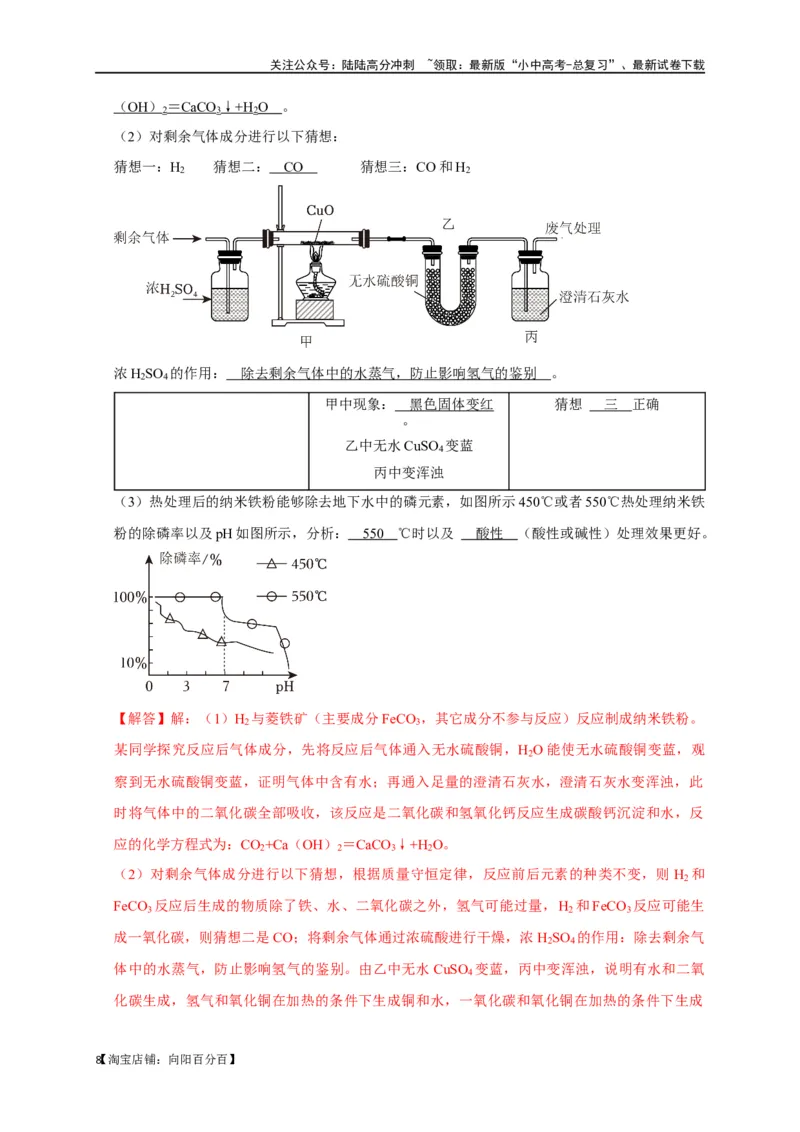
(2)对剩余气体成分进行以下猜想:
猜想一:H 猜想二: CO 猜想三:CO和H
2 2
浓H SO 的作用: 除去剩余气体中的水蒸气,防止影响氢气的鉴别 。
2 4
甲中现象: 黑色固体变红 猜想 三 正确
。
乙中无水CuSO 变蓝
4
丙中变浑浊
(3)热处理后的纳米铁粉能够除去地下水中的磷元素,如图所示450℃或者550℃热处理纳米铁
粉的除磷率以及pH如图所示,分析: 55 0 ℃时以及 酸性 (酸性或碱性)处理效果更好。
【解答】解:(1)H 与菱铁矿(主要成分FeCO ,其它成分不参与反应)反应制成纳米铁粉。
2 3
某同学探究反应后气体成分,先将反应后气体通入无水硫酸铜,H O能使无水硫酸铜变蓝,观
2
察到无水硫酸铜变蓝,证明气体中含有水;再通入足量的澄清石灰水,澄清石灰水变浑浊,此
时将气体中的二氧化碳全部吸收,该反应是二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,反
应的化学方程式为:CO +Ca(OH) =CaCO ↓+H O。
2 2 3 2
(2)对剩余气体成分进行以下猜想,根据质量守恒定律,反应前后元素的种类不变,则 H 和
2
FeCO 反应后生成的物质除了铁、水、二氧化碳之外,氢气可能过量,H 和FeCO 反应可能生
3 2 3
成一氧化碳,则猜想二是CO;将剩余气体通过浓硫酸进行干燥,浓H SO 的作用:除去剩余气
2 4
体中的水蒸气,防止影响氢气的鉴别。由乙中无水CuSO 变蓝,丙中变浑浊,说明有水和二氧
4
化碳生成,氢气和氧化铜在加热的条件下生成铜和水,一氧化碳和氧化铜在加热的条件下生成
【8 淘宝店铺:向阳百分百】关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
铜和二氧化碳,则甲中现象是:黑色固体变红;由此可知剩余气体中有氢气和一氧化碳,所以
猜想三正确。
(3)热处理后的纳米铁粉能够除去地下水中的磷元素,如图所示450℃或者550℃热处理纳米铁
粉的除磷率以及pH如图所示,由图可知,在550℃时以及酸性条件下处理效果更好。
故答案为:
(1)水;CO +Ca(OH) =CaCO ↓+H O;
2 2 3 2
(2)CO;除去剩余气体中的水蒸气,防止影响氢气的鉴别;黑色固体变红;三;
(3)550;酸性。
考点二.常见离子的检验方法及现象
10.(2022•贵阳)用如图装置进行实验(操作:打开活塞向锥形瓶中滴加Y后关闭活塞,一段时
间后打开弹簧夹)。下列选项正确的是( )
A.X是NH NO 固体,Y是水,Z是水,观察到导管口有气泡冒出
4 3
B.X是可能变质的NaOH固体,Y是稀盐酸,Z是水,观察到导管口有气泡冒出,证明NaOH
已经变质
C.X是CO ,Y是NaOH溶液,Z是Ca(OH) 溶液,观察到Ca(OH) 溶液倒流入锥形瓶中,
2 2 2
产生白色沉淀,不能证明CO 能与氢氧化钠反应
2
D.X是白色固体,Y是稀盐酸,Z是Ba(OH) 溶液,观察到烧杯中产生白色沉淀,则X含有
2
CO 2﹣
3
【解答】解:A、硝酸铵溶于水,温度降低,锥形瓶内压强减小,烧杯中水沿导管上升,故A错
误。
B、氢氧化钠变质是氢氧化钠与二氧化碳反应生成碳酸钠,碳酸钠与盐酸反应生成气体,但氢氧
化钠固体溶于水放热,瓶内压强增加,导管口也有气泡冒出,故B错误。
C、氢氧化钠与二氧化碳反应生成碳酸钠和水,瓶内压强减小,Ca(OH) 溶液倒流入锥形瓶中,
2
碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,但二氧化碳溶于水,也能使瓶内压强减小,
Ca(OH) 溶液倒流入锥形瓶中,氢氧化钙与二氧化碳反应也生成碳酸钙白色沉淀,故不能证
2
【9 淘宝店铺:向阳百分百】关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
明CO 能与氢氧化钠反应,故C正确。
2
D、碳酸根离子或碳酸氢根离子与盐酸反应都生成二氧化碳,二氧化碳与氢氧化钡反应生成碳酸
钡白色沉淀,故X含有碳酸根离子或碳酸氢根离子,故D错误。
故选:C。
11.(2022•苏州)向溶液X中加入氢氧化钠溶液,加热,产生的气体能使湿润的红色石蕊试纸变
蓝。则溶液X中一定含有的微粒是( )
A.Cl﹣ B.CO 2﹣ C.Ca2+ D.NH +
3 4
【解答】解:向溶液X中加入氢氧化钠溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝,
说明生成了氨气,则溶液X中一定含有的微粒是NH +。
4
故选:D。
12.(2022•眉山)某无色水溶液中可能含有以下离子中的几种:H+、Mg2+、Cu2+、Cl﹣、CO2−
、
3
SO2−
,为确定其成分,小芳进行了以下实验:
4
①经测定,溶液pH=1;
②取部分未知溶液加入过量NaOH溶液,有白色沉淀产生,过滤;
③取②的部分滤液加入BaCl 溶液,有白色沉淀产生。
2
分析上述实验,下列对溶液中含有离子的判断正确的是( )
A.一定含有H+、Mg2+,可能含有CO2−
3
B.一定含有H+、Mg2+、SO2−,可能含有Cl﹣
4
C.一定含有H+、Mg2+,可能含有Cu2+
D.一定含有H+、Mg2+、SO2−,可能含有Cu2+、Cl﹣
4
【解答】解:镁离子和碳酸根离子会生成溶于酸的碳酸镁沉淀,铜离子在溶液中显蓝色,镁离
子和氢氧根离子会生成氢氧化镁沉淀,铜离子和氢氧根离子会生成氢氧化铜沉淀,钡离子和硫
酸根离子反应生成不溶于酸的硫酸钡沉淀,和碳酸根离子反应生成溶于酸的碳酸钡沉淀。
①经测定,溶液pH=1,溶液中含有大量的氢离子,所以样品中一定不含碳酸根离子;
②取部分未知溶液加入过量NaOH溶液,有白色沉淀产生,过滤,所以样品中一定含有镁离子,
一定不含铜离子;
③取②的部分滤液加入BaCl 溶液,有白色沉淀产生,所以样品中一定含有硫酸根离子,题中
2
【10淘宝店铺:向阳百分百】关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
的现象不能确定是否含有氯离子,
A、一定含有H+、Mg2+、SO2−,一定不含碳酸根离子,故A错误;
4
B、一定含有H+、Mg2+、SO2−,可能含有Cl﹣,故B正确;
4
C、一定含有H+、Mg2+、SO2−,一定不含铜离子,故C错误;
4
D、一定含有H+、Mg2+、SO2−,可能含有Cl﹣,一定不含铜离子,故D错误。
4
故选:B。
13.(2022•丽水)某兴趣小组为探究“猪肝中的铁元素”,进行了以下实验:选用新鲜猪肝,如
图操作,将猪肝中的铁转化为铁离子,再用硫氰化钾溶液检验(硫氰化钾溶液遇铁离子变红
色)。有关该实验的说法正确的是( )
A.实验研究的问题是新鲜猪肝中是否含有铁离子
B.新鲜猪肝中的铁是以游离态形式存在的
C.实验中获得的土黄色混合液属于溶液
D.新鲜猪肝中含铁元素的证据是滴加硫氰化钾溶液后溶液变红
【解答】解:A、由题干信息可知,实验研究的问题是新鲜猪肝中是否含有铁元素,故A错误;
B、新鲜猪肝中的铁是以化合态形式(亚铁离子)存在的,故B错误;
C、实验中获得的土黄色混合液中有难溶性物质,属于悬浊液,故C错误;
D、因为硫氰化钾溶液遇铁离子变红色,则新鲜猪肝中含铁元素的证据是滴加硫氰化钾溶液后溶
液变红,故D正确。
故选:D。
14.(2023•邹城市校级二模)某实验废液中可能含有以下几种离子:Na+、Ca2+、Cl﹣、Ba2+、
SO2− 、CO2−
,现取两份100mL溶液进行如下实验:
4 3
(1)第一份加入AgNO 溶液,有白色沉淀生成;
3
(2)第二份加入适量稀硫酸,有无色气体生成;
【11淘宝店铺:向阳百分百】关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(3)向步骤(2)所得溶液中滴加BaCl 溶液,有白色沉淀生成。
2
根据上述实验,以下推测中正确的是( )
A.废液中一定存在Na+、CO2−,可能含有SO2−、Cl﹣
3 4
B.废液中一定存在Cl﹣、SO2− 、CO2− ,一定不存在Ca2+、Ba2+
4 3
C.废液中一定存在Na+、Cl﹣、CO2− 、SO2− ,一定不存在Ca2+、Ba2+
3 4
D.废液中一定存在Na+、Cl﹣、CO2− ,可能含有SO2−
3 4
【解答】解:A、由分析可知:废液中一定存在钠离子、碳酸根离子,可能存在硫酸根离子、氯
离子,故A正确;
B、由分析可知:废液中可能存在硫酸根离子、氯离子,故B错误;
C、由分析可知:废液中可能存在硫酸根离子、氯离子,故C错误;
D、由分析可知:废液中可能存在硫酸根离子、氯离子,故D错误。
故选:A。
15.(2023•济宁一模)某固体由Ba2+、Cu2+、Na+、Cl﹣、CO 2﹣、SO 2﹣中的几种离子构成,取一
3 4
定质量的该固体样品,进行如下实验:
①将固体溶于水得无色透明溶液,加入足量BaCl 溶液,过滤,得到白色沉淀
2
②在白色沉淀中加入过量稀硝酸,沉淀部分溶解
③在滤液中滴加足量AgNO 溶液,产生白色沉淀
3
由上述实验得出的下列判断中,正确的是( )
A.通过步骤①可以确定原固体中一定不含的离子只有Cu2+
B.无法确定该固体中是否含有Na+和Cl﹣
C.该固体由Na+、Cl﹣、CO 2﹣、SO 2﹣四种离子构成
3 4
D.将步骤①改为滴加Ba(NO ) 溶液,则通过步骤③可以确定固体中是否含有Cl﹣
3 2
【解答】解:①将固体溶于水得无色透明溶液,说明一定不含有铜离子,加入足量 BaCl 溶液,
2
过滤后得到白色沉淀,说明不会含有钡离子,可能含有碳酸根离子或是硫酸根离子,故产生的
沉淀可能是碳酸钡或是硫酸钡;
②在白色沉淀中加入过量稀硝酸沉淀全部溶解,说明沉淀是碳酸钡,原物质中一定含有碳酸根
离子,不含有硫酸根离子;
③在滤液中滴加足量AgNO 溶液,产生自色沉淀,由于步骤①加入了氯化钡,故不能确定是
3
【12淘宝店铺:向阳百分百】关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
否含有氯离子;
A、通过步骤①可以确定原固体中一定不含的离子有铜离子和钡离子,错误;
B、阳离子一定不含有铜离子和钡离子,故一定含有钠离子,错误;
C、由上述分析可知,该固体含有Na+、CO 2﹣,Cl﹣不能确定,错误;
3
D、将步骤①改为滴加Ba(NO ) 溶液,则通过步骤③可以确定固体中是否含有Cl﹣,正确。
3 2
故选:D。
16.(2023•泗水县四模)为确定某溶液中含有以下离子 H+、Mg2+、Ba2+、Cl﹣、CO 2﹣、NO ﹣中
3 3
的几种,进行了以下实验:①经测定,溶液pH=1;②取部分未知溶液,加入过量NaOH溶液,
有白色沉淀产生;③取②中部分溶液,加入Na CO 溶液,无明显现象。分析上述实验,下面
2 3
对溶液中含有离子的判断,正确的是( )
A.一定含有H+、Mg2+、Ba2+、Cl﹣、CO 2﹣、NO ﹣
3 3
B.一定含有H+、Mg2+、Cl﹣,一定不含有CO 2﹣
3
C.一定含有H+、Mg2+,可能同时含有Cl﹣、NO ﹣
3
D.一定含有H+、Ba2+、NO ﹣,一定不含有Cl﹣
3
【解答】解:A、由分析得:一定不含有CO 2﹣、Ba2+,故A错误;
3
B、不确定是否存在Cl﹣,故B错误;
C、一定含有H+、Mg2+,可能同时含有Cl﹣、NO ﹣,故C正确;
3
D、一定不含有Ba2+,故D错误。
故选:C。
17.(2022•济宁)某未知溶液中含有K+、NH +、Fe3+、Cl﹣、SO 2﹣、NO ﹣离子中的几种,为确
4 4 3
定溶液中可能含有的离子,进行以下实验探究:
(1)经观察,未知溶液呈浅黄色;
(2)取少量未知溶液,滴加足量的NaOH溶液并加热,有红褐色沉淀生成并伴有刺激性气味;
(3)另取少量未知溶液滴加Ba(NO ) 溶液,无明显现象。然后再滴加AgNO 溶液,有白色
3 2 3
沉淀生成。
请分析实验过程,推断:
溶液中一定存在的离子有 NH + 、 Fe 3+ 、 Cl ﹣ (填符号,下同),可能存在的离子有 K + 、
4
NO ﹣ ,一定不存在的离子是 SO 2 ﹣ 。
3 4
【解答】解:(1)经观察,未知溶液呈浅黄色,说明溶液中含有Fe3+;
(2)取少量未知溶液滴加足量的NaOH溶液并加热,有红褐色沉淀生成,说明生成了氢氧化铁
沉淀,则溶液中含有Fe3+;并伴有刺激性气味,说明生成了氨气,则说明溶液中含有NH +;
4
【13淘宝店铺:向阳百分百】关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(3)另取少量未知溶液滴加Ba(NO ) 溶液,无明显现象,说明溶液中不含硫酸根离子。然
3 2
后再滴加AgNO 溶液,有白色沉淀生成,说明生成了氯化银沉淀,说明溶液中含有Cl﹣;无法
3
确定K+、NO ﹣是否存在,
3
故溶液中一定存在的离子有NH +、Fe3+、Cl﹣;可能存在的离子有K+、NO ﹣,一定不存在的离
4 3
子是SO 2﹣。
4
故答案为:
NH +、Fe3+、Cl﹣;K+、NO ﹣;SO 2﹣。
4 3 4
一.选择题(共16小题)
1.(2023•迎泽区校级三模)下列有关气体的说法正确的是( )
A.仅用一盒火柴就可鉴别氢气、氧气、二氧化碳三种气体
B.氢气、氧气、二氧化碳三种气体是无色、无味、密度比空气大的气体
C.一氧化碳、二氧化碳均能与石灰水反应
D.氢气、一氧化碳还原氧化铜的反应类型都属于置换反应
【解答】解:A、将一燃着的火柴分别深入三种气体中,能够熄灭的是二氧化碳,燃烧更旺的是
氧气,能够燃烧发出蓝色火焰的是氢气,故A正确;
B、因为氢气的密度比空气的密度小,故B错误;
C、二氧化碳能使澄清石灰水变浑浊,一氧化碳不能与石灰水反应,故C错误;
D、置换反应是单质与化合物反应,生成另一种单质,另一种化合物,一氧化碳还原氧化铜的反
应中没有单质,故D错误。
故选:A。
2.(2023•白山一模)对某种溶液中的离子进行检验,下述结论中合理的是( )
A.先加BaCl 溶液,再加足量HNO 溶液,仍有白色沉淀,则该溶液一定含有SO2−
2 3 4
B.加入足量的CaCl 溶液,若产生白色沉淀,则该溶液中一定含有CO2−
2 3
C.加入酚酞溶液,溶液没变色,不能确定该溶液显中性
D.先加入稀盐酸,再加足量AgNO 溶液,若有白色沉淀,则该溶液中一定含有Cl﹣
3
【解答】解:A、钡离子能与硫酸根离子反应生成硫酸钡白色沉淀,硫酸钡不能与稀硝酸反应,
氯离子能与银离子反应生成氯化银白色沉淀,氯化银不能与稀硝酸反应,则在样品中先加氯化
【14淘宝店铺:向阳百分百】关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
钡溶液,再加足量稀硝酸溶液,仍有白色沉淀,则溶液中可能含有SO2− 或Ag+,故A不正确;
4
B、钙离子能与碳酸根离子反应生成碳酸钙白色沉淀,氯离子能与银离子反应生成氯化银白色沉
淀,在样品中加足量的氯化钙溶液,产生白色沉淀,则不一定含有CO2− ,也可能含有Ag+,故
3
B不正确;
C、酚酞溶液遇中性或酸性溶液均不变色,所以加入酚酞溶液,溶液没变色,不能确定该溶液显
中性,可能显酸性,故C正确;
D、在样品中先加盐酸使溶液呈酸性,引入氯离子,再加足量的硝酸银溶液,一定有白色沉淀,
不能确定溶液中含有氯离子,故D不正确。
故选:C。
3.(2023•青山区校级模拟)某固体由Ba2+、Cu2+、Na+、Cl﹣、CO 2﹣、SO 2﹣中的几种离子构成,
3 4
取一定质量的该固体样品,进行如下实验
:①将固体溶于水得无色透明溶液,加入足量BaCl 溶液过滤后得到5克白色沉淀。②在沉淀
2
中加入过量稀硝酸,仍有3克白色沉淀。③在滤液中滴加AgNO 溶液,产生白色沉淀。则该固
3
体中一定含有( )
A.Na+、CO 2﹣、SO 2﹣ B.Cu2+、CO 2﹣、SO 2﹣
3 4 3 4
C.Cl﹣、CO 2﹣、SO 2﹣ D.Ba2+、Na+、Cl﹣
3 4
【解答】解:①将固体溶于水得无色透明溶液,说明溶液中不含Cu2+;加入足量BaCl 溶液,
2
过滤后得到5克白色沉淀,沉淀可以是碳酸钡或硫酸钡或二者共存;②在沉淀中加入过量稀硝
酸,仍有3克白色沉淀,说明沉淀中含有硫酸钡,同时说明5克白色沉淀中含有能与稀硝酸反应
的物质,该物质应是碳酸钡,则说明该固体中一定含有CO 2﹣、SO 2﹣;
3 4
③在滤液中滴加AgNO 溶液,产生白色沉淀,加入足量BaCl 溶液中含有氯离子,由于氯离子
3 2
能与硝酸银反应生成生成氯化银沉淀,无法证明原固体中是否含有氯离子。
A、该固体中一定含有Na+、CO 2﹣、SO 2﹣,故选项正确;
3 4
Ba2+、SO 2﹣不能共存,故选项错误。
4
B、将固体溶于水得无色透明溶液,溶液中不含Cu2+,故选项错误;
C、溶液中不能只有阴离子,故选项错误;
D、Ba2+与CO 2﹣、SO 2﹣,不能共存,故选项错误;
3 4
故选:A。
4.(2023•亭湖区校级二模)推理是化学学习中重要的思维方法,下列推理合理的是( )
【15淘宝店铺:向阳百分百】关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.pH<7的溶液呈酸性,则酸溶液的pH一定小于7
B.溶液是均一稳定的液体,则均一稳定的液体一定是溶液
C.氧化物中都含有氧元素,则含有氧元素的化合物一定是氧化物
D.向未知溶液中加入BaCl 溶液,生成白色沉淀,则未知溶液中一定含SO2−
2 4
【解答】解:A.pH<7 的溶液呈酸性,则酸溶液的 pH一定小于 7,故A正确;
B.溶液是具有均一性和稳定性的混合物,故B错误;
C.由两种元素组成,其中一种元素是氧元素的化合物是氧化物,故C错误;
D.碳酸根离子也能与氯化钡反应生成白色沉淀,故D错误;
故选:A。
5.(2023•无为市校级模拟)如图,将胶头滴管中的物质X滴入装有物质Y的试管中,两种物质
充分混合。下列说法正确的是( )
A.X为水,若试管发烫,则Y一定是NaOH固体
B.X为BaCl 溶液,反应产生白色沉淀,则Y溶液中一定含有SO2−
2 4
C.X为Cu(NO ) 溶液,Y为Fe丝,根据现象可判断金属活动性:Fe>Cu
3 2
D.X为稀盐酸,Y为Ca(OH) ,该反应可应用于治疗胃酸过多症
2
【解答】解:A、X为水,若试管发烫,Y不一定是NaOH固体,还可能是生石灰或浓硫酸等,
错误;
B、X为BaCl 溶液,反应产生白色沉淀,则Y溶液中可能含有SO2−、CO2−或Ag+,错误;
2 4 3
C、X为Cu(NO ) 溶液,Y为铁丝,物质X滴入装有物质Y的试管中现象:铁丝表面有红色
3 2
固体析出,可判断金属活动性:Fe>Cu,正确;
D、X为稀盐酸,Y为Ca(OH) ,两者能发生中和反应,由于Ca(OH) 具有腐蚀性,该反应
2 2
不能用于治疗胃酸过多症,错误。
故选:C。
【16淘宝店铺:向阳百分百】关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
6.(2023•任城区校级二模)某待测液中可能含有大量Mg2+、Cu2+、Fe3+、K+、H+、Cl﹣、SO2−
、
4
OH﹣离子中的一种或几种,现通过以下实验进行检验:
(1)取少量待测液,仔细观察,呈无色;
(2)向上述待测液中滴加NaOH溶液至过量,先无明显现象,后有白色沉淀生成;过滤。
(3)向滤液中滴入BaCl 溶液,无现象;滴加酚酞溶液变红。
2
由上述实验得出的下列判断中,不正确的是( )
A.该待测液呈无色,一定不存在Cu2+、Fe3+
B.该待测液一定存在的离子H+、Mg2+、Cl﹣
C.该待测液可能存在的离子K+、Cl﹣
D.该待测液一定不存在的离子Cu2+、Fe3+、SO2−、OH﹣
4
【解答】解:A、由分析可知,该待测液呈无色,一定不存在Cu2+、Fe3+,故A正确;
B、由该待测液一定存在的离子H+、Mg2+,不含SO2−、OH﹣,一定含Cl﹣,故B正确;
4
C、由分析可知,实验中不含确定溶液中是否含有K+,即该待测液可能存在的离子K+,故C错
误;
D、该待测液一定不存在的离子Cu2+、Fe3+、SO2−、OH﹣,故D正确。
4
故选:C。
7.(2023•陈仓区模拟)将由两种无色气体组成的混合气体,依次通过如图所示的连续装置,各装
置内的现象是:A中液体质量增加,B中红棕色固体变黑,C中液体质量不变,D中出现沉淀。
根据上述现象可以判断该混合气体可能是( )
A.H O、CO B.H 、CO C.CO 、CO D.H O、CO
2 2 2 2 2 2
【解答】解:A、H O、CO 中没有还原性气体,故A错误;
2 2
B、H 、CO 中没有水蒸气,故B错误;
2 2
【17淘宝店铺:向阳百分百】关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C、CO 、CO中没有水蒸气,故C错误;
2
D、H O、CO中存在水蒸气和具有还原性气体CO,故D正确。
2
故选:D。
8.(2023•定远县校级二模)某固体由Ba2+、Cu2+、Na+、Cl﹣、CO 2﹣、SO 2﹣中的几种离子构成,
3 4
取一定质量的该固体样品,进行如下实验:
①将固体溶于水得无色透明溶液,加入足量BaCl 溶液,过滤后得到3克白色沉淀。
2
②在沉淀中加入过量稀硝酸,仍有2克白色沉淀。
③在滤液中滴加AgNO 溶液,产生白色沉淀。
3
则该固体中一定含有( )
A.Ba2+、Cl﹣、SO 2﹣ B.Cu2+、CO 2﹣、SO 2﹣
4 3 4
C.Ba2+、CO 2﹣、Cl﹣ D.Na+、CO 2﹣、SO 2﹣
3 3 4
【解答】解:①将固体溶于水得无色透明溶液,说明溶液中不含Cu2+;加入足量BaCl 溶液,
2
过滤后得到3克白色沉淀;②在沉淀中加入过量稀硝酸,仍有2克白色沉淀,说明沉淀中含有
硫酸钡,同时说明3克白色沉淀中含有能与稀硝酸反应的物质,该物质应是碳酸钡,则说明该固
体中一定含有CO 2﹣、SO 2﹣。
3 4
③在滤液中滴加AgNO 溶液,产生白色沉淀,加入足量BaCl 溶液中含有氯离子,由于氯离子
3 2
能与硝酸银反应生成生成氯化银沉淀,无法证明原固体中是否含有氯离子。
A、Ba2+、SO 2﹣不能共存,故选项错误。
4
B、将固体溶于水得无色透明溶液,溶液中不含Cu2+,故选项错误。
C、Ba2+、CO 2﹣不能共存,故选项错误。
3
D、该固体中一定含有Na+、CO 2﹣、SO 2﹣,故选项正确。
3 4
故选:D。
9.(2023•东莞市校级二模)已知某气体由H 、CO 、CO、CH 中的两种组成。将气体通过澄清的
2 2 4
石灰水,未出现浑浊现象;点燃气体,用蘸有澄清石灰水的烧杯罩住火焰,烧杯壁上有浑浊出
现。该混合气体成分推断合理的是( )
A.一定含有CO B.一定不含氢气
C.一定含有CO和CH D.可能是H 和CH
4 2 4
【解答】解:气体不能使石灰水变浑浊,则说明不含CO ,点燃气体后,澄清石灰水变浑浊,
2
而甲烷和氢气燃烧均生成二氧化碳,则说明混合气体中至少含有一氧化碳和甲烷中的一种,可
能含有氢气,即可能为一氧化碳和氢气,也可能为CH 和氢气,或CO、CH 和H 。
4 4 2
故选:D。
【18淘宝店铺:向阳百分百】关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
10.(2023•隆回县模拟)将含有N 、CO、H 、CO 和少量水蒸气的混合气体,随机依次通过如图
2 2 2
所示四个装置。(每个装置只通过一次,且反应或吸收充分;浓硫酸可吸收水;
高温
2NaOH+CO 2 ═Na 2 CO 3 +H 2 O;C+H 2 O ¯ CO+H 2 )下列说法错误的是( )
❑
A.最终剩余的气体中可能含有五种物质
B.若最终剩余气体中只含有一种物质,则一定是N
2
C.若最终只剩余N 和H O,则连接顺序可能为甲→丙→丁→乙
2 2
D.若连接顺序为甲→乙→丙→丁,则最终剩余气体为N 、CO 、H O
2 2 2
【解答】解:浓硫酸具有吸水性,氢氧化钠会与二氧化碳反应生成碳酸钠和水,碳和二氧化碳
高温生成一氧化碳,碳和水高温会生成一氧化碳和氢气,一氧化碳和氧化铜加热会生成铜和二
氧化碳,氢气和氧化铜加热会生成铜和二氧化碳。
A、将气体依次通过甲、乙、丁、丙,通过甲将水蒸气吸收,通过乙将二氧化碳吸收,通过氧化
铜将氢气转化成水蒸气,将一氧化碳转化成二氧化碳,通过足量的炭粉将水蒸气转化成一氧化
碳、氢气,将二氧化碳转化成一氧化碳,以及没有反应的氮气,所以最终剩余的气体中可能含
有氮气、一氧化碳、氢气三种物质,故A错误;
B、若最终剩余气体中只含有一种物质,将气体依次通过丙、丁、乙、甲,通过丙将水蒸气会转
化成一氧化碳、氢气,通过丁将一氧化碳、氢气转化成水蒸气和二氧化碳,通过乙将二氧化碳
吸收,通过甲将水蒸气吸收,最后剩余的一定是N ,故B正确;
2
C、连接顺序可能为甲→丙→丁→乙,通过甲将水蒸气吸收,通过丙将水蒸气会转化成一氧化碳、
氢气,通过丁将一氧化碳、氢气转化成水蒸气和二氧化碳,通过乙将二氧化碳吸收,最终只剩
余N 和H O,故C正确;
2 2
D、连接顺序为甲→乙→丙→丁,通过甲将水蒸气吸收,通过乙将二氧化碳吸收,通过丙将水蒸
气会转化成一氧化碳、氢气,通过丁将一氧化碳、氢气转化成水蒸气和二氧化碳,所以最终剩
【19淘宝店铺:向阳百分百】关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
余气体为N 、CO 、H O,故D正确。
2 2 2
故选:A。
11.(2023•安庆一模)为证明某气体中是否含有CO 、H 、CO、H O这四种成分,兴趣小组同学
2 2 2
设计了如图装置进行验证(实验开始前先向装置内通一段时间的 N ,)则下列判断有误的是(
2
)
A.只要看到A处澄清石灰水变浑浊就可证明该气体中含有CO
2
B.若C处CuO由黑变红,D处无水硫酸铜变蓝,则证明该气体中含有H
2
C.若C处CuO由黑变红,E处澄清石灰水变浑浊,F处气体被点燃,则证明该气体中含有CO
D.若要证明气体中是否含有H O,则还需在A装置前加一个盛有无水硫酸铜的U型管
2
【解答】解:A、二氧化碳能使澄清石灰水变浑浊,看到A处澄清石灰水变浑浊就可证明该气体
中含有CO ,故正确;
2
B、若C处CuO由黑变红,说明氧化铜被还原,D处无水硫酸铜变蓝,说明氢气还原氧化铜生
成了水,则证明该气体中含有H ,故正确;
2
C、由于气体进入C装置之前没有除去二氧化碳,E处澄清石灰水变浑浊,可能是有原混合气体
中的二氧化碳引起,若C处CuO由黑变红,F处气体被点燃,可能是有氢气引起的,则无法证
明该气体中含有CO,故错误;
D、若要证明气体中是否含有H O,则还需在A装置前加一个盛有无水硫酸铜的U型管,如果
2
硫酸铜变蓝色,说明含有H O,否则没有,故错误。
2
故选:C。
12.(2023•临渭区一模)将由三种无色气体组成的混合气体,依次通过如图所示的连续装置,各
装置内的现象是:A中出现沉淀,D中生成黑色物质,E中白色粉末变蓝,F中出现沉淀。根据
上 述 现 象 可 以 判 断 混 合 气 体 是 ( 无 水 CuSO 遇 水 变 蓝 ) ( )
4
【20淘宝店铺:向阳百分百】关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.CO 、H 、O B.N 、CO、H C.CO 、CO、O D.CO 、H 、CO
2 2 2 2 2 2 2 2 2
【解答】解:A.由CO 、H 、O 三种无色气体组成的混合气体,依次通过如图所示的连续装置,
2 2 2
各装置内的现象是:二氧化碳能够使澄清的石灰水变浑浊,所以A中出现沉淀;通过浓硫酸干
燥后得到的O 、H 的混合气体,进入D装置中,高温下加热,易发生危险,且与氧化铁反应后,
2 2
没有二氧化碳气体生成,不符合题意,故错误;
B.由N 、CO、H 三种无色气体组成的混合气体,依次通过如图所示的连续装置,A中不出现沉
2 2
淀,不符合题意,故错误;
C.由CO 、CO、O 三种无色气体组成的混合气体,依次通过如图所示的连续装置,各装置内的
2 2
现象是:二氧化碳能够使澄清的石灰水变浑浊,所以A中出现沉淀;通过浓硫酸干燥后得到的
O 、CO的混合气体,进入D装置中,高温下加热,易发生危险,且一氧化碳与氧化铁反应不产
2
生水蒸气,所以E中白色粉末不变蓝,不符合题意,故错误;
D.由CO 、H 、CO三种无色气体组成的混合气体,依次通过如图所示的连续装置,各装置内的
2 2
现象是:二氧化碳能够使澄清的石灰水变浑浊,所以A中出现沉淀;多余的二氧化碳可以被氢
氧化钠溶液吸收,通过浓硫酸干燥后得到的H 、CO的混合气体,进入D装置中,由于H 、CO
2 2
具有还原性,高温下能够还原氧化铁,所以D中生成黑色物质,E中白色粉末变蓝,有水蒸气
产生,说明气体中有氢气,F中出现沉淀,说明有二氧化碳气体产生,存在一氧化碳气体,符合
题意,故正确;
故选:D。
13.(2023•岱岳区二模)某无色溶液中可能含有以下离子中的一种或几种:Na+、NH+ 、Cl﹣、
4
Mg2+、Ba2+、SO2−、CO2−,现取少量溶液两份,进行如下实验:下列有关说法不正确的是(
4 3
)
【21淘宝店铺:向阳百分百】关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.原溶液中一定存在NH+ 、Cl﹣、SO2− 、CO2− ,一定不存在 Na+、Mg2+、Ba2+
4 4 3
B.原溶液中一定存在NH+ 、SO2−,一定不存在 Mg2+、Ba2+、CO2−
4 4 3
C.①中的反应实质为NH+ 和OH﹣结合生成NH 和H O
4 3 2
D.将②中氯化钡溶液换成硝酸钡溶液,则可确定原溶液中含有 Cl﹣
【解答】解:①第一份加足量NaOH溶液,加热,只产生有刺激性气味的气体,则是氢氧化钠
与铵根离子反应产生的氨气,故原溶液中一定含有铵根离子,没有镁离子;
②第二份加足量BaCl 溶液后,产生白色沉淀,向沉淀中加入稀硝酸,沉淀完全不溶解,故沉
2
淀为硫酸钡,原溶液中一定含有硫酸根离子,没有钡离子;钡离子能与碳酸根离子结合产生碳
酸钡沉淀,碳酸钡会溶于硝酸,故原溶液一定不含有碳酸根离子;由于加足量BaCl 溶液时引入
2
了氯离子,之后加硝酸银溶液有白色沉淀,不能证明原溶液中是否含有氯离子。
A、由分析可知,原溶液中一定存在NH+ 、SO2−,一定不存在 Mg2+、Ba2+、CO2−,故错误;
4 4 3
B、由分析可知,原溶液中一定存在NH+ 、SO2−,一定不存在 Mg2+、Ba2+、CO2−,故正确;
4 4 3
C、由分析可知,①中的反应实质为NH+ 和OH﹣结合生成NH 和H O,故正确;
4 3 2
D、将②中氯化钡溶液换成硝酸钡溶液,避免了引入Cl﹣,则可确定原溶液中含有 Cl﹣,故正确
故选:A。
14.(2023•邹城市二模)某待测液中可能含有大量Mg2+、Cu2+、Fe3+、K+、H+、NO−、SO2−、
3 4
OH﹣离子中的两种或两种以上,现通过以下实验进行检验:
①取少量待测液,仔细观察,呈无色;
②向上述待测液中滴加NaOH溶液,先无明显现象,后有白色沉淀生成;
③向上述待测液中加入BaCl 溶液,无现象。
2
【22淘宝店铺:向阳百分百】关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
由上述实验得出的下列判断中,正确的是( )
A.该待测液不能确定是否存在的离子是K+、OH﹣
B.该待测液中一定不存在的离子只有Cu2+、Fe3+、SO2−
4
C.该待测液中一定大量存在的离子是H+、Mg2+、NO−
3
D.该待测液呈无色,Mg2+、Cu2+、Fe3+的溶液都有颜色,一定都不能大量存在
【解答】解:①取少量待测液,仔细观察,呈无色,说明不含Cu2+、Fe3+;②向上述待测液中
滴加NaOH溶液,先无明显现象,后有白色沉淀生成,说明溶液存在氢离子,氢离子先与氢氧
根离子结合生成水分子,氢离子反应完,氢氧根离子再与Mg2+结合生成氢氧化镁白色沉淀;则
溶液中一定不含氢氧根离子,因为氢离子和氢氧根离子不能共存;③向上述溶液中加入BaCl
2
溶液,无现象,说明溶液中不含硫酸根离子,否则会产生硫酸钡白色沉淀,则溶液中的阴离子
一定是硝酸根离子。
A、该待测液不能确定是否存在的离子是K+,一定不含OH﹣,故选项说法错误。
B、该待测液中一定不存在的离子只有Cu2+、Fe3+、SO2−、OH﹣,故选项说法错误。
4
C、该待测液中一定大量存在的离子是H+、Mg2+、NO−,故选项说法正确。
3
D、该待测液呈无色,Cu2+、Fe3+的溶液都有颜色,一定都不能大量存在,Mg2+的溶液没有颜色,
由分析可知,该待测液一定含有镁离子,故选项说法错误。
故选:C。
15.(2023•龙凤区一模)某水溶液中可能含有以下离子中的一种或者几种:Na+、Cl﹣、Ca2+、
Ba2+、SO 2﹣、CO 2﹣,现取两份等质量的溶液进行如下实验:(1)第一份加入AgNO 溶液产
4 3 3
生白色沉淀;(2)第二份加入足量的Ba(NO ) 溶液产生白色沉淀,继续加入过量的稀硝酸,
3 2
沉淀部分溶解。根据上述实验现象,下列推测合理的是( )
A.一定存在Na+ B.可能存在Ba2+
C.一定存在Cl﹣ D.可能存在Ca2+
【解答】解:(1)向第一份中加入AgNO 溶液有沉淀产生,氯离子、硫酸根离子、碳酸根离子
3
能与银离子反应生成白色沉淀,说明某溶液中可能含有氯离子、硫酸根离子、碳酸根离子。
(2)向第二份中加入足量的Ba(NO ) 溶液,有白色沉淀产生,再向其中加入过量的稀硝酸,
3 2
沉淀部分溶解,说明沉淀中含有不溶于酸的硫酸钡,还含有能与酸反应的物质,则某溶液中一
定含有硫酸根离子,一定含有碳酸根离子。
【23淘宝店铺:向阳百分百】关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A、因为溶液中含有硫酸根离子与碳酸根离子,则溶液中不可能存在钡离子与钙离子,只有钠离
子是阳离子,溶液中一定含有钠离子,故选项说法正确。
B、某溶液中一定含有硫酸根离子,硫酸根离子和钡离子不能,则不可能存在Ba2+,故选项说法
错误。
C、向第一份中加入AgNO 溶液有沉淀产生,氯离子、硫酸根离子、碳酸根离子能与银离子反
3
应生成白色沉淀,无法确定溶液中是否存在氯离子,故选项说法错误。
D、某溶液一定含有碳酸根离子,碳酸根离子和钙离子不能共存,则一定不存在 Ca2+,故选项说
法错误。
故选:A。
16.(2023•官渡区一模)某工业尾气中含有H 、CO和CO 中的一种或几种,用如图装置检验其
2 2
成分(夹持装置已略去,无水硫酸铜遇水变蓝)。下列有关该实验说法错误的是( )
A.甲处应进行尾气处理
B.若将装置C和装置D调换,会影响实验结果
C.装置B的作用是除去气体样品中可能含有的CO
2
D.若装置E中黑色粉末变红,可证明气体样品中含有CO
【解答】解:A、该尾气中可能含有一氧化碳,未反应的一氧化碳散逸到空气中,会污染空气,
故甲处应进行尾气处理,故说法正确;
B、若将装置C和装置D调换,气体会从C装置中携带出水蒸气,会对氢气的检验产生干扰,
故说法正确;
C、二氧化碳能使澄清石灰水变浑浊,故装置A的作用是检验二氧化碳,二氧化碳能与氢氧化钠
反应生成碳酸钠和水,装置B的作用是除去气体中可能含有的二氧化碳,故说法正确;
D、一氧化碳和氧化铜在加热的条件下反应生成铜和二氧化碳,氢气和氧化铜在加热的条件下反
应生成铜和水,故装置E中黑色粉末变红,G中氢氧化钙溶液变浑浊,才能说明气体样品中含
有CO,因为氢气存在时,装置E中黑色粉末也能变红,故说法错误。
故选:D。
二.填空题(共3小题)
17.(2023•邹城市三模)某无色透明溶液中可能含有K+、H+、Ba2+、Cu2+、Cl﹣、CO2− 、SO2−
3 4
、NO−
中的几种,对其进行如下实验操作:
3
①取少量溶液,加入过量BaCl 溶液,有白色沉淀产生,过滤。
2
【24淘宝店铺:向阳百分百】关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
②向①过滤后的滤液中加入AgNO 溶液,有白色沉淀产生。
3
③向①过滤后的沉淀中加入过量稀盐酸,沉淀部分溶解,并有气体产生。
由以上实验事实推断,原溶液中一定含有的离子是 K + 、 CO2−、SO2− ,可能含有的离子是
3 4
Cl ﹣ 、 NO− 。
3
【解答】解:取少量溶液,加入过量BaCl 溶液,有白色沉淀产生,且向沉淀中加入过量稀盐酸,
2
沉淀部分溶解,并有气体产生。说明原溶液中必有CO2− 、SO2−
,加入的钡离子和碳酸根结合
3 4
成可以和盐酸反应生成二氧化碳的碳酸钡,和硫酸根结合成不和盐酸反应的硫酸钡,必不含
Ba2+、H+,因为不能和碳酸根离子、硫酸根离子共存。溶液无色透明,必不含Cu2+;所以阳离
子必有K+;由于②向①过滤后的滤液中加入AgNO 溶液,有白色沉淀产生,该沉淀是AgCl,
3
但Cl﹣的来源无法确定,因为前面添加了过量的BaCl 溶液,引入了Cl﹣,所以可能含有Cl﹣、
2
NO−;综上,原溶液中一定含有的离子是:K+、CO2−、SO2−;可能含有的离子是:Cl﹣、
3 3 4
NO−;故答案为:K+、CO2−、SO2−;Cl﹣、NO−。
3 3 4 3
18.(2023•任城区二模)某溶液中可能含有以下几种离子Na+、Ca2+、Ba2+、Cl﹣、SO2− 、CO2−
4 3
中的几种,为确定溶液中含有的离子,进行以下实验探究:
①取少量未知溶液,滴加AgNO 溶液产生白色沉淀;
3
②另取少量未知溶液,加入足量的Ba(NO ) 溶液,产生白色沉淀,静置过滤,向沉淀中加入
3 2
过量的稀硝酸,沉淀部分溶解。
请你根据实验现象,推测:
(1)原溶液中一定含有的离子为 N a + 、 SO2−、CO2− (填符号,下同),一定不存在的离
4 3
子为 C a 2 + 、 B a 2 + 。
(2)为验证可能存在的离子,你设计的实验方案为 取 ② 中的少量滤液,滴加硝酸银溶液,
若产生白色沉淀,说明存在氯离子 。
【解答】解:(1)第一份加入AgNO 溶液有沉淀产生,由于银离子能与氯离子、硫酸根离子、
3
碳酸根离子产生沉淀,说明溶液中含有Cl﹣或是碳酸根离子或者硫酸根离子;取样加入足量硝酸
【25淘宝店铺:向阳百分百】关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
钡溶液后产生白色沉淀,白色沉淀为碳酸钡或硫酸钡,其中碳酸钡溶于稀硝酸,硫酸钡不溶于
稀硝酸,加入过量稀硝酸后,沉淀部分溶解,说明白色沉淀使碳酸钡和硫酸钡的混合物,说明
原溶液中一定含有SO2− 、CO2− ;一定不含Ca2+、Ba2+,根据溶液不显电性溶液中肯定含有钠离
4 3
子。根据上述实验,溶液中一定没有Ca2+、Ba2+,溶液中一定含有的是Na+、SO2−、CO2−;可
4 3
能含有的是Cl﹣;
(2)为了验证可能存在的氯离子,可以取②中的少量滤液,滴加硝酸银溶液,若产生白色沉淀,
说明存在氯离子。
故答案为:(1)Na+、SO2−、CO2−;Ca2+、Ba2+;
4 3
(2)取②中的少量滤液,滴加硝酸银溶液,若产生白色沉淀,说明存在氯离子。
19.(2023•曲阜市一模)某溶液由Mg2+、Ba2+、Cu2+、Na+、Cl﹣、CO2− 、SO2− 、OH﹣中的几种
3 4
离子构成,为判定溶液中离子,进行如下实验:
(1)取一份溶液样品,加入足量NaOH溶液得到蓝白色沉淀;
(2)另取一份溶液样品,加入BaCl 溶液,无明显现象,继续滴加AgNO 溶液,产生白色沉淀。
2 3
请分析实验过程,推断:
溶液中一定存在的离子有 C l ﹣ 、 C u 2 + 、 M g 2 + (填符号,下同),可能存在的离子有
Na + 、 Ba 2+ ,一定不存在的离子是 CO2−、SO2− 、 OH ﹣ 。
3 4
【解答】解:加入足量NaOH溶液得到蓝白色沉淀,说明溶液中含有铜离子和镁离子,镁离子、
铜离子不能与氢氧根离子、碳酸根离子共存,因此一定没有氢氧根离子、碳酸根离子;另取一
份溶液样品,加入BaCl 溶液,无明显现象,说明溶液中不含有硫酸根离子;继续滴加 AgNO
2 3
溶液,产生白色沉淀,由于溶液中加入了氯化钡,因此不能确定溶液中是否含有氯离子;已经
确定一定有铜离子和镁离子,一定没有氢氧根离子、硫酸根离子和碳酸根离子,由于溶液有阳
离子必然有阴离子,所以一定有的阴离子是氯离子,可能含有钠离子、钡离子;由分析可知,
溶液中一定存在的离子有Cl﹣、Cu2+、Mg2+,可能存在的离子有Na+、Ba2+,一定不存在的离子
是CO2− 、SO2− 、OH﹣。
3 4
【26淘宝店铺:向阳百分百】关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
故答案为:Cl﹣、Cu2+、Mg2+;Na+、Ba2+;CO2− 、SO2− 、OH﹣。
3 4
三.解答题(共1小题)
20.(2023•曲阜市二模)某无色透明溶液中可能含有K+、H+、Ba2+、Cu2+、C1﹣、CO 2﹣、SO 2
3 4
﹣、NO ﹣中的几种,对其进行如下实验操作:
3
①取少量溶液,加入过量BaCl 溶液,有白色沉淀产生,过滤;
2
②向①过滤后的滤液中加入AgNO 溶液,有白色沉淀产生;
3
③向①过滤后的沉淀中加入过量稀盐酸,沉淀部分溶解,并有气体产生。
(1)由以上实验事实推断,原溶液中一定含有的离子是 K + 、 CO 2 ﹣ 、 SO 2 ﹣ ;可能含有的
3 4
离子是 C l ﹣ 、 NO ﹣ ;
3
(2)请写出③中发生反应的化学方程式 BaCO +2HCl = BaCl +H O+CO ↑ 。
3 2 2 2
【解答】解:(1)由分析可知,故原溶液中一定含有的离子是:K+、CO 2﹣、SO 2﹣;可能含有
3 4
的离子是:Cl﹣、NO ﹣;
3
(2)③中发生反应为碳酸钡和稀盐酸反应生成氯化钡、二氧化碳和水,该反应的化学方程式为:
BaCO +2HCl=BaCl +H O+CO ↑。
3 2 2 2
【27淘宝店铺:向阳百分百】