文档内容
绝密★启用前
大联考
2024——2025 学年高中毕业班阶段性测试(二)
化学
考生注意:
1.答题前,考生务必将自己的姓名、考生号填写在试卷和答题卡上,并将考生号条形码粘贴
在答题卡上的指定位置。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试
卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 O-16 Al-27 S-32 Cl-35.5 Cu-64 I-127
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1.下列乐器、头饰所指部件的主要成分与其他三项不能归为一类的是
A.三弦乐器中的钢丝琴弦 B.铜质大锣
C.头饰中的金簪 D.头饰上镶嵌的珍珠
2.我国科研人员在嫦娥五号带回的月球样本中,发现了富含水分子、铵和氯的未知矿物晶体,且该矿物中
氯的同位素组成和地球矿物显著不同。下列说法正确的是
A. 和 互为同素异形体
B.NH Cl的电子式为
4
C.该未知晶体中一定含极性键、非极性键和离子键
D.HO的形成过程可表示为
2
3.化学品在人们的生活中应用广泛。下列说法错误的是A.小苏打可用作面食膨松剂
B.纯碱可用作医用抗酸剂
C.二氧化硫可用作葡萄酒的添加剂
D.葡萄糖可用于急性低血糖的血糖回升
4.下列实验操作正确的是
A.用乙醇从碘水中萃取,分液获取乙醇的碘溶液
B.不小心将碱液滴在皮肤上,先用大量水冲洗,再涂抹NaHCO 溶液
3
C.将混有HCl的SO 依次通过饱和NaHSO 溶液、浓硫酸,可得纯净的SO
2 3 2
D.实验室中Li、Na、K等碱金属单质密封保存在煤油中
5.下列各组有机物的鉴别方法或试剂错误的是
A.锦纶和羊毛——灼烧法
B.苯和CCl ——水
4
C.葡萄糖和蔗糖——新制的氢氧化铜、加热
D.植物油和裂化汽油——酸性高锰酸钾溶液
6.若N 表示阿伏加德罗常数的值。下列说法正确的是
A
A.7.1gCl 完全溶解于水,转移电子数为0.1N
2 A
B.1L0.1mol/LNaClO溶液中,含氧原子数为0.1N
A
C.8.8g乙酸乙酯中含有的官能团数目为0.1N
A
D.标准状况下,224mL乙烯气体中成键电子数为0.1N
A
7.辛夷是《神农本草经·上品·木部》中的一味中草药,其提取物之一乙酸龙脑酯的结构简式如图所示。下列
有关乙酸龙脑酯的说法错误的是
A.分子式为C H O
12 20 2
B.其同分异构体中可能存在芳香族化合物
C.只含一种官能团
D.在酸性和碱性条件下均能发生取代反应
8.短周期主族元素W、X、Y、Z的原子序数依次递增,W是形成化合物种类最多的一种元素,X的单质是
空气中含量最多的物质,W、Z可形成结构为Z=W=Z的直线形分子,Y与Z同周期,且Y为该周期中原
子半径最大的元素。下列说法正确的是
A.W的氢化物一定为正四面体形分子
B.W、X,Z三种元素的最高价氧化物对应的水化物均为强酸
C.四种元素形成的简单氢化物中,Z的熔点最高
D.四种元素形成的某种化合物可用于Fe3+的检验
9.利用下列装置可进行气体的喷泉实验,下列组合不能实现喷泉实验的是选 A B C D
项
甲 NH 乙烯 NO SO
3 2 2
乙 HO 酸性KMnO 溶液 NaOH溶液 NaOH溶液
2 4
丙 HO 酸性KMnO 溶液 NaOH溶液 HO
2 4 2
10.下列指定反应的离子方程式书写正确的是
A.向Na2S2O3溶液中加入过量稀硫酸: +2H+=S↓+H O+SO ↑
2 2
B.向澄清石灰水中通入少量Cl:Ca(OH) +Cl=Ca2++Cl-+ClO-+H O
2 2 2 2
C.向Al (SO ) 溶液中通入过量NH :Al3++4NH+4H O=[Al(OH) ]-+4
2 4 3 3 3 2 4
D.用食醋和淀粉–KI溶液检验食盐中的KIO : +5I-+6H+=3I +3H O
3 2 2
11.下列陈述Ⅰ和陈述Ⅱ均正确且具有因果关系的是
选 陈述Ⅰ 陈述Ⅱ
项
A 搅拌烧杯中的Ba(OH) ·8H O和NH Cl晶体混合物,烧杯外壁发凉 碱与铵盐发生复分
2 2 4
解反应
B 用导线将插在苹果上的铁片、铜片与电流表连接,电流表指针偏转 铁的活泼性比铜强
C 将两支分别盛有HO 溶液(滴有几滴FeCl 溶液)的试管分别放入冷水和热水 FeCl 是HO 分解
2 2 3 3 2 2
中,热水中的试管产生气泡速率快 的催化剂
D 将吸有稀NaOH溶液的胶头滴管插入FeSO 溶液中,挤出胶头滴管中的溶 Fe(OH) ,Fe(OH)
4 2 3
液,先生成白色沉淀,然后变为灰绿色,最后变为红褐色沉淀 均为弱碱
A.A B.B C.C D.D
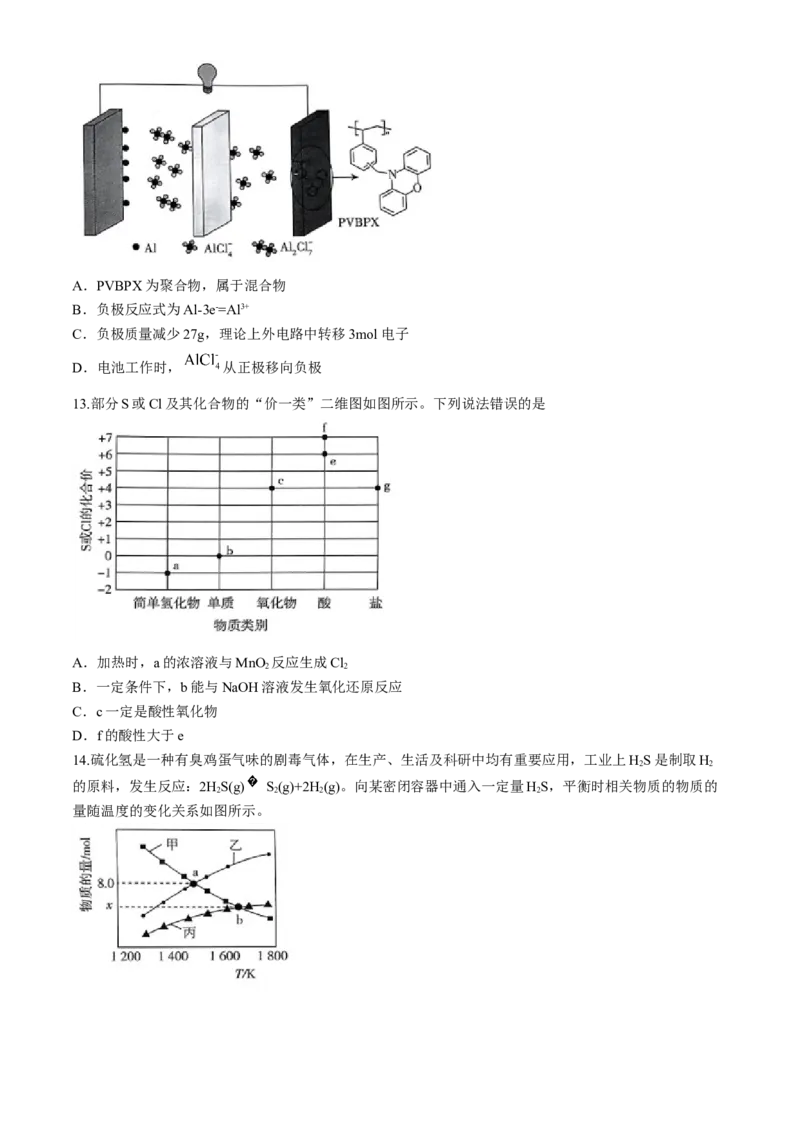
12.我国科技工作者研制出一种以PVBPX为正极材料的铝离子电池,工作原理如图所示,放电时电池总反
应为3PVBPX(AlCl )+2Al+6Cl-=3PVBPX+4 +2 ,正极反应式为PVBPX(AlCl )+2e-=PVBPX+2
4 2 4 2
。下列说法错误的是A.PVBPX为聚合物,属于混合物
B.负极反应式为Al-3e-=Al3+
C.负极质量减少27g,理论上外电路中转移3mol电子
D.电池工作时, 从正极移向负极
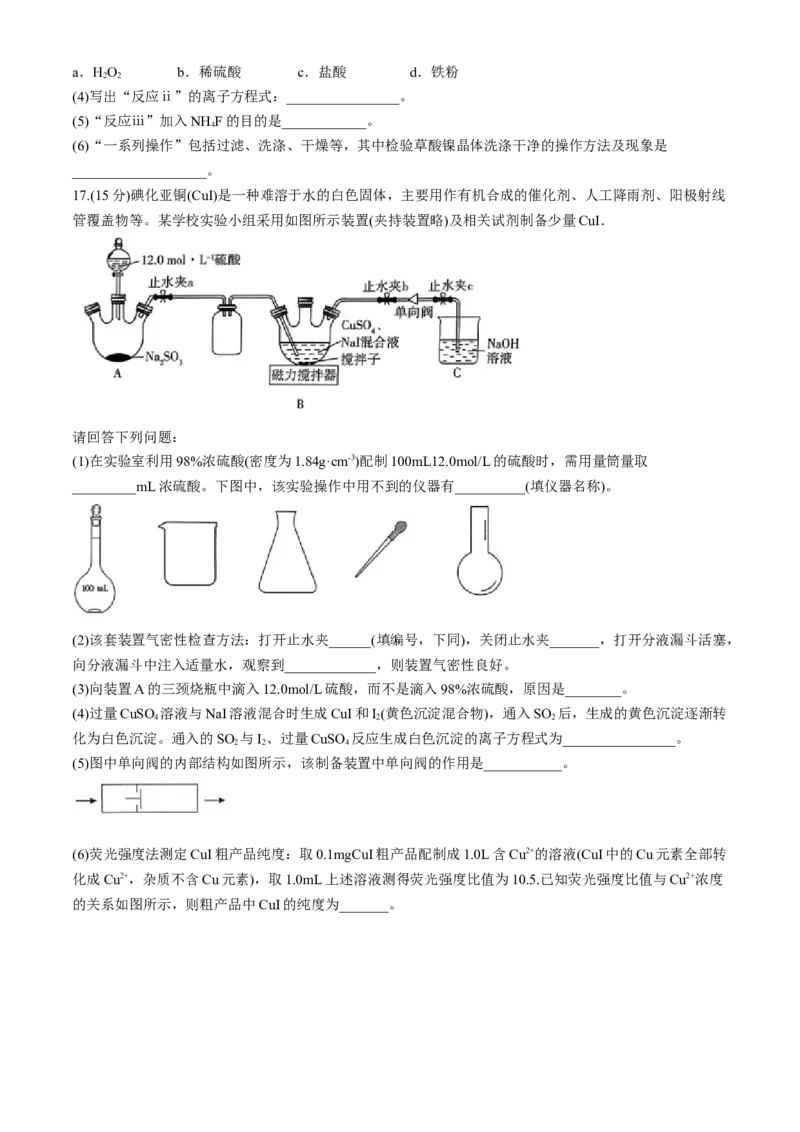
13.部分S或Cl及其化合物的“价一类”二维图如图所示。下列说法错误的是
A.加热时,a的浓溶液与MnO 反应生成Cl
2 2
B.一定条件下,b能与NaOH溶液发生氧化还原反应
C.c一定是酸性氧化物
D.f的酸性大于e
14.硫化氢是一种有臭鸡蛋气味的剧毒气体,在生产、生活及科研中均有重要应用,工业上HS是制取H
2 2
的原料,发生反应:2HS(g) S(g)+2H(g)。向某密闭容器中通入一定量HS,平衡时相关物质的物质的
2 2 2 2
量随温度的变化关系如图所示。下列说法正确的是
A.曲线甲、乙,丙分别代表HS、S、H
2 2 2
B.温度越高,HS分解速率越慢
2
C.a点HS的转化率为20%
2
D.图中b点的纵坐标x=
二、非选择题:本题共4小题,共58分。
15.(14分)海水是取之不尽、用之不竭的资源。以海水为资源可提取、合成各种各样的生活用品及化工产品,
海水与部分物质的转化关系如图所示:
请回答下列问题:
(1)由海水制备淡水的方法有_______(填一种)。
(2)转化②若在实验室完成,由“浓缩海水”制备“粗盐”的操作是_________。
(3)写出下列转化过程加入的试剂:③________(填化学式,下同)溶液﹑④_______溶液、⑤_______溶液。
(4)溶液丙中加入试剂X的作用是_______________。
(5)转化⑥和转化⑧的离子反应相同,该反应说明非金属性:Cl______Br(填“>”或“<”);转化⑥生成的
Br 用SO 水溶液吸收的离子方程式为_____________。
2 2
16.(15分)草酸镍晶体(NiC O·2H O)可用于制镍粉、Ni O 及含镍催化剂等。一种以含镍废渣(主要成分为
2 4 2 2 3
Ni,含CaO、FeO、SiO 等杂质)为原料制备草酸镍晶体的工艺流程如图所示。
2
请回答下列问题:
(1)NiC O 是一种草酸盐,草酸的结构简式是HOOCCOOH,草酸含有的官能团名称是______。
2 4
(2)写出“酸浸”时提高浸取速率的措施:__________________(填两条);利用滤渣a中的主要成分可制备
粗硅,工业上在1800~2000℃下制备粗硅的化学方程式是_____________。
(3)过一硫酸的结构式是 ,其在“反应ⅰ”中的作用是______________;下列试剂能代
替过一硫酸的是______(填标号)。a.HO b.稀硫酸 c.盐酸 d.铁粉
2 2
(4)写出“反应ⅱ”的离子方程式:________________。
(5)“反应ⅲ”加入NH F的目的是____________。
4
(6)“一系列操作”包括过滤、洗涤、干燥等,其中检验草酸镍晶体洗涤干净的操作方法及现象是
___________________。
17.(15分)碘化亚铜(CuI)是一种难溶于水的白色固体,主要用作有机合成的催化剂、人工降雨剂、阳极射线
管覆盖物等。某学校实验小组采用如图所示装置(夹持装置略)及相关试剂制备少量CuI.
请回答下列问题:
(1)在实验室利用98%浓硫酸(密度为1.84g·cm-3)配制100mL12.0mol/L的硫酸时,需用量筒量取
_________mL浓硫酸。下图中,该实验操作中用不到的仪器有__________(填仪器名称)。
(2)该套装置气密性检查方法:打开止水夹______(填编号,下同),关闭止水夹_______,打开分液漏斗活塞,
向分液漏斗中注入适量水,观察到_____________,则装置气密性良好。
(3)向装置A的三颈烧瓶中滴入12.0mol/L硫酸,而不是滴入98%浓硫酸,原因是________。
(4)过量CuSO 溶液与NaI溶液混合时生成CuI和I(黄色沉淀混合物),通入SO 后,生成的黄色沉淀逐渐转
4 2 2
化为白色沉淀。通入的SO 与I、过量CuSO 反应生成白色沉淀的离子方程式为________________。
2 2 4
(5)图中单向阀的内部结构如图所示,该制备装置中单向阀的作用是___________。
(6)荧光强度法测定CuI粗产品纯度:取0.1mgCuI粗产品配制成1.0L含Cu2+的溶液(CuI中的Cu元素全部转
化成Cu2+,杂质不含Cu元素),取1.0mL上述溶液测得荧光强度比值为10.5.已知荧光强度比值与Cu2+浓度
的关系如图所示,则粗产品中CuI的纯度为_______。(7)CuI能催化下列反应,下列说法正确的是______(填标号)。
(Ⅰ)+ ( Ⅱ) ( Ⅲ)+HBr
a.CuI能提高该转化过程的反应速率
b.化合物Ⅰ、Ⅱ、Ⅲ均为芳香经
c.化合物Ⅰ、Ⅱ、Ⅲ均为烃的衍生物
18.(14分)尿素是一种应用广泛的化工产品,广泛应用于农业、医学、工业等行业。
请回答下列问题:
(1)1828年,维勒《论尿素的人工合成》介绍了无机物合成尿素的方法,维勒合成尿素的方法是AgCNO(微
溶)+NHCl(aq)→NHCNO(氰酸铵)→CO(NH) 写出第一步生成氰酸铵的化学方程式:_________________;
4 4 2 2.
该反应中涉及的元素Ag与Cu同族,且比Cu多一个周期,则Ag在元素周期表中的位置为________;该反
应所涉及的非金属元素(H除外)中,简单氢化物最稳定的是________(填化学式)。
(2)在一定条件下,以CO 和NH 为原料合成尿素,该制备原理分两步完成,反应过程中的能量变化如图所
2 3
示。
①第二步反应NH COONH(s)=CO(NH )(s)+HO(g)为_______(填“放热”或“吸热”)反应。
2 4 2 2 2
②若2NH (g)+CO (g) CO(NH)(s)+HO(g)在恒温恒容密闭容器中进行,下列叙述能证明该反应达到平衡
3 2 2 2 2
状态的是______(填标号)。
A.容器内混合气体的压强不再发生变化
B.断裂6molN─H键的同时形成2molH-О键
C.容器内混合气体的密度不再发生变化
(3)清华大学化学工程系研究团队在电催化合成尿素领域取得进展,实现了常温常压下CO、NH 在铂碳催
3化剂上偶联的新方法,反应路径如图所示。
①步骤Ⅰ的产物异氰酸根离子(OCN-)中O为-2价,N为-3价,则步骤Ⅰ:CO+NH →OCN-为_______(填
3
“氧化”或“还原”)反应。
②OCNH的结构式为О=C=N-H,则步骤Ⅰ反应中断裂的化学键有______(填标号)。
a.C≡О键 b.C=N键 c.N-H键 d.C=О键
③步骤Ⅱ的离子方程式为_______________。
2024—2025 学年高中毕业班阶段性测试(二)
化学·答案
1 ~14小题,每小题3分,共42分。
1.D 2.D 3.B 4.C 5.D 6.C 7.B 8.D 9.B 10.A 11.B 12.B 13.C 14.D
15.(1)蒸馏法、电渗析法、离子交换法等(2分,任填一种)
(2)蒸发、冷却、过滤(合理即可,2分,没有“冷却”不扣分)
(3) BaCl ( 1分);Ca(OH) (2分);NaCO( 1分)
2 2 2 3
(4)除去溶液中过量的OH-, (合理即可,2分)
(5)>(2分);SO + Br+2H O= +2Br-+4H+(2分)
2 2 2
16.(1)羧基(1分)
(2)适当增大酸浸时硫酸的浓度、适当提高酸浸液的温度、将含镍废渣粉碎,搅拌等(合理即可,2分,任填
两条);SiO2+2C Si+2CO↑(2分)
(3)将Fe2+氧化为Fe3+(合理即可,2分);a(2分)
(4)3Ni(OH) +2Fe3+=3Ni2++2Fe(OH) (2分)
2 3
(5)除去溶液中的Ca2+(合理即可,2分)
(6)取最后一次洗涤液少许于试管中,先滴加盐酸,再滴加BaCl 溶液,溶液中不出现白色沉淀(合理即可,
2
2分)
17.(1)65.2(2分);锥形瓶、圆底烧瓶(2分)( 2)a、b(1分,少1个不得分);c(1分);分液漏斗中水很快停止流下(合理即可,1分)
(3)98%浓硫酸中H+浓度较小,制备SO 的离子反应几乎不能进行(合理即可,1分)
2
(4)2SO +I +2Cu2+ +4H O=2CuI+2 +8H+(2分)
2 2 2
(5)防止倒吸(1分)
(6)87.86% (2分)
(7) ac(2分)
18.(1)AgCNO+ NH Cl=AgCl+NH CNO(2分);第五周期IB族(2分);HO(2分)
4 4 2
(2)①吸热(1分)
②AC(2分)
(3)①氧化(1分);
②ac(2分)
③ +OCN-=CO(NH )(2分)
2 2