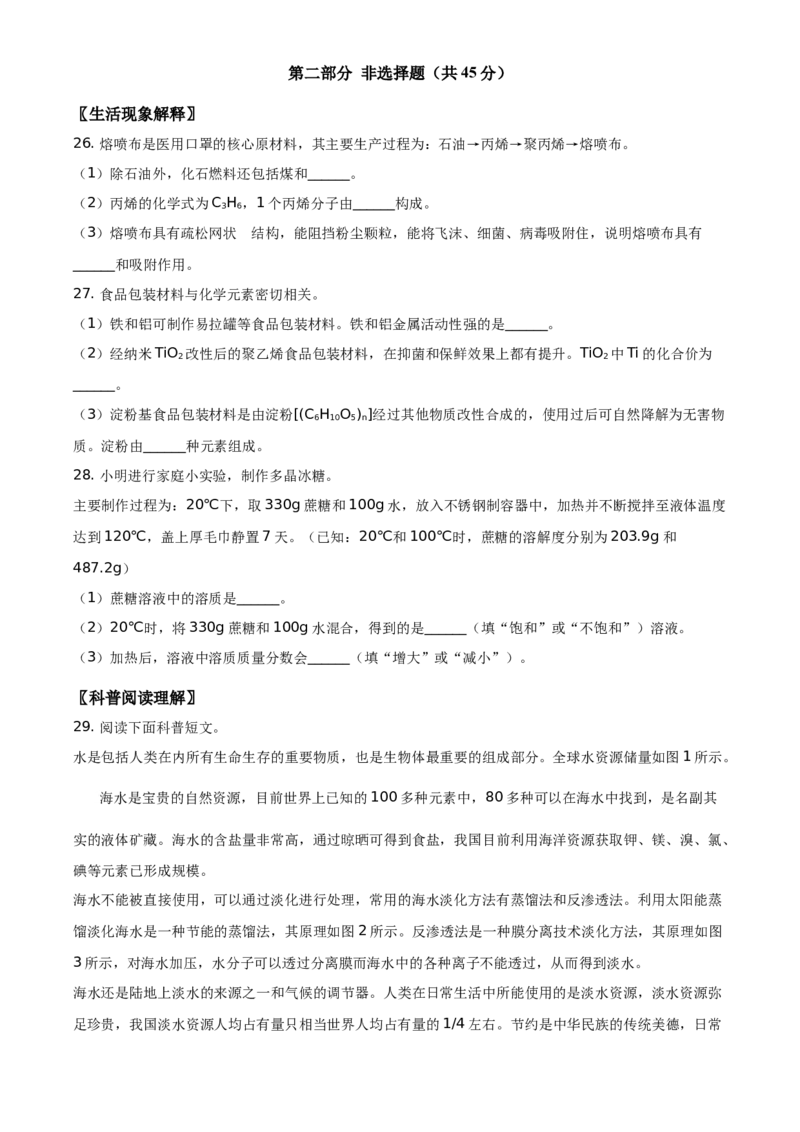文档内容
石景山区 2020-2021 学年第一学期初三期末试卷
化学
可能用到的相对原子质量:H 1 C 12 O 16
第一部分 选择题(共25分)
一、选择题(每小题只有一个选项符合题意。每小题1分。)
1. 空气成分中,体积分数最大的是( )
A. 氮气 B. 二氧化碳 C. 氧气 D. 稀有气体
2. 下列过程发生化学变化的是
A. 水蒸发 B. 矿石粉碎 C. 干冰升华 D. 蜡烛燃烧
3. 下列物质在氧气中燃烧,火星四射,生成黑色固体的是
A. 红磷 B. 木炭 C. 铁丝 D. 硫
4. 下列属于可回收垃圾的是
A. 铝制易拉罐 B. 一次性餐具 C. 菜叶 D. 鱼刺
5. 羟基磷酸钙[Ca (PO ) (OH) ]是构成人体骨骼的重要物质,其中属于金属元素的是
10 4 6 2
A. Ca B. O C. H D. P
6. 下列物质中,属于单质 的是
A. CO B. H SO C. N D. KCl
2 2 4 2
7. 下列气体能供给动植物呼吸的是
A. CO B. H C. O D. N
2 2 2 2
8. 王安石曾写下“遥知不是雪,为有暗香来”的诗句。能闻到梅花香气的原因是
A. 分子在不断运动 B. 分子质量小
C. 分子间有间隔 D. 分子由原子构成
9. 豆类、动物肝脏中含有丰富的铁和锌,这里的“铁”、“锌”是指( )
A. 原子 B. 分子 C. 元素 D. 单质
10. 下列物质中,属于溶液的是
A. 牛奶 B. 豆浆 C. 冰水 D. 食盐水
11. 下列实验操作中,不正确的是
A. 检查气密性 B. 取用固体C. 倾倒液体 D. 加热液体
12. 氧气可以用排水法进行收集 的原因是
A. 不易溶于水 B. 易溶于水 C. 密度比空气大 D. 密度比空气小
13. 一种铁原子的原子核内有 26 个质子和 30 个中子,该原子的核外电子数为
A. 4 B. 26 C. 30 D. 56
14. 下列物质属于纯净物的是
A. 空气 B. 二氧化锰 C. 自来水 D. 石灰石
15. 氢元素与氧元素的本质区别是
A. 质子数不同 B. 电子数不同 C. 中子数不同 D. 电子层数不同
16. 下列符号中,表示2个氯原子的是
A. Cl B. 2Cl C. 2Cl D. 2Cl-
2 2
17. 下列化学方程式书写正确的是
A. Fe+CuSO =FeSO +Cu B. Mg+H SO =MgSO +H O
4 4 2 4 4 2
C. Fe+O Fe O D. 3CO+Fe O =2Fe+3CO
2 3 4 2 3 2
18. 下列物质的名称与化学式不对应的是
A. 氯化铁 FeCl B. 碳酸 H CO C. 氯化钠 NaCl D. 氧化铝 Al O
2 2 3 2 3
19. 下列方法能鉴别空气、氧气和二氧化碳 3 瓶气体的是( )
A. 闻气味 B. 将集气瓶倒扣在水中
C. 观察颜色 D. 将燃着的木条伸入集气瓶中
20. 下列金属中,与稀硫酸反应后所得溶液颜色为浅绿色的是
A. 镁 B. 铝 C. 锌 D. 铁
21. 下列物质的用途中,利用其物理性质的是
A. CO 用于碳酸饮料 B. 干冰用作制冷剂
2
C. CH 用作燃料 D. O 用于炼钢
4 2
22. 向放有铁丝和铜丝的两支试管中加入溶液,不能证明铁和铜金属活动性强弱的是
A. 稀硫酸 B. AgNO 溶液 C. CuSO 溶液 D. 稀盐酸
3 423. 甲、乙的溶解度曲线如图所示。下列说法不正确的是
A. t ℃时,甲、乙两种物质溶解度相等
1
B. t ℃时,甲的溶解度大于乙的溶解度
2
C. t ℃时,甲的饱和溶液中溶质质量分数为40%
2
D. 甲和乙的溶解度都随温度升高而增大
24. 甲酸(HCOOH)具有清洁制氢的巨大潜力,其反应前后分子种类变化的微观示意图如下:
下列说法正确的是
A. 1个甲酸分子中含有3个原子 B. 该反应属于化合反应
C. 生成甲与乙的分子个数比为1:1 D. 乙中碳、氧元素质量比为3:4
25. 实验小组在密闭容器中用CO 和湿度两种传感器探究乙醇燃烧的产物。测定结果如下图所示。下列说
2
法不正确的是
A. 图1曲线说明乙醇燃烧有水产生
B. 根据图1,可推理得出乙醇中含有氢元素
C. 图2曲线说明乙醇燃烧有CO 产生
2
D. 根据图2,可推理得出乙醇中含有碳和氧元素第二部分 非选择题(共45分)
〖生活现象解释〗
26. 熔喷布是医用口罩的核心原材料,其主要生产过程为:石油→丙烯→聚丙烯→熔喷布。
(1)除石油外,化石燃料还包括煤和______。
(2)丙烯的化学式为C H ,1个丙烯分子由______构成。
3 6
(3)熔喷布具有疏松网状 的结构,能阻挡粉尘颗粒,能将飞沫、细菌、病毒吸附住,说明熔喷布具有
______和吸附作用。
27. 食品包装材料与化学元素密切相关。
(1)铁和铝可制作易拉罐等食品包装材料。铁和铝金属活动性强的是______。
(2)经纳米TiO 改性后的聚乙烯食品包装材料,在抑菌和保鲜效果上都有提升。TiO 中Ti的化合价为
2 2
______。
(3)淀粉基食品包装材料是由淀粉[(C H O ) ]经过其他物质改性合成的,使用过后可自然降解为无害物
6 10 5 n
质。淀粉由______种元素组成。
28. 小明进行家庭小实验,制作多晶冰糖。
主要制作过程为:20℃下,取330g蔗糖和100g水,放入不锈钢制容器中,加热并不断搅拌至液体温度
达到120℃,盖上厚毛巾静置7天。(已知:20℃和100℃时,蔗糖的溶解度分别为203.9g和
487.2g)
(1)蔗糖溶液中的溶质是______。
(2)20℃时,将330g蔗糖和100g水混合,得到的是______(填“饱和”或“不饱和”)溶液。
(3)加热后,溶液中溶质质量分数会______(填“增大”或“减小”)。
〖科普阅读理解〗
29. 阅读下面科普短文。
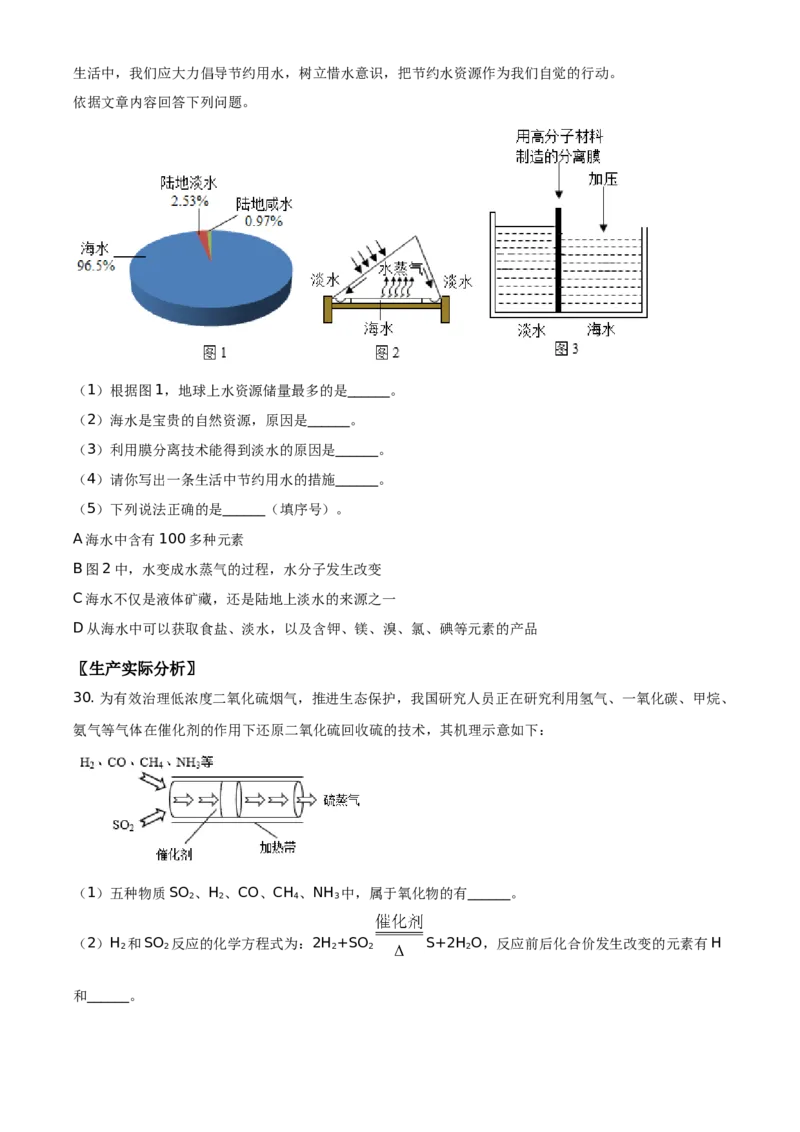
水是包括人类在内所有生命生存的重要物质,也是生物体最重要的组成部分。全球水资源储量如图1所示。
海水是宝贵的自然资源,目前世界上已知的100多种元素中,80多种可以在海水中找到,是名副其
实的液体矿藏。海水的含盐量非常高,通过晾晒可得到食盐,我国目前利用海洋资源获取钾、镁、溴、氯、
碘等元素已形成规模。
海水不能被直接使用,可以通过淡化进行处理,常用的海水淡化方法有蒸馏法和反渗透法。利用太阳能蒸
馏淡化海水是一种节能的蒸馏法,其原理如图2所示。反渗透法是一种膜分离技术淡化方法,其原理如图
3所示,对海水加压,水分子可以透过分离膜而海水中的各种离子不能透过,从而得到淡水。
海水还是陆地上淡水的来源之一和气候的调节器。人类在日常生活中所能使用的是淡水资源,淡水资源弥
足珍贵,我国淡水资源人均占有量只相当世界人均占有量的1/4左右。节约是中华民族的传统美德,日常生活中,我们应大力倡导节约用水,树立惜水意识,把节约水资源作为我们自觉的行动。
依据文章内容回答下列问题。
(1)根据图1,地球上水资源储量最多的是______。
(2)海水是宝贵的自然资源,原因是______。
(3)利用膜分离技术能得到淡水的原因是______。
(4)请你写出一条生活中节约用水的措施______。
(5)下列说法正确的是______(填序号)。
A海水中含有100多种元素
B图2中,水变成水蒸气的过程,水分子发生改变
C海水不仅是液体矿藏,还是陆地上淡水的来源之一
D从海水中可以获取食盐、淡水,以及含钾、镁、溴、氯、碘等元素的产品
〖生产实际分析〗
30. 为有效治理低浓度二氧化硫烟气,推进生态保护,我国研究人员正在研究利用氢气、一氧化碳、甲烷、
氨气等气体在催化剂的作用下还原二氧化硫回收硫的技术,其机理示意如下:
(1)五种物质SO 、H 、CO、CH 、NH 中,属于氧化物的有______。
2 2 4 3
(2)H 和SO 反应的化学方程式为:2H +SO S+2H O,反应前后化合价发生改变的元素有H
2 2 2 2 2
和______。(3)配平CO与SO 反应的化学方程式:_____CO+SO 2CO +_____S
2 2 2
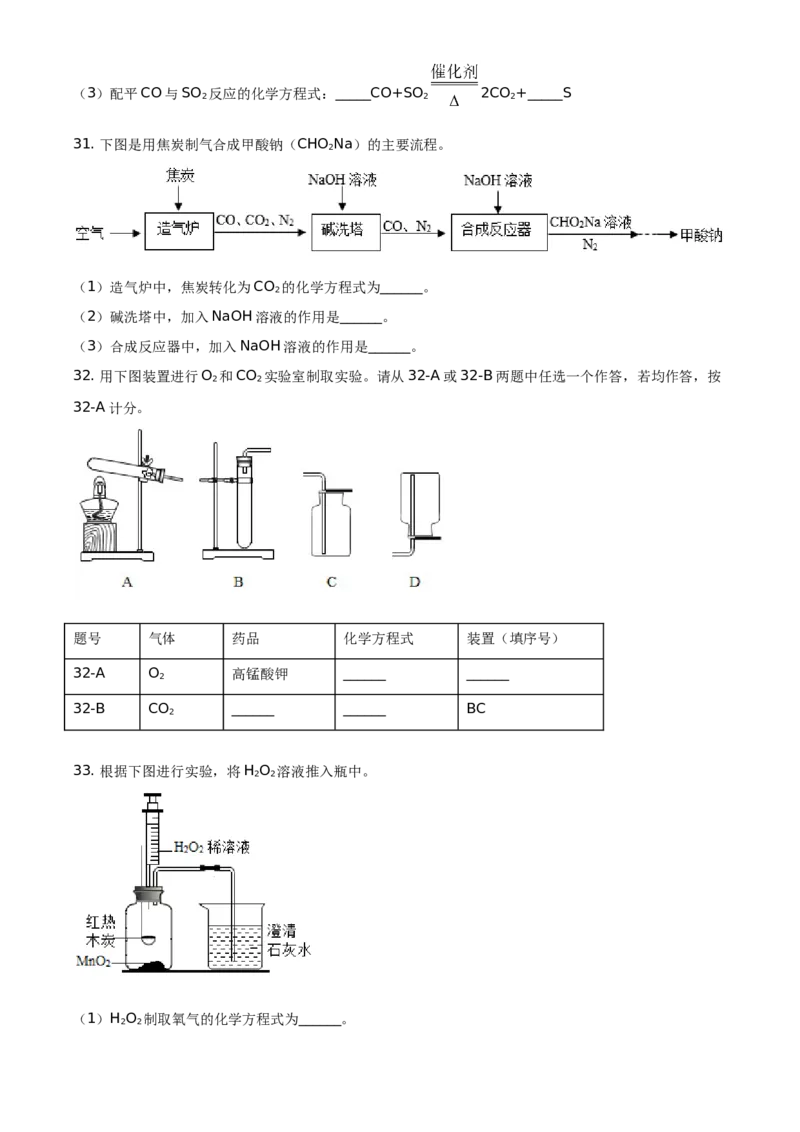
31. 下图是用焦炭制气合成甲酸钠(CHO Na)的主要流程。
2
(1)造气炉中,焦炭转化为CO 的化学方程式为______。
2
(2)碱洗塔中,加入NaOH溶液的作用是______。
(3)合成反应器中,加入NaOH溶液的作用是______。
32. 用下图装置进行O 和CO 实验室制取实验。请从32-A或32-B两题中任选一个作答,若均作答,按
2 2
32-A计分。
题号 气体 药品 化学方程式 装置(填序号)
32-A O 高锰酸钾 ______ ______
2
32-B CO ______ ______ BC
2
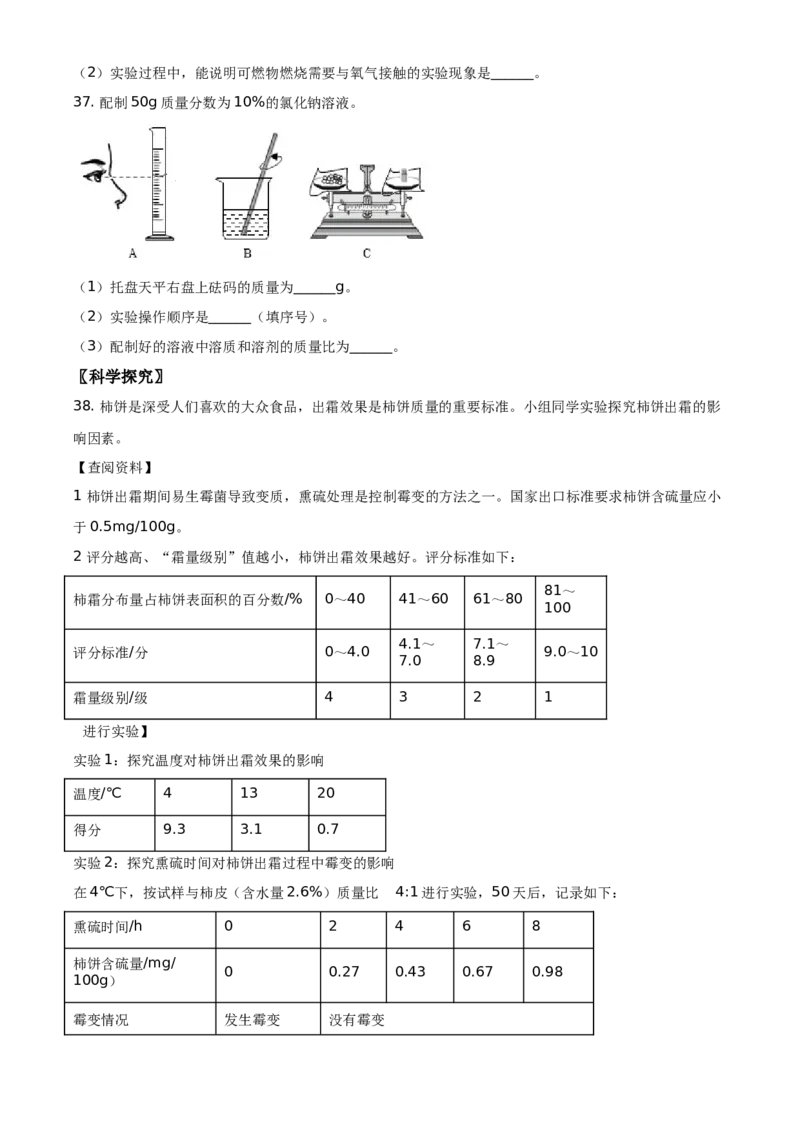
33. 根据下图进行实验,将H O 溶液推入瓶中。
2 2
(1)H O 制取氧气的化学方程式为______。
2 2(2)木炭燃烧阶段,观察到的现象有______。
(3)烧杯中发生反应的化学方程式为______。
34. 根据下图回答问题。
(1)图1实验,与电源正极相连的试管中生成的气体是______,发生反应的化学方程式为______。
(2)图2实验,观察到的现象是______,说明CO 具有的性质是______。
2
35. 利用下图装置(气密性良好)验证空气中氧气的含量。
将粗铁丝加热,迅速放入具支试管点燃红磷并迅速塞紧胶塞,反应停止待冷却后打开止水夹。
(1)红磷的作用是______。
(2)能说明空气中氧气约占1/5的现象是______。
36. 用下图装置(夹持装置已略去)探究燃烧的条件。
将2份等质量的红磷放在铁片两端,将右端红磷用细沙覆盖并加热一段时间,左端红磷发生燃烧;熄灭酒
精灯,拨开细沙,细沙下的红磷发生燃烧。
(1)铁片左端的红磷燃烧,说明铁具有的性质是______。(2)实验过程中,能说明可燃物燃烧需要与氧气接触的实验现象是______。
37. 配制50g质量分数为10%的氯化钠溶液。
(1)托盘天平右盘上砝码的质量为______g。
(2)实验操作顺序是______(填序号)。
(3)配制好的溶液中溶质和溶剂的质量比为______。
〖科学探究〗
38. 柿饼是深受人们喜欢的大众食品,出霜效果是柿饼质量的重要标准。小组同学实验探究柿饼出霜的影
响因素。
【查阅资料】
1 柿饼出霜期间易生霉菌导致变质,熏硫处理是控制霉变的方法之一。国家出口标准要求柿饼含硫量应小
于0.5mg/100g。
2 评分越高、“霜量级别”值越小,柿饼出霜效果越好。评分标准如下:
81~
柿霜分布量占柿饼表面积的百分数/% 0~40 41~60 61~80
100
4.1~ 7.1~
评分标准/分 0~4.0 9.0~10
7.0 8.9
霜量级别/级 4 3 2 1
【进行实验】
实验1:探究温度对柿饼出霜效果的影响
温度/℃ 4 13 20
得分 9.3 3.1 0.7
实验2:探究熏硫时间对柿饼出霜过程中霉变的影响
在4℃下,按试样与柿皮(含水量2.6%)质量比 为4:1进行实验,50天后,记录如下:
熏硫时间/h 0 2 4 6 8
柿饼含硫量/mg/
0 0.27 0.43 0.67 0.98
100g)
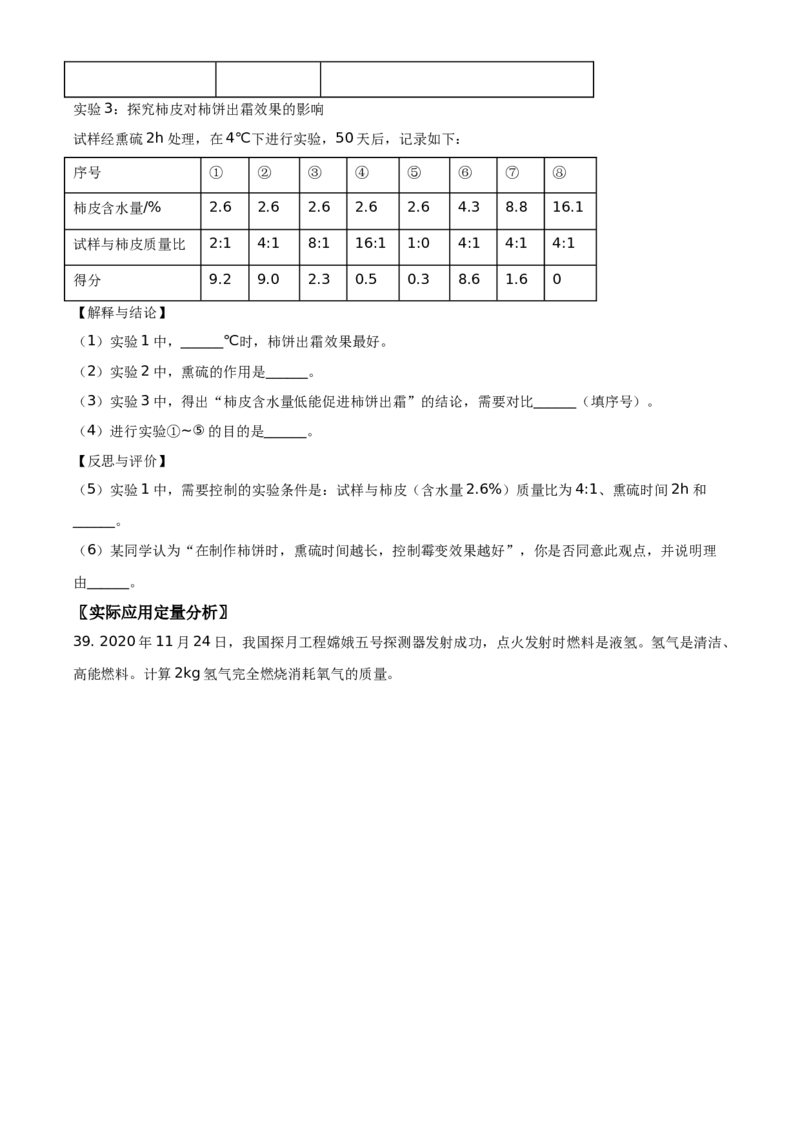
霉变情况 发生霉变 没有霉变实验3:探究柿皮对柿饼出霜效果的影响
试样经熏硫2h处理,在4℃下进行实验,50天后,记录如下:
序号 ① ② ③ ④ ⑤ ⑥ ⑦ ⑧
柿皮含水量/% 2.6 2.6 2.6 2.6 2.6 4.3 8.8 16.1
试样与柿皮质量比 2:1 4:1 8:1 16:1 1:0 4:1 4:1 4:1
得分 9.2 9.0 2.3 0.5 0.3 8.6 1.6 0
【解释与结论】
(1)实验1中,______℃时,柿饼出霜效果最好。
(2)实验2中,熏硫的作用是______。
(3)实验3中,得出“柿皮含水量低能促进柿饼出霜”的结论,需要对比______(填序号)。
(4)进行实验①~⑤的目的是______。
【反思与评价】
(5)实验1中,需要控制的实验条件是:试样与柿皮(含水量2.6%)质量比为4:1、熏硫时间2h和
______。
(6)某同学认为“在制作柿饼时,熏硫时间越长,控制霉变效果越好”,你是否同意此观点,并说明理
由______。
〖实际应用定量分析〗
39. 2020年11月24日,我国探月工程嫦娥五号探测器发射成功,点火发射时燃料是液氢。氢气是清洁、
高能燃料。计算2kg氢气完全燃烧消耗氧气的质量。本试卷的题干、答案和解析均由组卷网(http://zujuan.xkw.com)专业教师团队编校出品。
登录组卷网可对本试卷进行单题组卷、细目表分析、布置作业、举一反三等操作。
试卷地址:在组卷网浏览本卷
组卷网是学科网旗下的在线题库平台,覆盖小初高全学段全学科、超过900万精品解析试题。
关注组卷网服务号,可使用移动教学助手功能(布置作业、线上考试、加入错题本、错题训练)。
学科网长期征集全国最新统考试卷、名校试卷、原创题,赢取丰厚稿酬,欢迎合作。
钱老师 QQ:537008204 曹老师 QQ:713000635