文档内容
重庆乌江新高考协作体 2025 届高考质量调研(二)
化学试题
(分数:100分,时间:75分钟)
一、选择题
1. 下列表示正确的是
A. 基态 的电子排布式:
B. 二氯乙烷的结构简式:
C. 的电子式
D. 的VSEPR模型:
2. 下列含有非极性键的离子晶体是
①醋酸钠固体 ②氢氧化钾固体 ③过氧化钠固体
④金刚石 ⑤固态乙醇 ⑥氯化钙固体
A. ③⑥ B. ①③ C. ③④⑤ D. ②⑥
3. 下列有关物质的量浓度的叙述正确的是
A. 水中溶解了 后,所得溶液浓度为
B. 配制 的,需用 胆矾
C. 从 中取出 ,则这 的物质的量浓度是原溶液的1/10
D. 的 中,
4. 某同学在做钠的燃烧实验时,观察到火焰的颜色为( )
A. 红色 B. 紫色 C. 蓝色 D. 黄色
5. 主族元素Q、X、Y、Z、W的原子序数依次增大,且均不大于20,X与Y相邻,Y、W的最外层电子数之和等于Z的族序数,Z的最高正价和最低负价代数和为4,化合物YQ 可作为火箭推进剂,普遍用在
2 4
卫星和导弹的姿态控制上。下列说法错误的是
A. X和Z的单质均存在多种同素异形体
B. Q、Y和Z三种元素只能形成共价化合物
C. Q和W形成的化合物的水溶液呈碱性
D. WZXY溶液常用于Fe3+的检验
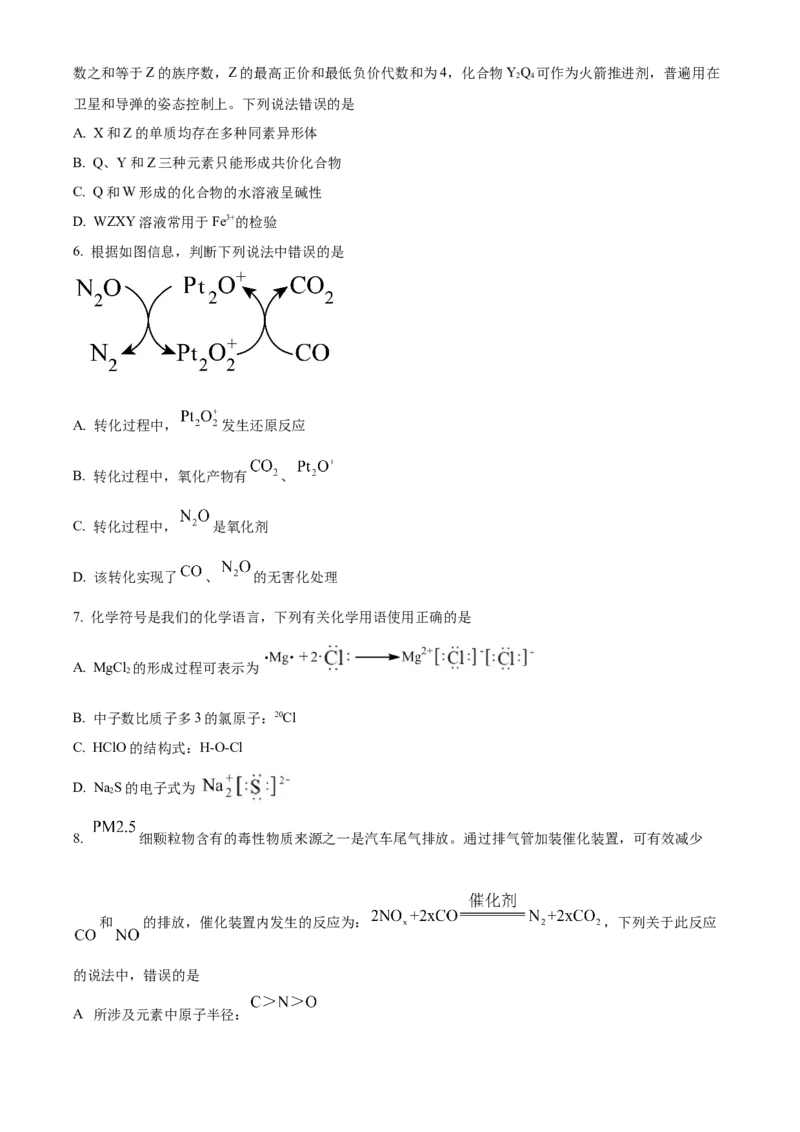
6. 根据如图信息,判断下列说法中错误的是
A. 转化过程中, 发生还原反应
B. 转化过程中,氧化产物有 、
C. 转化过程中, 是氧化剂
D. 该转化实现了 、 的无害化处理
7. 化学符号是我们的化学语言,下列有关化学用语使用正确的是
A. MgCl 的形成过程可表示为
2
B. 中子数比质子多3的氯原子:20Cl
C. HClO的结构式:H-O-Cl
D. NaS的电子式为
2
8. 细颗粒物含有的毒性物质来源之一是汽车尾气排放。通过排气管加装催化装置,可有效减少
和 的排放,催化装置内发生的反应为: ,下列关于此反应
的说法中,错误的是
.
A 所涉及元素中原子半径:B. 当 时,每生成 ,转移电子数为 为氧化产物
C. 氧化剂与还原剂的物质的量之比为1∶1时, 中氮元素的化合价为 价
D. 等物质的量 和 中,共用电子对数之比为3∶4
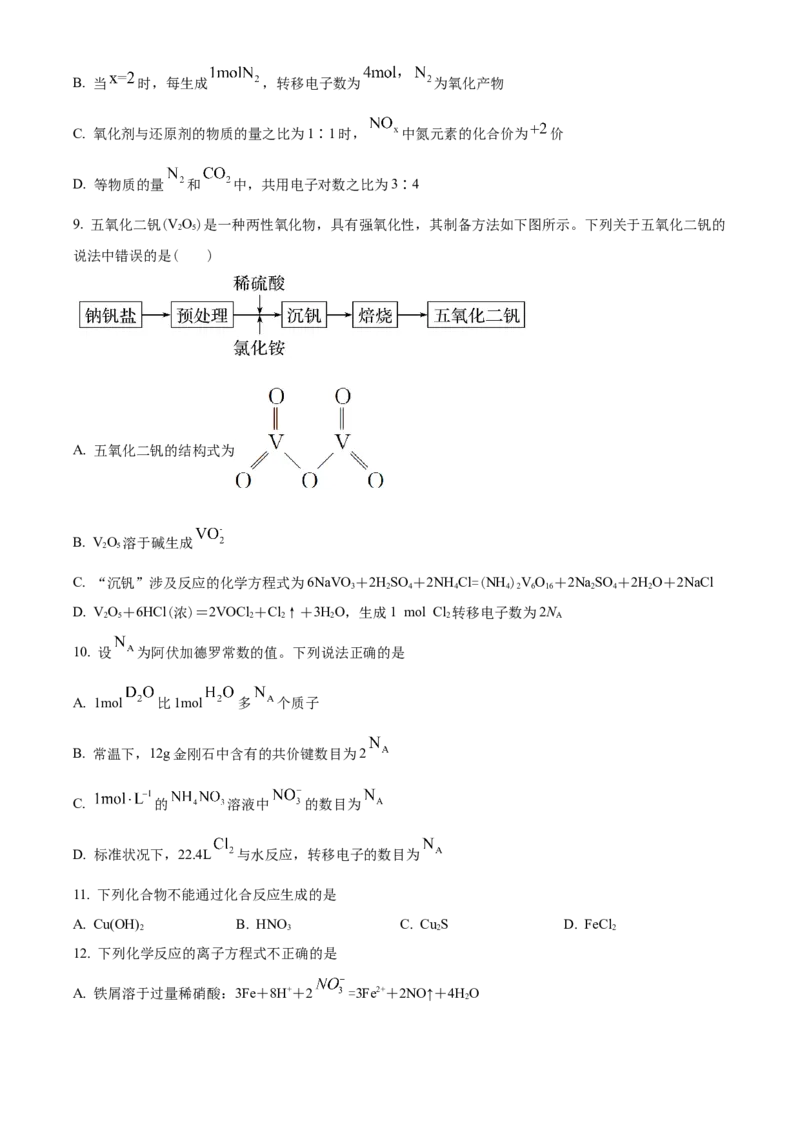
9. 五氧化二钒(VO)是一种两性氧化物,具有强氧化性,其制备方法如下图所示。下列关于五氧化二钒的
2 5
说法中错误的是( )
A. 五氧化二钒的结构式为
B. VO 溶于碱生成
2 5
C. “沉钒”涉及反应的化学方程式为6NaVO +2HSO +2NH Cl=(NH )VO +2NaSO +2HO+2NaCl
3 2 4 4 4 2 6 16 2 4 2
D. VO+6HCl(浓)=2VOCl +Cl↑+3HO,生成1 mol Cl 转移电子数为2N
2 5 2 2 2 2 A
10. 设 为阿伏加德罗常数的值。下列说法正确的是
A. 1mol 比1mol 多 个质子
B. 常温下,12g金刚石中含有的共价键数目为2
C. 的 溶液中 的数目为
D. 标准状况下,22.4L 与水反应,转移电子的数目为
11. 下列化合物不能通过化合反应生成的是
A. Cu(OH) B. HNO C. Cu S D. FeCl
2 3 2 2
12. 下列化学反应的离子方程式不正确的是
A. 铁屑溶于过量稀硝酸:3Fe+8H++2 =3Fe2++2NO↑+4HO
2B. Fe(OH) 溶于过量的HI溶液:2Fe(OH) +6H++2I-=2Fe2++I +6H O
3 3 2 2
C. 在AlCl 溶液中加入过量氨水:Al3++3NH·H O=Al(OH) ↓+3
3 3 2 3
D. 过量的NaHSO 溶液与Ba(OH) 溶液反应:2H++ +Ba2++2OH-=BaSO↓+2H O
4 2 4 2
13. 亚氯酸钠( )是一种高效氧化剂和漂白剂。种制备亚氯酸钠粗产品的工艺流程如下:
已知:纯 易分解爆炸; 在碱性溶液中稳定存在,在酸性溶液中分解为 和 。
下列说法正确的是
A. 发生器中鼓入空气的作用是将 氧化
B. 从母液中回收的主要物质是 和
C. 吸收塔内反应的离子方程式为
D. 理论上,每生产 至少需要通入 (标准状况)
14. 焦炭是重要的工业原料,用作冶金、燃料、制电石、制硅等,2C +SiO Si +2CO↑,3C +CaO
2
CaC +CO↑。设N 是阿伏加德罗常数的值,下列说法正确的是
2 A
A. 常温常压下,11.2L CO含有的分子数小于0.5N
A
B. 64g CaC 含有阴阳离子总数为3N
2 A
.
C 若12g焦炭参加反应,以上两个反应中焦炭均失去2N 个电子
A
D. lmol SiO 晶体含有共价键数目为2N
2 A
二、非选择题
15. “侯氏制碱法”是我国化工专家侯德榜为世界制碱工业作出的突出贡献。模拟“侯氏制碱法”以粗盐水为原
料制备纯碱的流程如图所示。回答下列问题:
(1)粗盐水中含有 杂质,提纯过程应加试剂为___________;沉淀A___________电解质(填“是”或
“不是”)。
(2)向溶液A中先通入___________至饱和(填“ ”或“ ”,下同),再向溶液中通入___________,
此时观察到溶液中有晶体析出,该反应的化学方程式为___________。
(3)溶液B中主要溶质的电离方程式为___________。
(4)此流程中可以循环利用的物质是___________。
16. 绿色化学的核心就是利用化学原理从源头上减少和清除工业生产对环境的污染。
(1)按照绿色化学的原则,最理想的“原子经济”就是反应物的原子全部转化为期望的最终产物,这时原子
的利用率为_________。
(2) 是甲基丙烯酸甲酯的结构简式。也可以写成CH=C(CH )COOCH 。
2 3 3
旧法合成它的反应是:(OH)
(CH)C = O+HCN→(CH)C(OH)CN
3 2 3 2
(CH)C(OH)CN + CH OH + H SO →CH= C(CH)COOCH +NHHSO
3 2 3 2 4 2 3 3 4 4
新法合成它的反应是:
CHC ≡ CH + CO + CH OH CH= C(CH)COOCH
3 3 2 3 3
①与旧法相比,新法的突出优点是_________
A.原料无爆炸危险 B.原料都是无毒物质
C.没有副产物,原子利用率高 D.对设备腐蚀性小
②计算:甲基丙烯酸甲酯旧法合成工艺的理论上原子利用率是_________。
(原子利用率=期望产物的总质量与生成物的总质量之比)
③写出聚甲基丙烯酸甲酯(又称有机玻璃)的结构简式_________
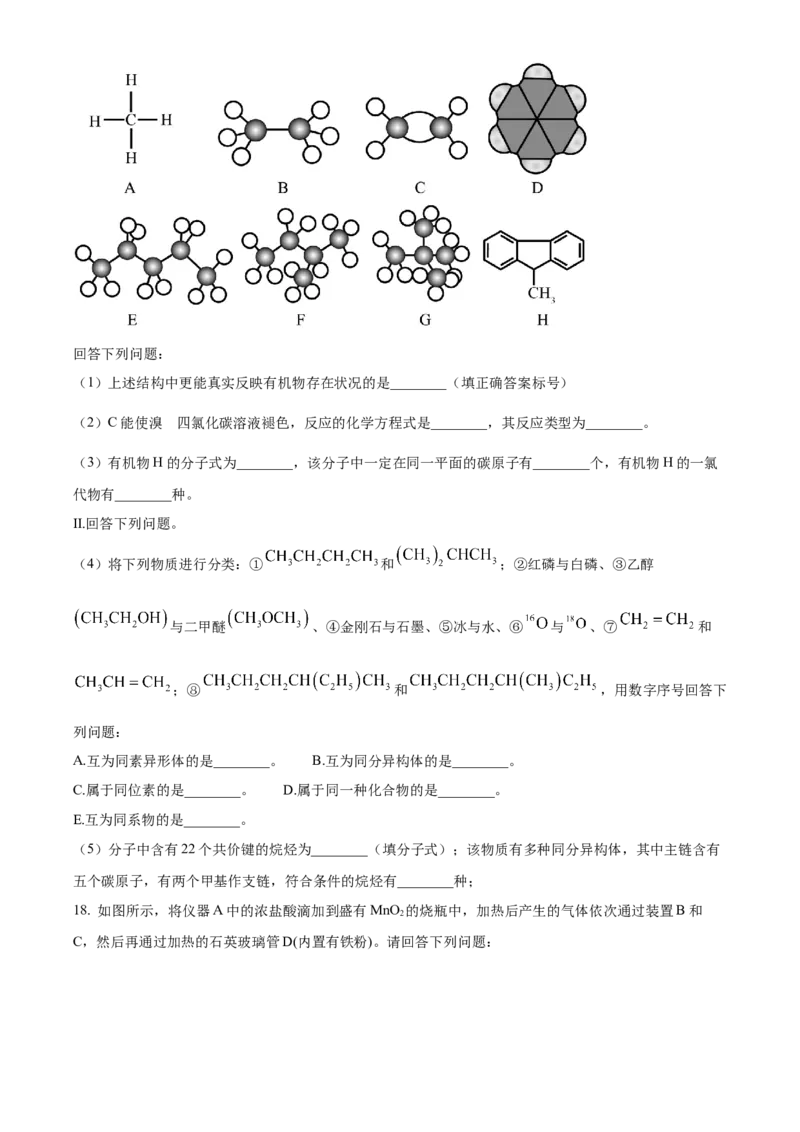
17. Ⅰ.有机物的种类和数目非常庞大,认识简单的有机物是我们学习有机化学的开始。现有如图所示几种
有机物的结构:回答下列问题:
(1)上述结构中更能真实反映有机物存在状况的是________(填正确答案标号)
的
(2)C能使溴 四氯化碳溶液褪色,反应的化学方程式是________,其反应类型为________。
(3)有机物H的分子式为________,该分子中一定在同一平面的碳原子有________个,有机物H的一氯
代物有________种。
Ⅱ.回答下列问题。
(4)将下列物质进行分类:① 和 ;②红磷与白磷、③乙醇
与二甲醚 、④金刚石与石墨、⑤冰与水、⑥ 与 、⑦ 和
;⑧ 和 ,用数字序号回答下
列问题:
A.互为同素异形体的是________。 B.互为同分异构体的是________。
C.属于同位素的是________。 D.属于同一种化合物的是________。
E.互为同系物的是________。
(5)分子中含有22个共价键的烷烃为________(填分子式);该物质有多种同分异构体,其中主链含有
五个碳原子,有两个甲基作支链,符合条件的烷烃有________种;
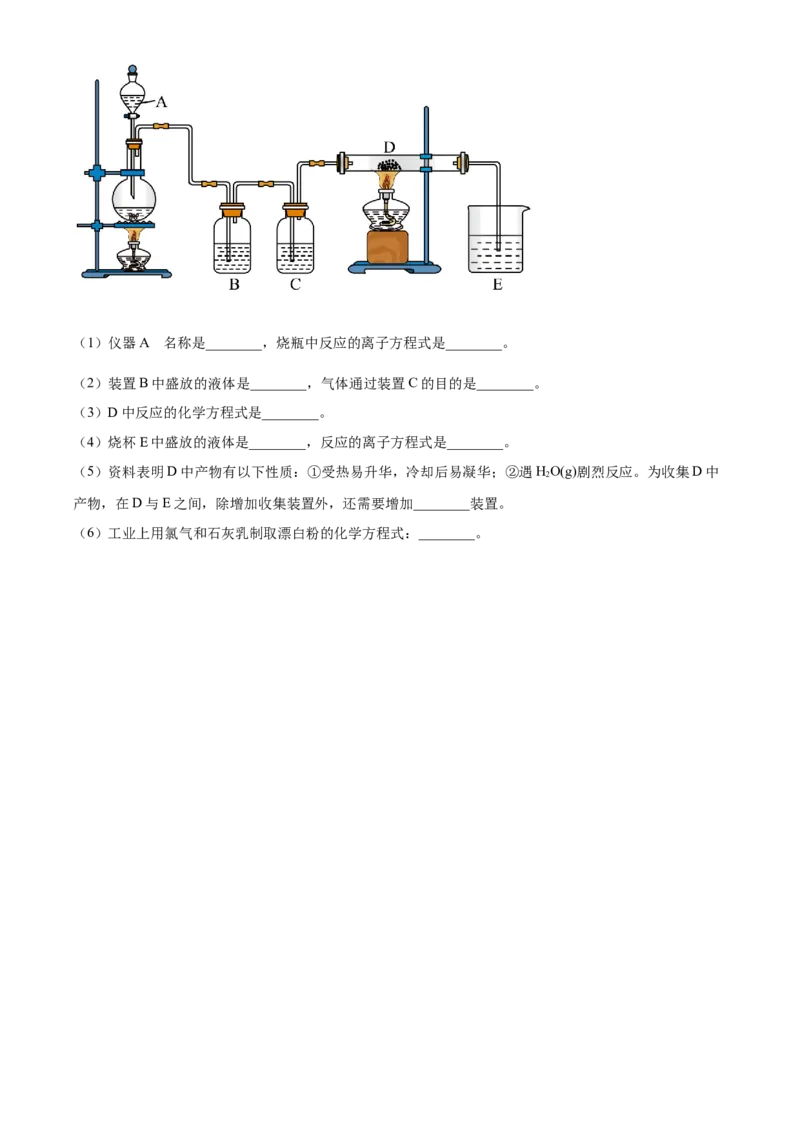
18. 如图所示,将仪器A中的浓盐酸滴加到盛有MnO 的烧瓶中,加热后产生的气体依次通过装置B和
2
C,然后再通过加热的石英玻璃管D(内置有铁粉)。请回答下列问题:的
(1)仪器A 名称是________,烧瓶中反应的离子方程式是________。
(2)装置B中盛放的液体是________,气体通过装置C的目的是________。
(3)D中反应的化学方程式是________。
(4)烧杯E中盛放的液体是________,反应的离子方程式是________。
(5)资料表明D中产物有以下性质:①受热易升华,冷却后易凝华;②遇HO(g)剧烈反应。为收集D中
2
产物,在D与E之间,除增加收集装置外,还需要增加________装置。
(6)工业上用氯气和石灰乳制取漂白粉的化学方程式:________。