文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
专题二 物质的推断
(试题分值:100分 测试时间:45分钟)
一、选择题(本题包括10小题,每小题4分,共40分.每小题只有一个正确答案)
1.在给定条件下,下列物质间的转化不能实现的是( )
A. B.
C. D.
【答案】A
【解析】A、硫在氧气中燃烧生成二氧化硫,则 不能实现,故选项符合题意;
B、碳酸氢铵在加热的条件下生成二氧化碳、水和氨气,则 能实现,故选项不符合题
意;
C、、过氧化氢在二氧化锰的催化作用下生成水和氧气,则 能实现,故选项不符合题意;
D、氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,则 能实现,故选项不符
合题意。
故选A。
2.箭头表示物质间在一定条件下通过一步化学反应就能实现转化,则下图的四组物质中,不能按箭头转
化的是( )
A. B.
C. D.
【答案】B
【解析】A、碳酸钙高温生成氧化钙,氧化钙和水生成氢氧化钙,氢氧化钙和二氧化碳生成碳酸钙沉淀,
正确;
B、氯化钠溶液电解可以得到氢氧化钠,氢氧化钠和硝酸生成硝酸钠,硝酸钠和氯化物反应不能生成沉淀
气体水,故不能转化为氯化钠,错误;
C、碳完全燃烧生成二氧化碳、不完全燃烧生成一氧化碳,一氧化碳燃烧生成二氧化碳、二氧化碳和碳高
温生成一氧化碳,正确;
D、硫酸和碳酸钠生成二氧化碳和水,二氧化碳和氢氧化钠生成水,正确;
故选B。
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
3.甲、乙、丙有如图所示的转化关系(“→”表示反应一步实现,部分物质和反应条件已略去),下列
各组物质按照甲、乙、丙的顺序不符合要求的是( )
A.C、CO、CO B.HO、HO、O
2 2 2 2 2
C.NaOH、NaCO、NaNO D.Ca(OH) 、CaCO 、CaCl
2 3 3 2 3 2
【答案】C
【解析】A、碳与氧气反应生成一氧化碳,一氧化碳燃烧生成二氧化碳,二氧化碳与碳在高温下反应生成
一氧化碳,故A不符合题意;
B、过氧化氢分解能生成水,水电解能生成氧气,氢气在氧气中燃烧生成水,故B不符合题意;
C、氢氧化钠与二氧化碳反应能生成碳酸钠,碳酸钠与硝酸反应能生成硝酸钠,但硝酸钠无法一步转化生
成碳酸钠,故C符合题意;
D、氢氧化钙与二氧化碳反应能生成碳酸钙,碳酸钙与盐酸反应能生成氯化钙,氯化钙与碳酸钠反应能生
成碳酸钙,故D不符合题意。
故选C。
4.如图中“→”表示两端的物质通过一步反应能转化.在给定条件下,下列选项所示的物质间的转化不
能实现的是( )
A. B.
C. D.
【答案】C
【解析】A、镁在氧气中燃烧生成氧化镁,氧化镁和硫酸反应生成硫酸镁和水,物质间转化均能实现,不
符合题意;
B、碳在氧气中燃烧生成二氧化碳气体,二氧化碳与水反应生成碳酸,物质间转化均能实现,不符合题
意;
C、氧化铁与一氧化碳在高温下生成铁和二氧化碳,铁与稀盐酸反应生成氯化亚铁,而不是氯化铁,该物
质间转化不能实现,符合题意;
D、氢氧化钠与二氧化碳反应生成碳酸钠和水,碳酸钠能与氯化钙溶液反应生成碳酸钙沉淀和氯化钠,物
质间转化均能实现,不符合题意。
故选C。
5.如图所示为甲、乙、丙、丁四种物质间的相互关系,涉及的反应均为初中化学常见反应(“—”表示相连
的两种物质能反应,“→”表示通过一步反应能实现转化),下列选项符合图示关系的是( )
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
选
甲 乙 丙 丁
项
A CuO H HSO Mg
2 2 4
B HCl Fe Fe O O
3 4 2
C O CO CO C
2 2
D Ca(OH) CO NaCO HCl
2 2 2 3
【答案】D
【解析】A、甲—乙反应是指氧化铜与氢气在加热条件下反应生成铜和水;甲—丙反应是指氧化铜与硫酸
反应生成硫酸铜和水;丙—丁反应是指硫酸和镁反应生成硫酸镁和氢气;丁→乙是指镁和稀硫酸反应生成
硫酸镁和氢气;丙→乙是指镁和稀硫酸反应生成硫酸镁和氢气,乙→丙不能一步反应实现转化,不符合题
意;
B、甲—乙是指铁和稀盐酸反应生成氯化亚铁和氢气;甲—丙反应是指盐酸和四氧化三铁反应生成盐和
水;丙—丁不反应,不符合题意;
C、甲—乙反应是指氧气和一氧化碳在点燃条件下反应生成二氧化碳;甲—丙不反应,不符合题意;
D、甲—乙反应是指氢氧化钙与二氧化碳气体反应生成碳酸钙沉淀和水;甲—丙氢氧化钙溶液和碳酸钠溶
液反应生成碳酸钙沉淀和氢氧化钠;丙—丁是指碳酸钠溶液和盐酸反应生成氯化钠、水和二氧化碳气体;
丁→乙是指盐酸和碳酸钠溶液反应生成二氧化碳气体;丙→乙是指碳酸钠溶液和盐酸反应生成二氧化碳;
乙→丙是指二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,符合题意;
故选:D。
6.物质转化是化学研究的重要内容。甲、乙、丙、丁是不同类别的常见物质,甲是单质,丁是配制波尔
多液的原料,转化关系如图(“—”表示相互反应,“→”表示一步转化,涉及的反应均为初中化学常见
反应)。下列说法正确的是( )
A.反应①一定是置换反应 B.反应②有氢气生成
C.反应③④一定有沉淀生成 D.丙是盐
【答案】A
【解析】甲、乙、丙、丁是不同类别的常见物质,甲是单质,丁是配制波尔多液的原料,甲与丁能反应,
所以丁是硫酸铜,甲是比铜活泼的常见金属(如铁等),甲能和乙反应且乙能转化为丁,所以乙是稀硫
酸,丙能和酸、盐反应,故丙是碱(如氢氧化钠等),带入验证,推理正确。
A、甲是铁等较活泼金属,丁是硫酸铜,反应①可以是活泼金属和硫酸铜反应生成铜和另一种硫酸盐,此
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
类反应是一种单质和一种化合物生成另一种单质和另一种化合物,属于置换反应,故说法正确;
B、乙是稀硫酸,丁是硫酸铜,反应②可以是氧化铜或氢氧化铜和稀硫酸反应生成硫酸铜和水,故说法错
误;
C、乙是稀硫酸,若丙是氢氧化钠,稀硫酸和氢氧化钠反应生成硫酸钠和水,没有沉淀生成,故说法错
误;
D、由分析可知,丙是碱,故说法错误。
故选A。
7.已知某溶液X是 溶液、 溶液之一,甲、乙、丙是 溶液、稀盐酸、 溶液中
的各一种,取三等份溶液X,分别向其中滴入适量的甲、乙、丙三种溶液,产生的实验现象如下表所示。
加入的物质 甲 乙 丙
实验现象 蓝色沉淀 无明显现象 白色沉淀
依据实验现象做出的下列推断中,合理的是( )
A.X是 溶液 B.乙是稀盐酸
C.甲与X发生了中和反应 D.表中蓝色沉淀和白色沉淀均可溶于稀硝酸
【答案】B
【解析】甲+X产生蓝色沉淀,能产生蓝色沉淀的氢氧根离子和铜离子、丙+X产生白色沉淀,能产生白色
沉淀的是银离子和氯离子,故可以判断,X是氯化铜溶液、甲是NaOH溶液、乙是稀盐酸,丙是AgNO 溶
3
液。
A、有上述分析可知X是CuCl 溶液,故错误;
2
B、有上述分析可知乙是稀盐酸,故正确;
C、甲与X是氢氧化钠和氯化铜反应产生氢氧化铜沉淀和氯化钠,是碱与盐的反应,不是酸碱中和反应,
故错误;
D、表中蓝色沉淀是氢氧化铜,能溶于稀硝酸,白色沉淀是氯化银,不能溶于稀硝酸,故错误。
故选B。
8.如图所示物质及变化均是初中化学常见的纯净物及反应。其中甲、乙、丙均是单质且由不同种元素组
成,丁是氧化物。“—”表示相连两种物质可以反应,“→”表示一种物质通过一步反应可以转化成另一
种物质。下列说法错误的是( )
A.甲→乙反应前后一定存在元素化合价的改变
B.甲、丙可以都是金属,且金属活动性:甲>丙
C. →丁的反应体现了氧气的氧化性
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
D.丁→丙的反应一定属于置换反应
【答案】D
【解析】A、甲、乙均为单质,单质中元素化合价为0,而化合物中元素的化合价不为零,则甲→乙反应前
后一定存在元素化合价的改变,该选项说法正确;
B、若甲、丙都是金属,且甲能把丙置换出来,则说明金属活动性顺序:甲>丙,该选项说法正确;
C、物质和氧气的反应属于氧化反应,其中体现了氧气的氧化物,该选项说法正确;
D、丁为氧化物,丙为单质,若丁为氧化铜,丙为铜,一氧化碳和氧化铜在加热条件下生成铜和二氧化
碳,不属于置换反应,该选项说法不正确。
故选D。
9.2022年北京冬奥会的成功举办,让我们领略了无穷的冰雪魅力,如图“雪花”顶角上的A、B、C、
D、E、F是初中化学常见的六种物质。其中D是金属单质,A、C是氧化物,A是黑色固体,C是气体;
B、E、F依次是酸、碱、盐,B的浓溶液能夺取纸张里的水分,生成黑色的炭, 俗称熟石灰, 的溶液
呈蓝色(图中“一”表示物质间能相互发生反应,“→”表示物质间能发生转化)。下列推断中不正确的是
( )
A.A、B、E、F是四种不同类别的化合物
B.A的化学式为Fe O
3 4
C.C和E发生的反应属于基本反应类型中的复分解反应
D.B和E发生反应的化学方程式为Ca(OH) +H SO =CaSO +2H O
2 2 4 4 2
【答案】C
【解析】B的浓溶液能夺取纸张里的水分,生成黑色的炭,所以B是硫酸,E俗称熟石灰,所以E是氢氧
化钙,F的溶液呈蓝色,硫酸会转化成F,所以F是硫酸铜,C会与氢氧化钙反应,所以C是二氧化碳,D
会与硫酸铜反应,所以D是铁,铁和A可以互相转化,A可以是四氧化三铁,经过验证,推断正确。
A、由分析可知,A是氧化物,B是酸,E是碱,F是盐,所以A、B、E、F是四种不同类别的化合物,故
选项说法正确;
B、由分析可知,A是四氧化三铁,其化学式为Fe O,故选项说法正确;
3 4
C、C和E发生的反应是二氧化碳与氢氧化钙反应生成碳酸钙和水,该反应不是两种化合物互相交换成分
生成另外两种化合物,不属于复分解反应,故选项说法错误;
D、B和E发生的反应为氢氧化钙和硫酸反应生成硫酸钙和水,反应的化学方程式为
Ca(OH) +H SO =CaSO +2H O,故选项说法正确;
2 2 4 4 2
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
故选:C。
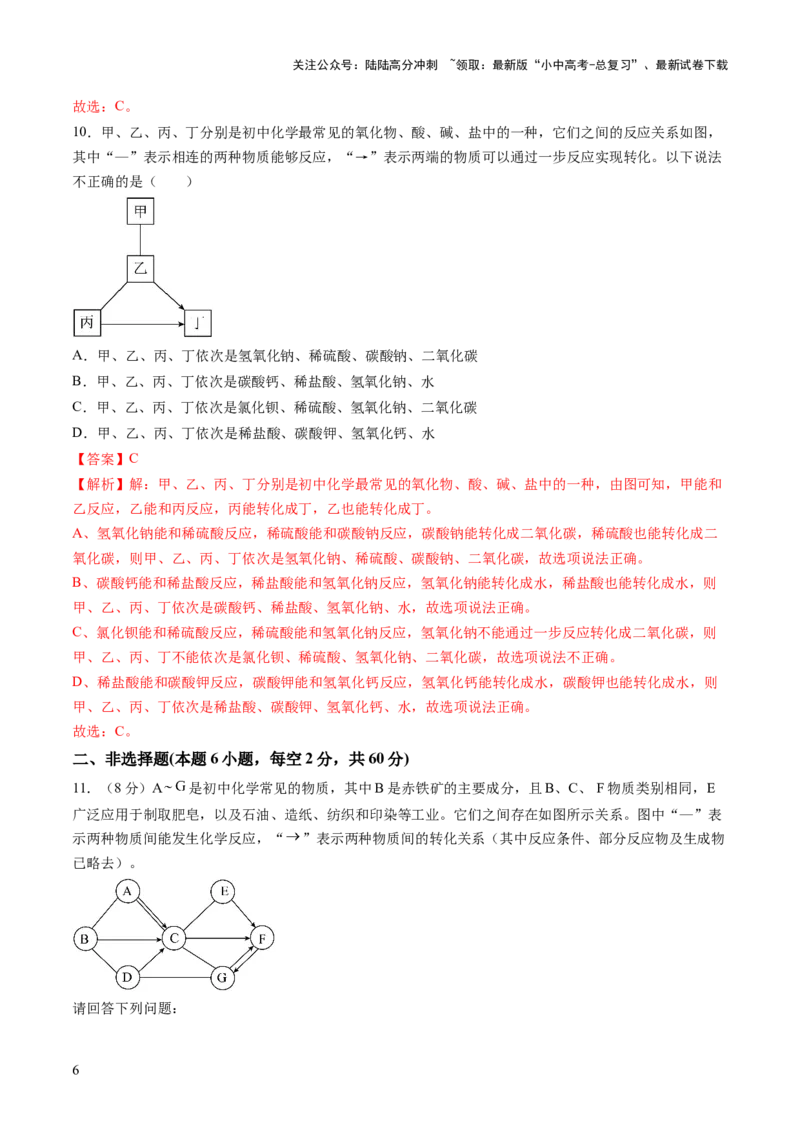
10.甲、乙、丙、丁分别是初中化学最常见的氧化物、酸、碱、盐中的一种,它们之间的反应关系如图,
其中“—”表示相连的两种物质能够反应,“→”表示两端的物质可以通过一步反应实现转化。以下说法
不正确的是( )
A.甲、乙、丙、丁依次是氢氧化钠、稀硫酸、碳酸钠、二氧化碳
B.甲、乙、丙、丁依次是碳酸钙、稀盐酸、氢氧化钠、水
C.甲、乙、丙、丁依次是氯化钡、稀硫酸、氢氧化钠、二氧化碳
D.甲、乙、丙、丁依次是稀盐酸、碳酸钾、氢氧化钙、水
【答案】C
【解析】解:甲、乙、丙、丁分别是初中化学最常见的氧化物、酸、碱、盐中的一种,由图可知,甲能和
乙反应,乙能和丙反应,丙能转化成丁,乙也能转化成丁。
A、氢氧化钠能和稀硫酸反应,稀硫酸能和碳酸钠反应,碳酸钠能转化成二氧化碳,稀硫酸也能转化成二
氧化碳,则甲、乙、丙、丁依次是氢氧化钠、稀硫酸、碳酸钠、二氧化碳,故选项说法正确。
B、碳酸钙能和稀盐酸反应,稀盐酸能和氢氧化钠反应,氢氧化钠能转化成水,稀盐酸也能转化成水,则
甲、乙、丙、丁依次是碳酸钙、稀盐酸、氢氧化钠、水,故选项说法正确。
C、氯化钡能和稀硫酸反应,稀硫酸能和氢氧化钠反应,氢氧化钠不能通过一步反应转化成二氧化碳,则
甲、乙、丙、丁不能依次是氯化钡、稀硫酸、氢氧化钠、二氧化碳,故选项说法不正确。
D、稀盐酸能和碳酸钾反应,碳酸钾能和氢氧化钙反应,氢氧化钙能转化成水,碳酸钾也能转化成水,则
甲、乙、丙、丁依次是稀盐酸、碳酸钾、氢氧化钙、水,故选项说法正确。
故选:C。
二、非选择题(本题6小题,每空2分,共60分)
11.(8分)A 是初中化学常见的物质,其中B是赤铁矿的主要成分,且B、C、 F物质类别相同,E
广泛应用于制取肥皂,以及石油、造纸、纺织和印染等工业。它们之间存在如图所示关系。图中“—”表
示两种物质间能发生化学反应,“ ”表示两种物质间的转化关系(其中反应条件、部分反应物及生成物
已略去)。
请回答下列问题:
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)请写出B物质的化学式 ,E物质的俗称是 。
(2)B与足量的D反应的实验现象是 。
(3)请写出 所发生反应的化学方程式 。
【答案】(1) 烧碱/火碱/苛性钠
(2)红棕色固体逐渐溶解至消失,溶液由无色变成黄色
(3)
【解析】A∼G是初中化学常见的物质,其中B是赤铁矿的主要成分,可推出B为氧化铁,且B、C、 F物
质类别相同,E广泛应用于制取肥皂,以及石油、造纸、纺织和印染等工业,可推出E为氢氧化钠,B能
转化为C,C能转化为F,E能转化为F,C能与E反应,可推出C为二氧化碳,F为水,C能与G反应,
G能与F相互转化,可推出G为氢氧化钙,A能与B反应,A能转化为C,A能与C反应,可推出A为
碳,B能与D反应,D能转化为C,D能与G反应,可推出D为酸,如稀盐酸,代入验证,符合题意。
(1)由分析可知,B为氧化铁,化学式为:Fe O;
2 3
E为氢氧化钠,氢氧化钠俗称烧碱、火碱、苛性钠;
(2)B与足量的D的反应为氧化铁和稀盐酸反应生成氯化铁和水,现象是:红棕色固体逐渐溶解至消
失,溶液由无色变成黄色;
(3)F→G的反应为氧化钙和水反应生成氢氧化钙,该反应的化学方程式为: 。
12.(10分)框图中A是人体胃液中含有的成分,B可用于改良酸性土壤,G是铁锈的主要成分,E、F、
I为无色气体。根据图示回答下列问题。
(1)写出有关物质的化学式:G: ,A: ;
(2)写出反应⑤观察到的实验现象: ;
(3)反应②的化学方程式为 ;
(4)反应④中所加试剂所属类别是________;
A.酸 B.碱 C.盐 D.氧化物
【答案】(1) HCl
(2)产生刺激性气味气体
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(3)
(4)C
【解析】A是人体胃液中含有的成分,所以A是HCl,B用于改良酸性土壤,所以B是氢氧化钙,盐酸和
氢氧化钙反应生成氯化钙和水,C通电条件下反应生成E和F,D反应能生成白色沉淀,则D为氯化钙,C
是水;G是铁锈的主要成分,故G是氧化铁;铁与水和氧气反应会生成氧化铁,故J是铁,F是氧气,E是
氢气;I是无色气体且M和氢氧化钙反应生成氯化钙、水和I,所以M是氯化铵,I是氨气,带入验证,推
断合理。
(1)由分析可知,G为氧化铁,化学式为Fe O;A为盐酸,化学式为HCl,故填:Fe O;HCl;
2 3 2 3
(2)由分析可知,反应⑤为氢氧化钙与氯化铵反应生成氯化钙、氨气(有刺激性气味)和水,可观察到
的现象是产生刺激性气味气体,故填:产生刺激性气味气体;
(3)反应②为水在通电的条件下生成氢气和氧气,反应的化学方程式为 ,故填:
;
(4)D为氯化钙,D与某物质反应生成白色沉淀,则与D反应的物质可能是可溶性的碳酸盐(如碳酸
钠,碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠)或硝酸银(硝酸银与氯化钙反应生成氯化银白色沉淀
和硝酸钙),均属于盐类,故选C。
13.(8分)有A、B、C、D四种溶液,分别是苛性钠溶液,硫酸镁溶液,稀硝酸,氯化铁溶液中的一
种。观察颜色,发现只有A与其余三种溶液颜色不同。
回答下列问题。
(1)A为 (填化学式),呈 色。
(2)A与B反应现象是 。
(3)写出B与D发生中和反应的化学方程式 。
【答案】(1)FeCl 黄
3
(2)产生红褐色沉淀
(3)
【解析】(1)苛性钠溶液、硫酸镁溶液、稀硝酸均为无色,氯化铁溶液为黄色,则A溶液为氯化铁溶
液,故填:FeCl ;黄;
3
(2)氯化铁与硫酸镁、稀硝酸均不反应,则B为苛性钠溶液(苛性钠是氢氧化钠的俗称),氯化铁与氢
氧化钠反应生成氢氧化铁沉淀和氯化钠,可观察到产生红褐色沉淀,故填:产生红褐色沉淀;
(3)B与D发生中和反应,B为苛性钠溶液(苛性钠是氢氧化钠的俗称),则D为稀硝酸,氢氧化钠与
稀硝酸反应生成硝酸钠和水,反应的化学方程式为 ,故填:
。
14.(14分)碱式碳酸铜Cu (OH)CO 受热分解产生三种氧化物B、C、D(分解过程中所有元素化合
2 2 3
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
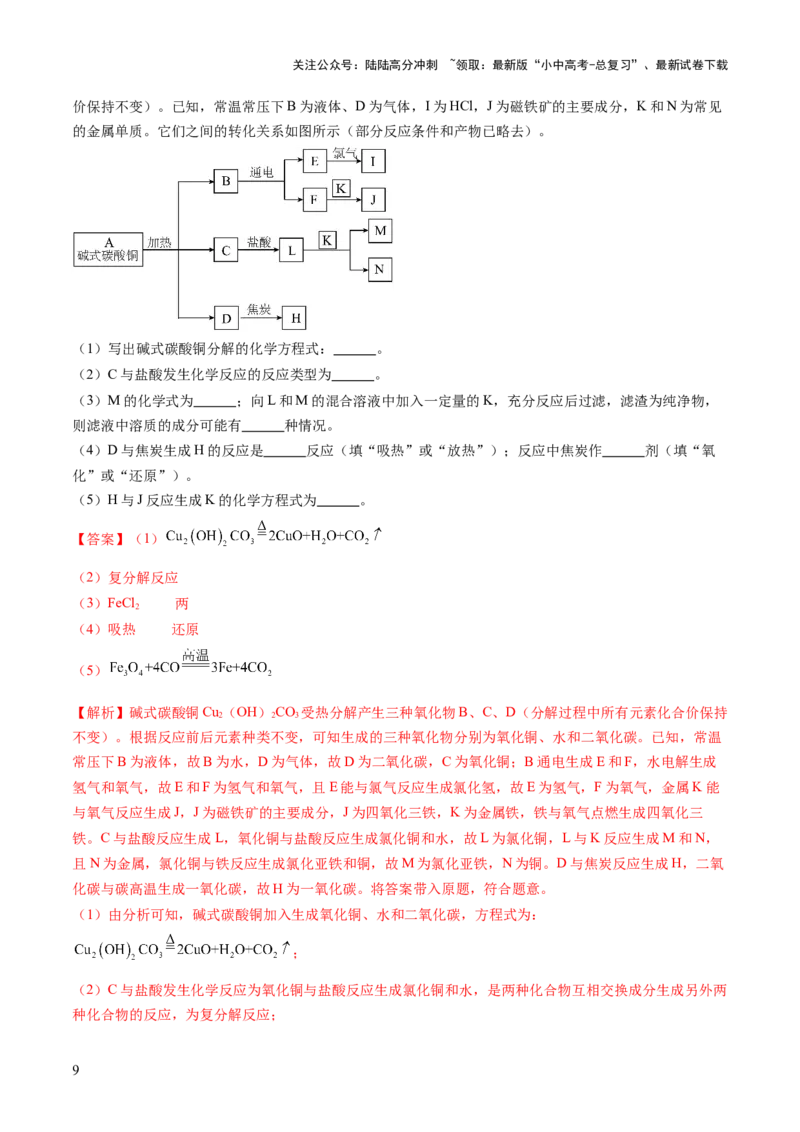
价保持不变)。已知,常温常压下B为液体、D为气体,I为HCl,J为磁铁矿的主要成分,K和N为常见
的金属单质。它们之间的转化关系如图所示(部分反应条件和产物已略去)。
(1)写出碱式碳酸铜分解的化学方程式: 。
(2)C与盐酸发生化学反应的反应类型为 。
(3)M的化学式为 ;向L和M的混合溶液中加入一定量的K,充分反应后过滤,滤渣为纯净物,
则滤液中溶质的成分可能有 种情况。
(4)D与焦炭生成H的反应是 反应(填“吸热”或“放热”);反应中焦炭作 剂(填“氧
化”或“还原”)。
(5)H与J反应生成K的化学方程式为 。
【答案】(1)
(2)复分解反应
(3)FeCl 两
2
(4)吸热 还原
(5)
【解析】碱式碳酸铜Cu (OH)CO 受热分解产生三种氧化物B、C、D(分解过程中所有元素化合价保持
2 2 3
不变)。根据反应前后元素种类不变,可知生成的三种氧化物分别为氧化铜、水和二氧化碳。已知,常温
常压下B为液体,故B为水,D为气体,故D为二氧化碳,C为氧化铜;B通电生成E和F,水电解生成
氢气和氧气,故E和F为氢气和氧气,且E能与氯气反应生成氯化氢,故E为氢气,F为氧气,金属K能
与氧气反应生成J,J为磁铁矿的主要成分,J为四氧化三铁,K为金属铁,铁与氧气点燃生成四氧化三
铁。C与盐酸反应生成L,氧化铜与盐酸反应生成氯化铜和水,故L为氯化铜,L与K反应生成M和N,
且N为金属,氯化铜与铁反应生成氯化亚铁和铜,故M为氯化亚铁,N为铜。D与焦炭反应生成H,二氧
化碳与碳高温生成一氧化碳,故H为一氧化碳。将答案带入原题,符合题意。
(1)由分析可知,碱式碳酸铜加入生成氧化铜、水和二氧化碳,方程式为:
;
(2)C与盐酸发生化学反应为氧化铜与盐酸反应生成氯化铜和水,是两种化合物互相交换成分生成另外两
种化合物的反应,为复分解反应;
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(3)由分析可知M为氯化亚铁,化学式为:FeCl ;
2
向L和M的混合溶液中加入一定量的K,即向氯化铜和氯化亚铁的混合溶液中加入一定量的铁,氯化铜与
铁反应生成铜和氯化亚铁,充分反应后过滤,滤渣为纯净物,则滤渣为铜,说明铁全部被氯化铜完全反应
掉,氯化铜可能过量,也可能与铁恰好完全反应,故滤液中溶质的成分可能为氯化亚铁或氯化铜和氯化亚
铁两种情况;
(4)D与焦炭生成H的反应,即二氧化碳与碳在高温条件下生成一氧化碳,属于吸热反应;
反应中焦炭得到氧,发生了氧化反应,作还原剂;
(5)H与J反应生成K,即一氧化碳在高温的条件下与四氧化三铁反应生成铁和二氧化碳,方程式为:
。
15.(10分)A~H是初中常见的物质。其中,A可用作补钙剂,E、F组成元素相同,H有紫红色金属光
泽。(“—”表示反应关系,“→”表示转化关系,部分反应物、生成物省略)
(1)E的化学式为 ,B的俗称是 。
(2)反应①属于基本反应类型中的 反应。
(3)反应②的化学方程式为 。
(4)反应③ 热量(填“放出”或“吸收”)。
【答案】(1) 生石灰
(2)复分解
(3)
(4)吸收
【解析】A可用作补钙剂,则A为碳酸钙;H有紫红色金属光泽,则H为铜;碳酸钙在高温条件下分解生
成氧化钙和二氧化碳,E、F组成元素相同,二氧化碳与碳在高温条件下反应生成一氧化碳,一氧化碳在氧
气中燃烧生成二氧化碳,则B为氧化钙、E为二氧化碳、F为一氧化碳;一氧化碳与氧化铜在加热条件下
反应生成铜和二氧化碳,则G为氧化铜;氧化钙与水反应生成氢氧化钙,氢氧化钙与二氧化碳反应生成碳
酸钙沉淀和水,则C为氢氧化钙;D能与碳酸钙、氧化铜反应,则D为酸。
(1)由分析可知,E为二氧化碳,其化学式为 ;B为氧化钙,其俗称为生石灰;
(2)由分析可知,D为酸、G为氧化铜,则反应①可以是盐酸与氧化铜反应生成氯化铜和水,该反应符合
两种化合物互相交换成分生成气体、沉淀或水,属于基本反应类型中的复分解反应;
(3)由分析可知,F为一氧化碳、G为氧化铜、H为铜,则反应②为一氧化碳与氧化铜在加热条件下反应
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
生成铜和二氧化碳,化学方程式为 ;
(4)由分析可知,E为二氧化碳、F为一氧化碳,则反应③为二氧化碳与碳在高温条件下反应生成一氧化
碳,该反应吸收热量。
16.(10分)现有一包不纯的NaSO 固体,可能含有NaCO、BaCO 、FeCl 、NH HCO 、NaCl中的一种
2 4 2 3 3 3 4 3
或几种,现做如下实验。
(1)取适量的固体微热,无氨味,则原固体中一定不含 。
(2)另取适量的固体加水溶解,得无色澄清溶液,则原固体中一定不含 。
(3)向步骤(2)所得溶液中加入过量的Ba(NO ) 溶液,过滤得白色固体A和无色滤液B.取固体A,
3 2
加入过量的稀硝酸,部分固体溶解,则原固体中一定含 ,写出部分固体溶解反应的化学方程式:
。
(4)取少量滤液B,滴加AgNO 溶液,产生白色沉淀,则原固体中一定含 。
3
【答案】(1)NH HCO /碳酸氢铵
4 3
(2)碳酸钡、氯化铁(或BaCO 、FeCl )
3 3
(3)硫酸钠、碳酸钠(或NaSO 、NaCO) BaCO +2HNO =Ba(NO )+H O+CO↑
2 4 2 3 3 3 3 2 2 2
(4)NaCl/氯化钠
【解析】(1)取适量的固体微热,无氨味,因为NH HCO 受热分解生成氨气、水和二氧化碳,则原固体
4 3
中一定不含:碳酸氢铵(或NH HCO );
4 3
(2)另取适量的固体加水溶解,得无色澄清溶液,因为BaCO 难溶于水,FeCl 溶液呈黄色,则原固体中
3 3
一定不含:碳酸钡、氯化铁(或BaCO 、FeCl );
3 3
(3)向步骤(2)所得溶液中加入过量的Ba(NO ) 溶液,过滤得白色固体A和无色滤液B.取固体A,
3 2
加入过量的稀硝酸,部分固体溶解,因为NaSO 和Ba(NO ) 反应生成不溶于酸的BaSO 沉淀,NaCO
2 4 3 2 4 2 3
和Ba(NO ) 反应生成溶于酸的BaCO 沉淀,则原固体中一定含:硫酸钠、碳酸钠(或NaSO 、
3 2 3 2 4
NaCO);部分固体溶解的反应是BaCO 和HNO 反应生成硝酸钡、水和二氧化碳,反应的化学方程式
2 3 3 3
为:BaCO +2HNO =Ba(NO )+H O+CO↑。
3 3 3 2 2 2
(4)取少量滤液B,滴加AgNO 溶液,产生白色沉淀,因为NaCl和AgNO 反应生成AgCl沉淀和
3 3
NaNO ,而实验过程中没有引入氯离子,则原固体中一定含:氯化钠(或NaCl)。
3
11