文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
主题二 物质的性质和应用
(试题分值:100分 测试时间:45分钟)
一、选择题(本题包括15小题,每小题3分,共45分.每小题只有一个正确答案)
1.下列关于空气的说法错误的是( )
A.空气中氮气的质量分数为78% B.稀有气体可用于制造电光源
C.氧气能供给生物呼吸 D.植树造林可以改善空气质量
2.下列实验现象描述正确的是( )
A.磷在空气中燃烧产生大量的白雾
B.木炭在空气中燃烧发出淡蓝色火焰
C.镁在氧气中燃烧发出耀眼的白光,生成黑色固体
D.铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体
3.水是生命之源,人类的生活、生产都离不开水。下列说法错误的是( )
A.如图是国家节水标志 B.煮沸可以降低水的硬度
C.长期饮用蒸馏水更有利于人体健康 D.工农业污染和生活污染是水体污染的主要来源
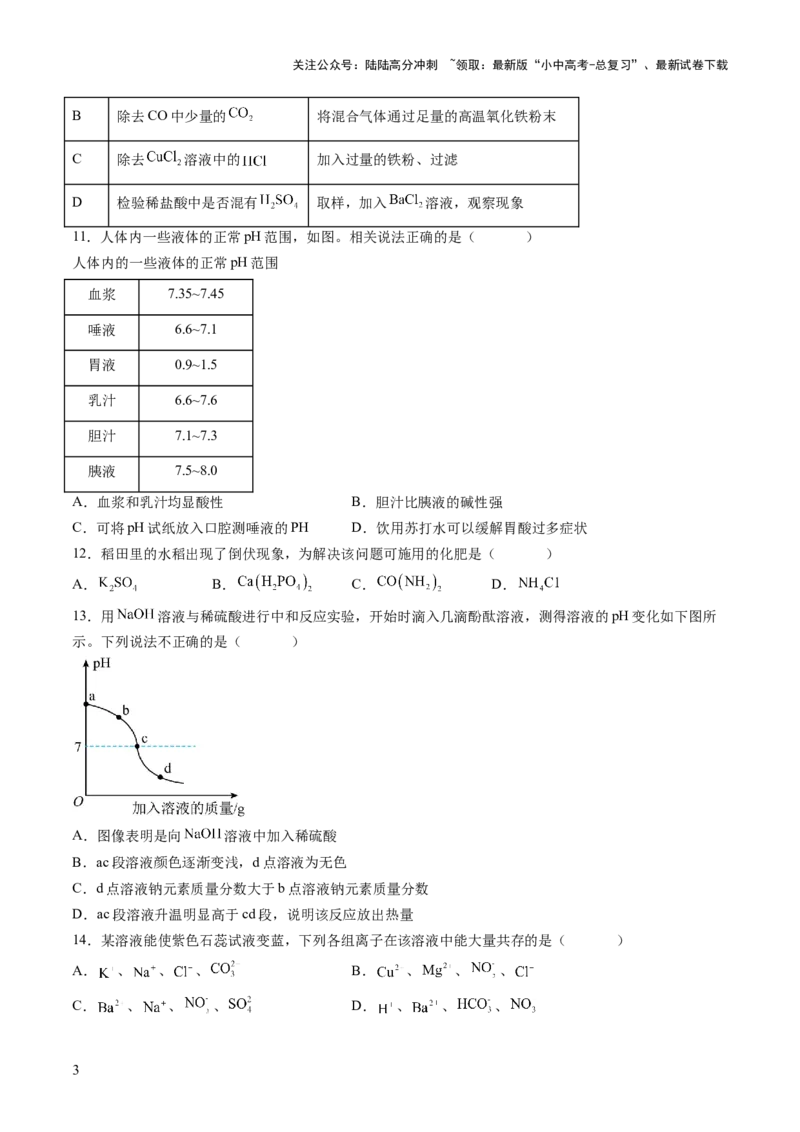
4.利用如图所示装置进行实验,探究水的组成。下列说法错误的是( )
A.玻璃管a中收集到的气体为氢气 B.反应生成氢气和氧气的质量比为
C.实验中电能转化为化学能 D.实验证明水是由氢、氧两种元素组成的
5.下列关于溶液的说法正确的是( )
A.溶液的溶剂一定是水
B.长期放置不会分层的液体一定是溶液
C.溶液是均一的、稳定的混合物
D.海水晒盐得到粗盐后的母液是氯化钠不饱和溶液
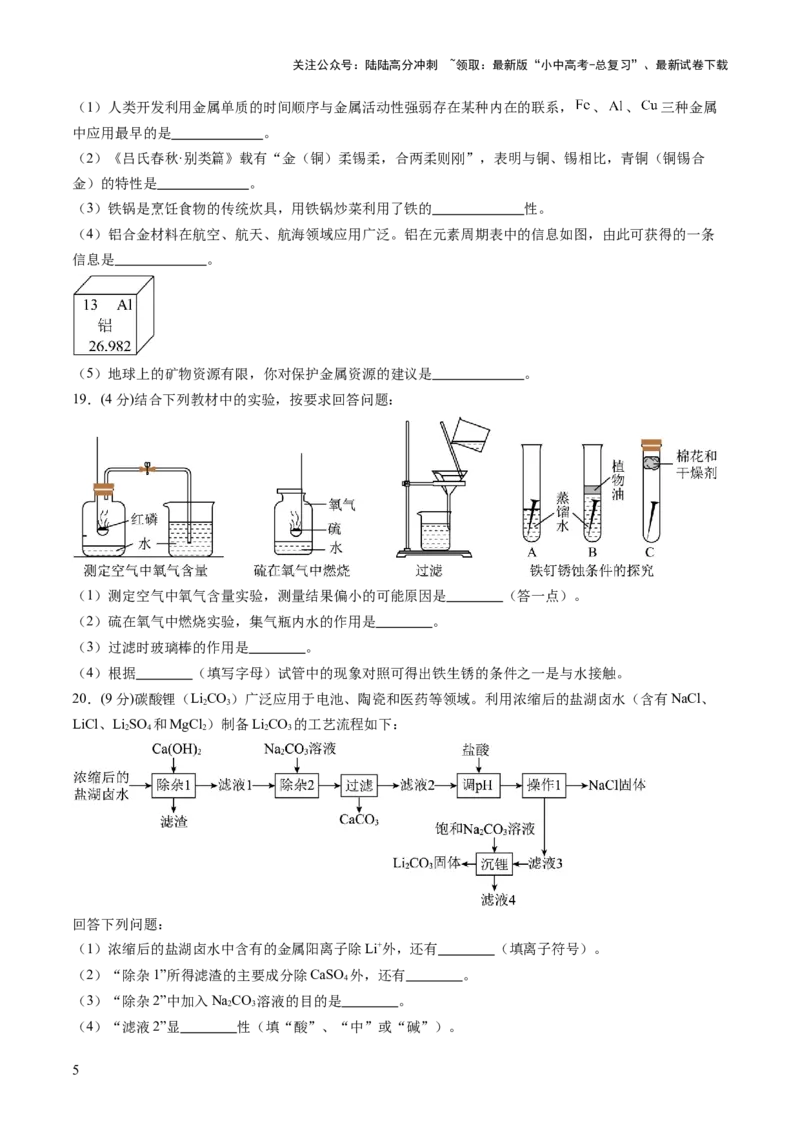
6.如图是甲、乙两种物质在水中的溶解度曲线(不含结晶水),下列说法正确的是( )
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.甲和乙的溶解度相等
B. ℃时,把20g乙加到50g水中,形成饱和溶液
C.若甲中混有少量的乙可采用蒸发结晶的方法提纯甲
D. ℃时甲的饱和溶液降温至 ℃,溶液中溶质的质量分数不变
7.下列关于金属和金属材料的说法中正确的是( )
A.生铁和钢的含碳量不同
B.黄铜比纯铜硬度小
C.合金属于合成材料
D.大多数金属在自然界中以单质形式存在
8.下列关于碳和碳的氧化物说法正确的是( )
A.干冰升华是化学变化
B.活性炭净化水的过程中发生的是物理变化
C.一氧化碳和二氧化碳元素组成相同,所以化学性质相同
D.石墨和金刚石都是由碳元素组成的单质,所以物理性质相同
9.人类开发利用金属的时间和金属的活动性有关。为探究金属的活动性强弱,用如图装置进行实验。下
列说法不正确的是( )
A.实验前需要打磨金属片,除去表面的氧化膜
B.若向甲、乙试管加入稀盐酸,只有锌片表面能产生气泡
C.若向乙试管加入ZnSO 溶液,能得出锌的金属活动性比铜强
4
D.若向甲、乙试管加入AgNO 溶液,能得出三种金属的活动性:Zn>Cu>Ag
3
10.物质的检验、鉴别、除杂是化学研究的重要方法。下列实验方案能达到目的的是( )
选
实验目的 实验方案
项
A 鉴别 和 将燃着的木条分别伸入气体中,观察现象
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
B 除去CO中少量的 将混合气体通过足量的高温氧化铁粉末
C 除去 溶液中的 加入过量的铁粉、过滤
D 检验稀盐酸中是否混有 取样,加入 溶液,观察现象
11.人体内一些液体的正常pH范围,如图。相关说法正确的是( )
人体内的一些液体的正常pH范围
血浆 7.35~7.45
唾液 6.6~7.1
胃液 0.9~1.5
乳汁 6.6~7.6
胆汁 7.1~7.3
胰液 7.5~8.0
A.血浆和乳汁均显酸性 B.胆汁比胰液的碱性强
C.可将pH试纸放入口腔测唾液的PH D.饮用苏打水可以缓解胃酸过多症状
12.稻田里的水稻出现了倒伏现象,为解决该问题可施用的化肥是( )
A. B. C. D.
13.用 溶液与稀硫酸进行中和反应实验,开始时滴入几滴酚酞溶液,测得溶液的pH变化如下图所
示。下列说法不正确的是( )
A.图像表明是向 溶液中加入稀硫酸
B.ac段溶液颜色逐渐变浅,d点溶液为无色
C.d点溶液钠元素质量分数大于b点溶液钠元素质量分数
D.ac段溶液升温明显高于cd段,说明该反应放出热量
14.某溶液能使紫色石蕊试液变蓝,下列各组离子在该溶液中能大量共存的是( )
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
15.下列各组溶液,不用其它试剂就能鉴别出来的是( )
A.CuSO 、NaOH、BaCl 、KCl B.CaCl 、KCO、NaCO、HCl
4 2 2 2 3 2 3
C.MgSO 、NaOH、Ba(NO )、KNO D.AgNO、NaCl、MgCl 、HNO
4 3 2 3 3 2 3
二、填空题(本题5小题,每空1分,化学方程式2分,共30分)
16.(6分)化学在生产、生活中有着广泛应用。现有①氧气②石墨③氖气④干冰⑤氢氧化钙⑥氯化钠,选择
适当的物质填空(填序号)。
(1)可用于人工降雨的是 。
(2)可用作干电池电极的是 。
(3)可用于制造电光源的是 。
(4)可供给人类呼吸的是 。
(5)可用作厨房调味品的是 。
(6)可用于配制波尔多液的是 。
17.(6分)兴趣小组取京杭大运河水样进行净化实验。
(1)设计:运河水中含有泥沙等不溶性杂质以及色素、异味、矿物质、微生物等。
①可以通过 (填操作名称)去除泥沙等不溶性杂质。
②下图为活性炭吸附后的微观图示,活性炭具有 结构,可以吸附色素和异味分子。
(2)净化:将饮用水瓶和纱布、活性炭等组合成如图所示装置进行水的净化。其中,装置制作较合理的
是 (选填“A”或“B”)。通过该装置净化后的水 (选填“适宜”或“不宜”)直接饮
用。
(3)总结:
①混合物分离的一般思路和方法是(将序号排序) 。
a.分析混合物成分 b.找到分离方法 c.寻找成分性质差异
②自制净水器净水材料的选择需要考虑的因素有(写一条) 。
18.(5分)人类的生产、生活离不开金属,金属材料的使用推动着人类文明的进步。
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)人类开发利用金属单质的时间顺序与金属活动性强弱存在某种内在的联系, 、 、 三种金属
中应用最早的是 。
(2)《吕氏春秋·别类篇》载有“金(铜)柔锡柔,合两柔则刚”,表明与铜、锡相比,青铜(铜锡合
金)的特性是 。
(3)铁锅是烹饪食物的传统炊具,用铁锅炒菜利用了铁的 性。
(4)铝合金材料在航空、航天、航海领域应用广泛。铝在元素周期表中的信息如图,由此可获得的一条
信息是 。
(5)地球上的矿物资源有限,你对保护金属资源的建议是 。
19.(4分)结合下列教材中的实验,按要求回答问题:
(1)测定空气中氧气含量实验,测量结果偏小的可能原因是 (答一点)。
(2)硫在氧气中燃烧实验,集气瓶内水的作用是 。
(3)过滤时玻璃棒的作用是 。
(4)根据 (填写字母)试管中的现象对照可得出铁生锈的条件之一是与水接触。
20.(9分)碳酸锂(LiCO)广泛应用于电池、陶瓷和医药等领域。利用浓缩后的盐湖卤水(含有NaCl、
2 3
LiCl、LiSO 和MgCl )制备LiCO 的工艺流程如下:
2 4 2 2 3
回答下列问题:
(1)浓缩后的盐湖卤水中含有的金属阳离子除Li+外,还有 (填离子符号)。
(2)“除杂1”所得滤渣的主要成分除CaSO 外,还有 。
4
(3)“除杂2”中加入NaCO 溶液的目的是 。
2 3
(4)“滤液2”显 性(填“酸”、“中”或“碱”)。
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
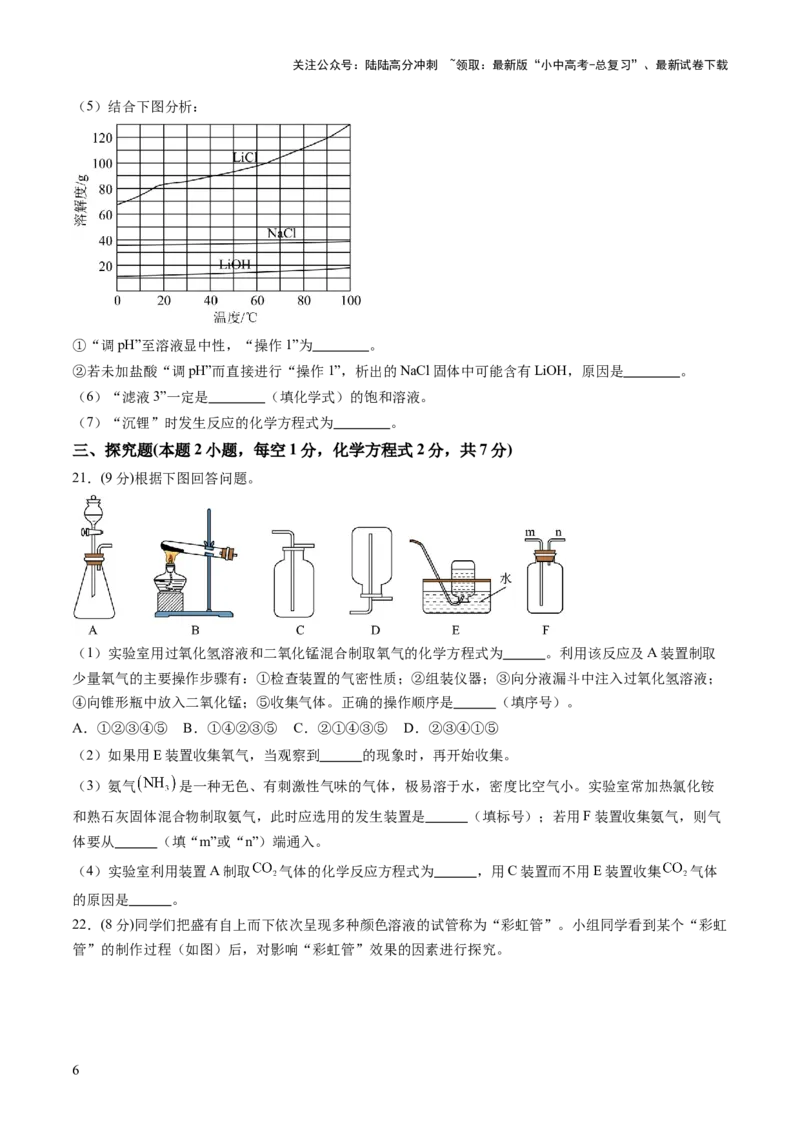
(5)结合下图分析:
①“调pH”至溶液显中性,“操作1”为 。
②若未加盐酸“调pH”而直接进行“操作1”,析出的NaCl固体中可能含有LiOH,原因是 。
(6)“滤液3”一定是 (填化学式)的饱和溶液。
(7)“沉锂”时发生反应的化学方程式为 。
三、探究题(本题2小题,每空1分,化学方程式2分,共7分)
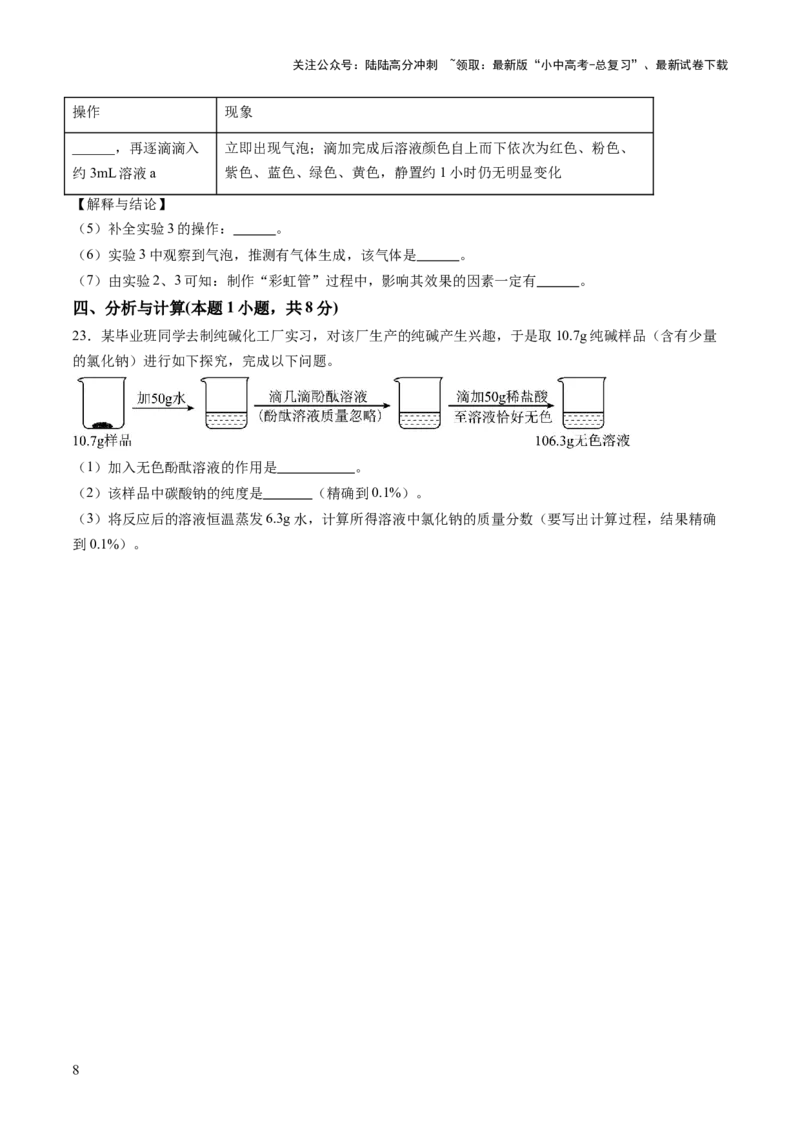
21.(9分)根据下图回答问题。
(1)实验室用过氧化氢溶液和二氧化锰混合制取氧气的化学方程式为 。利用该反应及A装置制取
少量氧气的主要操作步骤有:①检查装置的气密性质;②组装仪器;③向分液漏斗中注入过氧化氢溶液;
④向锥形瓶中放入二氧化锰;⑤收集气体。正确的操作顺序是 (填序号)。
A.①②③④⑤ B.①④②③⑤ C.②①④③⑤ D.②③④①⑤
(2)如果用E装置收集氧气,当观察到 的现象时,再开始收集。
(3)氨气 是一种无色、有刺激性气味的气体,极易溶于水,密度比空气小。实验室常加热氯化铵
和熟石灰固体混合物制取氨气,此时应选用的发生装置是 (填标号);若用F装置收集氨气,则气
体要从 (填“m”或“n”)端通入。
(4)实验室利用装置A制取 气体的化学反应方程式为 ,用C装置而不用E装置收集 气体
的原因是 。
22.(8分)同学们把盛有自上而下依次呈现多种颜色溶液的试管称为“彩虹管”。小组同学看到某个“彩虹
管”的制作过程(如图)后,对影响“彩虹管”效果的因素进行探究。
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
已知:“彩虹管”呈现出的颜色越多、保持时间越长,效果越好。
【进行实验】
实验1:用蒸馏水浸泡黑枸杞得到浸取液,分别滴入pH不同的无色溶液中,记录现象。
pH ≤3 4~5 6~8 9~11 12 ≥13
溶液颜色 红色 粉色 紫色 蓝色 绿色 黄色
实验2:向试管中加入6mL一定质量分数的盐酸、滴入5滴黑枸杞浸取液、振荡,再逐滴滴入约3mL一定
质量分数的NaOH溶液,之后记录溶液颜色。
盐酸中溶质的质量 NaOH溶液中溶质的质
实验 溶液颜色
分数/% 量分数/%
① 5 5 红色
自上而下依次为红色、蓝色、黄色,静置约6
② 5 10
分钟只剩红色、黄色
自上而下依次为红色、蓝色、黄色,静置约20
③ 5 15
分钟仍无明显变化
④ 10 5 自上而下为无色、红色
⑤ 10 10 红色
自上而下依次为红色、蓝色、黄色,静置约6
⑥ 10 15
分钟只剩红色、黄色
【解释与结论】
(1)向pH=7的无色溶液中滴加黑枸杞浸取液,溶液颜色变为 。
(2)盐酸与NaOH反应的化学方程式为 。
(3)实验2中,①②③的目的是 。
(4)实验2中,“彩虹管”效果最佳的是③,理由是 。
【进一步探究】
查阅资料发现,在NaOH溶液中加入一定量 可使“彩虹管”效果更好。小组同学设计实验3进行
验证,并与实验2中③对照。
实验3:向100mL质量分数为15%的NaOH溶液中加入 固体,搅拌后得到溶液a,进行如下实验
并记录。
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
操作 现象
______,再逐滴滴入 立即出现气泡;滴加完成后溶液颜色自上而下依次为红色、粉色、
约3mL溶液a 紫色、蓝色、绿色、黄色,静置约1小时仍无明显变化
【解释与结论】
(5)补全实验3的操作: 。
(6)实验3中观察到气泡,推测有气体生成,该气体是 。
(7)由实验2、3可知:制作“彩虹管”过程中,影响其效果的因素一定有 。
四、分析与计算(本题1小题,共8分)
23.某毕业班同学去制纯碱化工厂实习,对该厂生产的纯碱产生兴趣,于是取10.7g纯碱样品(含有少量
的氯化钠)进行如下探究,完成以下问题。
(1)加入无色酚酞溶液的作用是 。
(2)该样品中碳酸钠的纯度是 (精确到0.1%)。
(3)将反应后的溶液恒温蒸发6.3g水,计算所得溶液中氯化钠的质量分数(要写出计算过程,结果精确
到0.1%)。
8