文档内容
江苏省前黄中学2025届高三上学期期初检测试
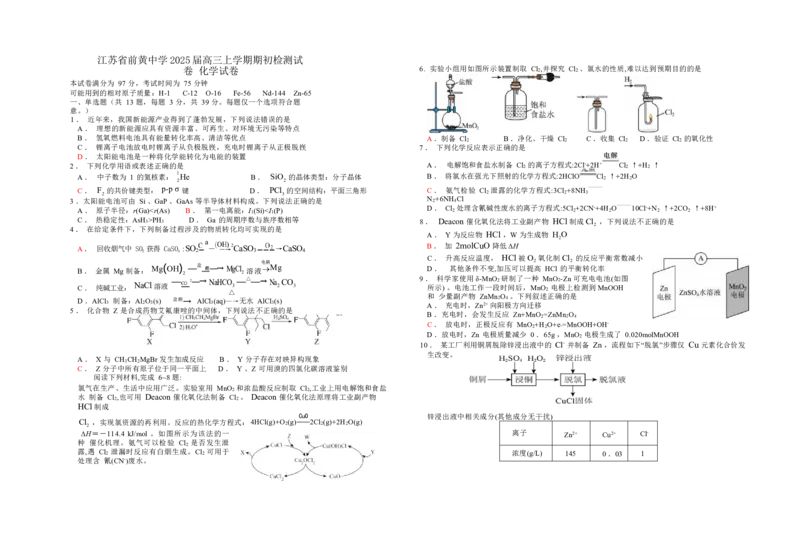
卷 化学试卷 6. 实验小组用如图所示装置制取 Cl ,并探究 Cl 、氯水的性质,难以达到预期目的的是
2 2
本试卷满分为 97 分,考试时间为 75 分钟
可能用到的相对原子质量:H-1 C-12 O-16 Fe-56 Nd-144 Zn-65
一、单选题(共 13 题,每题 3 分,共 39 分。每题仅一个选项符合题
意。)
1 . 近年来,我国新能源产业得到了蓬勃发展,下列说法错误的是
A . 理想的新能源应具有资源丰富、可再生、对环境无污染等特点
B . 氢氧燃料电池具有能量转化率高、清洁等优点 A .制备 Cl B .净化、干燥 Cl C .收集 Cl D .验证 Cl 的氧化性
2 2 2 2
C . 锂离子电池放电时锂离子从负极脱嵌,充电时锂离子从正极脱嵌 7 . 下列化学反应表示正确的是
D . 太阳能电池是一种将化学能转化为电能的装置
2 . 下列化学用语或表述正确的是 A . 电解饱和食盐水制备 Cl 2 的离子方程式:2Cl-+2H+ Cl 2 ↑+H 2 ↑
1
A . 中子数为 1 的氦核素: He B . SiO 的晶体类型:分子晶体 B . 将氯水在强光下照射的化学方程式:2HClO Cl 2 ↑+2H 2 O
2 2 —
C . F 的共价键类型: p-p σ 键 D . PCl 的空间结构:平面三角形 C . 氨气检验 Cl 泄露的化学方程式:3Cl +8NH
2 3 2 2 3
3 .太阳能电池可由 Si 、GaP 、GaAs 等半导体材料构成。下列说法正确的是 N 2 +6NH 4 Cl —
A . 原子半径:r(Ga)PH 3 D . Ga 的周期序数与族序数相等 8 . Deacon 催化氧化法将工业副产物 HCl 制成Cl ,下列说法不正确的是
2
4 . 在给定条件下,下列制备过程涉及的物质转化均可实现的是
A . Y 为反应物 HCl ,W 为生成物 H O
2
a
A . 回收烟气中 SO 2 获得 CaSO 4 :SO 2 ― 2CaSO 3 →CaSO 4 B . 加 2molCuO 降低ΔH
C . 升高反应温度, HCl 被O 氧化制Cl 的反应平衡常数减小
2 2
B . 金属 Mg 制备: Mg(OH) 2 — 盐 —→ MgCl 2 溶液 Mg D . 其他条件不变,加压可以提高 HCl 的平衡转化率
— 2—→ NaHCO —△—→ Na CO 9 . 科学家使用δ-MnO 2 研制了一种 MnO2-Zn 可充电电池(如图
C . 纯碱工业: NaCl 溶液 3 2 3 所示) 。电池工作一段时间后,MnO 2 电极上检测到MnOOH
△
D .AlCl 3 制备:Al 2 O 3 (s) 盐酸 → AlCl 3 (aq)—→无水 AlCl 3 (s) A
和
.
少
充
量
电
副
时
产
,
物
Z n
Z
2
n
+
M
向
n
阳
2O
极 4
。
方
下
向
列
迁
叙
移
述正确的是
5 . 化合物 Z 是合成药物艾氟康唑的中间体,下列说法不正确的是
B .充电时,会发生反应 Zn+MnO =ZnMn O
2 2 4
C . 放电时,正极反应有 MnO +H O+e=MnOOH+OH-
2 2 -
D .放电时,Zn 电极质量减少 0 .65g ,MnO 电极生成了 0.020molMnOOH
2
10 . 某工厂利用铜屑脱除锌浸出液中的 Cl- 并制备 Zn ,流程如下“脱氯”步骤仅 Cu 元素化合价发
生改变。
A . X 与 CH CH MgBr 发生加成反应 B . Y 分子存在对映异构现象
3 2
C . Z 分子中所有原子位于同一平面上 D . Y 、Z 可用溴的四氯化碳溶液鉴别
阅读下列材料,完成 6⁓8 题:
氯气在生产、生活中应用广泛。实验室用 MnO 和浓盐酸反应制取 Cl ,工业上用电解饱和食盐
2 2
水 制备 Cl ,也可用 Deacon 催化氧化法制备 Cl 。 Deacon 催化氧化法原理将工业副产物
2 2
HCl 制成
CuO 锌浸出液中相关成分(其他成分无干扰)
Cl ,实现氯资源的再利用。反应的热化学方程式:4HCl(g)+O (g)══2Cl (g)+2H O(g)
2 2 2 2
ΔH=-114.4 kJ/mol 。如图所示为该法的一 离子 Zn2+ Cu2+ Cl-
种 催化机理。氨气可以检验 Cl 是否发生泄
2
露,遇 Cl 2 泄漏时反应有白烟生成。Cl 2 可用于 浓度(g/L) 145 0 .03 1
处理含 氰(CN-)废水。下列说法正确的是
(H2
A . “浸铜”时应加入足量 H O ,确保铜屑溶解完全 C . 适当增加 n 起始 O ,有利于提高 H 2 的产率
B . “浸铜”反应: 2Cu+4H 2 + + 2 H 2 O 2 = 2Cu2+ +H 2 ↑ +2H 2 O D . 一定温度 n 下 起 , 始 ( 若 C H 增 3 大 OC 压强 3 ) ,CO 的平衡产量不变
C . “脱氯”反应: Cu+Cu2+ +2Cl- = 2CuCl
二、非选择题:共 4 题,共 58 分。
D . 脱氯液净化后电解,可在阳极得到 Zn
11 . 室温下,根据下列实验过程及现象,能验证相应实验结论的是 14 . (14 分)回收磁性合金钕铁硼( Nd Fe B)可制备半导
2 14
体 材料铁酸铋和光学材料氧化钕。
选项 实验过程及现象 实验结论
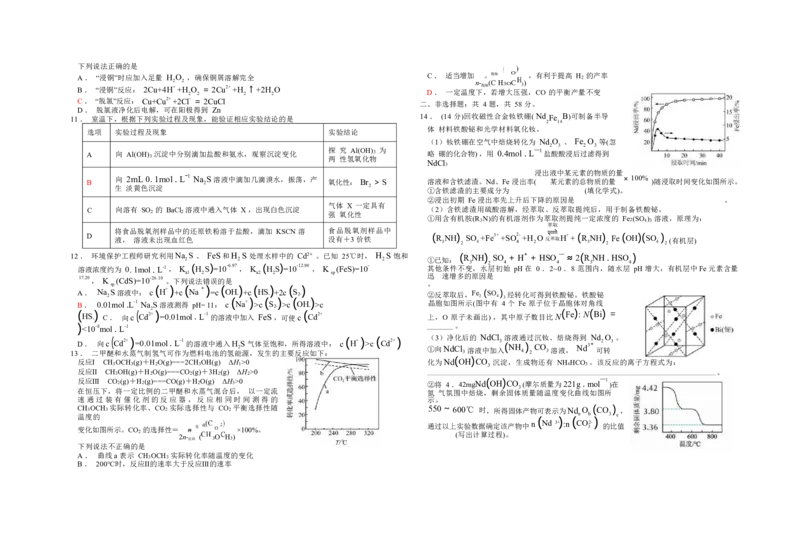
(1)钕铁硼在空气中焙烧转化为 Nd O 、 Fe O 等(忽
2 3 2 3
A 向 Al(OH) 沉淀中分别滴加盐酸和氨水,观察沉淀变化 探 究 Al(OH) 3 为 略 硼的化合物) ,用 0.4mol . L—1 盐酸酸浸后过滤得到
3 两 性氢氧化物
NdCl
3
浸出液中某元素的物质的量
B 向 2mL 0. 1mol . L —1 Na 2 S 溶液中滴加几滴溴水,振荡,产 氧化性: Br > S 溶液和含铁滤渣。Nd、Fe 浸出率( 某元素的总物质的量 × 1 0 0 % )随浸取时间变化如图所示。
生 淡黄色沉淀 2
①含铁滤渣的主要成分为 (填化学式)。
②浸出初期 Fe 浸出率先上升后下降的原因是 。
气体 X 一定具有
C 向溶有 SO 的 BaCl 溶液中通入气体 X ,出现白色沉淀 (2)含铁滤渣用硫酸溶解,经萃取、反萃取提纯后,用于制备铁酸铋。
2 2 强 氧化性
①用含有机胺(R
3
N)的有机溶剂作为萃取剂提纯一定浓度的 Fe2(SO
4
)
3
溶液,原理为:
将食品脱氧剂样品中的还原铁粉溶于盐酸,滴加 KSCN 溶 食品脱氧剂样品中
D 液, 溶液未出现血红色 没有+3 价铁 (R 3 NH) 2 SO 4 +Fe3+ +SO 2 4 - +H 2 O H+ + (R 3 NH) 2 Fe (OH)(SO 4 ) 2 (有机层)
12 . 环境保护工程师研究利用Na 2 S 、 FeS和H 2 S 处理水样中的 Cd2+ 。已知 25℃时, H 2 S 饱和 ①已知: (R NH) SO + H+ + HSO — ≈ 2(R NH . HSO )
3 2 4 4 3 4
溶液浓度约为 0. 1mol . L-1 , K (H S)=10-6.97 , K (H S)=10-12.90 , K (FeS)=10- 其他条件不变,水层初始 pH 在 0 .2~0 .8 范围内,随水层 pH 增大,有机层中Fe 元素含量
a1 2 a2 2 sp
迅 速增多的原因是
17.20 , K (CdS)=10-26.10 。下列说法错误的是
sp 。
A . Na 2 S 溶液中: c ( H+ ) +c ( Na + ) =c ( OH - ) +c ( HS - ) +2c ( S 2- ) ②反萃取后,Fe 2 (SO 4 ) 3 经转化可得到铁酸铋。铁酸铋
B . 0.01mol .L-1 Na 2 S 溶液测得 pH= 11: c ( Na+ ) >c ( S 2- ) >c ( OH - ) >c 晶胞如图所示(图中有 4 个 Fe 原子位于晶胞体对角线
( HS - ) C . 向c ( Cd2+ ) =0.01mol . L-1 的溶液中加入 FeS ,可使c ( Cd2+ 上,O 原子未画出) ,其中原子数目比N (Fe): N(Bi) =
) <10-8mol . L-1 _______。
(3)净化后的 NdCl 溶液通过沉钕、焙烧得到 Nd O 。
13 D . . 二 向 甲 c 醚 ( C 和 d 水 2+ 蒸 ) = 气 0. 制 01 氢 m 气 ol 可 . 作 L-1 为 的 燃 溶 料 液 电 中 池 通 的 入 氢 H 能 2 S 源 气 , 体 发 至 生 饱 的 和 主 , 要 所 反 得 应 溶 如 液 下 中 : : c ( H+ ) >c ( Cd2+ ) ①向NdCl 3 溶液中加入 3 (NH 4 ) 2 CO 3 溶液, Nd3+ 可 2 转 3
反应Ⅰ CH 3 OCH 3 (g)+H 2 O(g)===2CH 3 OH(g) ΔH 1 >0 化为Nd(OH)CO 3 沉淀,生成物还有 NH 4 HCO 3 。该反应的离子方程式为:
反应Ⅱ CH OH(g)+H O(g)===CO (g)+3H (g) ΔH >0 。
3 2 2 2 2
反应Ⅲ CO 2 (g)+H 2 (g)===CO(g)+H 2 O(g) ΔH 3 >0 ②将 4 .42mgNd(OH)CO (摩尔质量为221g . mol —1 )在
3
在恒压下,将一定比例的二甲醚和水蒸气混合后, 以一定流 氮 气氛围中焙烧,剩余固体质量随温度变化曲线如图所
速通过装有催化剂的反应器,反应相同时间测得的 示。
CH 3 OCH 3 实际转化率、CO 2 实际选择性与 CO 2 平衡选择性随 550 ~ 600℃ 时,所得固体产物可表示为Nd O (CO ) ,
温度的 a b 3 c
( ) ( )
n Nd 3 + : n C O 2-
变化如图所示。CO 的选择性= n 生 O ×100%。 通过以上实验数据确定该产物中 3 的比值
2
2n ( O H )
(写出计算过程)。
反应 3 3
下列说法不正确的是
A . 曲线a 表示 CH OCH 实际转化率随温度的变化
3 3
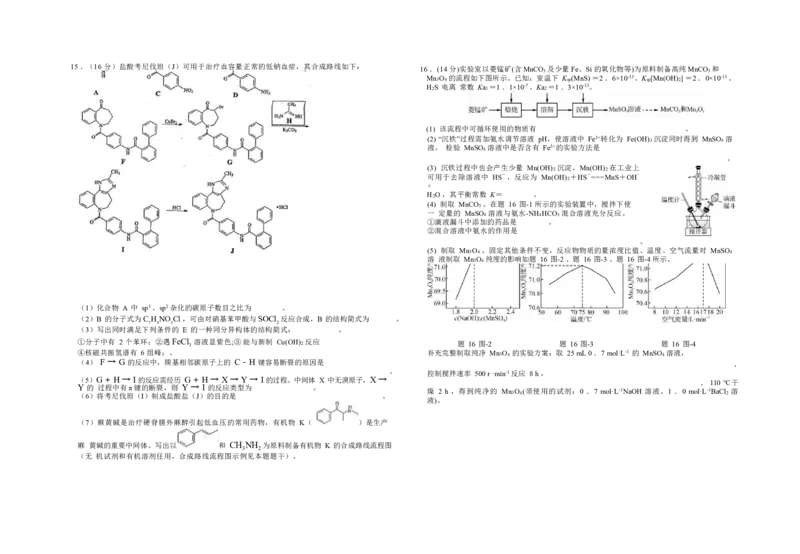
B . 200℃时,反应Ⅱ的速率大于反应Ⅲ的速率15 .(16 分)盐酸考尼伐坦(J)可用于治疗血容量正常的低钠血症,其合成路线如下: 16 .(14 分)实验室以菱锰矿(含MnCO 及少量Fe、Si 的氧化物等)为原料制备高纯MnCO 和
3 3
Mn3O
4
的流程如下图所示。已知:室温下 K
sp
(MnS) =2 .6×10-13、K
sp
[Mn(OH)
2
] =2 .0×10-13 、
H
2
S 电离 常数 Ka1 =1 .1×10-7 、Ka2 =1 .3×10-13。
(1) 该流程中可循环使用的物质有 。
(2) “沉铁”过程需加氨水调节溶液 pH,使溶液中 Fe3+转化为 Fe(OH) 沉淀同时得到 MnSO 溶
3 4
液。 检验 MnSO 溶液中是否含有 Fe3+的实验方法是
4
。
(3) 沉铁过程中也会产生少量 Mn(OH) 沉淀。Mn(OH) 在工业上
2 2
可用于去除溶液中 HS- ,反应为 Mn(OH) +HS-===MnS+OH-
2
+
H O ,其平衡常数 K= 。
2
(4) 制取 MnCO 。在题 16 图-1 所示的实验装置中,搅拌下使
3
一 定量的 MnSO 溶液与氨水-NH HCO 混合溶液充分反应。
4 4 3
①滴液漏斗中添加的药品是 。
②混合溶液中氨水的作用是
。
(5) 制取 Mn3O
4
。固定其他条件不变,反应物物质的量浓度比值、温度、空气流量对 MnSO
4
溶 液制取 Mn3O
4
纯度的影响如题 16 图-2 、题 16 图-3 、题 16 图-4 所示。
(1)化合物 A 中 sp3 、sp2 杂化的碳原子数目之比为 。
(2)B 的分子式为C H NO Cl ,可由对硝基苯甲酸与SOCl 反应合成,B 的结构简式为 。
7 4 3 2
(3)写出同时满足下列条件的 E 的一种同分异构体的结构简式: 。
①分子中有 2 个苯环;②遇FeCl 3 溶液显紫色;③能与新制 Cu(OH) 2 反应 题 16 图-2 题 16 图-3 题 16 图-4
④核磁共振氢谱有 6 组峰;。 补充完整制取纯净 Mn3O
4
的实验方案:取 25 mL 0 .7 mol·L-1 的 MnSO
4
溶液,
(4) F → G 的反应中,羰基相邻碳原子上的 C - H 键容易断裂的原因是 ,
。
控制搅拌速率 500 r ·min-1 反应 8 h ,
(5)G + H → I 的反应需经历 G + H → X → Y → I 的过程。中间体 X 中无溴原子,X → , 110 ℃干
Y 的 过程中有π键的断裂,则 Y → I 的反应类型为 。
(6)将考尼伐坦(I)制成盐酸盐(J)的目的是 。
燥 2 h ,得到纯净的 Mn3O
4
(须使用的试剂:0 .7 mol·L-1NaOH 溶液、1 .0 mol·L-1BaCl
2
溶
液)。
(7)麻黄碱是治疗硬脊膜外麻醉引起低血压的常用药物,有机物 K( )是生产
麻 黄碱的重要中间体。写出以 和 CH NH 为原料制备有机物 K 的合成路线流程图
3 2
(无 机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。17 . (14 分)甲醛释氢对氢能源和含甲醛污水处理有重要意义。
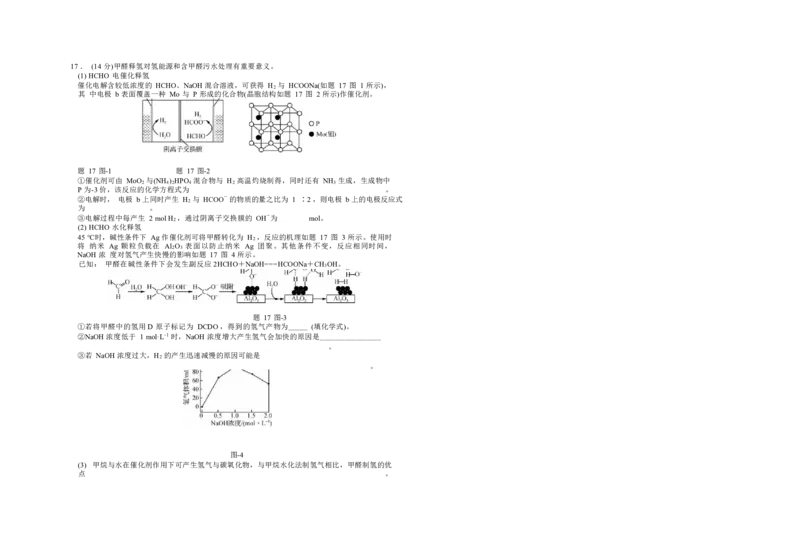
(1) HCHO 电催化释氢
催化电解含较低浓度的 HCHO、NaOH 混合溶液,可获得 H 与 HCOONa(如题 17 图 1 所示),
2
其 中电极 b 表面覆盖一种 Mo 与 P 形成的化合物(晶胞结构如题 17 图 2 所示)作催化剂。
题 17 图-1 题 17 图-2
①催化剂可由 MoO 与(NH ) HPO 混合物与 H 高温灼烧制得,同时还有 NH 生成,生成物中
2 4 2 4 2 3
P 为-3价,该反应的化学方程式为 。
②电解时, 电极 b 上同时产生 H 与 HCOO- 的物质的量之比为 1 ∶2 ,则电极 b 上的电极反应式
2
为 。
③电解过程中每产生 2 mol H ,通过阴离子交换膜的 OH-为 mol。
2
(2) HCHO 水化释氢
45 ℃时,碱性条件下 Ag 作催化剂可将甲醛转化为 H ,反应的机理如题 17 图 3 所示。使用时
2
将 纳米 Ag 颗粒负载在 Al O 表面以防止纳米 Ag 团聚。其他条件不变,反应相同时间,
2 3
NaOH 浓 度对氢气产生快慢的影响如题 17 图 4 所示。
已知: 甲醛在碱性条件下会发生副反应2HCHO+NaOH===HCOONa+CH OH。
3
题 17 图-3
①若将甲醛中的氢用D 原子标记为 DCDO ,得到的氢气产物为______ (填化学式)。
②NaOH 浓度低于 1 mol·L-1 时,NaOH 浓度增大产生氢气会加快的原因是_________________
。
③若 NaOH 浓度过大,H 的产生迅速减慢的原因可能是
2
。
图-4
(3) 甲烷与水在催化剂作用下可产生氢气与碳氧化物,与甲烷水化法制氢气相比,甲醛制氢的优
点 。