文档内容
(10)化学反应速率与化学平衡—高二化学人教版暑假作业本
1.工业上用 和 合成甲醇涉及以下反应:
Ⅰ.
Ⅱ.
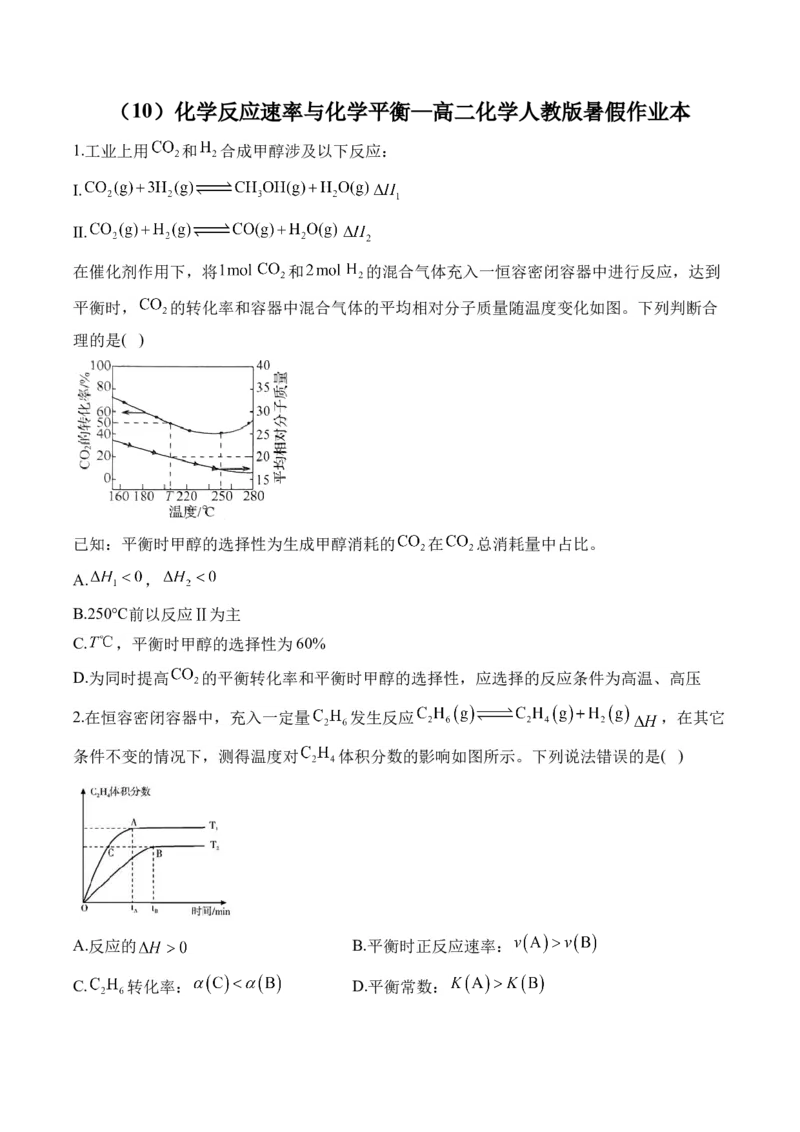
在催化剂作用下,将 和 的混合气体充入一恒容密闭容器中进行反应,达到
平衡时, 的转化率和容器中混合气体的平均相对分子质量随温度变化如图。下列判断合
理的是( )
已知:平衡时甲醇的选择性为生成甲醇消耗的 在 总消耗量中占比。
A. ,
B.250℃前以反应Ⅱ为主
C. ,平衡时甲醇的选择性为60%
D.为同时提高 的平衡转化率和平衡时甲醇的选择性,应选择的反应条件为高温、高压
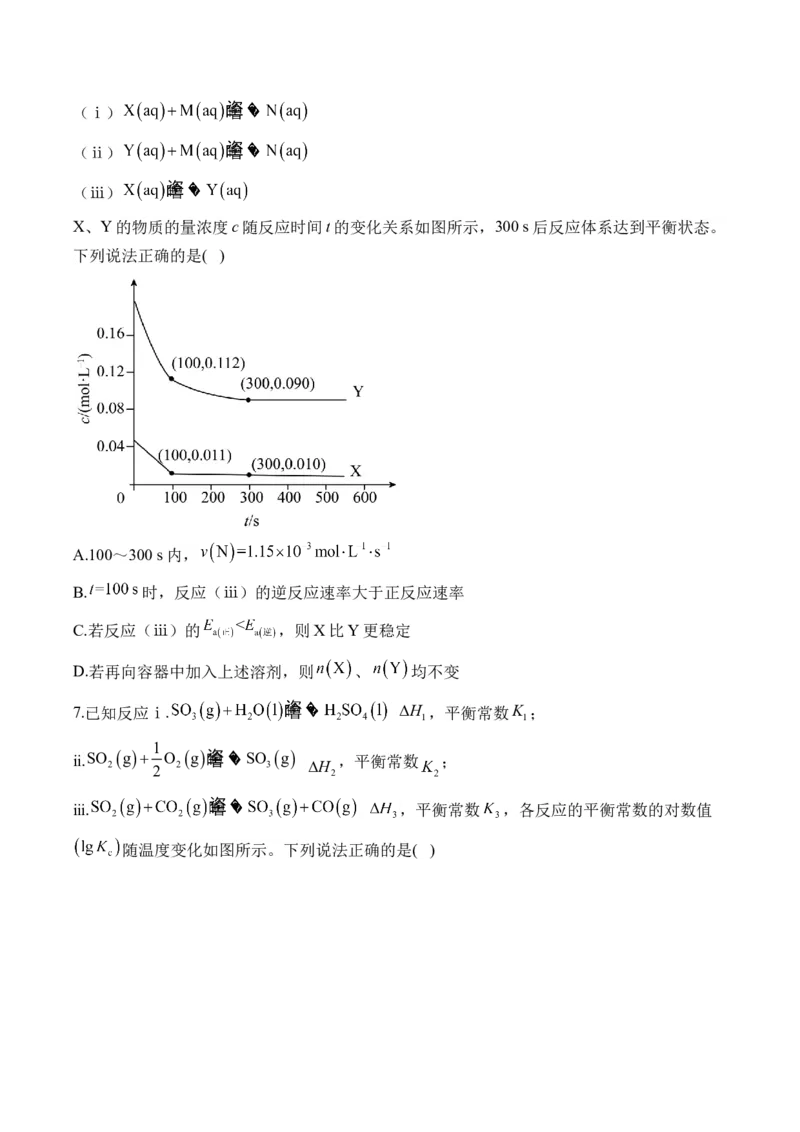
2.在恒容密闭容器中,充入一定量 发生反应 ,在其它
条件不变的情况下,测得温度对 体积分数的影响如图所示。下列说法错误的是( )
A.反应的 B.平衡时正反应速率:
C. 转化率: D.平衡常数:3.在恒温恒容密闭容器中充入一定量 ,发生如下反应:
反应②和③的速率方程分别为 和 ,其中 分别为反应②和③的速率
常数,反应③的活化能大于反应②。测得 的浓度随时间的变化如下表。
0 1 2 3 4 5
0.160 0.113 0.080 0.056 0.040 0.028
下列说法正确的是( )
A. 内,X的平均反应速率为
B.若增大容器容积,平衡时Y的产率增大
C.若 ,平衡时
D.若升高温度,平衡时 减小
4.反应 在一定温度下达到平衡。下列各种情况下,不能使平
衡发生移动的是( )
①温度、容积不变时,通入 气体
②移走一部分 固体
③容积不变,充入氮气
④充入氮气,保持压强不变
A.①②④ B.①③ C.①②③ D.②③
5.在密闭容器中进行反应: ,其中 、Z的起始浓度分别为0.1
、0.3 、0.2 ,在一定条件下,当反应达到平衡时,各物质的浓度有可
能是( )
A. B.
C. D.
6.常温下,向某溶剂(不参与反应)中加入一定量X、Y和M,所得溶液中同时存在如下平
衡:(ⅰ)
(ⅱ)
(ⅲ)
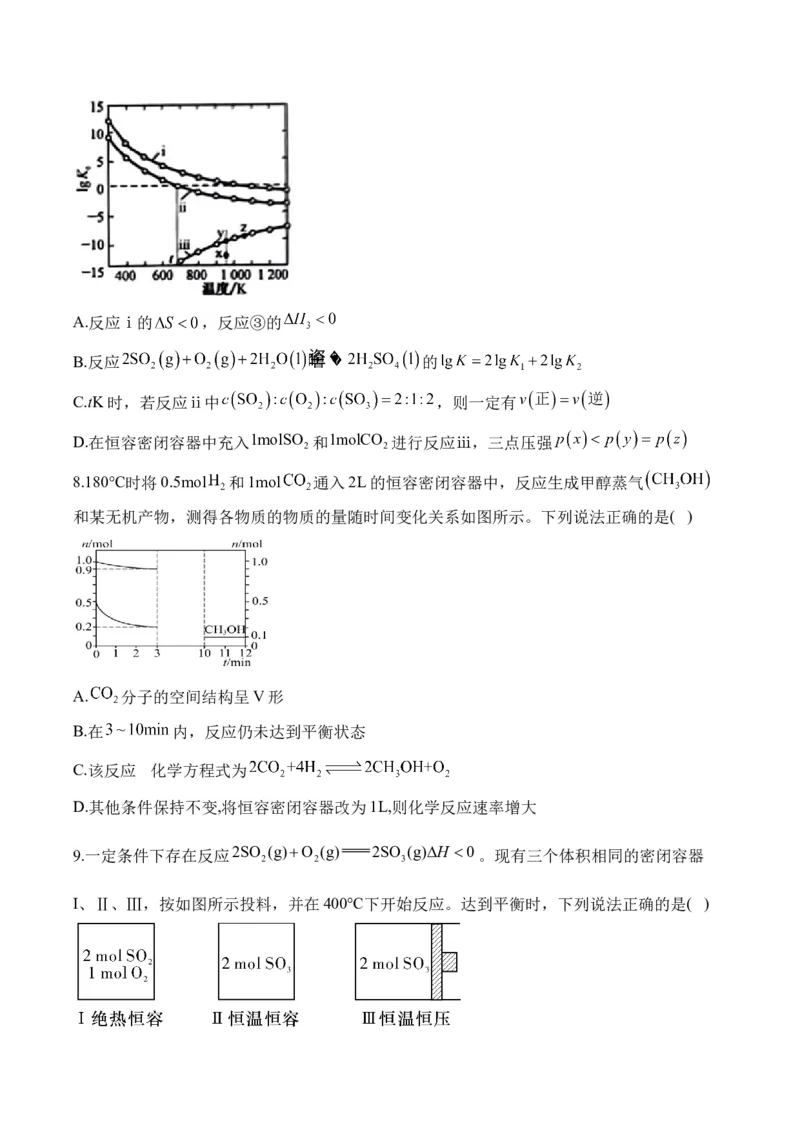
X、Y的物质的量浓度c随反应时间t的变化关系如图所示,300 s后反应体系达到平衡状态。
下列说法正确的是( )
A.100~300 s内,
B. 时,反应(ⅲ)的逆反应速率大于正反应速率
C.若反应(ⅲ)的 ,则X比Y更稳定
D.若再向容器中加入上述溶剂,则 、 均不变
7.已知反应ⅰ. H ,平衡常数K ;
1 1
1
ⅱ.SO g O g 噲垐 �� SO g ,平衡常数 ;
2 2 2 3 H
2
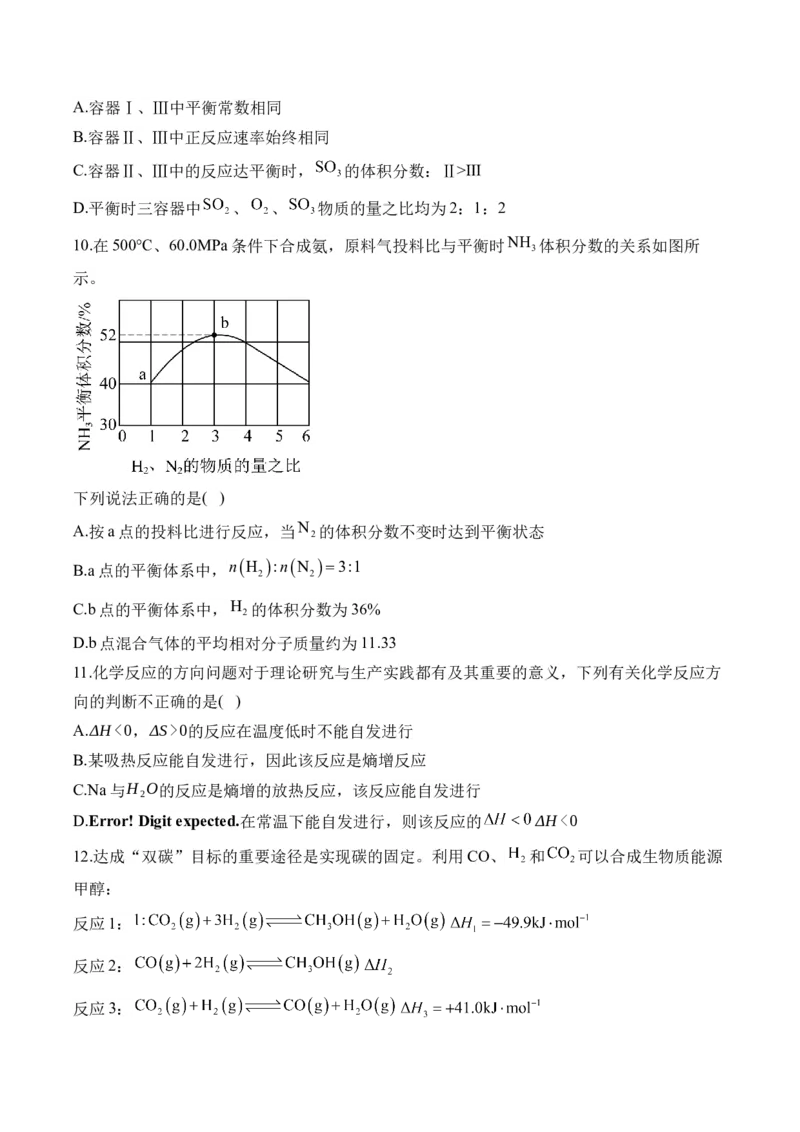
ⅲ. ,平衡常数 ,各反应的平衡常数的对数值
随温度变化如图所示。下列说法正确的是( )A.反应ⅰ的 ,反应③的
B.反应 的
C.tK时,若反应ⅱ中
,则一定有v正v逆
D.在恒容密闭容器中充入1molSO 和1molCO 进行反应ⅲ,三点压强
2 2
8.180℃时将0.5mol 和1mol 通入2L的恒容密闭容器中,反应生成甲醇蒸气
和某无机产物,测得各物质的物质的量随时间变化关系如图所示。下列说法正确的是( )
A. 分子的空间结构呈V形
B.在 内,反应仍未达到平衡状态
C.该反应 化学方程式为
的
D.其他条件保持不变,将恒容密闭容器改为1L,则化学反应速率增大
9.一定条件下存在反应2SO (g)O (g) 2SO (g)H 0。现有三个体积相同的密闭容器
2 2 3
I、Ⅱ、Ⅲ,按如图所示投料,并在400℃下开始反应。达到平衡时,下列说法正确的是( )A.容器Ⅰ、Ⅲ中平衡常数相同
B.容器Ⅱ、Ⅲ中正反应速率始终相同
C.容器Ⅱ、Ⅲ中的反应达平衡时, 的体积分数:Ⅱ>Ⅲ
D.平衡时三容器中 、 、 物质的量之比均为2:1:2
10.在500℃、60.0MPa条件下合成氨,原料气投料比与平衡时NH 体积分数的关系如图所
3
示。
下列说法正确的是( )
A.按a点的投料比进行反应,当N 的体积分数不变时达到平衡状态
2
B.a点的平衡体系中,nH :nN 3:1
2 2
C.b点的平衡体系中,H 的体积分数为36%
2
D.b点混合气体的平均相对分子质量约为11.33
11.化学反应的方向问题对于理论研究与生产实践都有及其重要的意义,下列有关化学反应方
向的判断不正确的是( )
A.ΔH<0,ΔS>0的反应在温度低时不能自发进行
B.某吸热反应能自发进行,因此该反应是熵增反应
C.Na与H O的反应是熵增的放热反应,该反应能自发进行
2
D.Error! Digit expected.在常温下能自发进行,则该反应的 ΔH<0
12.达成“双碳”目标的重要途径是实现碳的固定。利用CO、 和 可以合成生物质能源
甲醇:
反应1:
反应2:
反应3:回答下列问题:
(1)反应1在_______(填“较高温度”“较低温度”或“任何温度”)下能自发进行。
(2) _______ 。
(3)T℃时,向一恒容密闭容器中仅充入1molCO(g)和 ,仅发生反应2。下列
叙述错误的是___________(填标号)。
A.加入催化剂,反应速率增大
B.CO体积分数不变时,反应达到平衡状态
C.平衡后,充入氩气,平衡正向移动
D.平衡后,充入 ,CO平衡转化率增大
(4)在某催化剂作用下,反应2的历程如图所示(图中数据表示微粒的相对能量,*表示吸
附在催化剂表面上)。
控速反应方程式为_______。
(5)在某催化剂作用下,只发生反应: 。该反应的速
率方程式为 , (k为速率常数,只与温度、催化
剂有关)。830℃时该反应的平衡常数K=1,达到平衡后, _______(填“>”“<”或“=”,
下同) ,900℃时 _______ 。
(6) 时,在密闭容器甲、乙中,分别充入 和 ,它们分别在有水分子筛
(只允许水分子透过)和无水分子筛条件下仅发生反应1.测得 平衡转化率与压强关系如
图所示。①使用了水分子筛的容器是______(填“甲”或“乙”)。
②平衡常数 ______(填“>”“<”或“=”) ,M点 ______kPa。
(7) 时,向一体积为1L的恒容密闭容器中充入1molCO、 和 ,在一定
条件下发生上述3个反应,达到平衡时得到 和 ,此时 平衡转化
率为50%。该温度下,反应1的平衡常数K=______ 。(列出计算式)
答案以及解析
1.答案:C
2.答案:C
解析:A.根据“先拐线平衡数值大”,则 温度高,从 到 ,升高温度,乙烯体积分数增
大,说明平衡正向移动,则反应的 ,故A正确;
B. 温度高,则速率大,因此平衡时正反应速率: ,故B正确;
C.B、C两点乙烯体积分数相同,则乙烷消耗量相同,则 转化率相等,故C错误;
D.从 到 ,升高温度,乙烯体积分数增大,说明平衡正向移动,则平衡常数增大,即平衡
常数: ,故D正确;
综上所述,答案为C。
3.答案:D
解析:A.由表知0~2min内 ,生成
,但一部分X转化为Z,造成 ,则,故A错误;
B.过程①是完全反应,过程②是可逆反应,若增大容器容积相当于减小压强,对反应
平衡向气体体积增大的方向移动,即逆向移动,X的浓度增大,平衡时Y的
产率减小,故B错误;
C.由速率之比等于系数比,平衡时 ,即 ,若
,平衡时 ,故C错误;
D.反应③的活化能大于反应②, 正反应活化能-逆反应活化能<0,则
,该反应是放热反应,升高温度,平衡逆向移动,则平衡时 减
小,故D正确;
故选D。
4.答案:D
解析:①温度、容积不变时,通入 气体,与硫化氢反应生成S,硫化氢的浓度降低,平
衡向正反应方向移动,故①不符合;② 为固体,改变 固体的用量,不影响平
衡移动,故②符合;③容积不变,充入氮气,反应气体混合物各组分的浓度不变,平衡不移
动,故③符合;④充入氮气,保持压强不变,体积增大,反应气体混合物各组分的浓度降
低,压强降低,平衡向正反应方向移动,故④不符合;故选D。
5.答案:B
解析:若反应正向进行,假定完全反应,则
若反应逆向进行,假定完全反应,则
由于为可逆反应,物质不能完全转化,所以平衡时浓度范围为 、
、 ,综上分析只有B项正确。6.答案:B
解析:A.由图可知,100~300s内,生成物N的浓度变化量为(0.112—0.090)mol/L+(0.011
—0.010)mol/L=0.023mol/L,则n的反应速率为 ,故A错
误;
B.由图可知,300s时反应达到平衡,反应(ⅲ)的平衡常数 ,100s时反
应(ⅲ)的浓度熵 ,则反应向逆反应方向进行,逆反应速率大于正反应
速率,故B正确;
C.若反应(ⅲ)的 ,则该反应为反应物总能量大于生成物总能量的放热反应,X
的能量高于Y的能量,物质的能量越低越稳定,则Y比X更稳定,故C错误;
D.若再向容器中加入上述溶剂,平衡体系中各物质浓度均减小,反应(ⅰ)、(ⅱ)均向逆
反应方向移动,X、Y的物质的量均增大,故D错误;
故选B。
7.答案:B
解析:ⅰ的气体分子数减少, ,ⅲ的平衡常数随温度升高而增大, ,A项错
误;反应 为 ,K K2K2,B项正确;
1 2
设 , ,无法确定Q与 关系,C项错误;气体总物质的量
不变,压强只与温度有关, ,D项错误。
8.答案:D
9.答案:C
解析:A.A装置向正反应方向进行, ,III装置向逆反应方向
进行, ,因此两者的平衡常数不同,故错误;B.II是恒温恒
容状态,反应向逆反应方向进行,气体物质的量增大,压强增大,化学反应速率增大,III是
恒压状态,即II的压强大于III,II的化学反应速率大于III的,故错误;C.II是恒温恒容状
态,反应向逆反应方向进行,气体物质的量增大,压强增大,化学反应速率增大,达到平衡
所用的时间短,消耗的 的量小于III,因此 的体积分数:II>III,故正确;D.平衡时各
物质的浓度保持不变,但物质的量之比并不一定满足化学计量数之比,故错误。故选:C。10.答案:C
3H (g)N (g)2NH (g)
2 2 3
起始(mol) 1 1 0
解析:A.a点氢气和氮气为1:1投科,则:
转化(mol) 3a a 2a
平衡(mol) 1a 1a 2a
则总的物质的量为 , 伯体积分数为 ,为定值,故 的体积分数
N N
2 2
不变时,不能说明正逆反应速率相等,不能判断反应达到平衡状态,A错误;
B.a点氢气和氡气为1:1投料,平信时氨气体积分数为40%,则:
3H (g)N (g)2NH (g)
2 2 3
起始(mol) 1 1 0
转化(mol) 3a a 2a
平衡(mol) 1a 1a 2a
2a 2 1 5
则总的物质的量为22a, 0.4,a ,则nH :nN : 1:5,B错误;
22a 7 2 2 7 7
C.b点氢气和氮气为3:1投料,平德时氨气体积分数为52%,则:
3H (g)N (g)2NH (g)
2 2 3
起始(mol) 3 1 0
转化(mol) 3b b 2b
平衡(mol) 33 1b 2b
2b
则总的物质的量为 , 0.52, , 的体积分数为
42b 42b H
2
,C正确;
D.由C分析可知,b点混合气体的平均相对分子质量约为
3mol2g/mol1mol28g/mol
12.9g/mol11.33
,D错误。
(420.68)mol
11.答案:A
解析:A. 的反应在任何温度下都满足H TS 0,即任何温度下该反应均
能自发进行,故A错误;
B. 的反应可自发进行,则某吸热反应(H 0)能自发进行,因此该反应是熵增
反应,故B正确;C.Na和H O反应生成氢氧化钠和氢气,该反应放热并且生成气体混乱(或无序)程度变大,所
2
以 ,任何温度下H TS 0,该反应能自发进行,故C正确;
D.由化学计量数可知 ,在常温下能自发进行,则该反应的H 0,故D正确;
故选:A。
12.答案:(1)较低温度
(2)
(3)C
3
(4)CO*2H (g) HCO* H (g)
2 2 2
(5)=;>
(6)乙;=;75
(7)
解析:(1)反应1的S 0、H 0,在较低温度下能自发进行。
(2)由盖斯定律可知,反应1-反应3可得反应2,则
。
(3)A.催化剂能加快反应速率,加入催化剂,反应速率增大,故A正确;
B.CO体积分数不变时,说明正逆反应速率相等,反应达到平衡状态,故B正确;
C.恒容密闭容器中,平衡后,充入氩气,反应物和生成物的浓度不变,平衡不发生移动,故
C错误;
D.平衡后,充入H ,平衡正向移动,CO平衡转化率增大,故D正确;
2
故选C。
(4)由图可知, 的活化能最大,反应速率最慢,为控速反
应。
k cCOcH O
(5)达到平衡后, = , 正 = 2 K
v k cCO cH k cCO cH
正 正 2 2 逆 2 2
=1, =k ,该反应为吸热反应,升高温度,平衡常数增大,900℃时,
逆>1, > 。
(6)①使用了水分子隔离膜的反应器可以去除生成物 ,平衡正向移动, 平衡转化
率高,所以使用了水分子隔离膜的反应器是乙;
②平衡常数只受温度影响,a、b温度相同,平衡常数 = ,由已知条件列出“三段式”
M点 =75kPa。
(7)T℃ 时,向一体积为1L的恒容密闭容器中充入1molCO、 和3molH ,在一定
2 2
条件下发生上述3个反应,达到平衡时得到 和0.5molH O,此时 平衡转化
2
率为50%,则平衡时CO的物质的量为1mol-0.5×1mol=0.5mol,根据H原子守恒可知,平衡
时H 的物质的量为3mol-0.5mol-0.8mol×2=0.9mol,反应1的平衡常数
2
cH OcCH OH
0.50.8 0.8
K 2 3
。
cCO c3H 0.50.93 0.93
2 2