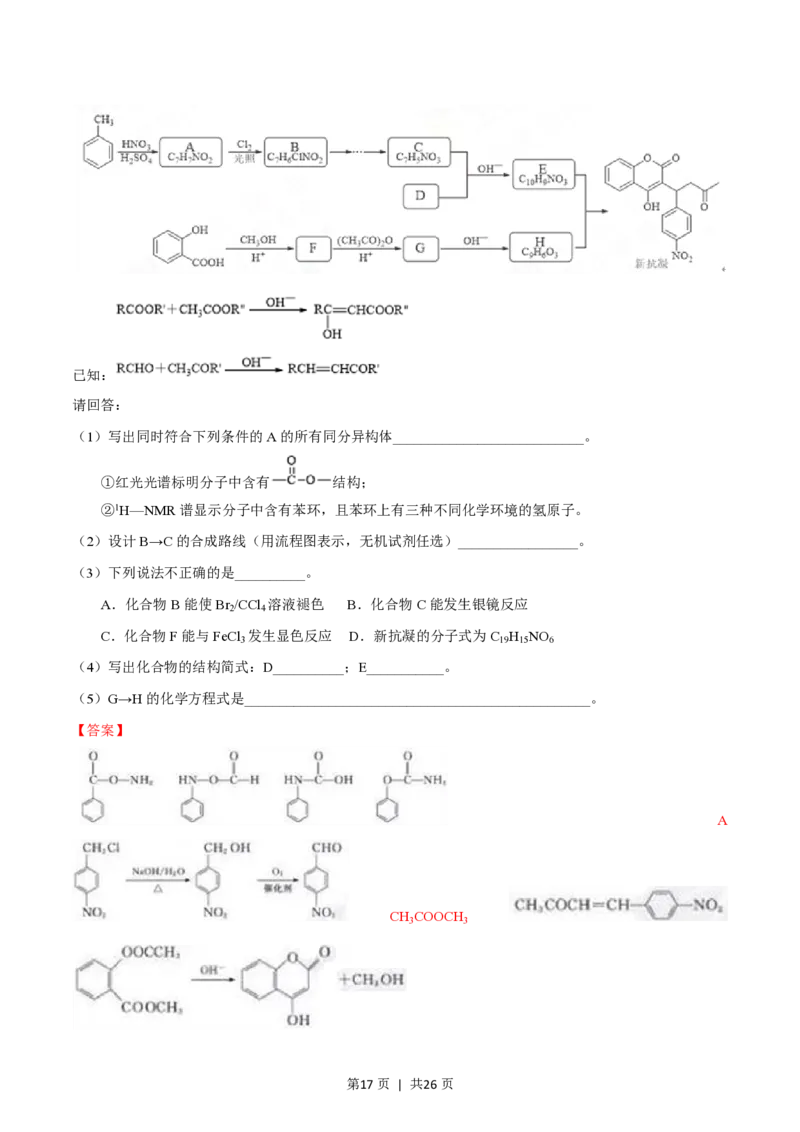
文档内容
2016 年 4 月浙江省普通高校招生选考科目考试化学试题
【整体分析】
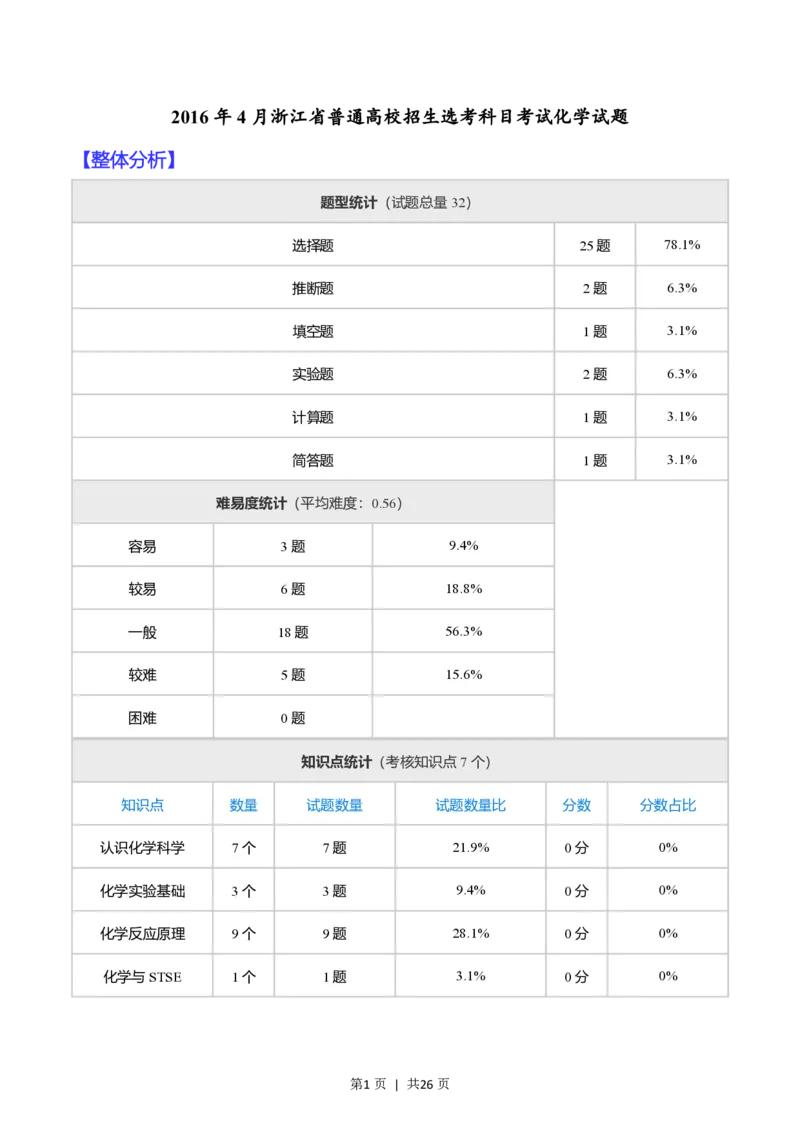
题型统计(试题总量32)
选择题 25题 78.1%
推断题 2题 6.3%
填空题 1题 3.1%
实验题 2题 6.3%
计算题 1题 3.1%
简答题 1题 3.1%
难易度统计(平均难度:0.56)
容易 3题 9.4%
较易 6题 18.8%
一般 18题 56.3%
较难 5题 15.6%
困难 0题
知识点统计(考核知识点7个)
知识点 数量 试题数量 试题数量比 分数 分数占比
认识化学科学 7个 7题 21.9% 0分 0%
化学实验基础 3个 3题 9.4% 0分 0%
化学反应原理 9个 9题 28.1% 0分 0%
化学与STSE 1个 1题 3.1% 0分 0%
第1页 | 共26页物质结构与性质 4个 4题 12.5% 0分 0%
常见无机物及其应用 4个 4题 12.5% 0分 0%
有机化学基础 4个 4题 12.5% 0分 0%
【题型考点分析】
题号 题型 知识点
1
选择题 酸碱混合时的定性判断及计算
2
选择题 盐溶液的酸碱性判断
3
选择题 电解质、非电解质概念
4
选择题 碳酸钠、碳酸氢钠混合物的有关求算
5
选择题 阿伏加德罗常数的应用
6
选择题 烃
7
选择题 化学电源
8
选择题 仪器使用与实验安全
9
选择题 共价键概念及判断
10
选择题 油脂的性质
11
选择题 一元强酸与一元弱酸的比较
12
选择题 分子结构与性质
13
选择题 氧化还原反应基本概念
14
选择题 化学平衡状态本质及特征
15
选择题 化学反应中能量变化的原因
16
填空题 有关铁及其化合物转化的流程题型
第2页 | 共26页17
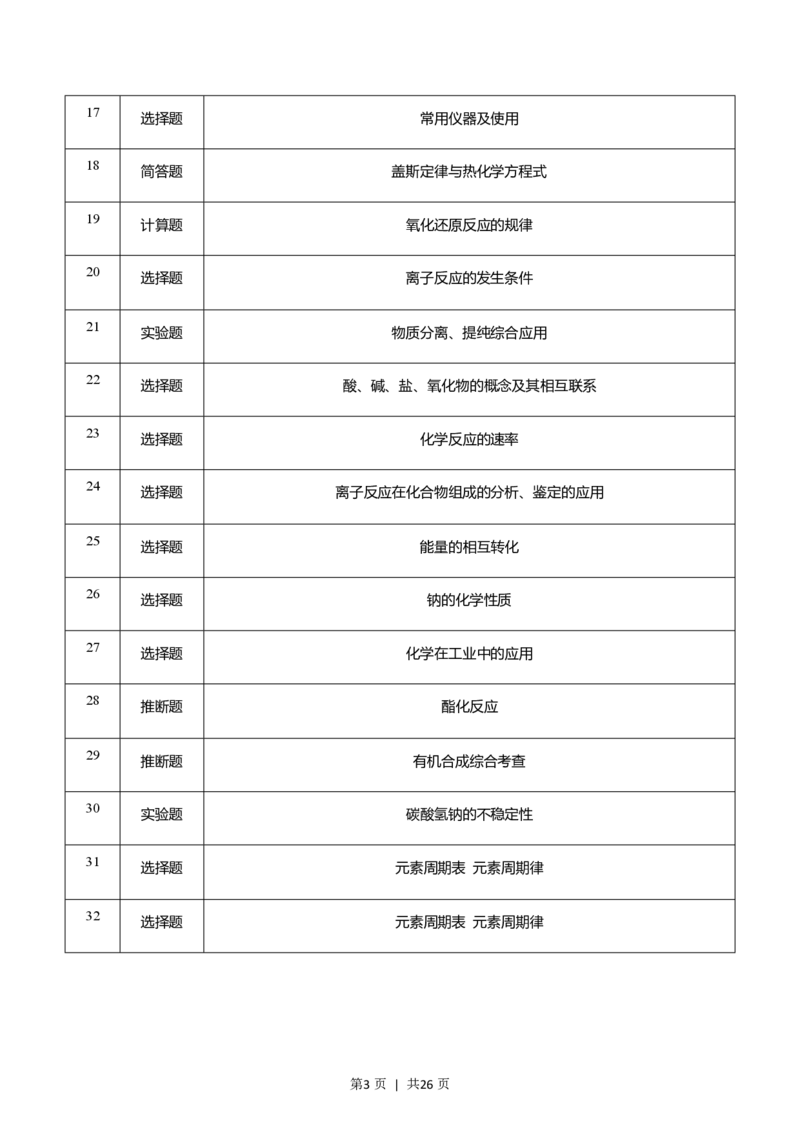
选择题 常用仪器及使用
18
简答题 盖斯定律与热化学方程式
19
计算题 氧化还原反应的规律
20
选择题 离子反应的发生条件
21
实验题 物质分离、提纯综合应用
22
选择题 酸、碱、盐、氧化物的概念及其相互联系
23
选择题 化学反应的速率
24
选择题 离子反应在化合物组成的分析、鉴定的应用
25
选择题 能量的相互转化
26
选择题 钠的化学性质
27
选择题 化学在工业中的应用
28
推断题 酯化反应
29
推断题 有机合成综合考查
30
实验题 碳酸氢钠的不稳定性
31
选择题 元素周期表 元素周期律
32
选择题 元素周期表 元素周期律
第3页 | 共26页第4页 | 共26页第 I卷(选择题)
1.下列属于氧化物的是
A.NaCl B.MgO C.H SO D.NaOH
2 4
【答案】B
【解析】A、氯化钠是由Na、Cl两种元素组成的化合物,不属于氧化物,故A错误;B、MgO是由两种元
素组成的且有一种是氧元素的化合物,属于氧化物,故B正确;C、硫酸是由三种元素组成的化合物,
不属于氧化物,故C错误;D、氢氧化钠是三种元素组成的化合物,不属于氧化物,故D错误;故选
B。
点睛:抓住氧化物的特征、熟悉常见的物质的组成是正确解答本题的关键。氧化物是只含有两种元素且其
中一种元素是氧元素的化合物。
2.仪器名称为“烧瓶”的是
A. B. C. D.
【答案】A
【解析】A.为烧瓶,故A正确; B.为量筒,故B错误;C.为容量瓶,故C错误;D.为分液漏斗,故
D错误;故选A。
3.下列属于非电解质的是( )
A.铜 B.硝酸钾
C.氢氧化钠 D.蔗糖
4.下列属于氧化还原反应的是
A.2KBr + Cl =2KCl + Br B.CaCO =CaO +CO ↑
2 2 3 2
第5页 | 共26页C.SO + H O=H SO D.MgCl + 2NaOH=Mg(OH) ↓ + NaCl
3 2 2 4 2 2
【答案】A
【解析】A.Br、Cl元素化合价发生变化,属于氧化还原反应,故A正确;B.分解反应,元素化合价没有
发生变化,不属于氧化还原反应,故B错误;C.为化合反应,元素化合价没有发生变化,不属于氧化
还原反应,故C错误;D.为复分解反应,元素化合价没有发生变化,不属于氧化还原反应,故D错
误;故选A。
5.下列物质的水溶液因水解而呈碱性的是
A.NaCl B.NH Cl C.Na CO D.NaOH
4 2 3
【答案】C
【解析】A.NaCl在溶液中不水解,其溶液为中性,故A错误;B.NH Cl为强酸弱碱盐,铵根离子在溶
4
液中水解,溶液呈酸性,故B错误;C.Na CO 为强碱弱酸盐,碳酸根离子水解,溶液呈碱性,满足
2 3
条件,故C正确;D.NaOH为强碱溶液,不满足条件,故D错误;故选C。
点睛:明确盐的水解原理为解答关键,注意掌握盐的类型及溶液性质。盐的水溶液因水解而呈碱性,说明
该盐属于强碱弱酸盐。
6.下列说法不正确的是
A.氯气可用于自来水的消毒 B.镁可用于制造信号弹和焰火
C.氢氧化铁胶体能用于净水 D.二氧化硫不可用于漂白纸浆
7.下列表示正确的是( )
A.CO 的电子式: B.乙炔的结构式:CH≡CH
2
C.CH 的球棍模型: D.Cl-的结构示意图:
4
【答案】D
【解析】A.CO 的电子式为 ,故A错误;B.乙炔的结构式为H-C≡C-H,故B错误;C.CH
2 4
第6页 | 共26页的球棍模型为 ,故C错误;D.Cl-的结构示意图为 ,故D正确。故选D。
点睛:结构式中的共价键需要一一表示,不能省略。
8.下列有关钠及其化合物的说法不正确的是
A.电解饱和食盐水可制取金属钠 B.钠与氧气反应的产物与反应条件有关
C.氧化钠与水反应生成氢氧化钠 D.钠可以从四氯化钛中置换出钛
【答案】A
【解析】A、电解饱和食盐水可以得到烧碱、氢气和氯气,电解熔融的氯化钠可以获得金属钠,故A错误;
B、钠在常温下和氧气反应生成氧化钠,在点燃条件下,和氧气反应生成淡黄色的过氧化钠,故B正确;
C、氧化钠是碱性氧化物与水反应生成碱,所以氧化钠与水反应生成氢氧化钠,故C正确;D、Na是
活泼金属,具有强还原性,所以钠可以从四氯化钛中置换出钛,利用了钠的强还原性,故D正确;故
选A。
9.下列说法正确的是
A.某试样焰色反应呈黄色,则试样中含有K+
B.广泛pH试纸测得某碱性溶液的pH为12.5
C.容量瓶不能用作溶解物质的容器
D.粗盐的提纯试验中,滤液在坩埚中加热蒸发结晶
10.下列说法不正确的是( )
A. C和 C是一种核素
B.红磷和白磷互为同素异形体
C.CH COOCH CH 和CH CH COOCH 是不同物质
3 2 3 3 2 3
D.CH CH OH可看成是由—C H 和—OH两种基团组成
3 2 2 5
【答案】A
【解析】A.12 C和14 C中子数不同,是不同种核素,故A错误;B.红磷与白磷是磷元素形成的结构不同
6 6
第7页 | 共26页单质,互为同素异形体,故B正确;C.CH COOCH CH 和CH CH COOCH 结构不同,是不同物质,
3 2 3 3 2 3
故C正确;D.CH CH OH可看成是由-C H 和-OH两种基团组成,故D正确;故选A。
3 2 2 5
11.下列说法正确的是
A.煤是无机化合物,天然气和石油是有机化合物
B.利用化石燃料燃烧放出的热量使水分解产生氢气,是氢能开发的研究方向
C.化学电源放电、植物光合作用都能发生化学变化,并伴随能量的转化
D.若化学过程中断开化学键放出的能量大于形成化学键所吸收的能量,则反应放热
【答案】C
【解析】A.煤是多种有机物和无机物的混合物,主要成分是碳单质,不是化合物,故A错误; B.化学燃
料是不可再生的,且不廉价,故B错误;C.化学电源放电、植物光合作用都有新物质生成,属于化学
变化,且都伴随着能量的变化,故C正确;D.从化学键角度判断反应是吸热还是放热的方法:旧键断
裂吸收能量大于新键生成释放能量,反应是吸热反应,反之是放热反应,故D错误;故选C。
12.可逆反应在一定条件下达到化学平衡时,下列说法不正确的是
A.正反应速率等于逆反应速率 B.反应物和生成物浓度不再发生变化
C.反应体系中混合物的组成保持不变 D.正、逆反应速率都为零
13.下列离子方程式正确的是
A.二氧化锰和浓盐酸反应:MnO +4H++4Cl-=Mn2++2Cl ↑+ 2H O
2 2 2
B.二氧化硅和氢氧化钠溶液反应:SiO + 2OH-=SiO 2- + H O
2 3 2
C.碳酸钡和稀硝酸反应:CO 2-+2H+=CO ↑+H O
3 2 2
D.铜和氯化铁溶液反应:Fe3++Cu=Fe2++Cu2+
【答案】B
【解析】A.二氧化锰和浓盐酸反应,离子方程式:MnO +4H++2Cl-=Mn2++Cl ↑+2H O,故A错误;B.二
2 2 2
氧化硅和氢氧化钠溶液反应,离子方程式:SiO +2OH-=SiO 2-+H O,故B正确;C.碳酸钡和稀硝酸反
2 3 2
第8页 | 共26页应,离子方程式:BaCO +2H+=CO ↑+H O+Ba2+,故C错误;D.铜和氯化铁溶液反应,离子方程式:
3 2 2
2Fe3++Cu=2Fe2++Cu2+,故D错误;故选B。
14.W、X、Y、Z、N、M六种主族元素,它们在周期表中位置如图所示,下列说法不正确的是
A.原子半径:Y>Z>W
B.单质的还原性:X>Y
C.溴与元素M同主族,最高价氧化物的水化物的酸性比M的强
D.元素N位于金属与非金属的分界线附近,可以推断N元素的单质可作半导体材料
【答案】C
【解析】A.同周期元素原子半径随着核电荷数增大而减小,所以原子半径Y>Z,同主族元素原子半径随着
原子序数增大而增大,所以原子半径Z>W,总之,原子半径:Y>Z>W,故A正确;B.单质的氧化性:
Y>X,所以单质的还原性:X>Y,故B正确;C.非金属性:溴 c(CH COOH) B.c(Cl-)= c(CH COO-)
3 3
C.等体积的盐酸和醋酸溶液分别与足量的Zn完全反应,盐酸产生的H 多
2
D.用同浓度的NaOH溶液分别与等体积的盐酸和醋酸溶液恰好反应完全,盐酸消耗的NaOH溶液体
积多
【答案】B
【解析】A.醋酸为弱电解质,在溶液中部分电离,pH相等时,醋酸浓度较大,即c(HCl)<c(CH COOH),
3
故 A 错误;B.溶液的 pH 相等,则两溶液中的氢离子、氢氧根离子浓度相等,根据电荷守恒可知
c(Cl-)=c(CH COO-),故B正确;C.等体积的盐酸和醋酸溶液分别与足量的Zn完全反应,由于醋酸的
3
浓度较大,则醋酸产生的H 多,故C错误;D.同浓度的NaOH溶液分别与等体积的盐酸和醋酸溶液
2
恰好反应完全,由于醋酸的浓度大于盐酸,则醋酸消耗的NaOH溶液体积多,故D错误;故选B。
点睛:明确弱电解质的电离特点为解答关键。注意掌握溶液酸碱性与溶液pH的关系,醋酸为弱电解质,氯
化氢是强电解质,pH相等时,醋酸浓度较大;物质的量浓度相等时,盐酸的pH较小,酸性较强。本
题的易错点为CD。
22.设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.1 mol FeI 与1 mol Cl 反应时转移的电子数为3N
2 2 A
第12页 | 共26页B.2 g H O与D O的混合物中所含中子、电子数目均为N
A
C.273 K、101 kPa下,28 g乙烯与丙烯混合物中含有C—H键的数目为5N
A
D.pH=1的H SO 溶液10 L,含H+的数目为2N
2 4 A
【答案】B
【解析】A、1molCl 只能提供2mol电子, 1 mol FeI 与1 mol Cl 反应时转移的电子数为2N ,故A错误;
2 2 2 A
B、H18O与D16O的摩尔质量均为20g/mol,故2g混合物的物质的量为0.1mol,且两者均含10个电子
2 2
和10个中子,故0.1mol混合物中含1N 个电子和1N 个中子,故B正确;C、乙烯和丙烯的最简式均
A A
为CH,故28g混合物中含有的CH 的物质的量为2mol,故含有的C-H键为4N 个,故C错误;D、
2 2 A
pH=1HSO 溶液PH=-lgc(H+)=1,HSO 溶液c(H+)=0.1mol/L,10L溶液n(H+)=1mol,所含H+数
2 4 2 4
目为N ,故D错误;故选B。
A
23.常温下,向20.00mL0.1000 mol·L-1的醋酸溶液中逐滴加入0.1000 mol·L-1的NaOH溶液,pH随NaOH
溶液体积的变化如图所示。下列说法不正确的是
A.在反应过程中,c(Na+)+ c(H+)= c(CH COO-)+ c(OH-)
3
B.pH=5时,c(CH COO-)> c(Na+)> c(H+)> c(OH-)
3
C.pH=6时,c(Na+)+ c(H+)-c(OH-)+ c(CH COOH)=0.1000 mol·Lˉ1
3
D.pH=7时,消耗NaOH溶液的体积小于20.00mL
第13页 | 共26页点睛:本题考查酸碱混合的定性判断及溶液pH的计算,明确各点对应溶质组成为解答关键。注意掌握电荷
守恒、物料守恒及盐的水解原理在判断离子浓度大小中的应用。本题的易错点为BC,需要熟练掌握电
解质溶液中的守恒关系。
24.向amolNaOH的溶液中通入bmolCO ,下列说法不正确的是
2
A.当a>2b时,发生的离子反应为:2OH-+CO =CO 2-+H O
2 3 2
B.当a