文档内容
(七)基元反应
(选择题1~3题,每小题5分,4~8题,每小题7分,共50分)
1.(2024·河南信阳模拟)基于非金属原子嵌入石墨烯三嗪基C N 中,用于催化一氧化碳加氢生成甲醇的
3 4
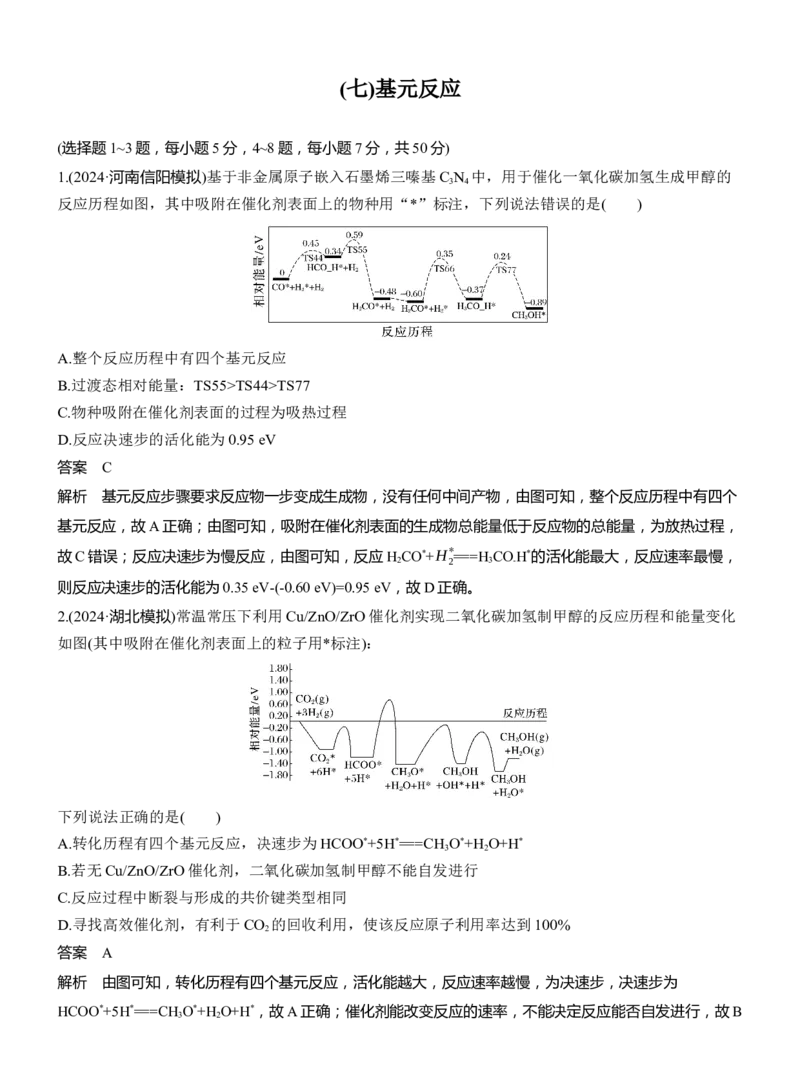
反应历程如图,其中吸附在催化剂表面上的物种用“*”标注,下列说法错误的是( )
A.整个反应历程中有四个基元反应
B.过渡态相对能量:TS55>TS44>TS77
C.物种吸附在催化剂表面的过程为吸热过程
D.反应决速步的活化能为0.95 eV
答案 C
解析 基元反应步骤要求反应物一步变成生成物,没有任何中间产物,由图可知,整个反应历程中有四个
基元反应,故A正确;由图可知,吸附在催化剂表面的生成物总能量低于反应物的总能量,为放热过程,
故C错误;反应决速步为慢反应,由图可知,反应H
CO*+H*
===H COH*的活化能最大,反应速率最慢,
2 2 3 -
则反应决速步的活化能为0.35 eV-(-0.60 eV)=0.95 eV,故D正确。
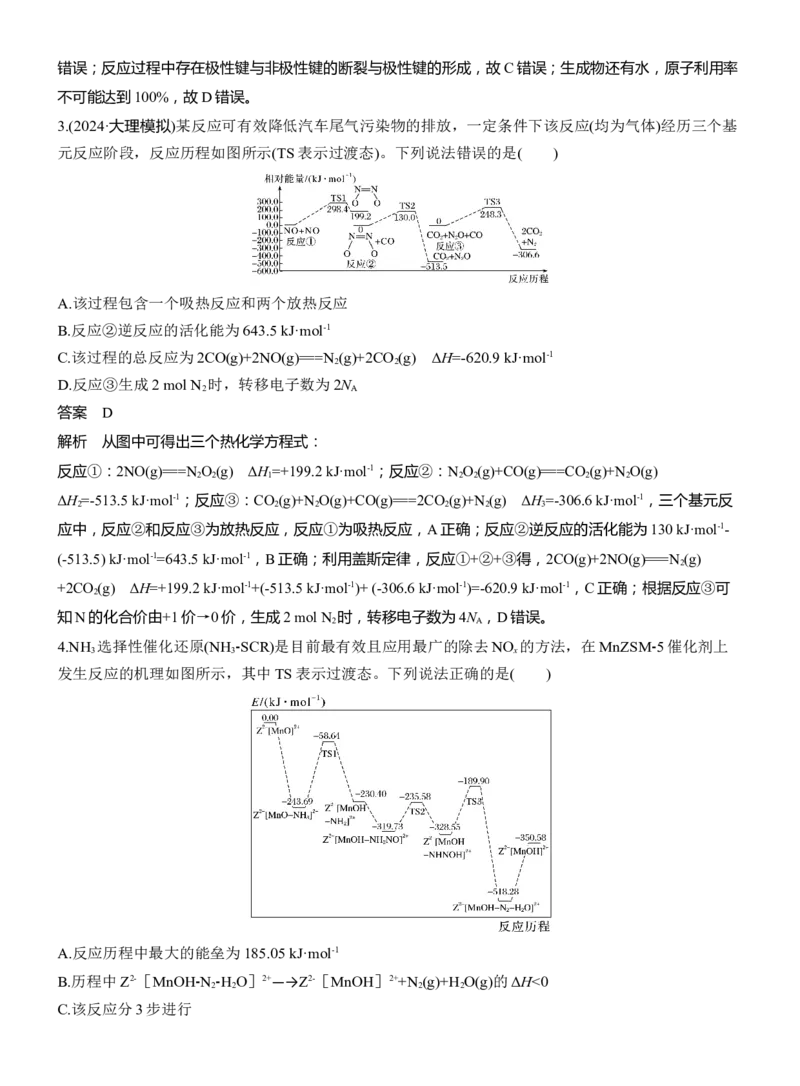
2.(2024·湖北模拟)常温常压下利用Cu/ZnO/ZrO催化剂实现二氧化碳加氢制甲醇的反应历程和能量变化
如图(其中吸附在催化剂表面上的粒子用*标注):
下列说法正确的是( )
A.转化历程有四个基元反应,决速步为HCOO*+5H*===CH O*+H O+H*
3 2
B.若无Cu/ZnO/ZrO催化剂,二氧化碳加氢制甲醇不能自发进行
C.反应过程中断裂与形成的共价键类型相同
D.寻找高效催化剂,有利于CO 的回收利用,使该反应原子利用率达到100%
2
答案 A
解析 由图可知,转化历程有四个基元反应,活化能越大,反应速率越慢,为决速步,决速步为
HCOO*+5H*===CH O*+H O+H*,故A正确;催化剂能改变反应的速率,不能决定反应能否自发进行,故B
3 2错误;反应过程中存在极性键与非极性键的断裂与极性键的形成,故C错误;生成物还有水,原子利用率
不可能达到100%,故D错误。
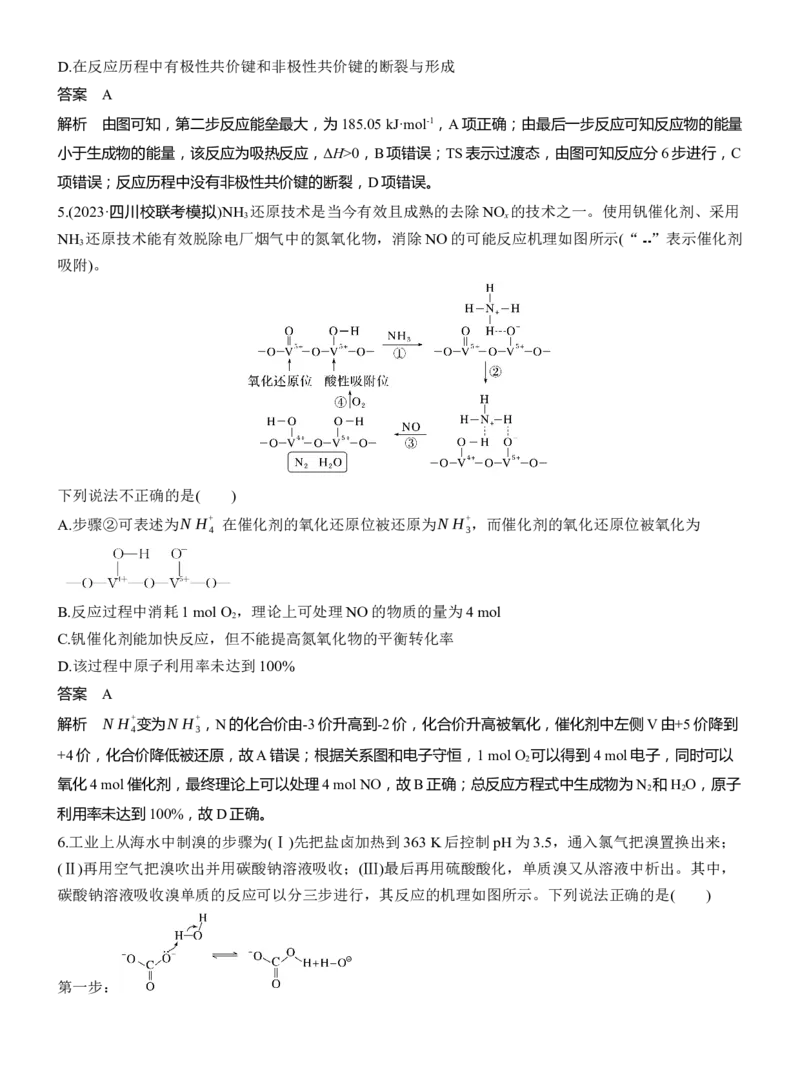
3.(2024·大理模拟)某反应可有效降低汽车尾气污染物的排放,一定条件下该反应(均为气体)经历三个基
元反应阶段,反应历程如图所示(TS表示过渡态)。下列说法错误的是( )
A.该过程包含一个吸热反应和两个放热反应
B.反应②逆反应的活化能为643.5 kJ·mol-1
C.该过程的总反应为2CO(g)+2NO(g)===N (g)+2CO (g) ΔH=-620.9 kJ·mol-1
2 2
D.反应③生成2 mol N 时,转移电子数为2N
2 A
答案 D
解析 从图中可得出三个热化学方程式:
反应①:2NO(g)===N O (g) ΔH =+199.2 kJ·mol-1;反应②:N O (g)+CO(g)===CO (g)+N O(g)
2 2 1 2 2 2 2
ΔH =-513.5 kJ·mol-1;反应③:CO (g)+N O(g)+CO(g)===2CO (g)+N (g) ΔH =-306.6 kJ·mol-1,三个基元反
2 2 2 2 2 3
应中,反应②和反应③为放热反应,反应①为吸热反应,A正确;反应②逆反应的活化能为130 kJ·mol-1-
(-513.5) kJ·mol-1=643.5 kJ·mol-1,B正确;利用盖斯定律,反应①+②+③得,2CO(g)+2NO(g)===N (g)
2
+2CO (g) ΔH=+199.2 kJ·mol-1+(-513.5 kJ·mol-1)+ (-306.6 kJ·mol-1)=-620.9 kJ·mol-1,C正确;根据反应③可
2
知N的化合价由+1价→0价,生成2 mol N 时,转移电子数为4N ,D错误。
2 A
4.NH
3
选择性催化还原(NH 3⁃SCR)是目前最有效且应用最广的除去NO
x
的方法,在MnZSM⁃5催化剂上
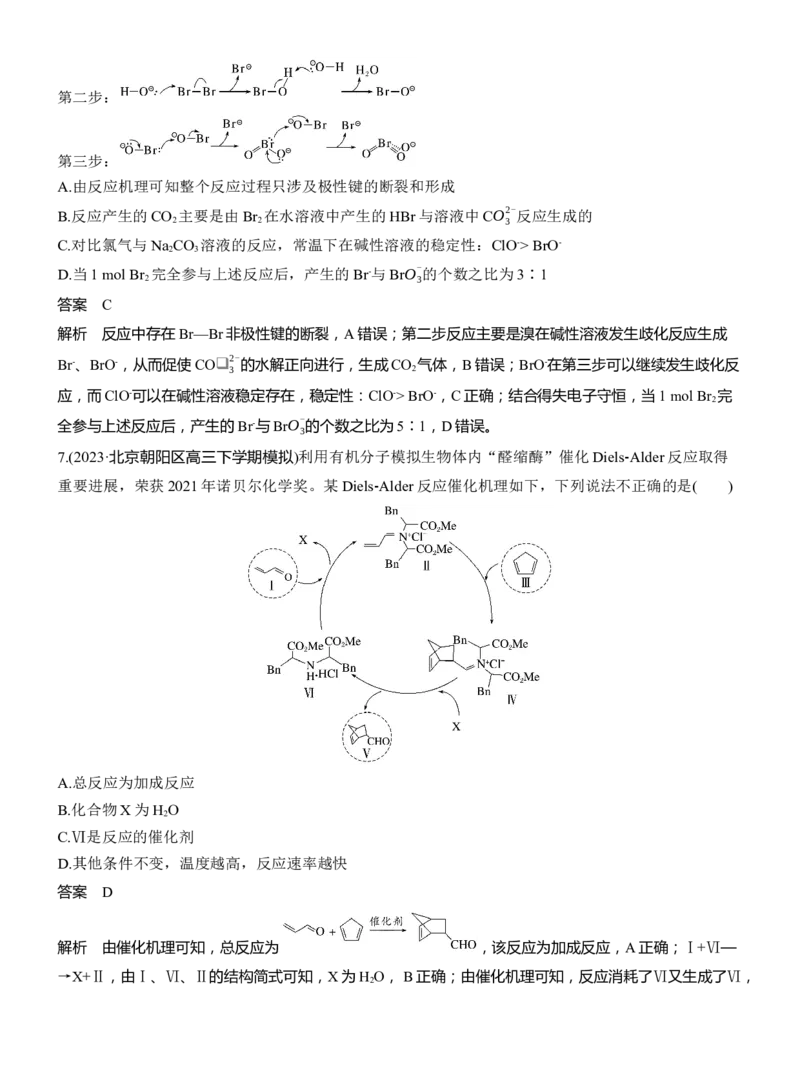
发生反应的机理如图所示,其中TS表示过渡态。下列说法正确的是( )
A.反应历程中最大的能垒为185.05 kJ·mol-1
B.历程中Z2-[MnOH⁃N 2⁃H
2
O]2+―→Z2-[MnOH]2++N
2
(g)+H
2
O(g)的ΔH<0
C.该反应分3步进行D.在反应历程中有极性共价键和非极性共价键的断裂与形成
答案 A
解析 由图可知,第二步反应能垒最大,为185.05 kJ·mol-1,A项正确;由最后一步反应可知反应物的能量
小于生成物的能量,该反应为吸热反应,ΔH>0,B项错误;TS表示过渡态,由图可知反应分6步进行,C
项错误;反应历程中没有非极性共价键的断裂,D项错误。
5.(2023·四川校联考模拟)NH 还原技术是当今有效且成熟的去除NO 的技术之一。使用钒催化剂、采用
3 x
NH 还原技术能有效脱除电厂烟气中的氮氧化物,消除NO的可能反应机理如图所示(“ ”表示催化剂
3
吸附)。
下列说法不正确的是( )
A.步骤②可表述为N H+ 在催化剂的氧化还原位被还原为N H+ ,而催化剂的氧化还原位被氧化为
4 3
B.反应过程中消耗1 mol O ,理论上可处理NO的物质的量为4 mol
2
C.钒催化剂能加快反应,但不能提高氮氧化物的平衡转化率
D.该过程中原子利用率未达到100%
答案 A
解析 N H+ 变为N H+ ,N的化合价由-3价升高到-2价,化合价升高被氧化,催化剂中左侧V由+5价降到
4 3
+4价,化合价降低被还原,故A错误;根据关系图和电子守恒,1 mol O 可以得到4 mol电子,同时可以
2
氧化4 mol催化剂,最终理论上可以处理4 mol NO,故B正确;总反应方程式中生成物为N 和H O,原子
2 2
利用率未达到100%,故D正确。
6.工业上从海水中制溴的步骤为(Ⅰ)先把盐卤加热到363 K后控制pH为3.5,通入氯气把溴置换出来;
(Ⅱ)再用空气把溴吹出并用碳酸钠溶液吸收;(Ⅲ)最后再用硫酸酸化,单质溴又从溶液中析出。其中,
碳酸钠溶液吸收溴单质的反应可以分三步进行,其反应的机理如图所示。下列说法正确的是( )
第一步:第二步:
第三步:
A.由反应机理可知整个反应过程只涉及极性键的断裂和形成
B.反应产生的CO 主要是由Br 在水溶液中产生的HBr与溶液中CO2-反应生成的
2 2 3
C.对比氯气与Na CO 溶液的反应,常温下在碱性溶液的稳定性:ClO-> BrO-
2 3
D.当1 mol Br
完全参与上述反应后,产生的Br-与BrO-
的个数之比为3∶1
2 3
答案 C
解析 反应中存在Br—Br非极性键的断裂,A错误;第二步反应主要是溴在碱性溶液发生歧化反应生成
Br-、BrO-,从而促使CO❑
2-
的水解正向进行,生成CO 气体,B错误;BrO-在第三步可以继续发生歧化反
3 2
应,而ClO-可以在碱性溶液稳定存在,稳定性:ClO-> BrO-,C正确;结合得失电子守恒,当1 mol Br 完
2
全参与上述反应后,产生的Br-与BrO-
的个数之比为5∶1,D错误。
3
7.(2023·北京朝阳区高三下学期模拟)利用有机分子模拟生物体内“醛缩酶”催化Diels⁃Alder反应取得
重要进展,荣获2021年诺贝尔化学奖。某Diels⁃Alder反应催化机理如下,下列说法不正确的是( )
A.总反应为加成反应
B.化合物X为H O
2
C.Ⅵ是反应的催化剂
D.其他条件不变,温度越高,反应速率越快
答案 D
解析 由催化机理可知,总反应为 ,该反应为加成反应,A正确;Ⅰ+Ⅵ—
→X+Ⅱ,由Ⅰ、Ⅵ、Ⅱ的结构简式可知,X为H O, B正确;由催化机理可知,反应消耗了Ⅵ又生成了Ⅵ,
2Ⅵ是反应的催化剂,C正确;通常其他条件不变,温度越高,反应速率越快,但是酶作催化剂时,高温使
酶失去活性降低反应速率,D错误。
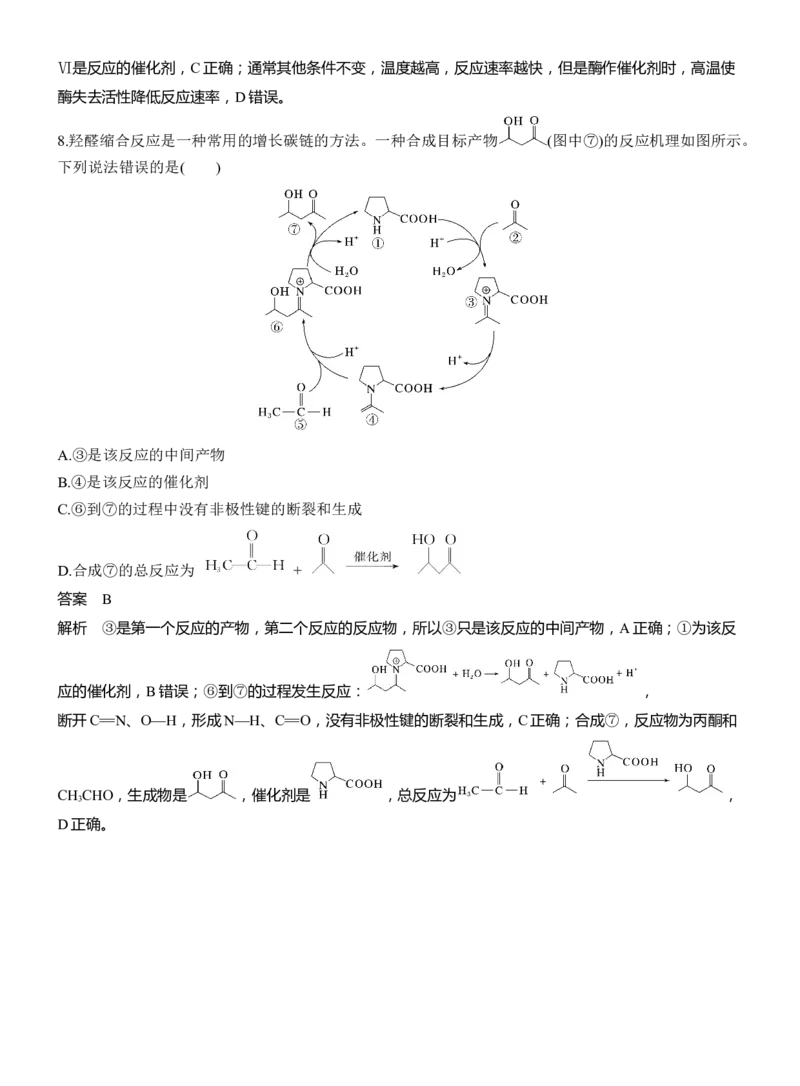
8.羟醛缩合反应是一种常用的增长碳链的方法。一种合成目标产物 (图中⑦)的反应机理如图所示。
下列说法错误的是( )
A.③是该反应的中间产物
B.④是该反应的催化剂
C.⑥到⑦的过程中没有非极性键的断裂和生成
D.合成⑦的总反应为 +
答案 B
解析 ③是第一个反应的产物,第二个反应的反应物,所以③只是该反应的中间产物,A正确;①为该反
应的催化剂,B错误;⑥到⑦的过程发生反应: ,
断开C==N、O—H,形成N—H、C==O,没有非极性键的断裂和生成,C正确;合成⑦,反应物为丙酮和
CH CHO,生成物是 ,催化剂是 ,总反应为 ,
3
D正确。