文档内容
【基础知识】分子结构与性质
考点八 配合物、超分子
【必备知识】
一、配合物
1、相关概念
配位键与配合物:由一个原子单方面提供孤电子对而另一个原子接受孤电子对形成的共价键中配位键。配
位键属于共价键。金属离子或原子与某些离子或分子以配位键结合形成的化合物称为配合物(水合金属离
子除外)。
2、组成
中心离子或原子:有空轨道,一般是带正电的金属离子,特别是过渡金属离子,如Fe3+、Cu2+、Zn2+、Ag+
等,但也有电中性的原子如B。
配体:其中的配位原子(配体中直接同中心离子或原子配合的原子)有孤电子对。配体可以是分子,如CO、
NH 、HO等,也可以是离子,如F-、Cl-、Br-、I-、CN-、SCN-、OH-等。
3 2
3、表示:常用“→”来表示配位键,箭头指向接受孤电子对的原子,如NH可表示为 ,在
NH中,虽然有一个N—H键形成过程与其他3个N—H键形成过程不同,但是一旦形成之后,4个共价键
就完全相同。
4、如何判断物质中有无配位健?中心原子共价键数超过未成对电子数。
5、如何算配位数?配位数≠配位键数目
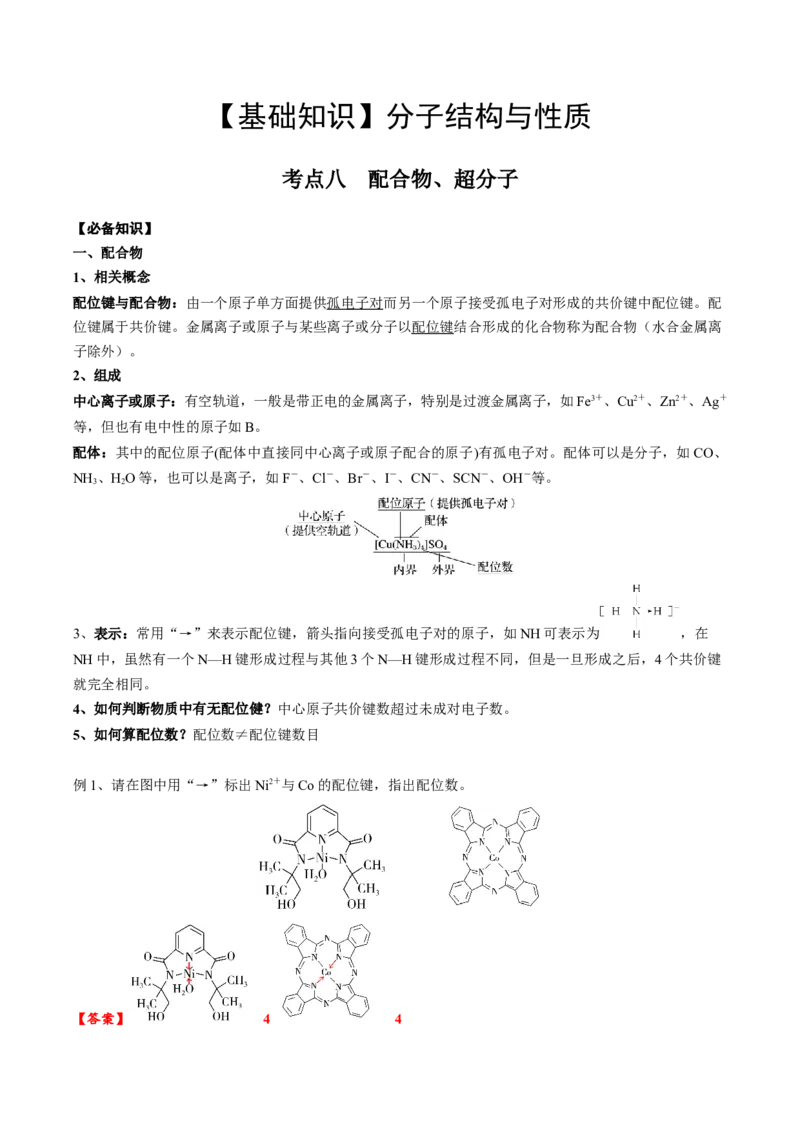
例1、请在图中用“→”标出Ni2+与Co的配位键,指出配位数。
【答案】 4 4例2、回答下列问题
(1)(2016 江苏卷)[Zn(CN) ]2-中Zn2+与CN-的C原子形成配位键。不考虑空间构型,[Zn(CN) ]2-的结构
4 4
可用示意图表示为____________。
(2)AlCl 在熔融态、气态和非极性溶剂中均以二聚体的形式存在,写出其二聚体的结构示意图
3
。
(3)[2019·新课标Ⅲ]FeCl 中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl 的结构式为
3 3
________,其中Fe的配位数为_____________。
(4)CO为配合物中常见的配体。CO作配体时,提供孤电子对的通常是C原子而不是O原子,其原因是
________________________________________________________________________。
(5)配位化学创始人维尔纳发现,取 CoCl ·6NH (黄色)、CoCl ·5NH (紫红色)、CoCl ·4NH (绿色)和
3 3 3 3 3 3
CoCl ·4NH (紫色)四种化合物各1 mol,分别溶于水,加入足量硝酸银溶液,立即产生氯化银,沉淀的量分
3 3
别为3 mol、2 mol、1 mol和1 mol。
①请根据实验事实用配合物的形式写出它们的化学式。
CoCl ·6NH _______________________,CoCl ·4NH (绿色和紫色)________________。
3 3 3 3
②上述配合物中,中心离子的配位数都是__________________________________________。
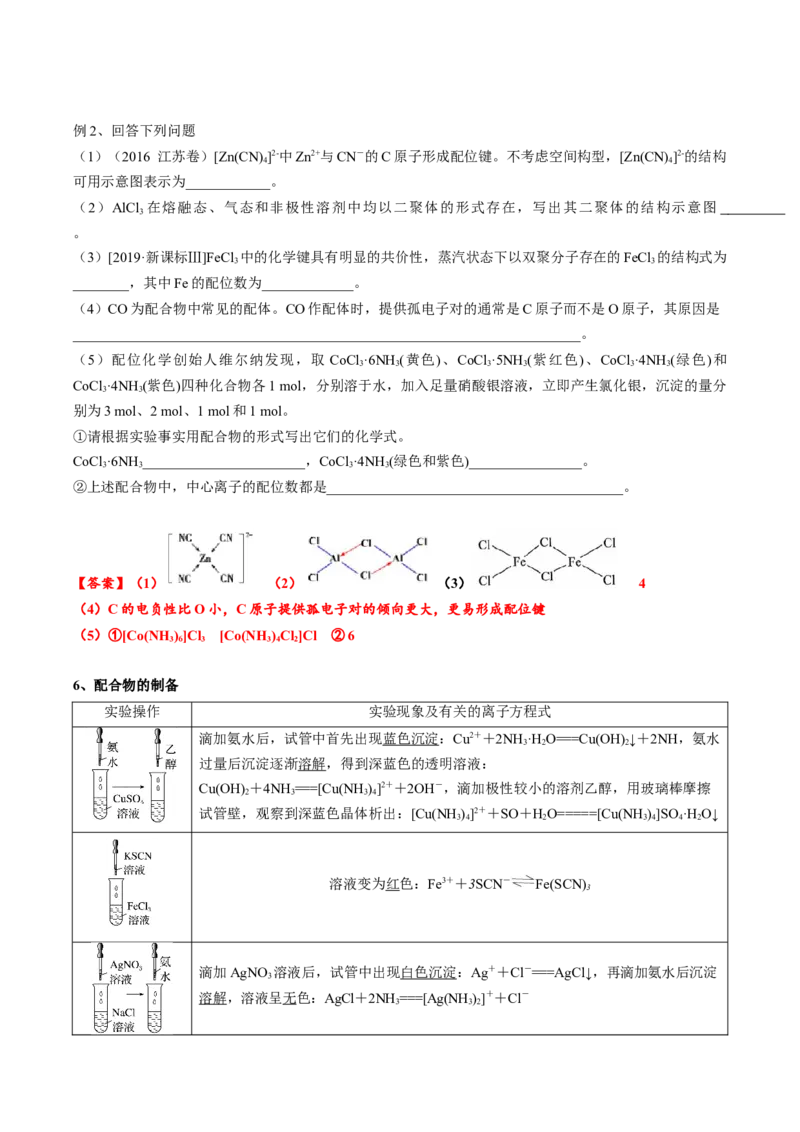
【答案】(1) (2) (3) 4
(4)C的电负性比O小,C原子提供孤电子对的倾向更大,更易形成配位键
(5)①[Co(NH )]Cl [Co(NH )Cl ]Cl ②6
3 6 3 3 4 2
6、配合物的制备
实验操作 实验现象及有关的离子方程式
滴加氨水后,试管中首先出现蓝色沉淀:Cu2++2NH ·H O===Cu(OH) ↓+2NH,氨水
3 2 2
过量后沉淀逐渐溶解,得到深蓝色的透明溶液:
Cu(OH) +4NH ===[Cu(NH)]2++2OH-,滴加极性较小的溶剂乙醇,用玻璃棒摩擦
2 3 3 4
试管壁,观察到深蓝色晶体析出:[Cu(NH )]2++SO+HO=====[Cu(NH )]SO ·H O↓
3 4 2 3 4 4 2
溶液变为红色:Fe3++3SCN- Fe(SCN)
3
滴加AgNO 溶液后,试管中出现白色沉淀:Ag++Cl-===AgCl↓,再滴加氨水后沉淀
3
溶解,溶液呈无色:AgCl+2NH ===[Ag(NH )]++Cl-
3 3 2二、超分子
1、概念:超分子是由两种或两种以上的分子通过分子间相互作用形成的分子聚集体。
2、超分子内分子间的作用力:非共价键,包括氢键、静电作用、疏水作用以及一些分子与金属离子形成
的弱配位键等。
3、重要特征及应用:分子识别、自组装等、
【易错辨析】
1、配位键实质上是一种特殊的共价键( )
2、提供孤电子对的微粒既可以是分子,也可以是离子( )
3、有配位键的化合物就是配位化合物( )
4、配位化合物都很稳定( )
5、在配合物[Co(NH )Cl]Cl 中的Cl-均可与AgNO 反应生成AgCl沉淀( )
3 5 2 3
6、Ni(CO) 是配合物,它是由中心原子与配体构成的( )
4
7、 中含24 mol共价键( )
【答案】 1.√ 2.√ 3.× 4.× 5.× 6.√ 7.√
【跟踪练习】
1、关于化学式为[TiCl(H O) ]Cl ·H O的配合物,下列说法正确的是( )
2 5 2 2
A.配体是Cl-和HO,配位数是8 B.中心离子是Ti4+,配离子是[TiCl(H O) ]2+
2 2 5
C.内界和外界中Cl-的数目比是1∶2
D.在1 mol该配合物中加入足量AgNO 溶液,可以得到3 mol AgCl沉淀
3
【答案】 C
【解析】 配合物[TiCl(H O) ]Cl·HO中配体是Cl-和HO,配位数是6,故A错误;中心离子是Ti3+,
2 5 2 2 2
故B错误;加入足量AgNO 溶液,外界Cl-与Ag+反应,内界Cl-不与Ag+反应,1 mol该配合物只能生
3
成2 mol AgCl沉淀,故D错误。
2、(2023年浙江1月选考)共价化合物Al Cl 中所有原子均满足8电子稳定结构,一定条件下可发生反应:
2 6
Al Cl+2NH =2Al(NH )Cl ,下列说法不正确的是( )
2 6 3 3 3
A. Al Cl 的结构式为 B. Al Cl 为非极性分子
2 6 2 6
C. 该反应中NH 的配位能力大于氯 D. Al Br 比Al Cl 更难与NH 发生反应
3 2 6 2 6 3
【答案】D
【解析】A.由双聚氯化铝分子中所有原子均满足8电子稳定结构可知,分子的结构式为,故A正确;
B.双聚氯化铝分子为结构对称的非极性分子,故B正确;
C.由反应方程式可知,氨分子更易与具有空轨道的铝原子形成配位键,配位能力大于氯原子,故C正
确;
D.溴元素的电负性小于氯元素,原子的原子半径大于氯原子,则铝溴键弱于铝氯键,所以双聚溴化铝的
铝溴键更易断裂,比双聚氯化铝更易与氨气反应,故D错误。
3、下列关于超分子的说法中,不正确的是( )
A.超分子是由两种或两种以上的分子必须通过氢键相互作用形成的分子聚集体
B.将C 加入一种空腔大小适配C 的“杯酚”中会形成超分子
60 60
C.碱金属离子虽然不是分子,但冠醚在识别碱金属离子时,形成的也是超分子
D.超分子的重要特征是自组装和分子识别
【答案】 A
【解析】 将C 加入一种空腔大小适配C 的“杯酚”中,两分子间的作用力为分子间作用力,能形成超
60 60
分子,B正确;冠醚是皇冠状的分子,有不同大小的空穴,会与合适的碱金属离子形成超分子,C正确;
超分子的两大特征为分子识别和自组装,D正确。
4、冠醚是一种超分子,它能否适配碱金属离子与其空腔直径和离子直径有关。二苯并-18-冠-6与K+形成
的配离子的结构如图所示。下列说法错误的是( )
冠醚 冠醚空腔直径/pm 适合的粒子(直径/pm)
15-冠-5 170~220 Na+(204)
18-冠-6 260~320 K+(276)、Rb+(304)
21-冠-7 340~430 Cs+(334)
A.冠醚可以用来识别碱金属离子 B.二苯并-18-冠-6也能适配Li+
C.该冠醚分子中碳原子杂化方式有2种 D.一个配离子中配位键的数目为6
【答案】 B
【解析】 由表知,碱金属离子在冠醚空腔直径范围内,冠醚与碱金属离子的包含物都是超分子,可以识
别碱金属离子,A正确;Li+半径小于Na+;则二苯并-18-冠-6不能适配Li+,B错误;该冠醚分子中苯环
碳原子为sp2杂化、其他碳链上的碳原子为sp3杂化,C正确;由结构简式可知,一个配离子中配位键的数
目为6,D正确。
5、过渡金属配合物的一些特有性质的研究正受到许多研究人员的关注,因为这方面的研究无论是理论上
还是工业应用上都有重要意义。氯化铁溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配
离子结构如图所示。下列有关该配离子的说法正确的是( )A.1 mol该配离子中含有π键的个数是6×6.02×1023 B.该配离子中碳原子的杂化类型均为sp2杂化
C.该配离子含有的非金属元素中电负性最大的是碳
D.该配离子中含有的化学键有离子键、共价键、配位键
【答案】 A
【解析】 该配离子中碳原子的杂化类型有sp2、sp3杂化,故B错误;该配离子含有的非金属元素有C、
O、H,电负性最大的是氧,故C错误;该配离子中含有的化学键有共价键、配位键,故D错误。
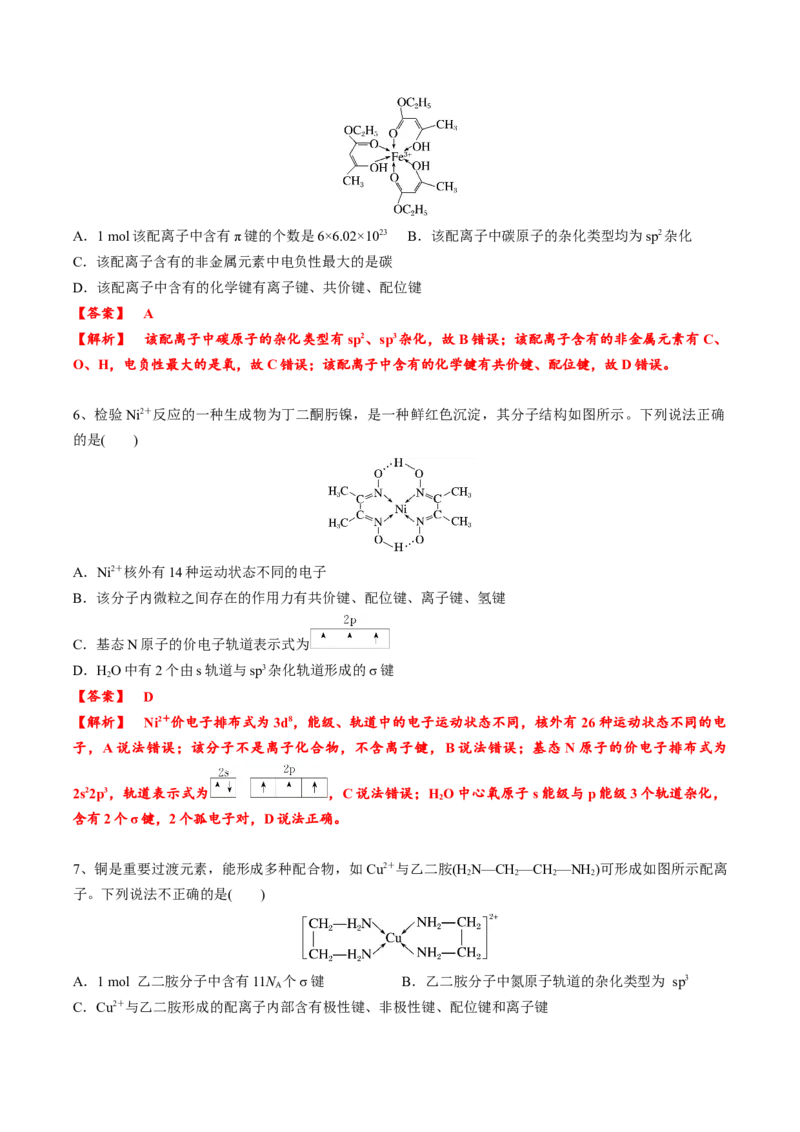
6、检验Ni2+反应的一种生成物为丁二酮肟镍,是一种鲜红色沉淀,其分子结构如图所示。下列说法正确
的是( )
A.Ni2+核外有14种运动状态不同的电子
B.该分子内微粒之间存在的作用力有共价键、配位键、离子键、氢键
C.基态N原子的价电子轨道表示式为
D.HO中有2个由s轨道与sp3杂化轨道形成的σ键
2
【答案】 D
【解析】 Ni2+价电子排布式为3d8,能级、轨道中的电子运动状态不同,核外有 26种运动状态不同的电
子,A说法错误;该分子不是离子化合物,不含离子键,B说法错误;基态N原子的价电子排布式为
2s22p3,轨道表示式为 ,C说法错误;HO中心氧原子s能级与p能级3个轨道杂化,
2
含有2个σ键,2个孤电子对,D说法正确。
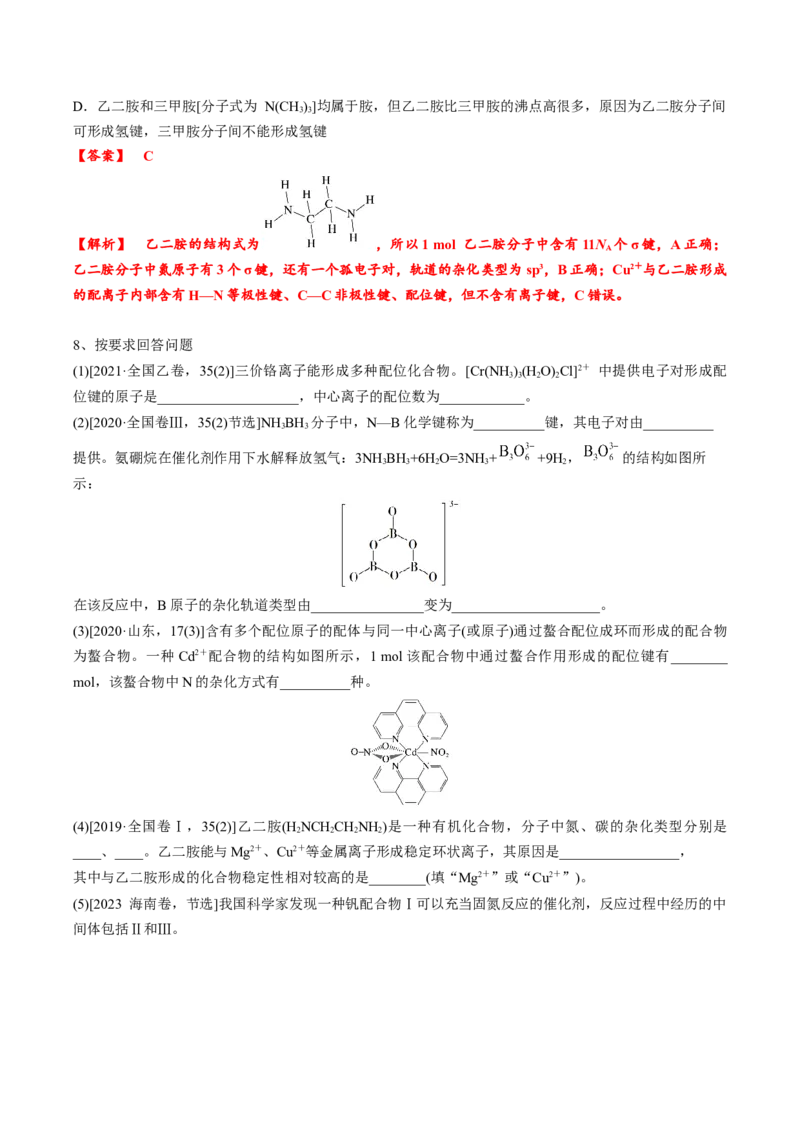
7、铜是重要过渡元素,能形成多种配合物,如Cu2+与乙二胺(H N—CH —CH—NH )可形成如图所示配离
2 2 2 2
子。下列说法不正确的是( )
A.1 mol 乙二胺分子中含有11N 个σ键 B.乙二胺分子中氮原子轨道的杂化类型为 sp3
A
C.Cu2+与乙二胺形成的配离子内部含有极性键、非极性键、配位键和离子键D.乙二胺和三甲胺[分子式为 N(CH )]均属于胺,但乙二胺比三甲胺的沸点高很多,原因为乙二胺分子间
3 3
可形成氢键,三甲胺分子间不能形成氢键
【答案】 C
【解析】 乙二胺的结构式为 ,所以1 mol 乙二胺分子中含有11N 个σ键,A正确;
A
乙二胺分子中氮原子有3个σ键,还有一个孤电子对,轨道的杂化类型为sp3,B正确;Cu2+与乙二胺形成
的配离子内部含有H—N等极性键、C—C非极性键、配位键,但不含有离子键,C错误。
8、按要求回答问题
(1)[2021·全国乙卷,35(2)]三价铬离子能形成多种配位化合物。[Cr(NH )(H O) Cl]2+ 中提供电子对形成配
3 3 2 2
位键的原子是____________________,中心离子的配位数为____________。
(2)[2020·全国卷Ⅲ,35(2)节选]NH BH 分子中,N—B化学键称为__________键,其电子对由__________
3 3
提供。氨硼烷在催化剂作用下水解释放氢气:3NH BH+6H O=3NH + +9H , 的结构如图所
3 3 2 3 2
示:
在该反应中,B原子的杂化轨道类型由________________变为_____________________。
(3)[2020·山东,17(3)]含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物
为螯合物。一种Cd2+配合物的结构如图所示,1 mol该配合物中通过螯合作用形成的配位键有________
mol,该螯合物中N的杂化方式有__________种。
(4)[2019·全国卷Ⅰ,35(2)]乙二胺(H NCH CHNH )是一种有机化合物,分子中氮、碳的杂化类型分别是
2 2 2 2
____、____。乙二胺能与Mg2+、Cu2+等金属离子形成稳定环状离子,其原因是_________________,
其中与乙二胺形成的化合物稳定性相对较高的是________(填“Mg2+”或“Cu2+”)。
(5)[2023 海南卷,节选]我国科学家发现一种钒配合物Ⅰ可以充当固氮反应的催化剂,反应过程中经历的中
间体包括Ⅱ和Ⅲ。配合物Ⅰ中钒的配位原子有4种,它们是_______。
【答案】 (1)N、O、Cl 6 (2)配位 N sp3 sp2 (3)6 1 (4)sp3 sp3 乙二胺的两个N提
供孤电子对与金属离子形成配位键 Cu2+ (5)C、O、P、Cl
【解析】 (1)[Cr(NH )(H O) Cl]2+中三价铬离子提供空轨道,N、O、Cl提供孤电子对,中心离子的配位
3 3 2 2
数为N、O、Cl三种原子的个数之和,即3+2+1=6。
(2)B原子最外层有3个电子,其与3个H原子形成共价键后,其价层电子对只有3对,还有一个空轨道;
在NH 中,N原子有一对孤对电子,故在NH BH 分子中,N—B键为配位键,其电子对由N原子提供。
3 3 3
NH BH 分子中,B原子的价层电子对数为4,故其杂化方式为sp3。NH BH 在催化剂的作用下水解生成氢
3 3 3 3
气和B O3-,由图中信息可知,B O3-中每个B原子只形成3个σ键,其中的B原子的杂化方式为sp2,因
3 6 3 6
此,B原子的杂化轨道类型由sp3变为sp2。
(3)由题给图示可知,1个Cd2+与C、N杂环上的4个N原子分别形成4个配位键,与2个O原子分别形成
2个配位键,因此1 mol该配合物中通过螯合作用形成的配位键有6 mol。
(4)乙二胺分子中,1个N原子形成3个单键,还有一个孤电子对,价电子对数为4,采取sp3杂化;1个C
原子形成4个单键,没有孤电子对,价电子对数为4,采取sp3杂化。乙二胺中2个氮原子提供孤电子对与
金属镁离子或铜离子形成稳定的配位键,故能形成稳定环状离子。由于铜离子半径大于镁离子,形成配位
键时头碰头重叠程度较大,其与乙二胺形成的化合物较稳定。
9、回答下列问题:
(1)CuSO ·5H O(胆矾)中含有水合铜离子而呈蓝色,写出胆矾晶体中水合铜离子的结构简式(必须将配位键
4 2
表示出来):_________________________________________________。
(2)向硫酸铜溶液中加入过量氨水,可生成[Cu(NH )]2+配离子。已知NF 与NH 的空间结构都是三角锥
3 4 3 3
形,但NF 不易与Cu2+形成配离子的原因是______________________________________。
3
(3)向黄色的三氯化铁溶液中加入无色的 KSCN溶液,溶液变成红色,该反应在有的教材中用方程式 FeCl
3
+3KSCN===Fe(SCN) +3KCl表示。经研究表明,Fe(SCN) 是配合物,Fe3+与SCN-不仅能以1∶3的个数比
3 3
配合,还可以以其他个数比配合,请按要求填空:
①Fe3+与SCN-反应时,Fe3+提供________,SCN-提供________,二者通过配位键结合。
②所得Fe3+与SCN-的配合物中,主要是Fe3+与SCN-以个数比1∶1配合所得离子显红色,含该离子的配合
物的化学式是____________。
【答案】 (1) (2)F的电负性大于N,N—F成键电子偏向F,导致NF 中的N原子
3
核对孤电子对的吸引力增强,难以形成配位键,故NF 不易与Cu2+形成配离子
3(3)①空轨道 孤电子对 ②[Fe(SCN)]Cl
2