文档内容
【基础知识】分子结构与性质
考点四 大 π 键(离域 π 键)
【必备知识】
定义: 个及以上原子构成离子团或分子中,原子有彼此平行的未参与杂化的 轨道电子连贯重叠
在一起,构成π型化学键,又称离域或共轭大π键。
条件:①原子在同一平面或直线;②中心原子 或 杂化(若提供d轨道则中心原子应为sp3d杂
化)。
表示:πn (m:参与形成大π键的原子数;n:参与形成大π键的电子数,n<2m)
m
分析方法——图示法
分析步骤:①判断出中心原子杂化方式,并画出σ键。②未成对电子优先形成大π键。
例:用图示法表示下列物质的大π键
物质 图示 解析
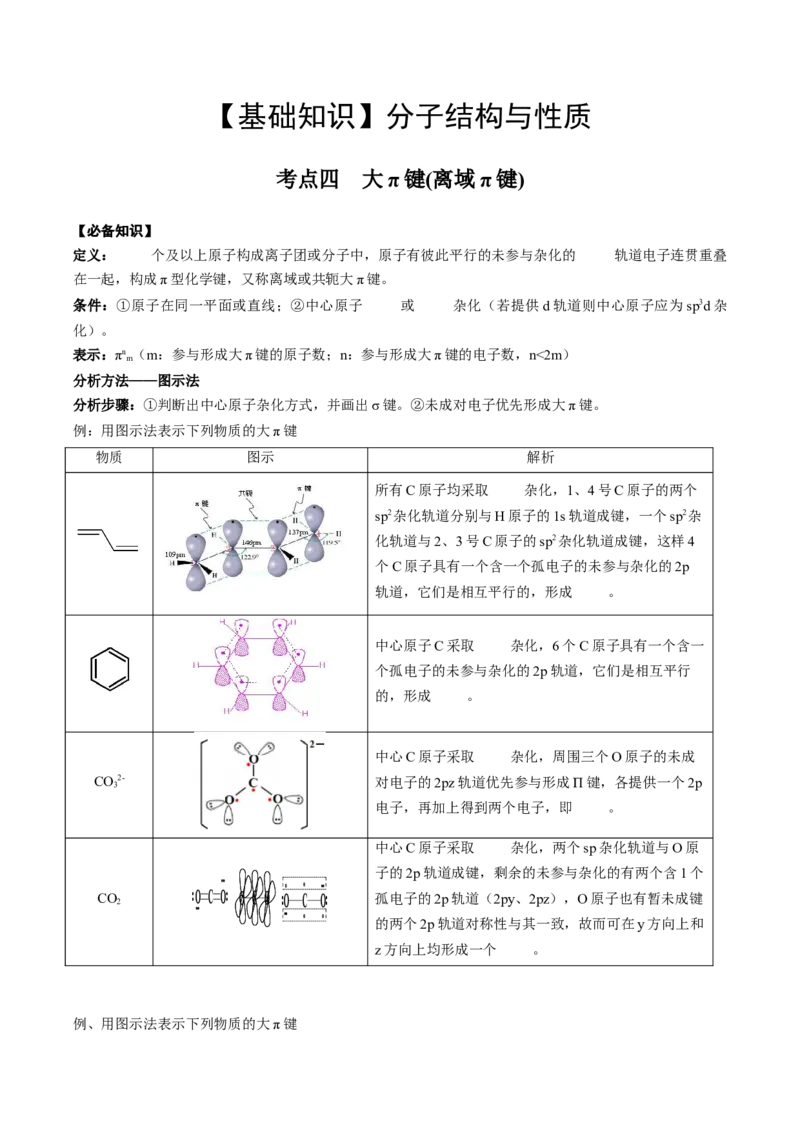
所有C原子均采取 杂化,1、4号C原子的两个
sp2杂化轨道分别与H原子的1s轨道成键,一个sp2杂
化轨道与2、3号C原子的sp2杂化轨道成键,这样4
个C原子具有一个含一个孤电子的未参与杂化的2p
轨道,它们是相互平行的,形成 。
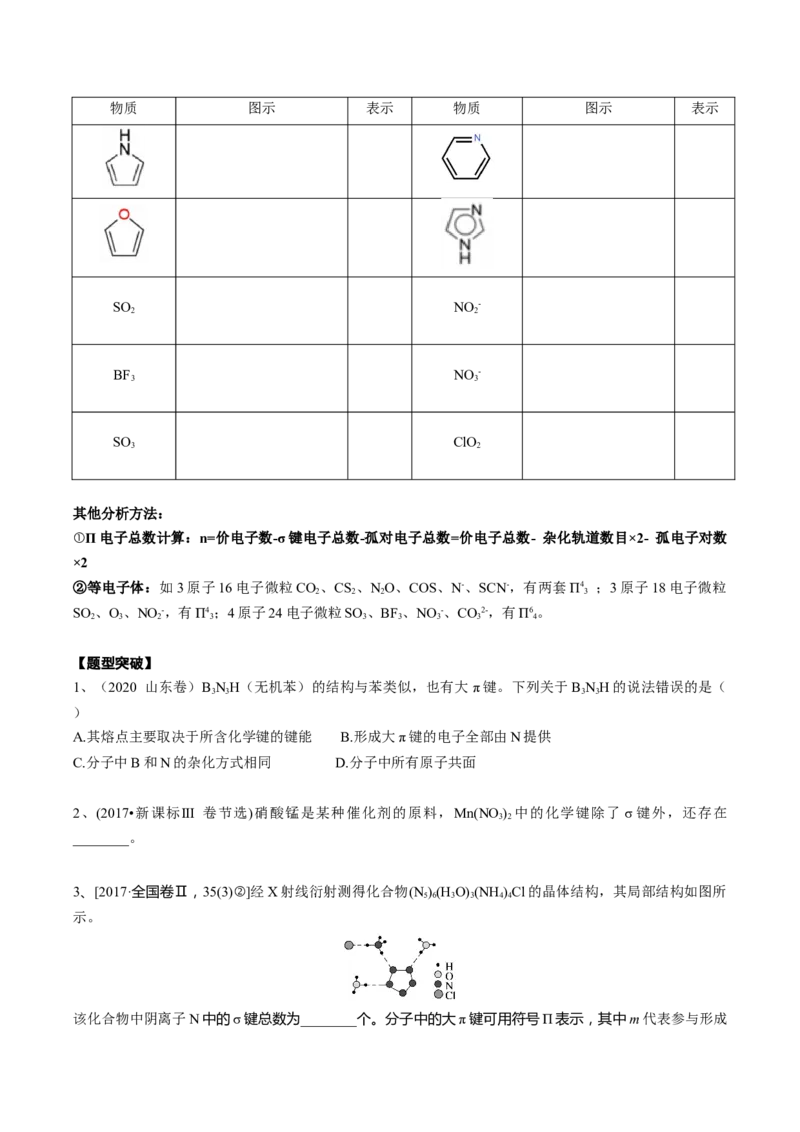
中心原子C采取 杂化,6个C原子具有一个含一
个孤电子的未参与杂化的2p轨道,它们是相互平行
的,形成 。
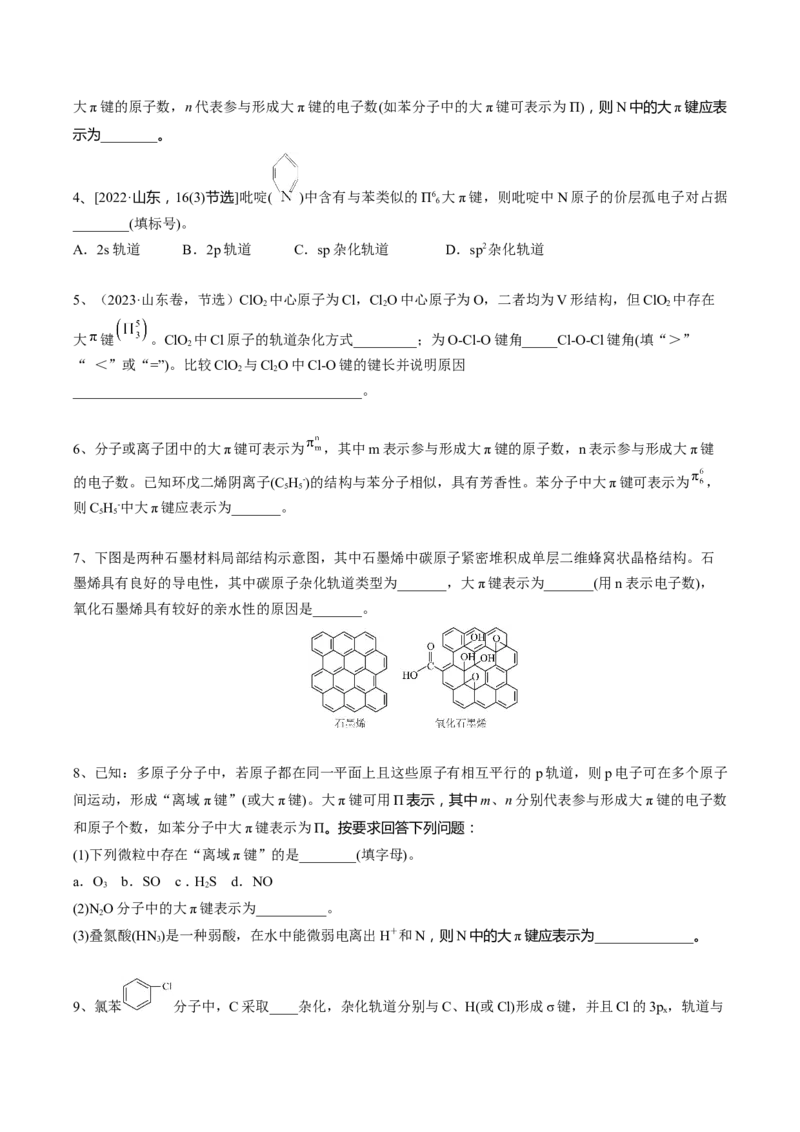
中心C原子采取 杂化,周围三个O原子的未成
CO2- 对电子的2pz轨道优先参与形成Π键,各提供一个2p
3
电子,再加上得到两个电子,即 。
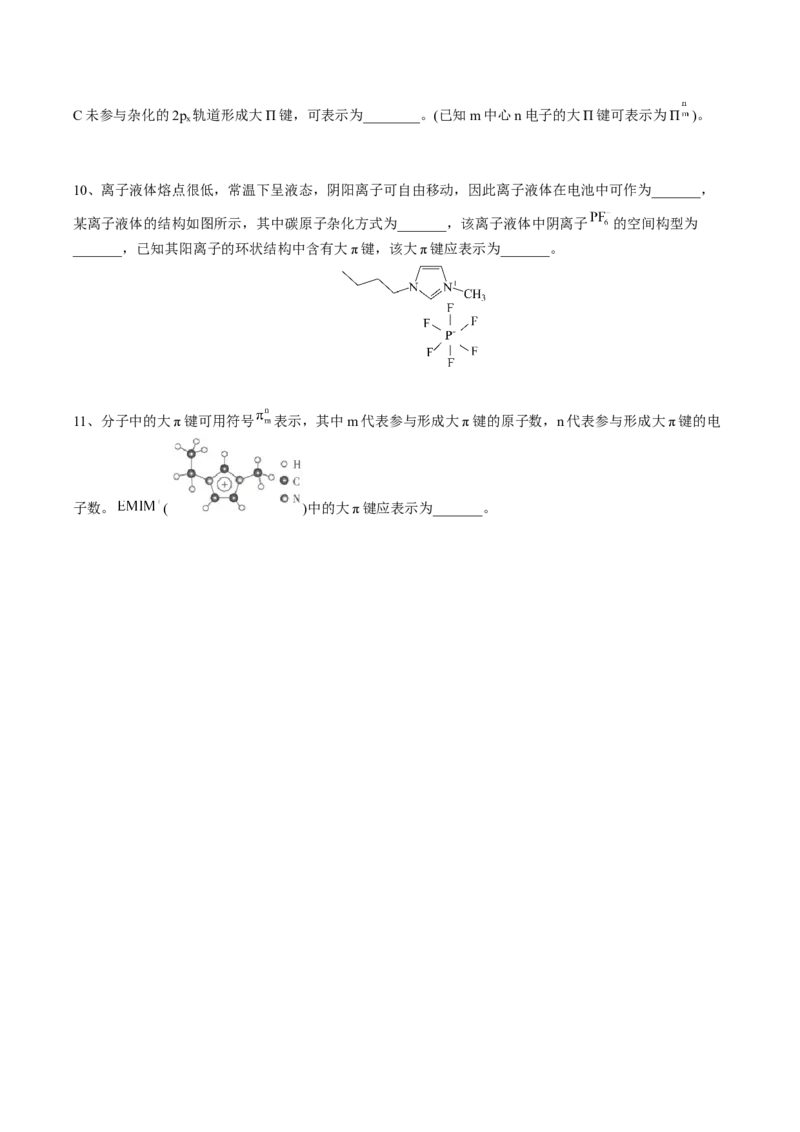
中心C原子采取 杂化,两个sp杂化轨道与O原
子的2p轨道成键,剩余的未参与杂化的有两个含1个
CO O C O O C O O C O 孤电子的2p轨道(2py、2pz),O原子也有暂未成键
2
的两个2p轨道对称性与其一致,故而可在y方向上和
z方向上均形成一个 。
例、用图示法表示下列物质的大π键物质 图示 表示 物质 图示 表示
SO NO -
2 2
BF NO -
3 3
SO ClO
3 2
其他分析方法:
①Π电子总数计算:n=价电子数-σ键电子总数-孤对电子总数=价电子总数- 杂化轨道数目×2- 孤电子对数
×2
②等电子体:如3原子16电子微粒CO 、CS 、NO、COS、N-、SCN-,有两套Π4 ;3原子18电子微粒
2 2 2 3
SO 、O、NO -,有Π4;4原子24电子微粒SO 、BF、NO -、CO2-,有Π6。
2 3 2 3 3 3 3 3 4
【题型突破】
1、(2020 山东卷)B NH(无机苯)的结构与苯类似,也有大 π键。下列关于B NH的说法错误的是(
3 3 3 3
)
A.其熔点主要取决于所含化学键的键能 B.形成大π键的电子全部由N提供
C.分子中B和N的杂化方式相同 D.分子中所有原子共面
2、(2017•新课标III 卷节选)硝酸锰是某种催化剂的原料,Mn(NO) 中的化学键除了 σ键外,还存在
3 2
________。
3、[2017·全国卷Ⅱ,35(3)②]经X射线衍射测得化合物(N )(H O) (NH )Cl的晶体结构,其局部结构如图所
5 6 3 3 4 4
示。
该化合物中阴离子N中的σ键总数为________个。分子中的大π键可用符号Π表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π),则N中的大π键应表
示为________。
4、[2022·山东,16(3)节选]吡啶( )中含有与苯类似的Π6 大π键,则吡啶中N原子的价层孤电子对占据
6
________(填标号)。
A.2s轨道 B.2p轨道 C.sp杂化轨道 D.sp2杂化轨道
5、(2023·山东卷,节选)ClO 中心原子为Cl,ClO中心原子为O,二者均为V形结构,但ClO 中存在
2 2 2
大 键 。ClO 中Cl原子的轨道杂化方式_________;为O-Cl-O键角_____Cl-O-Cl键角(填“>”
2
“ <”或“=”)。比较ClO 与ClO中Cl-O键的键长并说明原因
2 2
_________________________________________。
6、分子或离子团中的大π键可表示为 ,其中m表示参与形成大π键的原子数,n表示参与形成大π键
的电子数。已知环戊二烯阴离子(C H-)的结构与苯分子相似,具有芳香性。苯分子中大π键可表示为 ,
5 5
则C H-中大π键应表示为_______。
5 5
7、下图是两种石墨材料局部结构示意图,其中石墨烯中碳原子紧密堆积成单层二维蜂窝状晶格结构。石
墨烯具有良好的导电性,其中碳原子杂化轨道类型为_______,大π键表示为_______(用n表示电子数),
氧化石墨烯具有较好的亲水性的原因是_______。
8、已知:多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p电子可在多个原子
间运动,形成“离域π键”(或大π键)。大π键可用Π表示,其中m、n分别代表参与形成大π键的电子数
和原子个数,如苯分子中大π键表示为Π。按要求回答下列问题:
(1)下列微粒中存在“离域π键”的是________(填字母)。
a.O b.SO c.HS d.NO
3 2
(2)N O分子中的大π键表示为__________。
2
(3)叠氮酸(HN )是一种弱酸,在水中能微弱电离出H+和N,则N中的大π键应表示为______________。
3
9、氯苯 分子中,C采取____杂化,杂化轨道分别与C、H(或Cl)形成σ键,并且Cl的3p,轨道与
xC未参与杂化的2p 轨道形成大Π键,可表示为________。(已知m中心n电子的大Π键可表示为Π )。
x
10、离子液体熔点很低,常温下呈液态,阴阳离子可自由移动,因此离子液体在电池中可作为_______,
某离子液体的结构如图所示,其中碳原子杂化方式为_______,该离子液体中阴离子 的空间构型为
_______,已知其阳离子的环状结构中含有大π键,该大π键应表示为_______。
11、分子中的大π键可用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电
子数。 ( )中的大π键应表示为_______。