文档内容
2022 届高三化学二轮复习元素周期表 元素周期律专题练习
一、选择题(共17题)
1.下列对Na、Mg、Al的有关性质的叙述正确的是
A.原子半径:Na<Mg<Al B.碱性:NaOH>Mg(OH) >Al(OH)
2 3
C.金属性:Na<Mg<Al D.第一电离能:Na<Mg<Al
2.下列关于钠元素的几种表达式错误的是
A.Na+的电子排布图
B.Na+的结构示意图:
C.基态Na原子的电子排布式:1s22s22p53s2
D.基态Na原子的价电子排布式:3s1
3.W、Q、X、Y、Z属于周期表中前20号元素,且原子序数依次增大。W元素最外层电子数是次外层的
3倍,Q是所在周期中原子半径最大的元素,X是地壳中含量最高的金属元素,Y元素最高化合价与最低
化合价代数和为4,Z和Q同主族。下列判断正确的是
A.原子半径:r(Q)>r(X)>r(Y)>r(Z) B.简单氢化物的热稳定性:W<Y
C.最高价氧化物对应水化物的碱性:Q>X>Z D.Q、X、Y最高价氧化物对应水化物两两之间均能反
应
4.下列事实中,能说明氯原子得电子能力比硫原子强的是
①盐酸的酸性比氢硫酸(HS水溶液)酸性强 ②HCl的稳定性比HS大 ③Cl 与铁反应生成FeCl ,而S
2 2 2 3
与铁反应生成FeS ④Cl 能与HS反应生成S ⑤还原性:Cl-Y> W
B.Z的氧化物的水化物是强酸C.NaY的水溶液不能存放在玻璃试剂瓶中
D.X与Z具有相同的最高化合价
6.短周期元素的四种离子 、 、 、 都具有相同的电子层结构,下列说法错误的是
A.四种离子的质子数:
B.四种元素的电负性:Z>W>Y>X
C.四种离子的半径:
D.四种元素原子的最外层电子数目:W>Z>X>Y
7.下列对一些实验事实的理论解释正确的是
选项 实验事实 理论解释
深蓝色的[Cu(NH )]SO 溶液中加入乙醇析出
A 3 4 4 乙醇增强了溶剂的极性,降低晶体的溶解度
晶体
B 用KSCN检验溶液中的Fe3+ Fe3+遇SCN-生成血红色沉淀
C CH 熔点低于CO 碳氢键比碳氧键的键长短、键能大
4 2
D 氮原子的第一电离能大于氧原子 氮原子2p能级半充满
A.A B.B C.C D.D
8.X、Y、Z、Q、R 是五种短周期主族元素,原子序数依次增大。X、Y 最高正价与最低负价之和均为
0,Q与X同主族,Z的氧化物是大气的主要污染物之一,Z与R的最外层电子数之和为8,下列说法正确
的是
A.原子半径大小顺序为:R>Q>Z>Y>X
B.Y的氢化物的沸点一定低于Z的氢化物
C.Z、Q、R的最高价氧化物对应的水化物两两之间可以相互反应
D.元素Q、R分别与氯元素形成的化合物均为离子化合物
9.下列对碱金属性质叙述错误的是
A.都可以保存在煤油中
B.都可以与水反应产生氢气
C.它们的熔点比较低,导热性和导电性很好
D.随核电荷数增加电子层数也增加
10.主族元素M、X、Y、Z的原子序数依次增加,且均不大于20;M原子的最外层电子数与次外层电子
数之和为8;Y、Z是处于不同周期的金属元素;X、Y、Z原子最外层电子数之和为11。下列说法正确的是
A.简单离子半径:Y Z >X>W
C.W、Y组成的化合物中各微粒均达8电子稳定结构
D.最简单氢化物的稳定性:Z > X
12.下列叙述中,正确的是
A.1s电子云界面图是一个球面,电子云中的每个小黑点代表一个电子
B.NaH中的σ键是由两个原子的s、p轨道以“头碰头”方式重叠形成的
C.对于组成结构相似的分子,一定是相对分子质量越大,熔、沸点越高
D.在现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为光谱分析
13.甲~辛等元素在周期表中的相对位置如图所示。甲与戊的原子序数相差3,戊是空气中含量最多的元
素,丁与辛是同周期元素。下列说法正确的是( )
A.丙不能与水发生反应
B.己和氯气反应的产物只有一种
C.丙与庚的原子核外电子数相差13
D.乙形成的氧化膜疏松,不能保护内层金属
14.W、Q、Y和Z为短周期元素,它们在周期表中的位置如图所示,这4种元素的原子最外 层电子数之和为21。下列说法不正确的是
A.Q的原子半径比Y的大
B.Z的氧化物的水化物的酸性比WW的强
C.Y的氢化物可能具有强氧化性
D.Q与W或Y形成的化学键类型相同
15.下列说法不符合ⅦA族元素性质特征的是
A.易形成-1价离子 B.从上到下原子半径逐渐减小
C.从上到下非金属性逐渐减弱 D.从上到下氢化物的稳定性依次减弱
16.W、X、Y、Z均是短周期主族元素,X、Y、Z处于同一周期,W、X、Z的简单离子具有相同的电子
层结构,W的最高价氧化物对应的水化物与其氢化物能反应生成盐,X的氧化物既能溶于酸又能溶于碱,
Y的最高正价与最低负价的代数和为0。下列说法正确的是
A.离子半径:W>X>Z B.原子半径:Z>X>Y
C.单质的熔点:W>Z>Y D.最高正价:Z>W>X
17.原子序数依次递增的四种短周期元素可形成简单离子X2-、Y+、Z3+、M2-,下列说法错误的是
A.工业上常采用电解法冶炼Z单质
B.气态氢化物的稳定性:HX>HM
2 2
C.离子半径由大到小:M2->Y+>Z3+>X2-
D.X、Y形成的化合物中阳离子、阴离子个数比一定是2:1
二、综合题(共6题)
18.某小组探究元素周期律,甲根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一
次性完成N、C、Si的非金属性强弱比较的研究;乙根据置换反应的规律,利用下图装置完成O元素的非
金属性比S强的研究。回答:
(1)图中A装置名称是______________。(2)从以下所给物质中选出甲同学设计的实验所用到物质:
①稀HNO 溶液 ②稀盐酸 ③碳酸钙 ④NaSiO 溶液 ⑤SiO
3 2 3 2
试剂A与C分别为_________(填序号);试管中发生反应的离子方程式为_______________.有同学认为此实
验不能说明N、C、S的非金属性强弱,你认为原因是_________________
(3)乙同学设计的实验所用到试剂A为________;如果C试剂为硫化氢的水溶液,则试管中可以观察到的现
象为_______________
19.A、B、C、D是四种常见的有机物,其中,A是一种气态烃,在标准状况下的密度是1.25g/L,其产
量是衡量一个国家石油化工发展水平的标志之一;C的分子式为C HO;B和C在浓硫酸和加热的条件下
2 4 2
发生反应,生成的有机物有特殊的香味;A、B、C、D在一定条件下的转化关系如图所示(反应条件已省
略):
根据以上材料和你所学的化学知识回答下列问题:
(1)B中所含官能团名称________,C中所含官能团名称________
(2)丙烯酸(CH=CH—COOH)。的性质可能有(______)
2
①加成反应②取代反应③加聚反应④中和反应⑤氧化反应
a.只有①③
b.只有①③④
c.只有①③④⑤
d.①②③④⑤
(3)写出下列反应方程式
①A→B____________________________________________
反应类型为______________
②丙烯酸+B→丙烯酸乙酯___________________________
反应类型为_____________(4)聚丙烯酸的结构简式_____________,丙烯中最多有________个原子共面。
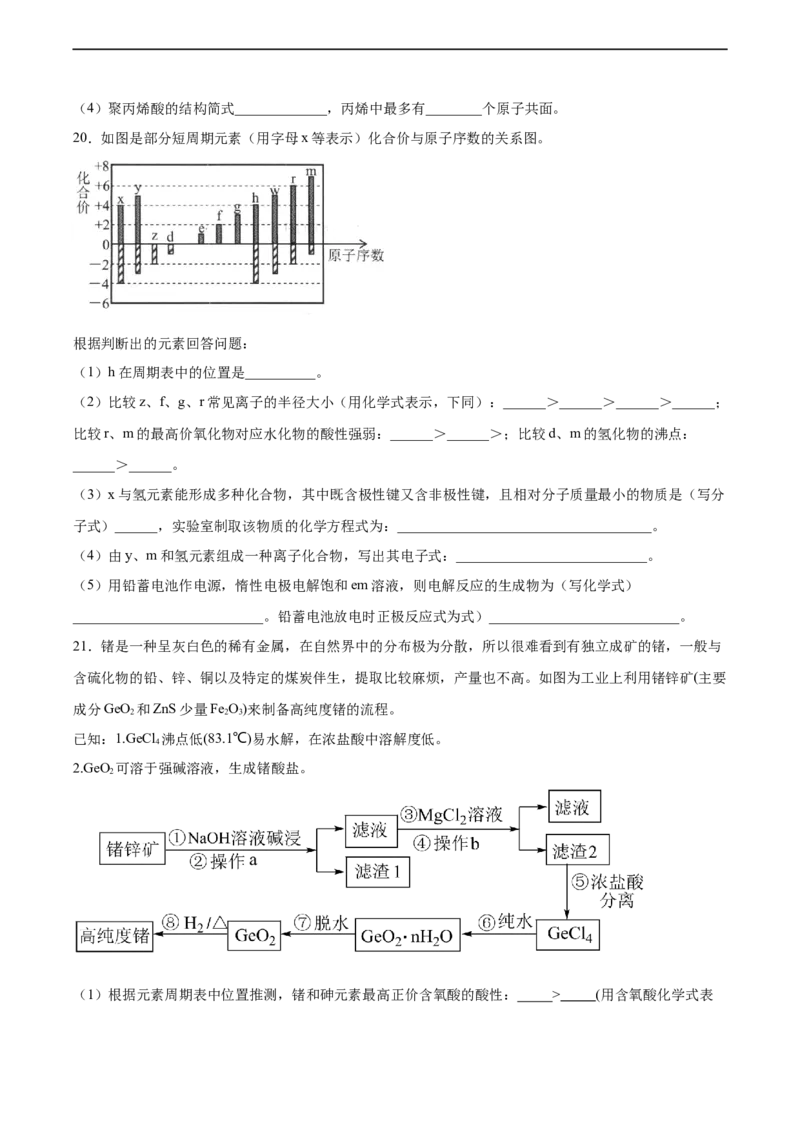
20.如图是部分短周期元素(用字母x等表示)化合价与原子序数的关系图。
根据判断出的元素回答问题:
(1)h在周期表中的位置是__________。
(2)比较z、f、g、r常见离子的半径大小(用化学式表示,下同):______>______>______>______;
比较r、m的最高价氧化物对应水化物的酸性强弱:______>______>;比较d、m的氢化物的沸点:
______>______。
(3)x与氢元素能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质是(写分
子式)______,实验室制取该物质的化学方程式为:____________________________________。
(4)由y、m和氢元素组成一种离子化合物,写出其电子式:___________________________。
(5)用铅蓄电池作电源,惰性电极电解饱和em溶液,则电解反应的生成物为(写化学式)
___________________________。铅蓄电池放电时正极反应式为式)___________________________。
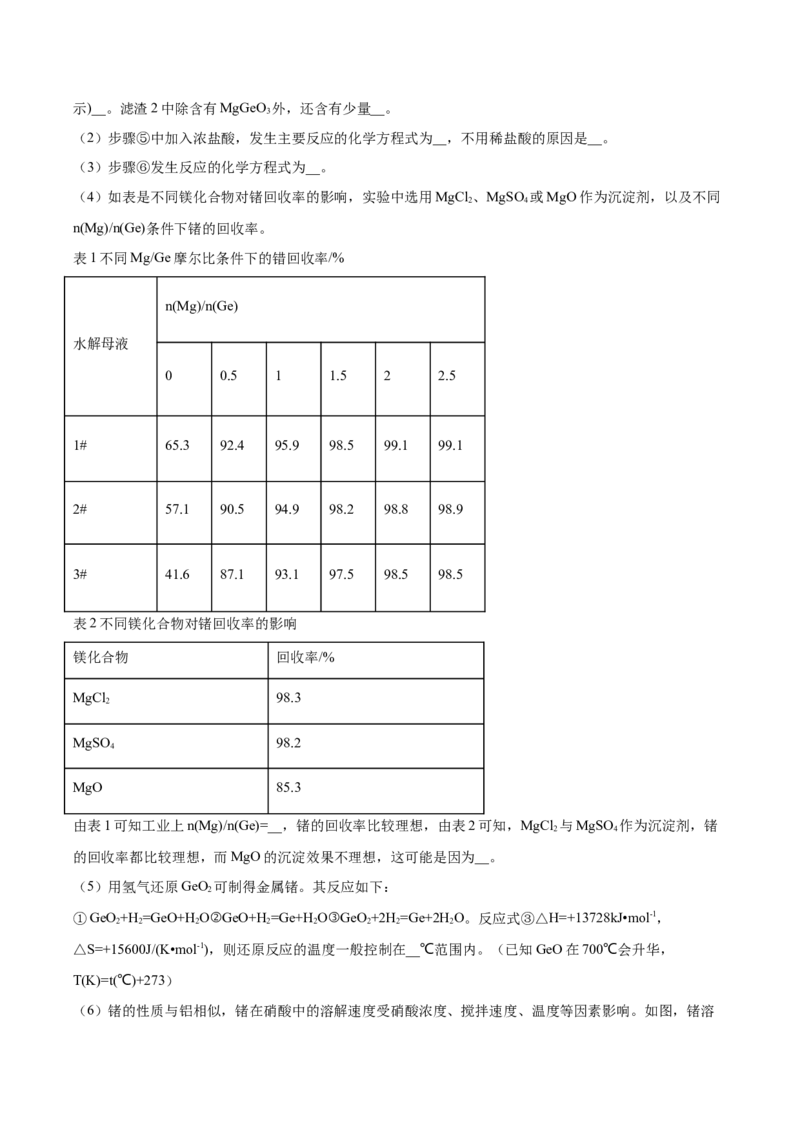
21.锗是一种呈灰白色的稀有金属,在自然界中的分布极为分散,所以很难看到有独立成矿的锗,一般与
含硫化物的铅、锌、铜以及特定的煤炭伴生,提取比较麻烦,产量也不高。如图为工业上利用锗锌矿(主要
成分GeO 和ZnS少量Fe O)来制备高纯度锗的流程。
2 2 3
已知:1.GeCl 沸点低(83.1℃)易水解,在浓盐酸中溶解度低。
4
2.GeO 可溶于强碱溶液,生成锗酸盐。
2
(1)根据元素周期表中位置推测,锗和砷元素最高正价含氧酸的酸性: > (用含氧酸化学式表示)__。滤渣2中除含有MgGeO 外,还含有少量__。
3
(2)步骤⑤中加入浓盐酸,发生主要反应的化学方程式为__,不用稀盐酸的原因是__。
(3)步骤⑥发生反应的化学方程式为__。
(4)如表是不同镁化合物对锗回收率的影响,实验中选用MgCl 、MgSO 或MgO作为沉淀剂,以及不同
2 4
n(Mg)/n(Ge)条件下锗的回收率。
表1不同Mg/Ge摩尔比条件下的错回收率/%
n(Mg)/n(Ge)
水解母液
0 0.5 1 1.5 2 2.5
1# 65.3 92.4 95.9 98.5 99.1 99.1
2# 57.1 90.5 94.9 98.2 98.8 98.9
3# 41.6 87.1 93.1 97.5 98.5 98.5
表2不同镁化合物对锗回收率的影响
镁化合物 回收率/%
MgCl 98.3
2
MgSO 98.2
4
MgO 85.3
由表1可知工业上n(Mg)/n(Ge)=__,锗的回收率比较理想,由表2可知,MgCl 与MgSO 作为沉淀剂,锗
2 4
的回收率都比较理想,而MgO的沉淀效果不理想,这可能是因为__。
(5)用氢气还原GeO 可制得金属锗。其反应如下:
2
①GeO +H =GeO+H O②GeO+H =Ge+H O③GeO +2H =Ge+2H O。反应式③△H=+13728kJ•mol-1,
2 2 2 2 2 2 2 2
△S=+15600J/(K•mol-1),则还原反应的温度一般控制在__℃范围内。(已知GeO在700℃会升华,
T(K)=t(℃)+273)
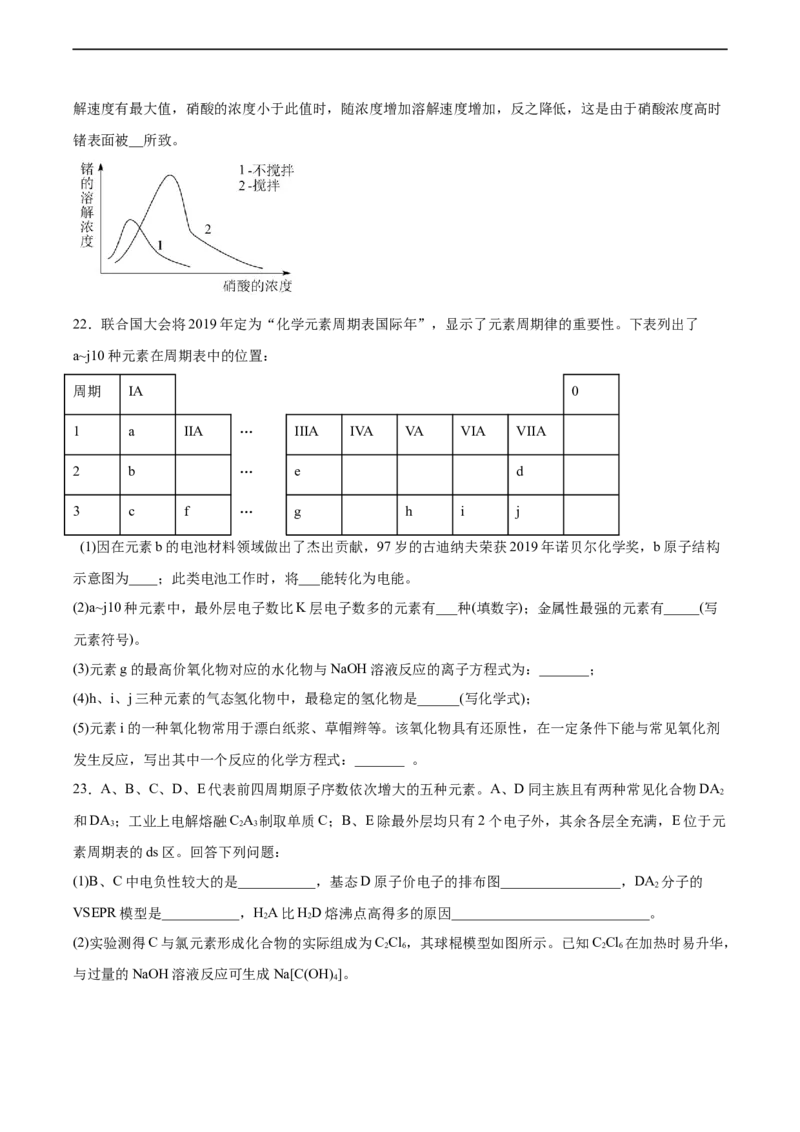
(6)锗的性质与铝相似,锗在硝酸中的溶解速度受硝酸浓度、搅拌速度、温度等因素影响。如图,锗溶解速度有最大值,硝酸的浓度小于此值时,随浓度增加溶解速度增加,反之降低,这是由于硝酸浓度高时
锗表面被__所致。
22.联合国大会将2019年定为“化学元素周期表国际年”,显示了元素周期律的重要性。下表列出了
a~j10种元素在周期表中的位置:
周期 IA 0
1 a IIA … IIIA IVA VA VIA VIIA
2 b … e d
3 c f … g h i j
(1)因在元素b的电池材料领域做出了杰出贡献,97岁的古迪纳夫荣获2019年诺贝尔化学奖,b原子结构
示意图为____;此类电池工作时,将___能转化为电能。
(2)a~j10种元素中,最外层电子数比K层电子数多的元素有___种(填数字);金属性最强的元素有_____(写
元素符号)。
(3)元素g的最高价氧化物对应的水化物与NaOH溶液反应的离子方程式为:_______;
(4)h、i、j三种元素的气态氢化物中,最稳定的氢化物是______(写化学式);
(5)元素i的一种氧化物常用于漂白纸浆、草帽辫等。该氧化物具有还原性,在一定条件下能与常见氧化剂
发生反应,写出其中一个反应的化学方程式:_______ 。
23.A、B、C、D、E代表前四周期原子序数依次增大的五种元素。A、D同主族且有两种常见化合物DA
2
和DA ;工业上电解熔融C A 制取单质C;B、E除最外层均只有2个电子外,其余各层全充满,E位于元
3 2 3
素周期表的ds区。回答下列问题:
(1)B、C中电负性较大的是___________,基态D原子价电子的排布图_________________,DA 分子的
2
VSEPR模型是___________,HA比HD熔沸点高得多的原因____________________________。
2 2
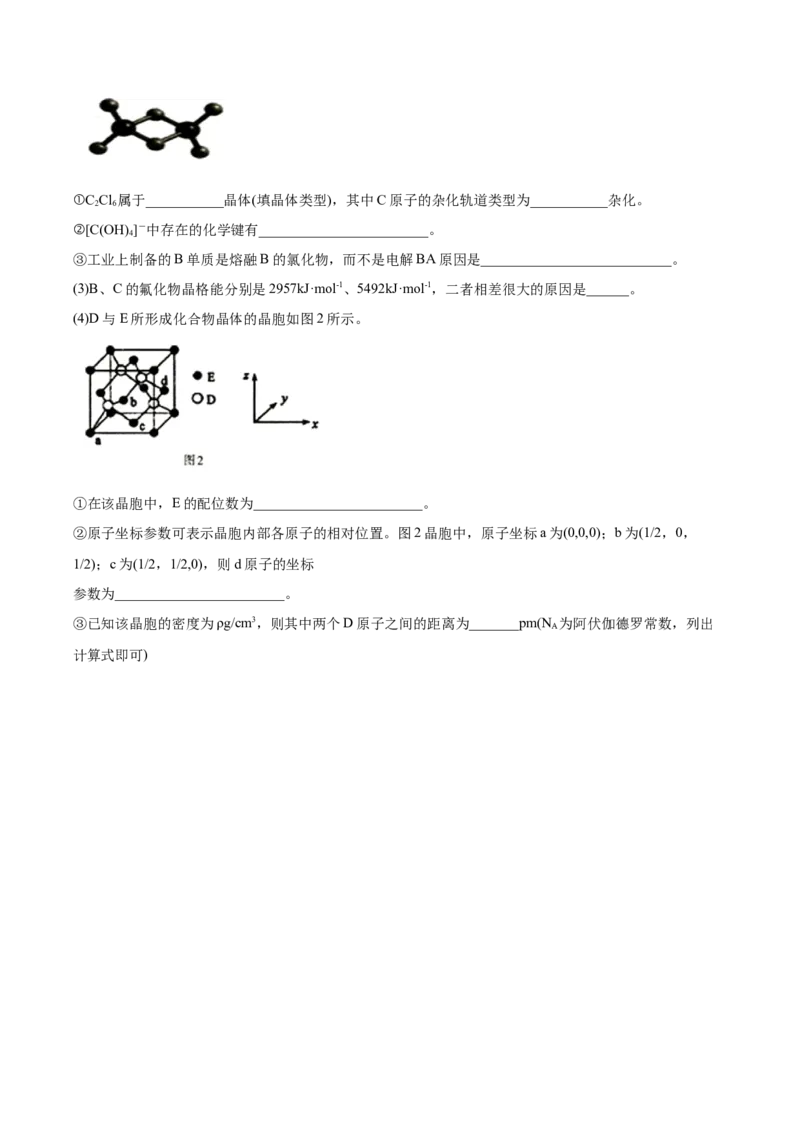
(2)实验测得C与氯元素形成化合物的实际组成为C Cl,其球棍模型如图所示。已知C Cl 在加热时易升华,
2 6 2 6
与过量的NaOH溶液反应可生成Na[C(OH) ]。
4①C Cl 属于___________晶体(填晶体类型),其中C原子的杂化轨道类型为___________杂化。
2 6
②[C(OH) ]-中存在的化学键有________________________。
4
③工业上制备的B单质是熔融B的氯化物,而不是电解BA原因是___________________________。
(3)B、C的氟化物晶格能分别是2957kJ·mol-1、5492kJ·mol-1,二者相差很大的原因是______。
(4)D与E所形成化合物晶体的晶胞如图2所示。
①在该晶胞中,E的配位数为________________________。
②原子坐标参数可表示晶胞内部各原子的相对位置。图2晶胞中,原子坐标a为(0,0,0);b为(1/2,0,
1/2);c为(1/2,1/2,0),则d原子的坐标
参数为________________________。
③已知该晶胞的密度为ρg/cm3,则其中两个D原子之间的距离为_______pm(N 为阿伏伽德罗常数,列出
A
计算式即可)参考答案
1.B
【详解】
A.同周期主族元素自左至右原子半径依次减小,所以原子半径Na>Mg>Al,故A错误;
B.非金属性越强最高价氧化物对应的水化物的碱性越强,金属性Na>Mg>Al,所以碱性:
NaOH>Mg(OH) >Al(OH) ,故B正确;
2 3
C.同周期元素自左至右金属性减弱,所以金属性Na>Mg>Al,故C错误;
D.同周期元素第一电离能自左至右呈增大趋势,但Mg原子最外层为全满状态,第一电离
能大于相邻元素,所以第一电离能:NaAl > C > N > H,A错误;
B.Y的氢化物碳原子数可能比较多,常温的时候可能为固态,沸点较大,B错误;
C.Z、Q、R的最高价氧化物对应的水化物分别为硝酸,氢氧化钠,氢氧化铝,这些物质
两两之间可以相互反应,C正确;
D.AlCl 为共价化合物,不是离子化合物,D错误;
3
故选C。
9.A
【详解】
A.锂的密度小于煤油,浮在煤油表面,不能隔绝空气,故A错误;B.碱金属均为活泼金
属,能与水反应生成氢气,故B正确;C.碱金属的熔点均较低,有良好的导电和导热性,
故C正确;D.碱金属随着原子序数的增加,原子核外电子层数增加,故D正确;故选
A。
10.B
【分析】
主族元素M、X、Y、Z的原子序数依次增加,且均不大于20;M原子的最外层电子数与
次外层电子数之和为8,则M含有2个 电子层,最外层含有6个电子,为O元素;Y、Z
是处于不同周期的金属元素,二者原子序数大于O,则Y、Z分别位于第三、第四周期;Y
只能为Na、Mg、Al的一种,X的原子序数大于O小于Y,则X为F元素;X、Y、Z原子
最外层电子数之和为11,X、Y的最外层电子数之和为11-7=4,若X为Mg,则Y为Ca元
素,若X为Al,则Y为K,据此解答。
【详解】
根据分析可知:M为O,X为F,Y为Mg或Al,Z为Ca或K。A. 氧离子、氟离子、镁离子(铝离子)都含有2个电子层,核电荷数越大离子半径越小,
则离子半径Y S>O>H,故B正确;
C.H、Na组成的化合物为NaH,氢离子最外层电子数为2,没有达到8电子稳定结构,故C
错误;
D.元素的非极性越强,最简单氢化物的稳定性越强,氧元素的非金属性强于硫元素,则水
的稳定性强于硫化氢,故D错误;
故选B。
12.D
【解析】
试题分析:A、小黑点代表电子某时刻在此经过,故错误;B、NaH属于离子化合物,没有
共价键,故错误;C、还要看是否含有分子间氢键,如HO和HS,结构相似,但HO含
2 2 2
有分子间氢键,因此HO的熔沸点比HS高,故错误;D、原子光谱和元素一一对应,故
2 2
正确。
考点:考查电子云、共价键、熔沸点高低等知识。
13.C
【详解】
戊是空气中含量最多的元素,则戊是N元素,甲与戊的原子序数相差3,则甲是Be,可推
知乙是Mg,丙是Ca,丁是Sc元素,戊是N,己是P,庚是As,辛是Ge。
A.丙是Ca,Ca是活泼的金属,能够与水反应产生Ca(OH) 和H,A错误;
2 2
B.己是P,P与Cl 反应产生PCl 、PCl ,产物不只有一种,B错误;
2 3 5
C.丙是Ca,原子序数是20,庚是As,原子序数是33,二者的原子序数差为33-20=13,C
正确;D.乙是Mg,乙形成的氧化膜MgO非常致密,能对内层的金属起保护作用,D错误;
故合理选项是C。
14.B
【解析】
【分析】
设元素Q的原子最外层电子数为x,可得方程式为:x+x+x+2+x+3=21,解得x=4。W、
Q、Y和Z为短周期元素,则W、Y、Q、Z分别为C、O、Si、Cl,据此答题。
【详解】
A.Y、Q分别为O、Si,周期数越大,元素电子层数越多,原子半径越大,所以Si的原子
半径比O的大,故A正确;
B.应描述为最高价氧化物对应水化物的酸性,不是最高价氧化物,则不一定,如碳酸酸性
比次氯酸酸性强,故B错误;
C.O的氢化物为HO或HO,若为HO,具有强氧化性,故C正确;
2 2 2 2 2
D.O与Si形成的化合物为SiO,所含化学键为共价键,O与C形成的化合物为CO,所含
2 2
化学键为共价键,类型相同,故D正确。
故选B。
15.B
【详解】
A.因ⅦA族元素最高正价为+7价,则最低价为7−8=−1价,最外层为7个电子,易得到
一个电子,达到稳定结构,即易形成−1价离子,故A符合ⅦA族元素性质特征;
B.ⅦA族元素从上到下电子层数增多,则原子半径增大,故B不符合ⅦA族元素性质特
征;
C.ⅦA族元素从上到下得电子的能力减弱,则非金属性逐渐减弱,故C符合ⅦA族元素
性质特征;
D.ⅦA族元素从上到下非金属性减弱,则对应的氢化物的稳定性依次减弱,故D符合
ⅦA族元素性质特征;
答案选B。
16.B
【详解】
试题分析:W、X、Y、Z均是短周期主族元素,W的最高价氧化物对应的水化物与其氢化
物能反应生成盐,则W为N元素;X的氧化物既能溶于酸又能溶于碱,则X为Al;X、
Y、Z处于同一周期,即均处于第三周期,Y的最高正价与最低负价的代数和为0,Y为Si
元素;W、X、Z的简单离子具有相同的电子层结构,则Z为Na或Mg。A.电子层结构相
同,核电荷数越大离子半径越小,离子半径:W>Z>X,A项错误;B.同周期自左而右
原子半径减小,原子半径,Z>X>Y,B项正确;C.W单质为氮气,属于分子晶体,Z单
质为Na或Mg,Y单质为原子晶体,熔点Y>Z>W,C项错误;D.Z的最高正价为+1或
+2,W的最高正价为+5,X的最高正价为+3,最高正价:W>X>Y,D项错误;答案选B。
【考点定位】考查元素的推断,元素周期律的应用等知识。
17.C
【解析】A.Z为Al元素,常用电解熔融的氧化铝的方法制备铝,故A正确;B.元素的
非金属性越强,其氢化物越稳定,非金属性:O大于S,则气态氢化物的稳定性:HO强
2
于HS,故B正确;C.电子层数越多离子半径越大,电子排布相同的离子,原子序数越大,
2
离子半径越小,所以S2->O2->Na+>Al3+,则Y2->X2->Y+>M3+,故C错误;D.X、Y
形成的化合物为NaO或NaO,阴、阳离子个数比一定是1∶2,故D正确;故选C。
2 2 2
18.分液漏斗 ①④ CO+H O+ =H SiO+ HNO 有挥发性也会和硅酸
2 2 2 3 3
钠反应生成硅酸 双氧水 有淡黄色浑浊出现
【分析】
甲的思路:A中放N的最高价含氧酸的水溶液即稀硝酸,B中放碳酸钙,稀硝酸和碳酸钙
反应产生碳酸,碳酸分解产生二氧化碳进入右侧试管中,右侧试管中发生二氧化碳、水和
硅酸钠反应产生白色的胶状硅酸沉淀,即看到右侧试管中出现白色胶状沉淀,说明酸性:
硝酸>碳酸>硅酸,证明非金属性:N>C>Si;
乙的思路:A中放过氧化氢,B中放MnO ,过氧化氢和二氧化锰反应产生氧气,C中放硫
2
化氢的水溶液,氧气和硫化氢在右侧试管中反应产生淡黄色浑浊物,证明氧气置换出了硫
化氢中的S,证明非金属性:O>S,据此解答。
【详解】
(1)由仪器的结构特征,可知A为分液漏斗;
(2)探究元素非金属性,由图可知应是利用最高价含氧酸的酸性强弱比较,所以A中试剂为
稀硝酸,B中为碳酸钙,C中为NaSiO 溶液;试管中为NaSiO 溶液中通CO 生成硅酸白
2 3 2 3 2
色沉淀,发生反应的离子方程式为CO+H O+ =H SiO+ ;通入试管中的CO 气体
2 2 2 3 2
中混有挥发性的硝酸,硝酸也能与硅酸钠溶液反应生成硅酸,无法确定CO 是否与与硅酸
2
钠溶液反应,即不能说明N、C、S的非金属性强弱;
(3)乙同学欲证明氧的非金属性比硫强,需要通过实验证明氧气能制取硫单质来实现,则试
剂A为HO,在MnO 催化作用下分解生成氧气;生成的氧气通入盛有硫化氢的水溶液中,
2 2 2
有淡黄色浑浊出现,说明有硫生成,O的非金属性强于S。
19.羟基 羧基 d CH =CH +HO CHCHOH 加成反应
2 2 2 3 2
取代(酯化)反应
7
【详解】
A、B、C、D是四种常见的有机物,其中A是一种气态烃,在标准状况下的密度是1.25g/L,其产量是衡量一个国家石油化工发展水平的标志之一,所以A是乙烯;乙烯和水
发生加成反应生成B是乙醇,C的分子式为C HO,这说明乙醇被酸性高锰酸钾氧化生成
2 4 2
乙酸,即C是乙酸,B和C在浓硫酸和加热的条件下发生反应,生成的有机物有特殊的香
味,D是乙酸乙酯;则
(1)乙醇中所含官能团名称为羟基,乙酸中所含官能团名称为羧基;(2)丙烯酸含有碳
碳双键,可发生加成反应、加聚反应和氧化反应,含有羧基,可发生取代反应、中和反应,
答案选d;(3)①根据以上分析可知A→B是乙烯和水的加成反应,方程式为CH=CH +
2 2
HO CHCHOH;②丙烯酸和乙醇发生酯化反应生成丙烯酸乙酯,方程式为
2 3 2
CH=CHCOOH+CH CHOH CH=CHCOOCH CH+H O;(4)丙烯酸发生加聚反应生
2 3 2 2 2 3 2
成聚丙烯酸,结构简式为 。碳碳双键是平面形结构,又因为单键可以旋
转,所以丙烯中最多有7个原子共面。
20.第三周期第ⅣA族 S2- O2- Mg2+ Al3+ HClO H SO HF
4 2 4
HCl C H CaC + 2H O→CH≡CH↑+ Ca(OH) NaOH、
2 2 2 2 2
H、Cl PbO +4H++SO2--2e-=2H O+PbSO
2 2 2 4 2 4
【分析】
根据元素的化合价与原子序数的关系图可知,x、y、z、d为第二周期元素,e、f、g、h、
w、r、m为第三周期元素,则e为Na元素、f为Mg元素、g为Al元素、h为Si元素、w
为P元素、r为S元素、m为Cl元素;z、d只有负价,没有正价,z为O元素、d为F元素,
则x为C元素、y为N元素。结合元素周期律分析解答。
【详解】
根据上述分析,x为C元素、y为N元素、z为O元素、d为F元素、e为Na元素、f为Mg
元素、g为Al元素、h为Si元素、w为P元素、r为S元素、m为Cl元素。
(1)h为Si元素,在周期表中位于第三周期第ⅣA族,故答案为第三周期第ⅣA族;
(2)一般而言,电子层数越多,半径越大,电子层数相同,原子序数越大,半径越小,则
z、f、g、r常见离子的半径大小为S2->O2->Mg2+>Al3+;非金属性越强,最高价氧化物对
应水化物的酸性越强,r、m的最高价氧化物对应水化物的酸性HClO>HSO ;HF分子间
4 2 4
能够形成氢键,沸点较高,d、m的氢化物的沸点HF>HCl,故答案为S2-;O2-;Mg2+;
Al3+;HClO;HSO ;HF;HCl;
4 2 4
(3)x与氢元素能形成的化合物为烃类,其中既含极性键又含非极性键,且相对分子质量最
小的物质是乙炔,实验室用电石与水反应制取乙炔,反应的化学方程式为CaC +
2
2HO→CH≡CH↑+ Ca(OH) ,故答案为C H;CaC + 2H O→CH≡CH↑+ Ca(OH) ;
2 2 2 2 2 2 2
(4)由y、m和氢元素组成一种离子化合物为氯化铵, 氯化铵属于离子化合物,铵根离子中存在共价键,电子式为 ,故答案为 ;
(5)用铅蓄电池作电源,惰性电极电解饱和NaCl溶液,反应的方程式为2NaCl+2HO
2
2NaOH+H↑+Cl↑;铅蓄电池放电时,PbO 为正极,电极反应式为PbO +4H++SO2--2e-
2 2 2 2 4
=2H O+PbSO ,故答案为NaOH、H、Cl;PbO +4H++SO2--2e-=2H O+PbSO 。
2 4 2 2 2 4 2 4
21.
(1) HAsO >H GeO Mg(OH)
3 4 2 3 2
(2) MgGeO +6HCl(浓)=MgCl +GeCl +3H O HCl浓度大可抑制四价锗水解,获得
3 2 4 2
GeCl 沉淀
4
(3)GeCl +(2+n)H O=GeO •H O+4HCl
4 2 2 2
(4) 1.5 MgCl 与MgSO 在水溶液中都可以电离出Mg2+,而MgO则不能
2 4
(5)607~700
(6)钝化
【分析】
酸浸锗锌矿(主要成分GeO 和ZnS少量Fe O),碱浸出液中含有四价锗和氢氧化钠,滤渣1
2 2 3
为Fe O、ZnS,滤液中氯化镁溶液,滤渣2得到含有Ge的沉淀和氢氧化镁,将沉淀
2 3
MgGeO 到用浓盐酸溶解生成GeCl ,GeCl 在浓盐酸中溶解度低,过滤后得到GeCl ,
3 4 4 4
GeCl 在纯水中水解生成GeO ·nH O,GeO ·nH O既水后再次得到GeO ,用氢气加热还原
4 2 2 2 2 2
GeO 得到高纯度Ge,以此来解析;
2
(1)
砷是第四周期第V A族,锗在第四周期第IV A,非金属性砷大于锗HASO > H GeO 碱浸
3 4 2 4
过程加氢氧化钠,MgGeO 外,还含有少量Mg(OH) ;
3 2
(2)
MgGeO +6HC1(浓)=MgC1 +GeC1 +3H O,HC1浓度大可抑制四价锗水解,同时GeCl 在浓
3 2 4 2 4
盐酸中溶解度低,易获得GeCl 沉定;
4
(3)
GeCl 和纯水反应生成GeO ·nH O,反应的化学方程式为:
4 2 2
GeCl +(2+n)H O=GeO ·nH O+4HC1;
4 2 2 2
(4)
当Mg / Ge摩尔比达到1.5时,锗的回收率比较理想,继续增加Mg / Ge摩尔比对锗回收率
的影响不是非常明显因此,将Mg /Ge摩尔比确定为1.5. MgC1 与MgSO 在水溶液中都可
2 4
以电离出Mg2+,而MgO则不能;
(5)
使还原反应进行,反应③ΔG=ΔH-TΔS= +13728kJ/ mol-15.6kJ/(K•mol-1)T<0,T > 880K,即
温度高于880- 273 = 607℃,由于GeO在700C会升华,所以还原反应的温度一船控制在
607C~ 700C范围内;(6)
Ge与A1在周期表中处于对角线,Ge 的性质与A1相似,HNO 浓度高时,Ge 的溶解速率
3
随浓度增加而降低,这是由于HNO 浓度高时钝化加剧所致;
3
22. 化学 6 Na Al(OH) +OH-= AlO -+2H O HCl 2SO +O
3 2 2 2 2
2SO 或SO +Cl+2H O=HSO +2HCl等
3 2 2 2 2 4
【分析】
根据元素周期表可得元素a:H、b:Li、c:Na、d:F、e:B、f:Mg、g:Al、h:P、i:
S、j:Cl。
【详解】
(1) b为Li,核电荷数和核外电子数是3,所以原子结构示意图为 ;锂电池工作时,
是原电池,原电池将化学能转化为电能。
(2) K层有2个电子,最外层电子数比K层电子数多的元素有F、B、Al、P、S、Cl,共有6
种;同周期元素金属性从左到右逐渐减弱,同主族元素从上到下金属性逐渐增强,所以金
属性最强的元素是Na;
(3) 元素g的最高价氧化物对应的水化物是Al(OH) ,Al(OH) 是两性氢氧化物,与碱反应
3 3
生成盐和水,所以与NaOH溶液反应的离子方程式为Al(OH) +OH-= AlO -+2H O;
3 2 2
(4)h、i、j三种元素的气态氢化物为PH 、HS、HCl,同周期元素非金属性从左到右逐渐增
3 2
强,非金属性越强,氢化物越稳定,最稳定的氢化物是HCl;
(5)元素i的一种氧化物SO 常用于漂白纸浆、草帽辫等。SO 具有还原性,能与氧化剂反应,
2 2
如:2SO +O 2SO 或SO +Cl+2H O=HSO +2HCl等。
2 2 3 2 2 2 2 4
23.铝(或Al) 平面三角形 水分子间存在氢键 分子 sp3
极性共价键、配位键(或共价键、配位键) 熔融MgCl 融能导电,可电解;MgO熔点高,
2
电解能耗大 Al3+比Mg2+电荷高、半径小,AlF 的晶格能比MgCl 大得多 4 (1,
3 2
1/2,1/2) × ×1010
【分析】
A、B、C、D、E代表前四周期原子序数依次增大的五种元素。A、D同主族且有两种常见
化合物DA 和DA ,因此A是O,D是S;工业上电解熔融C A 制取单质C,则C是Al;
2 3 2 3
B、E除最外层均只有2个电子外,其余各层全充满,E位于元素周期表的ds区,因此B是Mg,E是Zn。
【详解】
(1)同周期自左向右金属性逐渐减弱,金属性越强,则电负性越小,则Al的电负性大于
Mg;基态S原子价电子排布式为3s23d4,其排布图为 ;SO 分子中价层电
2
子对数是2+ (6-2×2)=3,所以其VSEPR模型是平面三角形;由于HO分子间存在氢键,
2
HS分子间存在范德华力,因此HO比HS熔沸点高得多;
2 2 2
(2)①Al Cl 的熔沸点较低,易升华,属于分子晶体;其中Al原子形成4个共价键,杂化轨
2 6
道类型为sp3杂化;
②[Al(OH)]-中存在的化学键有O-H间的极性共价键、Al-O间的配位键;
4
③由于熔融MgCl 能导电,可电解,但MgO熔沸点高,电解熔融MgO能耗大,所以工业
2
上制备Mg的单质是电解熔融氯化镁,而不是电解氧化镁;
(3)Al3+比Mg2+电荷多、半径小,形成的离子键键能大,则AlF 的晶格能比MgCl 大得多;
3 2
(4)①在该晶胞中,Zn的周围最近且距离相等的S原子有4个,则锌的配位数为4;
②根据晶胞结构可知d原子位于右侧面心处,所以坐标参数为(0,1/2,1/2);
③该晶胞中S和Zn的原子个数均是4个,晶胞的密度为ρ g/cm3,则晶胞的边长是
cm。两个S原子之间的距离为面对角线的一半,即为 × cm= ×
×1010pm。