文档内容
专项提能特训 8 有关“元素推断实验探究”的综合考察
1.X、Y和W为原子序数依次递增的短周期元素,X和Y同主族,Y和W的气态氢化物具
有相同的电子数,X的单质只有氧化性。
(1)写出实验室制取W 反应的离子方程式:__________________________________________。
2
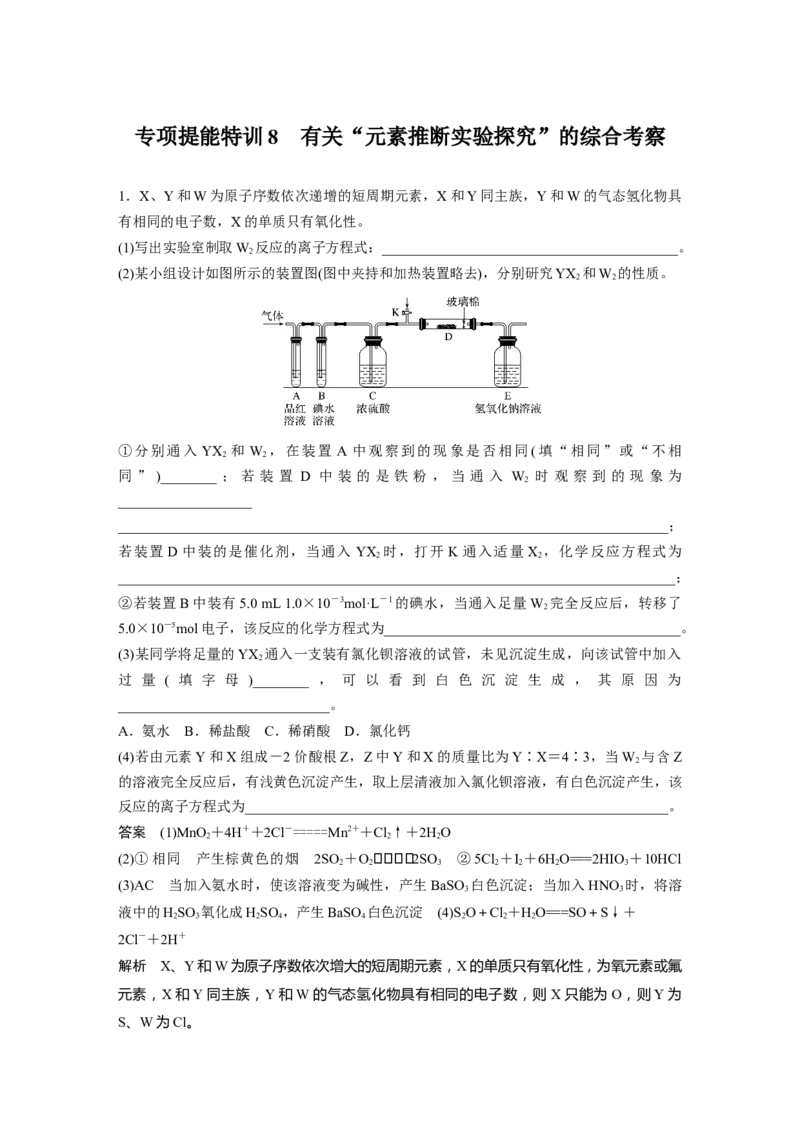
(2)某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究YX 和W 的性质。
2 2
①分别通入 YX 和 W ,在装置 A 中观察到的现象是否相同(填“相同”或“不相
2 2
同 ” )________ ; 若 装 置 D 中 装 的 是 铁 粉 , 当 通 入 W 时 观 察 到 的 现 象 为
2
___________________
______________________________________________________________________________;
若装置 D 中装的是催化剂,当通入 YX 时,打开 K 通入适量 X ,化学反应方程式为
2 2
_______________________________________________________________________________;
②若装置B中装有5.0 mL 1.0×10-3mol·L-1的碘水,当通入足量W 完全反应后,转移了
2
5.0×10-5mol电子,该反应的化学方程式为__________________________________________。
(3)某同学将足量的YX 通入一支装有氯化钡溶液的试管,未见沉淀生成,向该试管中加入
2
过 量 ( 填 字 母 )________ , 可 以 看 到 白 色 沉 淀 生 成 , 其 原 因 为
______________________________。
A.氨水 B.稀盐酸 C.稀硝酸 D.氯化钙
(4)若由元素Y和X组成-2价酸根Z,Z中Y和X的质量比为Y∶X=4∶3,当W 与含Z
2
的溶液完全反应后,有浅黄色沉淀产生,取上层清液加入氯化钡溶液,有白色沉淀产生,该
反应的离子方程式为____________________________________________________________。
答案 (1)MnO +4H++2Cl-=====Mn2++Cl↑+2HO
2 2 2
(2)①相同 产生棕黄色的烟 2SO +O2SO ②5Cl +I +6HO===2HIO +10HCl
2 2 3 2 2 2 3
(3)AC 当加入氨水时,使该溶液变为碱性,产生BaSO 白色沉淀;当加入HNO 时,将溶
3 3
液中的HSO 氧化成HSO ,产生BaSO 白色沉淀 (4)S O+Cl+HO===SO+S↓+
2 3 2 4 4 2 2 2
2Cl-+2H+
解析 X、Y和W为原子序数依次增大的短周期元素,X的单质只有氧化性,为氧元素或氟
元素,X和Y同主族,Y和W的气态氢化物具有相同的电子数,则 X只能为O,则Y为
S、W为Cl。(1)实验室通常用二氧化锰与浓盐酸在加热的条件下制备氯气,反应的离子方程式为 MnO +
2
4H++2Cl-=====Mn2++Cl↑+2HO。(2)①二氧化硫与品红化合生成无色物质,氯气与水
2 2
反应生成次氯酸,次氯酸具有强氧化性,将品红氧化为无色物质,二氧化硫与氯气都可以使
品红溶液褪色,在装置A中观察到的现象相同;氯气与铁反应产生棕黄色的烟;二氧化硫
在催化剂、加热条件下与氧气反应生成三氧化硫,反应的化学方程式为 2SO +
2
O2SO 。
2 3
②若装置B中装有5.0 mL 1.0×10-3mol·L-1的碘水,当通入足量Cl 完全反应后,转移的电
2
子为5.0×10-5mol,令碘元素在氧化产物中的化合价为a,则根据电子转移守恒有5.0×
10-3L×1.0×10-3mol·L-1×2×a=5.0×10-5mol,解得 a=+5,所以碘单质被氧化为
HIO ,则该反应的化学方程式为5Cl +I +6HO===2HIO +10HCl。(3)当加入氨水时,使该
3 2 2 2 3
溶液变为碱性,产生BaSO 白色沉淀;加入盐酸和氯化钙不能使二氧化硫与氯化钡发生反应;
3
当加入HNO 时,将溶液中的HSO 氧化成HSO ,产生BaSO 白色沉淀。(4)由元素S和O
3 2 3 2 4 4
组成-2价酸根Z,Z中Y和X的质量比为4∶3,则n(S)∶n(O)=∶=2∶3,则Z为SO,
2
当Cl 与含SO的溶液完全反应后,有浅黄色沉淀产生,说明生成S单质,取上层清液加入
2 2
氯化钡溶液,有白色沉淀产生,说明生成SO,氯气被还原为Cl-,该反应的离子方程式为
SO+Cl+HO===SO+S↓+2Cl-+2H+。
2 2 2
2.A、B、C、D、E为含同一种元素的常见物质。C物质只由一种元素组成,在1个C分子
中形成共价键的电子数与分子中所含电子数之比为3∶7。C和E均可与氧气在一定条件下
反应生成A。请回答以下问题:
(1)常温下将气体 B 通入水中发生反应,生成 A 和 D,则该反应的离子方程式是
_____________________________________________________________________________。
(2)写出E与氧气反应生成A的化学方程式:________________________________________。
(3)D和E生成的化合物在某温度下加热分解,同时生成两种氧化物。且在此过程中,若有
0.5 mol该化合物完全反应,转移电子数为2 mol。写出该反应的化学方程式:
______________________________________________________________________________。
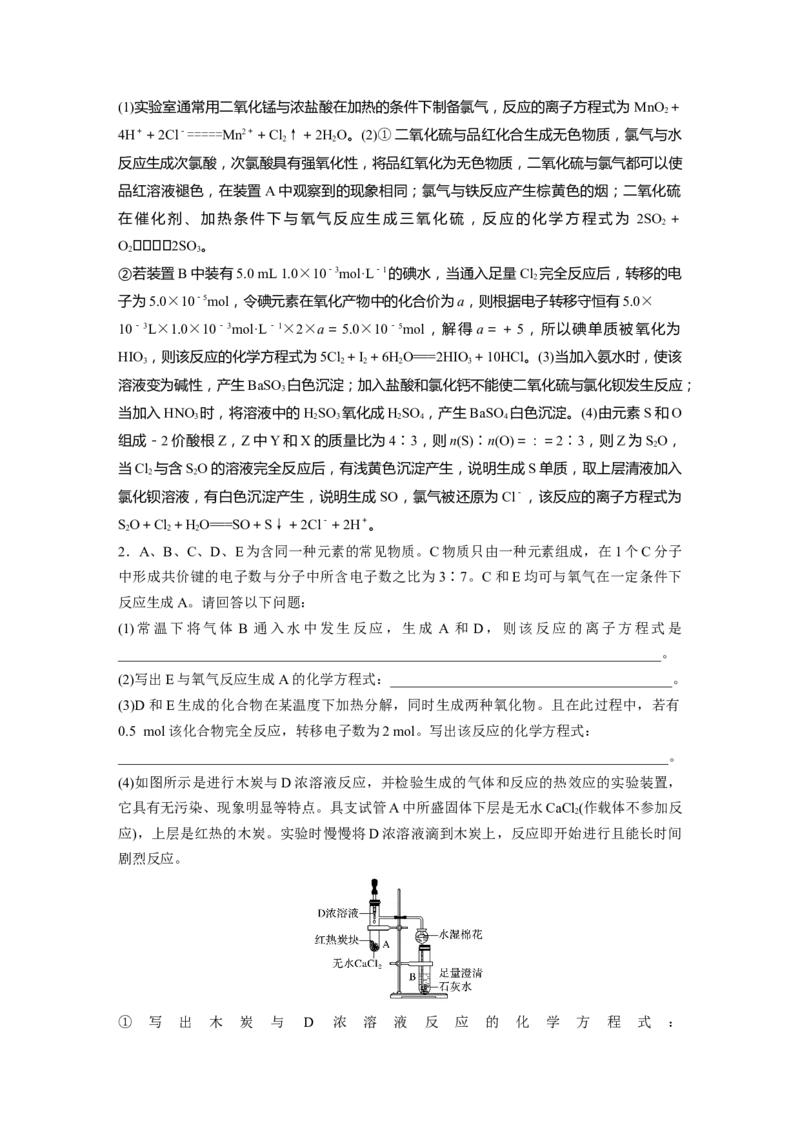
(4)如图所示是进行木炭与D浓溶液反应,并检验生成的气体和反应的热效应的实验装置,
它具有无污染、现象明显等特点。具支试管A中所盛固体下层是无水CaCl (作载体不参加反
2
应),上层是红热的木炭。实验时慢慢将D浓溶液滴到木炭上,反应即开始进行且能长时间
剧烈反应。
① 写 出 木 炭 与 D 浓 溶 液 反 应 的 化 学 方 程 式 :__________________________________________
_______________________________________________________________________________
。
②该反应为________(填“吸热”或“放热”)反应。
③试管B内出现的现象为_______________________________________________________。
④在实验临近结束时,发现滴管中的D浓溶液难以滴下。若想再滴入几滴D浓溶液使木炭
反 应 完 全 , 最 简 单 的 办 法 是
__________________________________________________________
_______________________________________________________________________________
。
答案 (1)3NO +HO===2H++2NO+NO
2 2
(2)4NH +5O=====4NO+6HO (3)NH NO =====2HO+NO↑ (4)①C+4HNO(浓)
3 2 2 4 3 2 2 3
=====CO↑+4NO ↑+2HO ②放热 ③试管内有红棕色气体生成,石灰水变浑浊 ④摇
2 2 2
动试管B,使上部的气体溶于石灰水
解析 C物质只由一种元素组成,说明C为单质,在1个C分子中形成共价键的电子数与分
子中所含电子数之比为3∶7,如C为双原子分子,则C原子核外有7个电子,形成的单质
中含有3个共用电子对,C为N ,C、E均可与氧气在一定条件下反应生成 A,则A为
2
NO,E为NH ,由(1)信息可知B为NO ,D为HNO,结合对应物质的性质和题目要求解答
3 2 3
该题。
(1)常温下NO 通入水中发生反应,生成NO和HNO ,发生反应的离子方程式为 3NO +
2 3 2
HO===2H++2NO+NO。(2)NH 在催化剂、加热条件下,与氧气反应生成NO和HO,发
2 3 2
生反应的化学方程式为 4NH +5O=====4NO+6HO。(3)HNO 和 NH 生成的化合物为
3 2 2 3 3
NH NO ,在某温度下加热分解,同时生成两种氧化物,其中一种为HO,反应中N元素的
4 3 2
化合价既升高,又降低,则另一种氮的氧化物既为氧化产物,又为还原产物,其中 N元素
从+5价降为x价,则(5-x)×0.5 mol=2 mol,解得x=+1,即产物为NO,故反应的化学
2
方程式:NH NO =====2HO+NO。(4)①木炭与浓硝酸溶液在加热条件下生成NO 、CO 和
4 3 2 2 2 2
水,发生反应的化学方程式为C+4HNO(浓)=====CO↑+4NO ↑+2HO。②浓硝酸滴到
3 2 2 2
红热的木炭上,能长时间剧烈反应,说明该反应为放热反应,利用放出的热量维持反应持续
进行。③NO 和CO 的混合气体经过水湿棉花,NO 溶于水生成NO,NO遇试管B上方空
2 2 2
气中的氧气生成红棕色气体NO ,CO 通入澄清石灰水变浑浊,有碳酸钙生成。④滴管中的
2 2
D浓溶液难以滴下,说明容器内气体压强较大,则只要摇动试管B,使上部的气体溶于石灰
水,降低容器内压强,就可继续滴入浓硝酸使木炭反应完全。
3.X、Y、Z、J、Q五种短周期主族元素,原子序数依次增大。元素Z在地壳中含量最高,
J元素的焰色反应呈黄色,Q的最外层电子数与其电子总数之比为3∶8,X能与J形成离子
化合物,且J+的半径大于X-的半径,Y的氧化物是形成酸雨的主要物质之一。请回答:(1)Q元素在周期表中的位置为_______________________________________________。
(2)将这五种元素原子半径从大到小排列,排在第三的元素原子是__________(填元素符号)。
(3)元素的非金属性Z________(填“>”或“<”)Q。下列各项中,不能说明这一结论的事实
有________(填字母)。
A.Q的氢化物的水溶液放置在空气中会变浑浊
B.Z与Q之间形成的化合物中元素的化合价
C.Z和Q的单质的状态
D.Z和Q在周期表中的位置
(4)X与Y可形成分子A,也可形成阳离子B,A、B在水溶液中酸、碱性恰好相反,写出阳
离子B的立体构型为________,离子中键角为_______________________________________;
X与Q在一定条件下可以形成极不稳定的原子个数比为1∶1的化合物,该化合物分子中既
有极性键又有非极性键,写出该分子的结构式:___________________________________。
(5)M和N均为上述五种元素中的三种组成的化合物,且M和N都为强电解质,M和N溶液
反 应 既 有 沉 淀 出 现 又 有 气 体 产 生 , 写 出 M 和 N 反 应 的 化 学 方 程 式 :
______________________
_______________________________________________________________________________
。
答案 (1)第三周期ⅥA族 (2)N (3)> C
(4)正四面体 109°28′ H—S—S—H
(5)Na SO+HSO ===NaSO +S↓+SO ↑+HO
2 2 3 2 4 2 4 2 2
解析 Z元素在地壳中含量最高,Z为O元素;J元素的焰色反应呈黄色,J为Na元素;Q
的原子序数大于J,Q的最外层电子数与其电子总数之比为3∶8,Q为S元素;Y的原子序
数小于Z,Y的氧化物是形成酸雨的主要物质之一,Y为N元素;X的原子序数小于Y,X
能与J形成离子化合物且J+的半径大于X-的半径,X为H元素。
4.原子序数依次增大的X、Y、Z、W、M五种短周期主族元素中,X、Y两元素间能形成
原子个数比分别为1∶1和1∶2的固态化合物A和B,Y是短周期元素中失电子能力最强的
元素,W、M的最高价氧化物对应的水化物化学式分别为HWO 、HMO ,Z的单质能与盐
3 4 4
酸反应。
(1)根据上述条件不能确定的元素是__________(填代号),A的电子式为________________,
举例说明Y、Z的金属性相对强弱:_____________________________(写出一个即可)。
(2)W能形成多种含氧酸及相应的盐,其中NaH WO 能与盐酸反应但不能与NaOH溶液反应,
2 2
则下列说法正确的是________________(填字母)。
A.HWO 是三元酸
3 2
B.HWO 是一元弱酸
3 2
C.NaH WO 是酸式盐
2 2
D.NaH WO 不可能被硝酸氧化
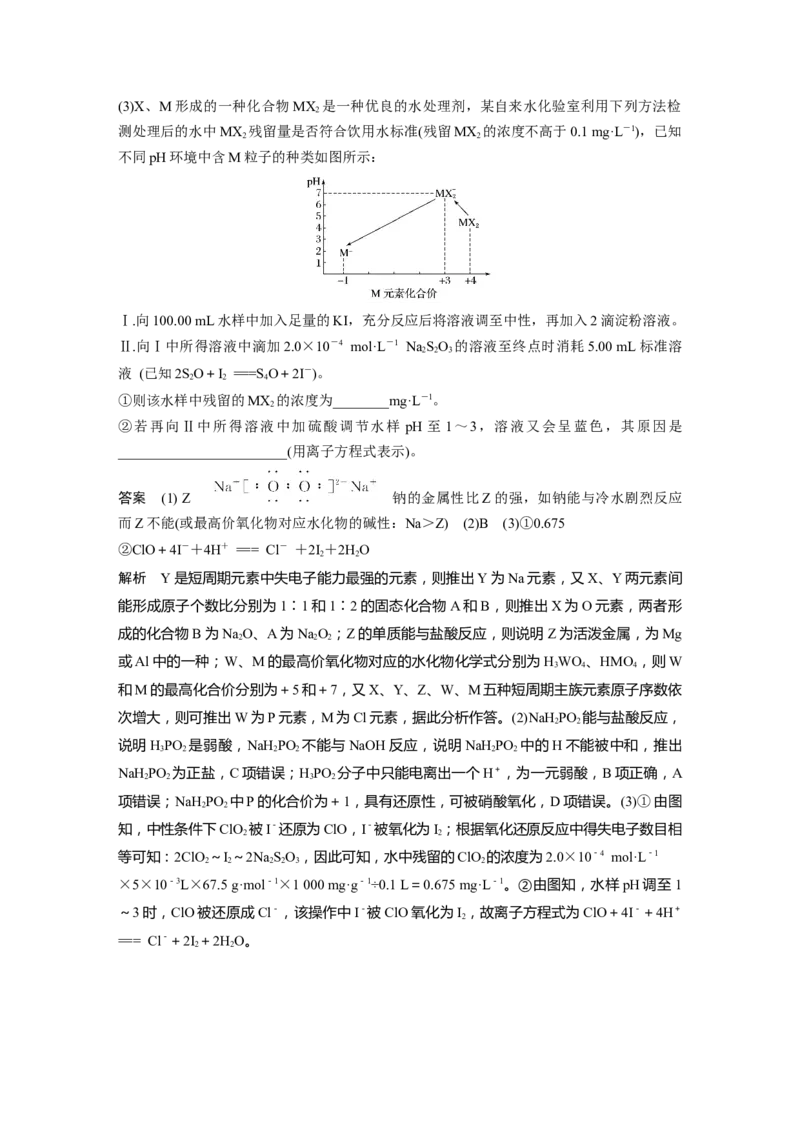
2 2(3)X、M形成的一种化合物MX 是一种优良的水处理剂,某自来水化验室利用下列方法检
2
测处理后的水中MX 残留量是否符合饮用水标准(残留MX 的浓度不高于0.1 mg·L-1),已知
2 2
不同pH环境中含M粒子的种类如图所示:
Ⅰ.向100.00 mL水样中加入足量的KI,充分反应后将溶液调至中性,再加入2滴淀粉溶液。
Ⅱ.向Ⅰ中所得溶液中滴加2.0×10-4 mol·L-1 Na SO 的溶液至终点时消耗5.00 mL标准溶
2 2 3
液 (已知2SO+I ===SO+2I-)。
2 2 4
①则该水样中残留的MX 的浓度为________mg·L-1。
2
②若再向Ⅱ中所得溶液中加硫酸调节水样 pH 至 1~3,溶液又会呈蓝色,其原因是
________________________(用离子方程式表示)。
答案 (1) Z 钠的金属性比Z的强,如钠能与冷水剧烈反应
而Z不能(或最高价氧化物对应水化物的碱性:Na>Z) (2)B (3)①0.675
②ClO+4I-+4H+ === Cl- +2I+2HO
2 2
解析 Y是短周期元素中失电子能力最强的元素,则推出Y为Na元素,又X、Y两元素间
能形成原子个数比分别为1∶1和1∶2的固态化合物A和B,则推出X为O元素,两者形
成的化合物B为NaO、A为NaO ;Z的单质能与盐酸反应,则说明Z为活泼金属,为Mg
2 2 2
或Al中的一种;W、M的最高价氧化物对应的水化物化学式分别为HWO 、HMO ,则W
3 4 4
和M的最高化合价分别为+5和+7,又X、Y、Z、W、M五种短周期主族元素原子序数依
次增大,则可推出W为P元素,M为Cl元素,据此分析作答。(2)NaH PO 能与盐酸反应,
2 2
说明HPO 是弱酸,NaH PO 不能与NaOH反应,说明NaH PO 中的H不能被中和,推出
3 2 2 2 2 2
NaH PO 为正盐,C项错误;HPO 分子中只能电离出一个H+,为一元弱酸,B项正确,A
2 2 3 2
项错误;NaH PO 中P的化合价为+1,具有还原性,可被硝酸氧化,D项错误。(3)①由图
2 2
知,中性条件下ClO 被I-还原为ClO,I-被氧化为I;根据氧化还原反应中得失电子数目相
2 2
等可知:2ClO ~I~2NaSO,因此可知,水中残留的ClO 的浓度为2.0×10-4 mol·L-1
2 2 2 2 3 2
×5×10-3L×67.5 g·mol-1×1 000 mg·g-1÷0.1 L=0.675 mg·L-1。②由图知,水样pH调至1
~3时,ClO被还原成Cl-,该操作中I-被ClO氧化为I ,故离子方程式为ClO+4I-+4H+
2
=== Cl-+2I+2HO。
2 2