文档内容
2023 届河北省高三年级开学考试
化学试题
(考试时长:75分钟总分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号、考场号、座位号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需
改动,用橡皮擦干净后,再选涂其它答案标号。回答非选择题时,将答案写在答题卡上。写在本试
卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H1C12O16Cl35.5
第I卷(选择题共43分)
一、单项选择题:本题共9小题,每小题3分,共27分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1.北京冬奥会火炬接力火种灯的创意源于被誉为“中华第一灯”的长信宫灯。西汉长信宫灯
设计巧妙环保,是一件既实用、又美观的灯具珍品。下列说法错误的是
A.铝合金的硬度大于纯铝
B.青铜器表面破损易生成铜绿
C.丙烷和动物油脂均属于烃类D.两灯所用燃料充分燃烧的产物均不污染环境
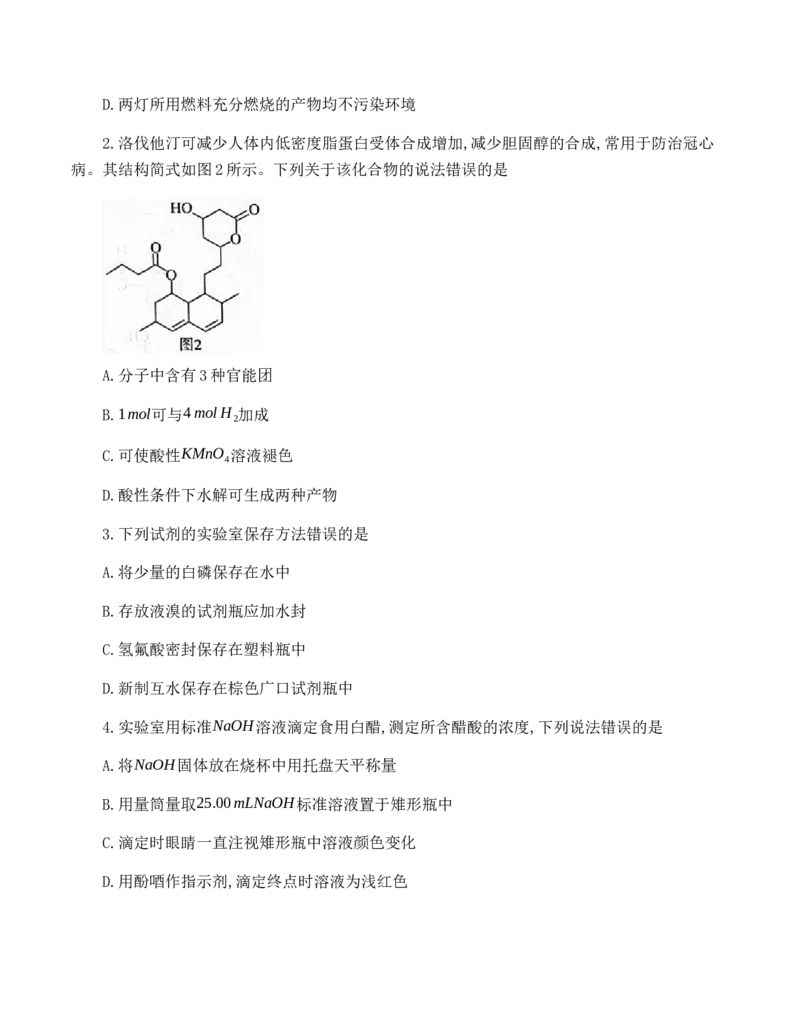
2.洛伐他汀可减少人体内低密度脂蛋白受体合成增加,减少胆固醇的合成,常用于防治冠心
病。其结构简式如图2所示。下列关于该化合物的说法错误的是
A.分子中含有3种官能团
B.1mol可与4molH 加成
2
C.可使酸性KMnO 溶液褪色
4
D.酸性条件下水解可生成两种产物
3.下列试剂的实验室保存方法错误的是
A.将少量的白磷保存在水中
B.存放液溴的试剂瓶应加水封
C.氢氟酸密封保存在塑料瓶中
D.新制互水保存在棕色广口试剂瓶中
4.实验室用标准NaOH溶液滴定食用白醋,测定所含醋酸的浓度,下列说法错误的是
A.将NaOH固体放在烧杯中用托盘天平称量
B.用量筒量取25.00mLNaOH标准溶液置于雉形瓶中
C.滴定时眼睛一直注视雉形瓶中溶液颜色变化
D.用酚唒作指示剂,滴定终点时溶液为浅红色5.❑ 210Po具有放射性,其衰变反应为:❑ 210P→❑ APb+❑ 4He。已知半衰期指含放射性原子的
84 84 z 2
样品中,放射性元素原子核有50%发生衰变所需的时间,❑ 210Po的半衰期为138天。列说法错误的
84
是
A.❑ APb的相对原子质量为206
Z
B.Po元素的价层电子排布为6s26p4
C.研究发现烟草中含❑ 210Po和❑ 209P ,它们互为同位素
0
D.质量为64g的❑ 210Po经276天得到❑ APb的质量为47.09g
84 2
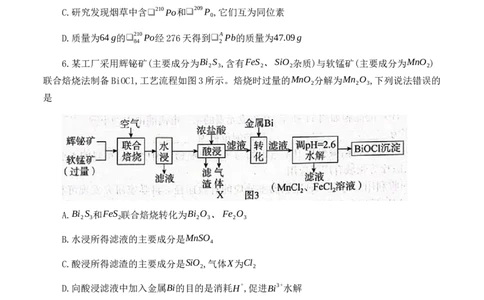
6.某工厂采用辉铋矿(主要成分为Bi S ,含有FeS 、SiO 杂质)与软锰矿(主要成分为MnO )
2 3 2 2 2
联合焙烧法制备BiOCl,工艺流程如图3所示。焙烧时过量的MnO 分解为Mn O ,下列说法错误的
2 2 3
是
A.Bi S 和FeS 联合焙烧转化为Bi O 、Fe O
2 3 2 2 3 2 3
B.水浸所得滤液的主要成分是MnSO
4
C.酸浸所得滤渣的主要成分是SiO ,气体X为Cl
2 2
D.向酸浸滤液中加入金属Bi的目的是消耗H+,促进Bi3+水解
7.材料是人类赖以生存和发展的物质基础。下列说法错误的是
A.新型陶瓷与传统陶瓷的化学成分不同
B.酚醛树脂和聚酯纤维均属于有机高分子材料
C.聚酰胺纤维中的锦纶是较早通过加聚反应合成的纤维D.高纯度的单晶硅、二氧化硅属于新型无机非金属材料
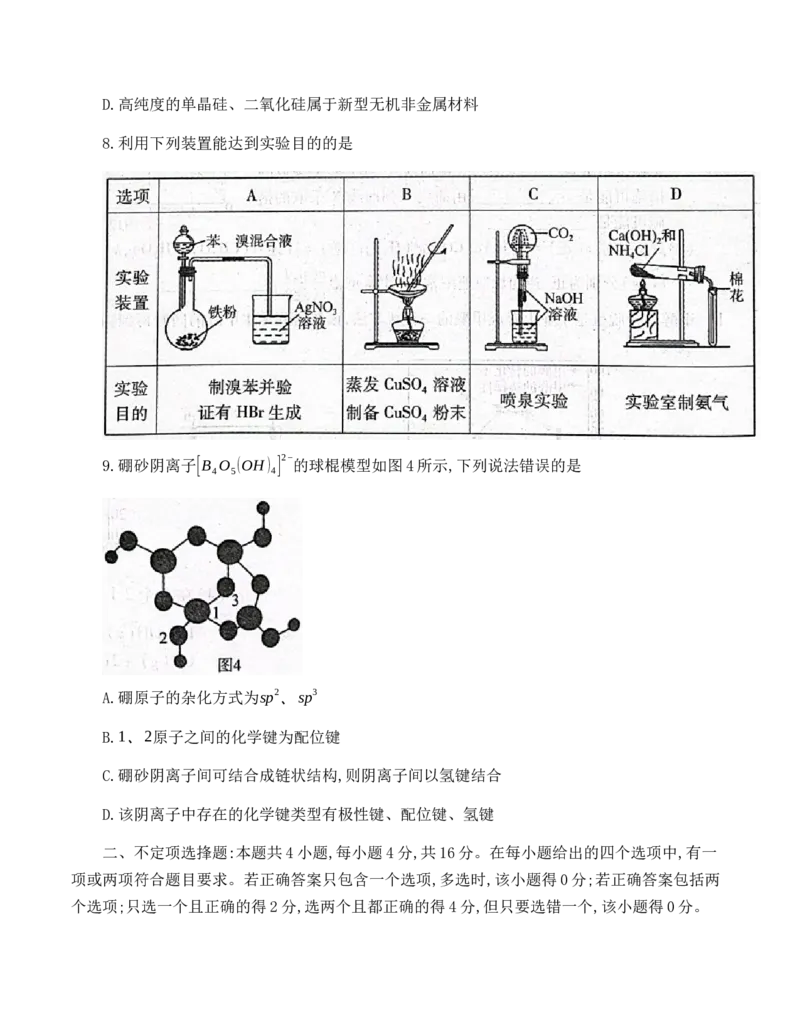
8.利用下列装置能达到实验目的的是
2−
9.硼砂阴离子[B O (OH) ] 的球棍模型如图4所示,下列说法错误的是
4 5 4
A.硼原子的杂化方式为sp2、sp3
B.1、2原子之间的化学键为配位键
C.硼砂阴离子间可结合成链状结构,则阴离子间以氢键结合
D.该阴离子中存在的化学键类型有极性键、配位键、氢键
二、不定项选捀题:本题共4小题,每小题4分,共16分。在每小题给出的四个选项中,有一
项或两项符合题目要求。若正确答案只包含一个选项,多选时,该小题得0分;若正确答案包括两
个选项;只选一个且正确的得2分,选两个且都正确的得4分,但只要选错一个,该小题得0分。10.W、X、Y、Z是原子序数依次增大的短周期主族元素,其最外层电子数之和为
18。W、X、Y分别位于不同周期,X与Y同主族,W的最低负价与Z的最高正价的代数和等于6,
下列说法错误的是
A.W分别与X、Y形成的简单化合物的键角:前者大于后者
B.Y与Z形成的化合物中各原子不一定满足8电子稳定结构
C.Z分别与X、Y形成的化合物均可与水反应生成两种酸
D.Y的一种单质分子呈正四面体结构,键角为60∘
11. 有机物M与N在 NaOH 溶液中发生如图5所示的反应,生成有机物L 下列说法正确的是
∘
A.N还有3种含苯环的同分异构体
B.L分子存在顺反异构体
C.M、N、L均可与溴水发生加成反应
D.L分子中的所有碳原子可能在同一平面上
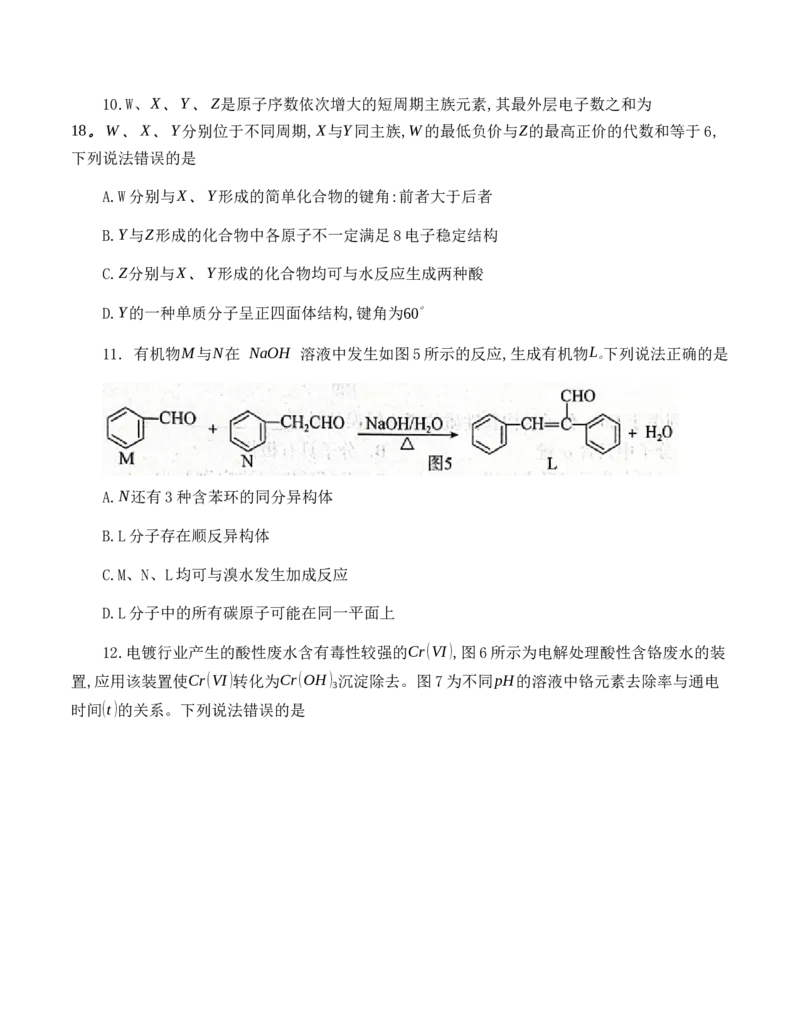
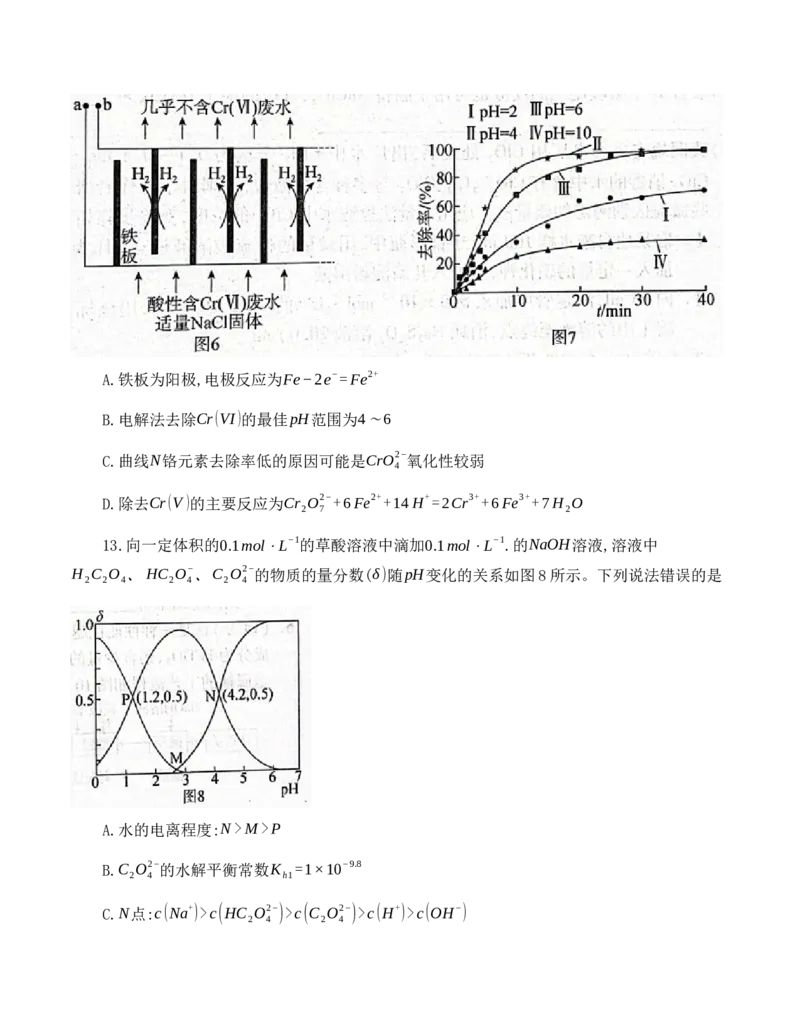
12.电镀行业产生的酸性废水含有毒性较强的Cr(VI),图6所示为电解处理酸性含铬废水的装
置,应用该装置使Cr(VI)转化为Cr(OH) 沉淀除去。图7为不同pH的溶液中铬元素去除率与通电
3
时间(t)的关系。下列说法错误的是A.铁板为阳极,电极反应为Fe−2e−=Fe2+
B.电解法去除Cr(VI)的最佳pH范围为4∼6
C.曲线N铬元素去除率低的原因可能是CrO2−氧化性较弱
4
D.除去Cr(V)的主要反应为Cr O2−+6Fe2++14H+=2Cr3++6Fe3++7H O
2 7 2
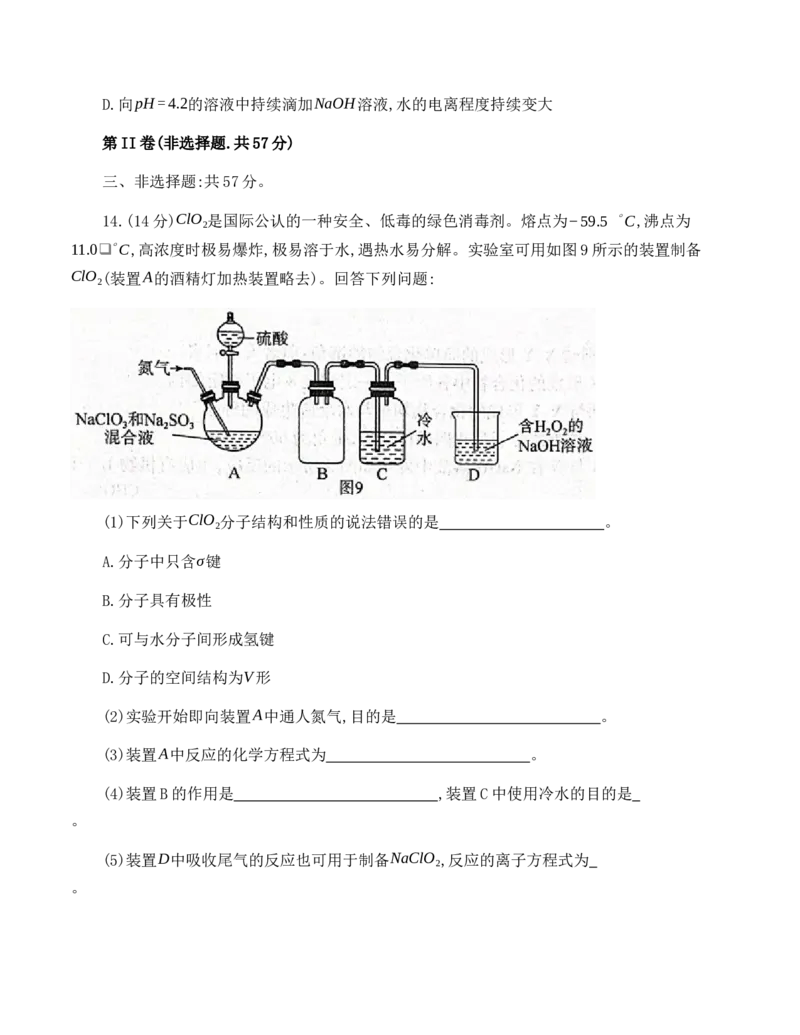
13.向一定体积的0.1mol⋅L−1的草酸溶液中滴加0.1mol⋅L−1.的NaOH溶液,溶液中
H C O 、HC O−、C O2−的物质的量分数(δ)随pH变化的关系如图8所示。下列说法错误的是
2 2 4 2 4 2 4
A.水的电离程度:N>M>P
B.C O2−的水解平衡常数K =1×10−9.8
2 4 h1
C.N点:c(Na+)>c(HC O2−)>c(C O2−)>c(H+)>c(OH−)
2 4 2 4D.向pH=4.2的溶液中持续滴加NaOH溶液,水的电离程度持续变大
第II卷(非选择题.共57分)
三、非选择题:共57分。
14.(14分)ClO 是国际公认的一种安全、低毒的绿色消毒剂。熔点为−59.5 ∘C,沸点为
2
11.0❑∘C,高浓度时极易爆炸,极易溶于水,遇热水易分解。实验室可用如图9所示的装置制备
ClO (装置A的酒精灯加热装置略去)。回答下列问题:
2
(1)下列关于ClO 分子结构和性质的说法错误的是 。
2
A.分子中只含σ键
B.分子具有极性
C.可与水分子间形成氢键
D.分子的空间结构为V形
(2)实验开始即向装置A中通人氮气,目的是 。
(3)装置A中反应的化学方程式为 。
(4)装置B的作用是 ,装置C中使用冷水的目的是
。
(5)装置D中吸收尾气的反应也可用于制备NaClO ,反应的离子方程式为
2
。(6)我国规定自来水厂用ClO 处理后,出厂水中ClO 余量为0.1∼0.8mg⋅L−1。针对ClO 消毒
2 2 2
的水中含有ClO−、Cl 、ClO−等多种含氯微粒,我国科学工作者研制出能将这些微粒区别测定的
2 2 3
碘量法。应用磺量法检测水中ClO 的浓度,实验步骤如下:
2
I.取某地自来水样100mL于雉形瓶中,用微量的稀硫酸溶液调至pH为1∼3,然后加入一定量
的碘化钾,并加入几滴淀粉溶液。
II.向25mL滴定管中加入5.0×10−5mol−L−1的Na S O 溶液,用该标准液滴定步骤I中的溶液至
2 2 3
终点,消耗Na S O 溶液20.00mL。
2 2 3
已知:①ClO 在酸性条件下的还原产物为Cl−;
2
②2S O2−+I =S O2−+2I−。
2 3 2 4 6
计算水样中ClO 的浓度是 mg⋅L−1。步骤II滴定终点的判断依据是
2
,如果滴定结束时仰视读取滴定管中溶液的体积,则测定结果将 (填“偏大”、偏
小”或“无影响”)。
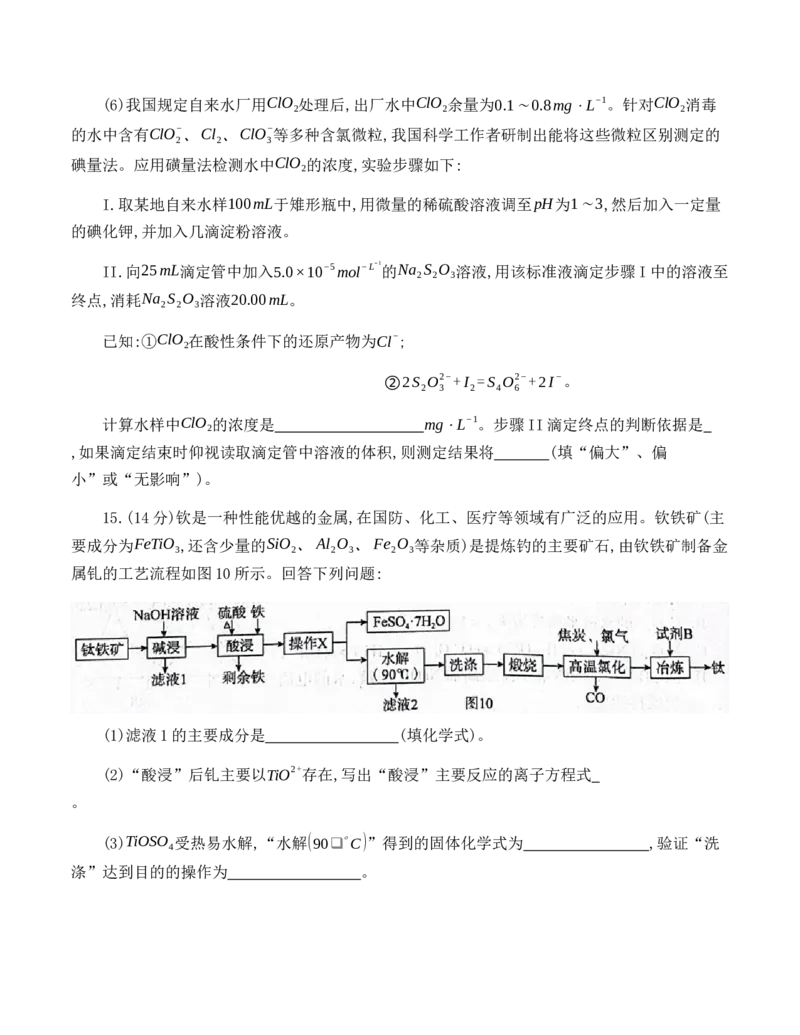
15.(14分)钦是一种性能优越的金属,在国防、化工、医疗等领域有广泛的应用。钦铁矿(主
要成分为FeTiO ,还含少量的SiO 、Al O 、Fe O 等杂质)是提炼钓的主要矿石,由钦铁矿制备金
3 2 2 3 2 3
属钆的工艺流程如图10所示。回答下列问题:
(1)滤液1的主要成分是 (填化学式)。
(2)“酸浸”后钆主要以TiO2+存在,写出“酸浸”主要反应的离子方程式
。
(3)TiOSO 受热易水解,“水解(90❑∘C)”得到的固体化学式为 ,验证“洗
4
涤”达到目的的操作为 。(4)“高温氯化”反应的化学方程式为 ,“冶炼”加入的试剂B为
。
(5)已知TiCl 的熔点为−25❑∘C,沸点为135.25❑∘C,分析说明能否直接电解液态TiCl 制备金
4 4
属钛 。
(6)FeTiO 的晶胞如图11所示,其组成元素的第一电离能由大到小顺序为
3
,Ti-的配位数为 。
16.(14分)甲醛有毒,被世界卫生组织列为一类致癌物。但甲醛是重要的工业原料,在化工、
纺织、医疗等领域有广泛应用。
I.回收利用CO 是一种减弱温室效应的有效途径。科学家研究发现可利用回收的CO 与H 反
2 2 2
应制备甲醛。
已知:①甲醛的燃烧热为524kJ⋅mol−1
②H 的燃烧热为285.8kJ⋅mol−1
2
③H O(g)=H O(l)ΔH=−44kJg ⋅mol−1
2 2
(1)CO 与H 制备甲醛的反应CO (g)+2H (g)=CH O(g)+H O(g)△H= 。
2 2 2 2 2 2
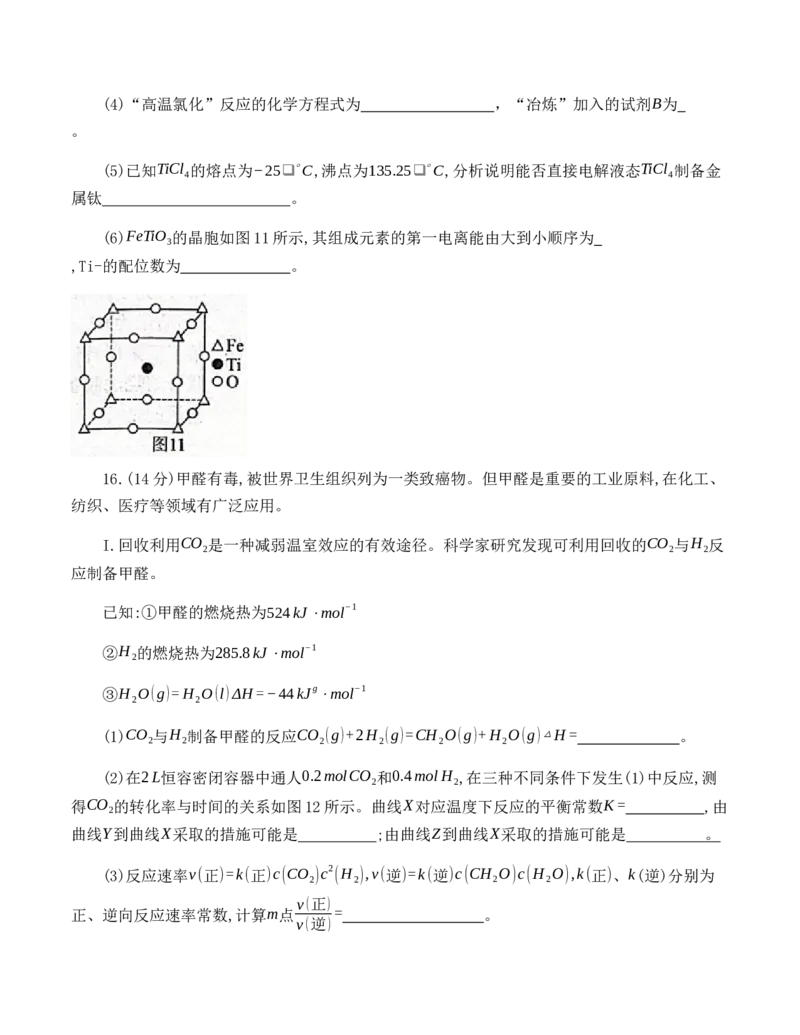
(2)在2L恒容密闭容器中通人0.2molCO 和0.4molH ,在三种不同条件下发生(1)中反应,测
2 2
得CO 的转化率与时间的关系如图12所示。曲线X对应温度下反应的平衡常数K= ,由
2
曲线Y到曲线X采取的措施可能是 ;由曲线Z到曲线X采取的措施可能是 。
(3)反应速率v(正)=k(正)c(CO )c2 (H ),v(逆)=k(逆)c(CH O)c(H O),k(正)、k(逆)分别为
2 2 2 2
v(正)
正、逆向反应速率常数,计算m点 = 。
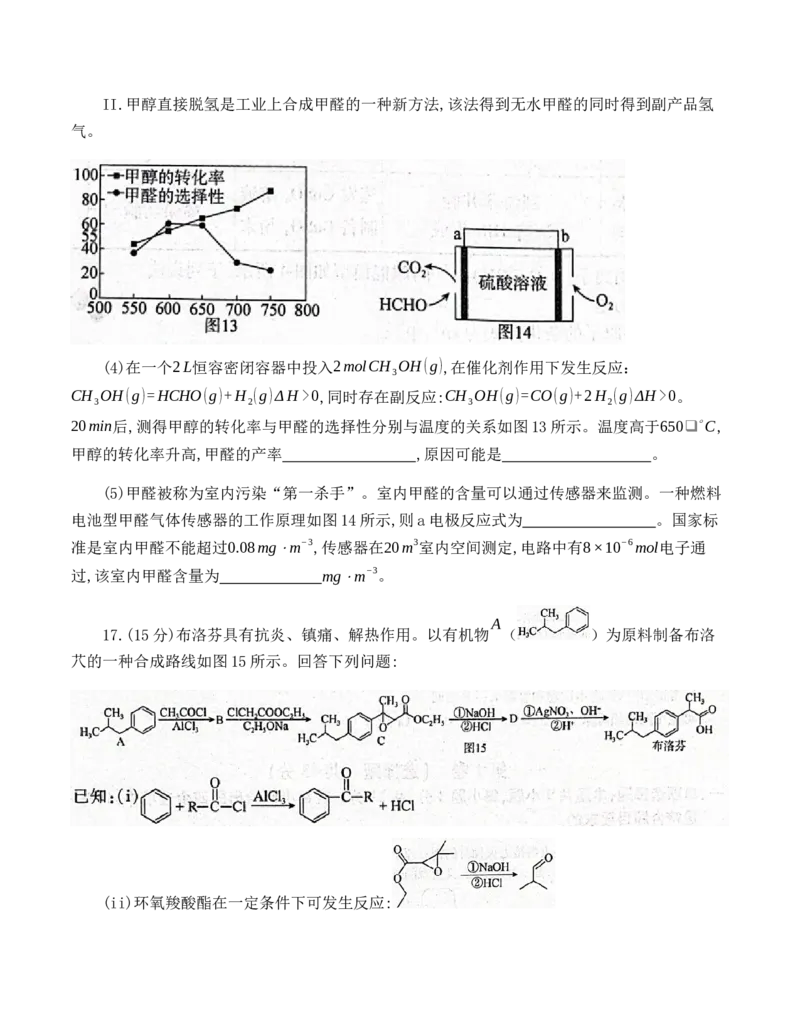
v(逆)II.甲醇直接脱氢是工业上合成甲醛的一种新方法,该法得到无水甲醛的同时得到副产品氢
气。
(4)在一个2L恒容密闭容器中投入2molCH OH(g),在催化剂作用下发生反应:
3
CH OH(g)=HCHO(g)+H (g)ΔH>0,同时存在副反应:CH OH(g)=CO(g)+2H (g)ΔH>0。
3 2 3 2
20min后,测得甲醇的转化率与甲醛的选择性分别与温度的关系如图13所示。温度高于650❑∘C,
甲醇的转化率升高,甲醛的产率 ,原因可能是 。
(5)甲醛被称为室内污染“第一杀手”。室内甲醛的含量可以通过传感器来监测。一种燃料
电池型甲醛气体传感器的工作原理如图14所示,则a电极反应式为 。国家标
准是室内甲醛不能超过0.08mg⋅m−3,传感器在20m3室内空间测定,电路中有8×10−6mol电子通
过,该室内甲醛含量为 mg⋅m−3。
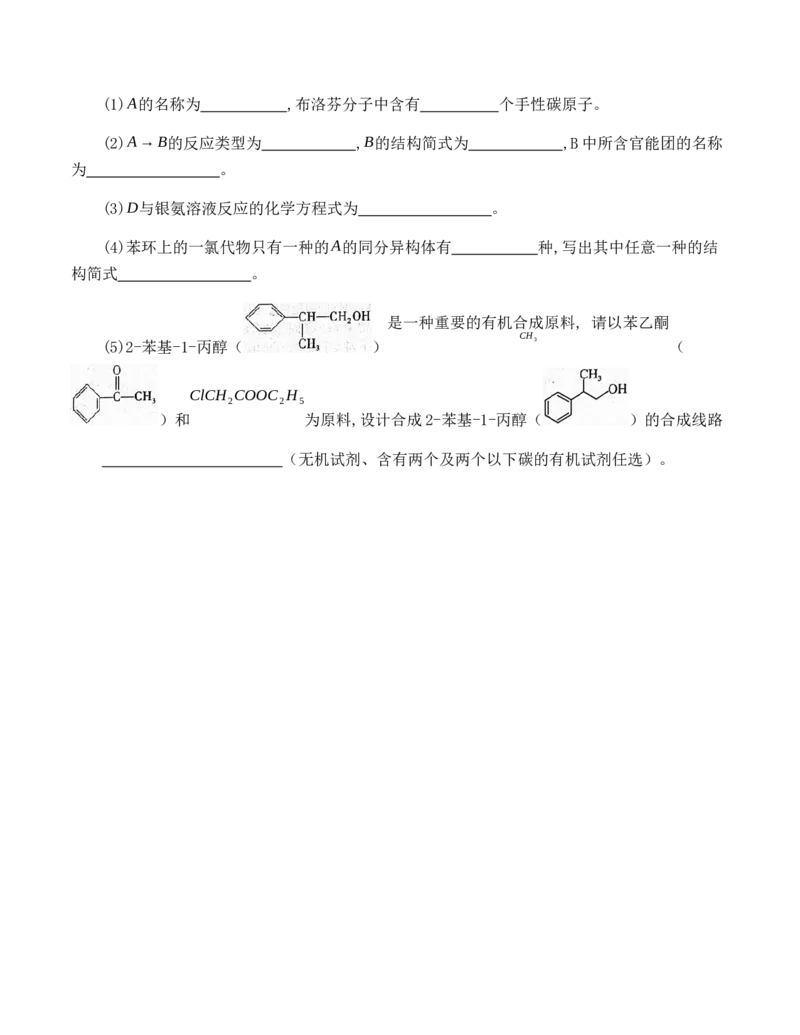
A
17.(15分)布洛芬具有抗炎、镇痛、解热作用。以有机物 ( )为原料制备布洛
䒔的一种合成路线如图15所示。回答下列问题:
(ii)环氧羧酸酯在一定条件下可发生反应:(1)A的名称为 ,布洛芬分子中含有 个手性碳原子。
(2)A→B的反应类型为 ,B的结构简式为 ,B中所含官能团的名称
为 。
(3)D与银氨溶液反应的化学方程式为 。
(4)苯环上的一氯代物只有一种的A的同分异构体有 种,写出其中任意一种的结
构简式 。
是一种重要的有机合成原料, 请以苯乙酮
CH
(5)2-苯基-1-丙醇( ) 3 (
ClCH COOC H
2 2 5
)和 为原料,设计合成2-苯基-1-丙醇( )的合成线路
(无机试剂、含有两个及两个以下碳的有机试剂任选)。下载最新免费模拟卷,到公众号:一枚试卷君