文档内容
热点强化 15 速率常数与化学平衡常数的关系
1.假设基元反应(能够一步完成的反应)为aA(g)+bB(g)===cC(g)+dD(g),其速率可表示为
v=k·ca(A)·cb(B),式中的k称为反应速率常数或速率常数,它表示单位浓度下的化学反应速
率,与浓度无关,但受温度、催化剂、固体表面性质等因素的影响,通常反应速率常数越大,
反应进行得越快。不同反应有不同的速率常数。
2.正、逆反应的速率常数与平衡常数的关系
对于基元反应aA(g)+bB(g)cC(g)+dD(g),v正 =k
正
·ca(A)·cb(B),v逆 =k
逆
·cc(C)·cd(D),平
衡常数K==,反应达到平衡时v正 =v逆 ,故K=。
[示例] 温度为 T ,在三个容积均为 1 L 的恒容密闭容器中仅发生反应:CH(g)+
1 4
H 2 O(g)CO(g)+3H 2 (g) ΔH=+206.3 kJ·mol-1,该反应中,正反应速率为 v 正 =k
正
·c(CH
4
)·c(H
2
O),逆反应速率为v逆 =k
逆
·c(CO)·c3(H
2
),k
正
、k
逆
为速率常数,受温度影响。
已知T 时,k =k ,则该温度下,平衡常数K =____;当温度改变为T 时,若k =1.5k ,
1 正 逆 1 2 正 逆
则T________T(填“>”“=”或“<”)。
2 1
答案 1 >
解析 解题步骤及过程:
步骤1 代入特殊值:
平衡时v =v ,即
正 逆
k ·c(CH)·c(H O)=k ·c(CO)·c3(H );
正 4 2 逆 2
步骤2 适当变式求平衡常数,
K ==;k =k ,K =1
1 正 逆 1
步骤3 求其他
K ==;k =1.5k ,K =1.5;
2 正 逆 2
1.5>1,平衡正向移动,升高温度平衡向吸热方向移动;则T>T。
2 1
1.NO 与NO 之间存在反应:NO(g)2NO (g)。将一定量的NO 放入恒容密闭容器中,
2 4 2 2 4 2 2 4
在一定条件下,该反应 NO 、NO 的消耗速率与自身压强间存在关系:v(N O)=
2 4 2 2 4
k·p(N O),v(NO )=k·p2(NO ),其中k 、k 是与反应温度有关的常数。则一定温度下,k 、
1 2 4 2 2 2 1 2 1
k 与平衡常数K 的关系是k=________。
2 p 1
答案 K k
p 2
解 析 K = , 平 衡 时 NO 、 NO 的 消 耗 速 率 之 比 为 v(NO )∶v(N O) =
p 2 2 4 2 2 4
[k·p2(NO )]∶[k·p(N O)]=2∶1。
2 2 1 2 42.利用NH 的还原性可以消除氮氧化物的污染,其中除去NO的主要反应如下:
3
4NH (g)+6NO(g)5N(g)+6HO(l) ΔH<0
3 2 2
已知该反应速率v正 =k
正
·c4(NH
3
)·c6 (NO),v逆 =k
逆
·cx(N
2
)·cy(H
2
O) (k
正
、k
逆
分别是正、逆反
应速率常数),该反应的平衡常数K=,则x=________,y=________。
答案 5 0
解析 当反应达到平衡时有v =v ,即k ·c4(NH )·c6 (NO)=k ·cx(N )·cy(H O),变换可得
正 逆 正 3 逆 2 2
=,该反应的平衡常数K==,所以x=5,y=0。
3.2NO(g)+O(g)2NO (g)的反应历程如下:
2 2
反应Ⅰ:2NO(g)NO(g)(快) ΔH<0
2 2 1
v 1正 =k 1正 ·c2(NO),v 1逆 =k 1逆 ·c(N 2 O 2 );
反应Ⅱ:N 2 O 2 (g)+O 2 (g)2NO 2 (g)(慢) ΔH 2 <0 v 2 正 =k 2 正 ·c(N 2 O 2 )·c(O 2 ),v 2 逆 =k 2
·c2(NO )。
逆 2
(1)一定条件下,反应2NO(g)+O(g)2NO (g)达到平衡状态,平衡常数K=__________(用
2 2
含k 、k 、k 、k 的代数式表示)。反应Ⅰ的活化能E ______(填“>”“<”或“=”)
1正 1逆 2正 2逆 Ⅰ
反应Ⅱ的活化能E 。
Ⅱ
(2)已知反应速率常数k随温度的升高而增大,则升高温度后 k 增大的倍数__________k
2正 2逆
增大的倍数(填“大于”“小于”或“等于”)。
答案 (1) < (2)小于
解析 (1)反应达平衡状态时,v =v 、v =v ,所以v ·v =v ·v ,即k ·c2(NO)·
1正 1逆 2正 2逆 1正 2正 1逆 2逆 1正
k ·c(N O)·c(O ) = k ·c(N O)·k ·c2(NO ) , 则 有 K = = ; 因 为 决 定 2NO(g) +
2 正 2 2 2 1 逆 2 2 2 逆 2
O(g)2NO (g)速率的是反应Ⅱ,所以反应Ⅰ的活化能E 小于反应Ⅱ的活化能E 。
2 2 Ⅰ Ⅱ
4.肌肉中的肌红蛋白(Mb)与 O 结合生成 MbO ,其反应原理可表示为 Mb(aq)+
2 2
O(g)MbO (aq),该反应的平衡常数可表示为K=。在37 ℃条件下达到平衡时,测得肌
2 2
红蛋白的结合度(α)与 p(O 2 )的关系如图所示[α=×100%]。研究表明正反应速率 v 正 =k
正
·c(Mb) · p(O
2
),逆反应速率v逆 =k
逆
·c(MbO
2
)(其中k
正
和k
逆
分别表示正反应和逆反应的速
率常数)。
(1)试写出平衡常数K与速率常数k 、k 之间的关系式为K=________(用含有k 、k 的式
正 逆 正 逆
子表示)。
(2)试求出图中c点时,上述反应的平衡常数K=________ kPa-1。已知k =60 s-1,则速率
逆常数k =______s-1·kPa-1。
正
答案 (1) (2)2 120
解析 (1)可逆反应达到平衡状态时,v =v ,所以k ·c(Mb)·p(O )=k ·c(MbO ),=,而
正 逆 正 2 逆 2
平衡常数K==。(2)c点时,p(O )=4.50 kPa,肌红蛋白的结合度α=90%,代入平衡常数表
2
达式中可得K==kPa-1=2 kPa-1;K=,则k =K·k =2 kPa-1×60 s-1=120 s-1·kPa-1。
正 逆
5.乙烯、环氧乙烷是重要的化工原料,用途广泛。
实验测得 2CH
2
==CH
2
(g)+O
2
(g)2 (g) ΔH<0 中,v
逆
=k
逆
·c2( ),v
正
=k
正
·c2
(CH==CH)·c(O )(k 、k 为速率常数,只与温度有关)。
2 2 2 正 逆
(1)反应达到平衡后,仅降低温度,下列说法正确的是________(填字母)。
A.k 、k 均增大,且k 增大的倍数更多
正 逆 正
B.k 、k 均减小,且k 减小的倍数更少
正 逆 正
C.k 增大、k 减小,平衡正向移动
正 逆
D.k 、k 均减小,且k 减小的倍数更少
正 逆 逆
(2)若在1 L的密闭容器中充入1 mol CH ==CH(g)和1 mol O (g),在一定温度下只发生上述
2 2 2
反应,经过10 min反应达到平衡,体系的压强变为原来的0.875倍,则0~10 min内v(O )=
2
________,=________。
答案 (1)B (2)0.025 mol·L-1·min-1 0.75
解析 (1)该反应是放热反应,反应达到平衡后,仅降低温度,k 、k 均减小,平衡向放热
正 逆
方向即正向进行,正反应速率大于逆反应速率,因此k 减小的倍数更少。
正
(2) 2CH==CH(g)+O(g)2 (g)
2 2 2
开始/mol 1 1 0
转化/mol 2x x 2x
平衡/mol 1-2x 1-x 2x
=0.875,x=0.25 mol,则0~10 min内v(O )===0.025 mol·
2
L-1·min-1,k ·c2( )=k ·c2(CH==CH)·c(O ),==0.75。
逆 正 2 2 2
6.乙烯气相直接水合法过程中会发生乙醇的异构化反应:C HOH(g)CHOCH (g) ΔH
2 5 3 3
=+50.7 kJ·mol-1,该反应的速率方程可表示为 v 正 =k 正 ·c(C 2 H 5 OH)和 v 逆 =k
·c(CHOCH ),k 和k 只与温度有关。该反应的活化能 E ________(填“>”“=”或
逆 3 3 正 逆 a(正)
“<”)E ,已知:T ℃时,k =0.006 s-1,k =0.002 s-1,该温度下向某恒容密闭容器
a(逆) 正 逆
中充入1.5 mol乙醇和4 mol甲醚,此时反应________(填“正向”或“逆向”)进行。
答案 > 正向
解析 该反应焓变大于0,焓变=正反应活化能-逆反应活化能,所以 E >E ;反应达
a(正) a(逆)
到平衡时正、逆反应速率相等,即k ·c(C HOH)=k ·c(CHOCH ),所以有==K,T ℃时,
正 2 5 逆 3 3
k =0.006 s-1,k =0.002 s-1,所以该温度下平衡常数K==3,所以该温度下向某恒容密
正 逆闭容器中充入1.5 mol乙醇和4 mol甲醚时,浓度商Q=<3,所以此时反应正向进行。
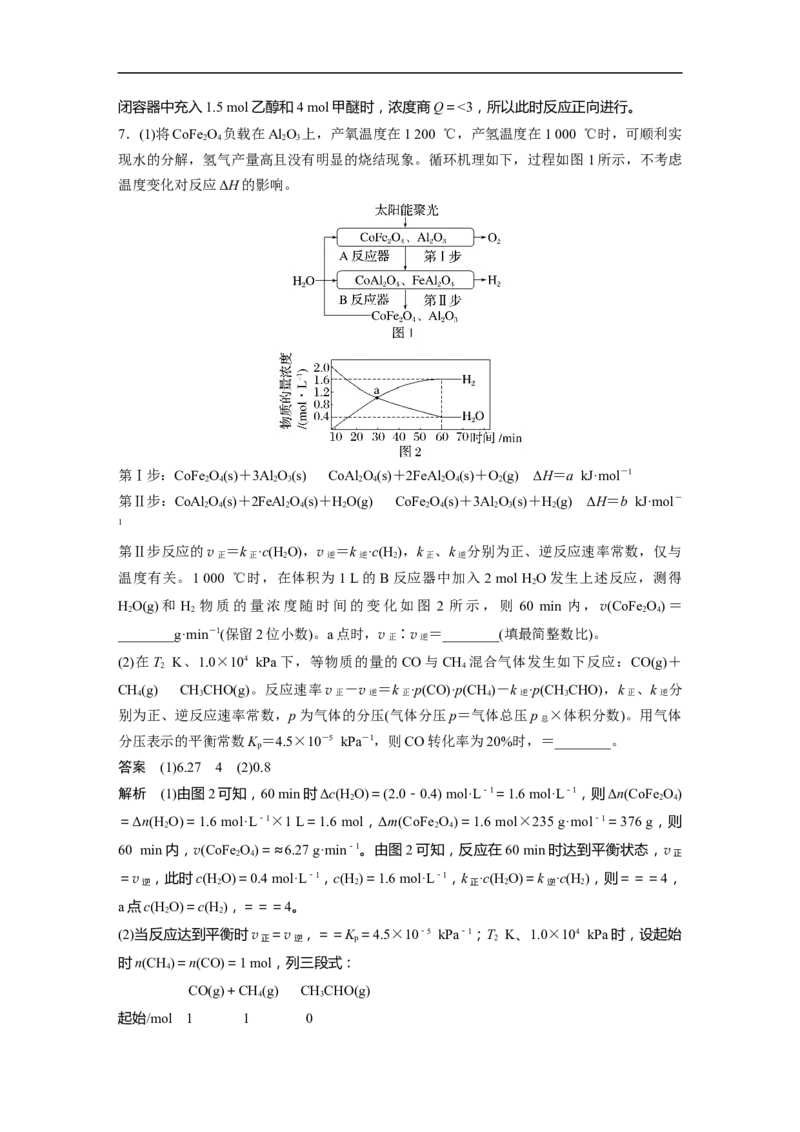
7.(1)将CoFe O 负载在Al O 上,产氧温度在1 200 ℃,产氢温度在1 000 ℃时,可顺利实
2 4 2 3
现水的分解,氢气产量高且没有明显的烧结现象。循环机理如下,过程如图1所示,不考虑
温度变化对反应ΔH的影响。
第Ⅰ步:CoFe O(s)+3Al O(s)CoAl O(s)+2FeAl O(s)+O(g) ΔH=a kJ·mol-1
2 4 2 3 2 4 2 4 2
第Ⅱ步:CoAl O(s)+2FeAl O(s)+HO(g)CoFe O(s)+3Al O(s)+H(g) ΔH=b kJ·mol-
2 4 2 4 2 2 4 2 3 2
1
第Ⅱ步反应的v正 =k
正
·c(H
2
O),v逆 =k
逆
·c(H
2
),k
正
、k
逆
分别为正、逆反应速率常数,仅与
温度有关。1 000 ℃时,在体积为1 L的B反应器中加入2 mol H O发生上述反应,测得
2
HO(g)和 H 物质的量浓度随时间的变化如图 2 所示,则 60 min 内,v(CoFe O)=
2 2 2 4
________g·min-1(保留2位小数)。a点时,v正 ∶v逆 =________(填最简整数比)。
(2)在T K、1.0×104 kPa下,等物质的量的CO与CH 混合气体发生如下反应:CO(g)+
2 4
CH
4
(g)CH
3
CHO(g)。反应速率v正 -v逆 =k
正
·p(CO)·p(CH
4
)-k
逆
·p(CH
3
CHO),k
正
、k
逆
分
别为正、逆反应速率常数,p为气体的分压(气体分压p=气体总压p ×体积分数)。用气体
总
分压表示的平衡常数K =4.5×10-5 kPa-1,则CO转化率为20%时,=________。
p
答案 (1)6.27 4 (2)0.8
解析 (1)由图2可知,60 min时Δc(H O)=(2.0-0.4) mol·L-1=1.6 mol·L-1,则Δn(CoFe O)
2 2 4
=Δn(H O)=1.6 mol·L-1×1 L=1.6 mol,Δm(CoFe O )=1.6 mol×235 g·mol-1=376 g,则
2 2 4
60 min内,v(CoFe O)=≈6.27 g·min-1。由图2可知,反应在60 min时达到平衡状态,v
2 4 正
=v ,此时c(H O)=0.4 mol·L-1,c(H )=1.6 mol·L-1,k ·c(H O)=k ·c(H ),则===4,
逆 2 2 正 2 逆 2
a点c(H O)=c(H ),===4。
2 2
(2)当反应达到平衡时v =v ,==K =4.5×10-5 kPa-1;T K、1.0×104 kPa时,设起始
正 逆 p 2
时n(CH)=n(CO)=1 mol,列三段式:
4
CO(g)+CH(g)CHCHO(g)
4 3
起始/mol 1 1 0变化/mol 0.2 0.2 0.2
最终/mol 0.8 0.8 0.2
所以p(CH)=p(CO)=×1.0×104 kPa=×104 kPa,p(CHCHO)=×1.0×104 kPa=×104 kPa,
4 3
所以v =k ·p(CO)·p(CH)=k ××104 kPa××104 kPa,v =k ·p(CHCHO)=k ××104
正 正 4 正 逆 逆 3 逆
kPa,=×=4.5×10-5×=0.8。