热点强化 14 应用“等效平衡”判断平衡移动的结果
1.等效平衡的含义
在一定条件(恒温恒容或恒温恒压)下,同一可逆反应体系,不管是从正反应开始,还是从逆
反应开始,还是正、逆反应同时投料,达到化学平衡状态时,任何相同组分的百分含量(质
量分数、物质的量分数、体积分数等)均相同。
2.等效平衡的判断方法
(1)恒温恒容条件下反应前后气体体积改变的反应
判断方法:极值等量即等效。
例如:2SO (g)+O(g) 2SO (g)
2 2 3
① 2 mol 1 mol 0
② 0 0 2 mol
③ 0.5 mol 0.25 mol 1.5 mol
④ a mol b mol c mol
上述①②③三种配比,按化学方程式的化学计量数关系均转化为反应物,则 SO 均为2
2
mol,O 均为1 mol,三者建立的平衡状态完全相同。
2
④中a、b、c三者的关系满足:c+a=2,+b=1,即与上述平衡等效。
(2)恒温恒压条件下反应前后气体体积改变的反应
判断方法:极值等比即等效。
例如:2SO (g)+O(g)2SO (g)
2 2 3
① 2 mol 3 mol 0
② 1 mol 3.5 mol 2 mol
③ a mol b mol c mol
按化学方程式的化学计量数关系均转化为反应物,则①②中=,故互为等效平衡。
③中a、b、c三者关系满足:=,即与①②平衡等效。
(3)恒温条件下反应前后气体体积不变的反应
判断方法:无论是恒温恒容,还是恒温恒压,只要极值等比即等效,因为压强改变对该类反
应的化学平衡无影响。
例如:H(g) + I(g)2HI(g)
2 2
① 1 mol 1 mol 0
② 2 mol 2 mol 1 mol
③ a mol b mol c mol
①②两种情况下,n(H )∶n(I)=1∶1,故互为等效平衡。
2 2
③中a、b、c三者关系满足∶=1∶1或a∶b=1∶1,c≥0,即与①②平衡等效。3.虚拟“中间态”法构建等效平衡
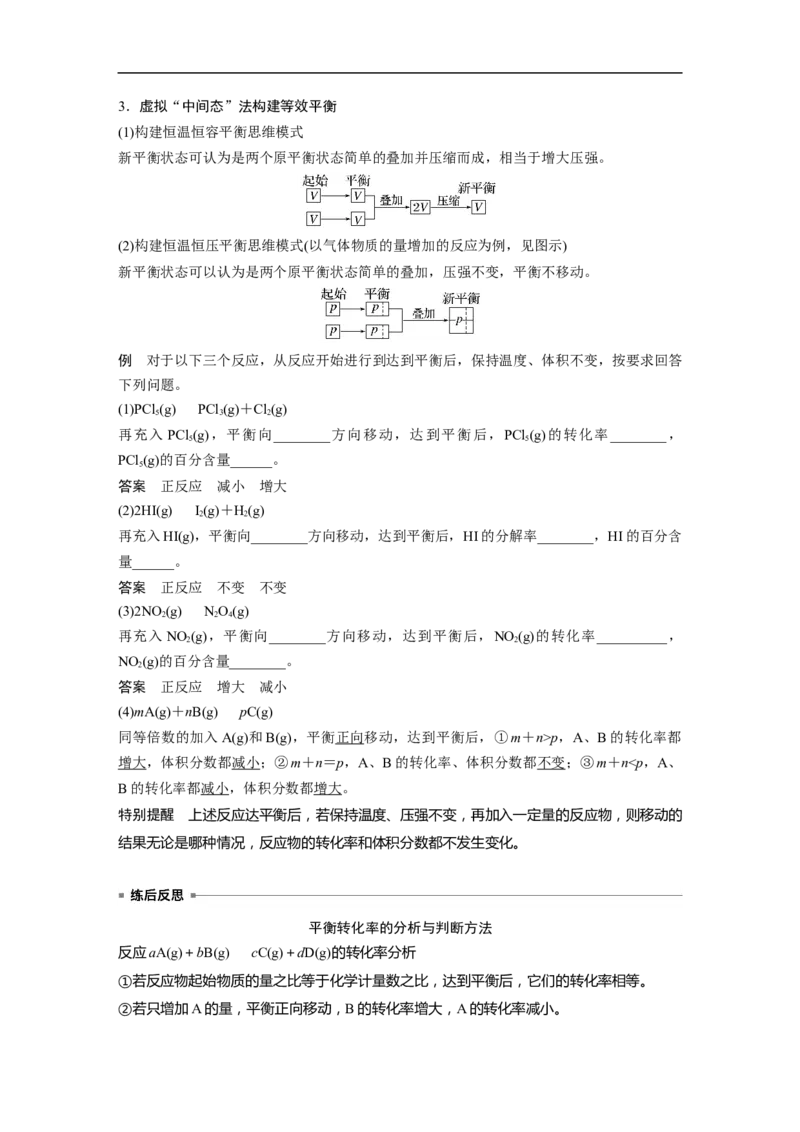
(1)构建恒温恒容平衡思维模式
新平衡状态可认为是两个原平衡状态简单的叠加并压缩而成,相当于增大压强。
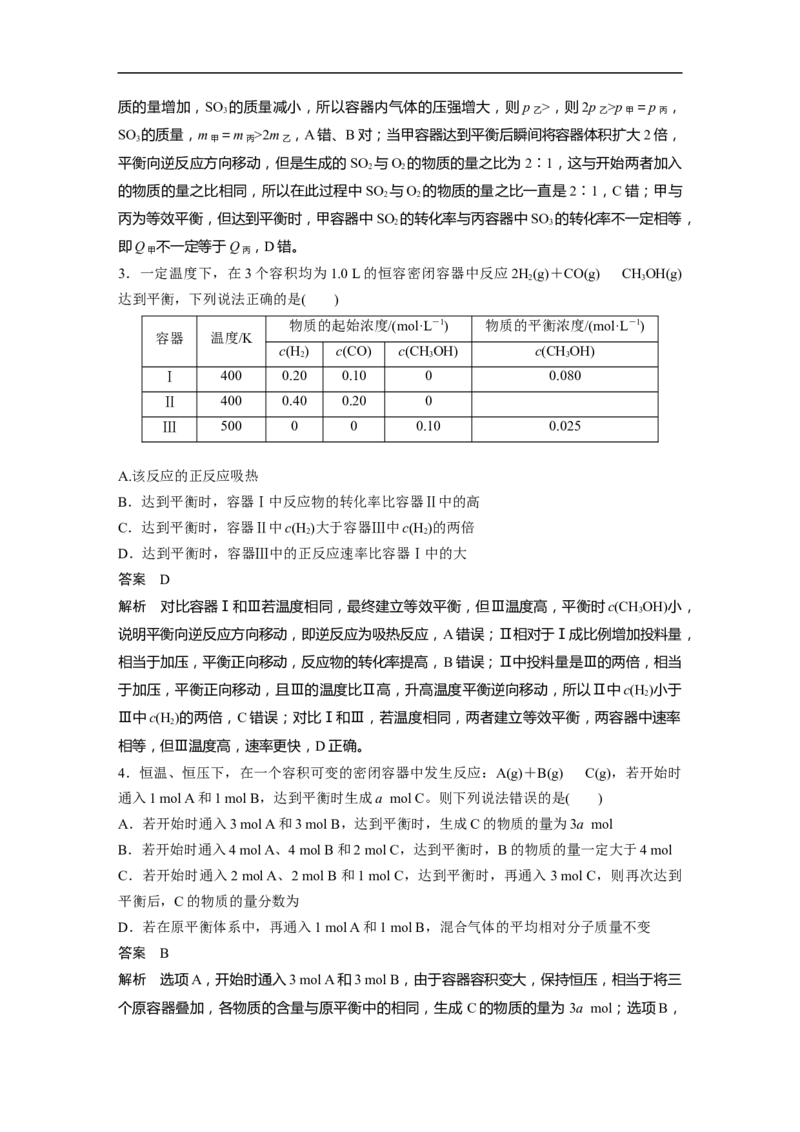
(2)构建恒温恒压平衡思维模式(以气体物质的量增加的反应为例,见图示)
新平衡状态可以认为是两个原平衡状态简单的叠加,压强不变,平衡不移动。
例 对于以下三个反应,从反应开始进行到达到平衡后,保持温度、体积不变,按要求回答
下列问题。
(1)PCl (g)PCl (g)+Cl(g)
5 3 2
再充入 PCl (g),平衡向________方向移动,达到平衡后,PCl (g)的转化率________,
5 5
PCl (g)的百分含量______。
5
答案 正反应 减小 增大
(2)2HI(g)I(g)+H(g)
2 2
再充入HI(g),平衡向________方向移动,达到平衡后,HI的分解率________,HI的百分含
量______。
答案 正反应 不变 不变
(3)2NO (g)NO(g)
2 2 4
再充入NO (g),平衡向________方向移动,达到平衡后,NO (g)的转化率__________,
2 2
NO (g)的百分含量________。
2
答案 正反应 增大 减小
(4)mA(g)+nB(g)pC(g)
同等倍数的加入A(g)和B(g),平衡正向移动,达到平衡后,①m+n>p,A、B的转化率都
增大,体积分数都减小;②m+n=p,A、B的转化率、体积分数都不变;③m+n
丙>乙>丁
C.A的转化率为甲<乙<丙<丁
D.B的浓度为丁>丙>乙>甲
答案 D
解析 以乙为基准,丙相当于增大压强,平衡逆向移动,A的转化率降低;丁相当于在乙的
基础上增加B的浓度,平衡正向移动,A的转化率升高;甲相当于在丙的基础上降低B的
浓度,平衡逆向移动,A的转化率降低,因此,A的转化率关系为甲<丙<乙<丁。以乙为基
准,甲相当于在乙的基础上增加A的浓度,平衡正向移动,B的浓度减少;丙相当于在乙的
基础上增大压强,平衡逆向移动,B的浓度增大;丁相当于在丙的基础上降低A的浓度,平
衡逆向移动,B的浓度增大,因此,B的浓度大小关系为丁>丙>乙>甲。
2.已知2SO (g)+O (g)2SO (g) ΔH=-197 kJ·mol-1。向同温、同体积的三个密闭
2 2 3
容器中分别充入气体:(甲) 2 mol SO 和1 mol O ;(乙) 1 mol SO 和0.5 mol O ;(丙) 2 mol
2 2 2 2
SO 。恒温、恒容下反应达平衡时,下列关系一定正确的是( )
3
A.容器内压强p:p =p >2p
甲 丙 乙
B.SO 的质量m:m =m >2m
3 甲 丙 乙
C.c(SO )与c(O )之比为k:k =k >k
2 2 甲 丙 乙
D.反应放出或吸收热量的数值Q:Q =Q >2Q
甲 丙 乙
答案 B
解析 因为反应2SO (g)+O(g)2SO (g)在恒温恒容的条件下进行,根据等效平衡的原理
2 2 3
可知,甲与丙最后达到平衡时SO 、O 、SO 的物质的量、容器内的压强、SO 与O 的比值
2 2 3 2 2
都相同;乙相当于在甲容器达到平衡后,将容器的体积瞬间扩大为原来的2倍。设甲达到平
衡时容器内的压强为p ,此时容器内瞬间压强减小为,平衡向逆反应方向移动,气体的物
甲质的量增加,SO 的质量减小,所以容器内气体的压强增大,则p >,则2p >p =p ,
3 乙 乙 甲 丙
SO 的质量,m =m >2m ,A错、B对;当甲容器达到平衡后瞬间将容器体积扩大2倍,
3 甲 丙 乙
平衡向逆反应方向移动,但是生成的SO 与O 的物质的量之比为2∶1,这与开始两者加入
2 2
的物质的量之比相同,所以在此过程中SO 与O 的物质的量之比一直是2∶1,C错;甲与
2 2
丙为等效平衡,但达到平衡时,甲容器中SO 的转化率与丙容器中SO 的转化率不一定相等,
2 3
即Q 不一定等于Q ,D错。
甲 丙
3.一定温度下,在3个容积均为1.0 L的恒容密闭容器中反应2H(g)+CO(g)CHOH(g)
2 3
达到平衡,下列说法正确的是( )
物质的起始浓度/(mol·L-1) 物质的平衡浓度/(mol·L-1)
容器 温度/K
c(H ) c(CO) c(CHOH) c(CHOH)
2 3 3
Ⅰ 400 0.20 0.10 0 0.080
Ⅱ 400 0.40 0.20 0
Ⅲ 500 0 0 0.10 0.025
A.该反应的正反应吸热
B.达到平衡时,容器Ⅰ中反应物的转化率比容器Ⅱ中的高
C.达到平衡时,容器Ⅱ中c(H )大于容器Ⅲ中c(H )的两倍
2 2
D.达到平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的大
答案 D
解析 对比容器Ⅰ和Ⅲ若温度相同,最终建立等效平衡,但Ⅲ温度高,平衡时c(CHOH)小,
3
说明平衡向逆反应方向移动,即逆反应为吸热反应,A错误;Ⅱ相对于Ⅰ成比例增加投料量,
相当于加压,平衡正向移动,反应物的转化率提高,B错误;Ⅱ中投料量是Ⅲ的两倍,相当
于加压,平衡正向移动,且Ⅲ的温度比Ⅱ高,升高温度平衡逆向移动,所以Ⅱ中c(H )小于
2
Ⅲ中c(H )的两倍,C错误;对比Ⅰ和Ⅲ,若温度相同,两者建立等效平衡,两容器中速率
2
相等,但Ⅲ温度高,速率更快,D正确。
4.恒温、恒压下,在一个容积可变的密闭容器中发生反应:A(g)+B(g)C(g),若开始时
通入1 mol A和1 mol B,达到平衡时生成a mol C。则下列说法错误的是( )
A.若开始时通入3 mol A和3 mol B,达到平衡时,生成C的物质的量为3a mol
B.若开始时通入4 mol A、4 mol B和2 mol C,达到平衡时,B的物质的量一定大于4 mol
C.若开始时通入2 mol A、2 mol B和1 mol C,达到平衡时,再通入3 mol C,则再次达到
平衡后,C的物质的量分数为
D.若在原平衡体系中,再通入1 mol A和1 mol B,混合气体的平均相对分子质量不变
答案 B
解析 选项A,开始时通入3 mol A和3 mol B,由于容器容积变大,保持恒压,相当于将三
个原容器叠加,各物质的含量与原平衡中的相同,生成 C的物质的量为3a mol;选项B,无法确定平衡移动的方向,不能确定平衡时B的物质的量一定大于4 mol;选项C,根据题
给数据可计算出达到平衡时C的物质的量分数为。
5.在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得
反应达到平衡时的有关数据如下[已知N(g)+3H(g)2NH (g)
2 2 3
ΔH=-92.4 kJ·mol-1]:
容器 甲 乙 丙
反应物投入量 1 mol N 、3 mol H 2 mol NH 4 mol NH
2 2 3 3
NH 的浓度/ (mol·L-1) c c c
3 1 2 3
反应的能量变化 放出a kJ 吸收b kJ 吸收c kJ
体系压强/Pa p p p
1 2 3
反应物转化率 α α α
1 2 3
下列说法正确的是( )
A.2c>c B.a+b=92.4
1 3
C.2p1
2 3 1 3
答案 B
解析 采用“一边倒”的方法知甲、乙是两个相同的装置,且甲中生成的NH 与乙中分解
3
的NH 的和为2 mol,B正确;而丙中加入的NH 是乙中的两倍,开始时c =2c ,但丙中压
3 3 3 2
强亦是乙中的两倍,增大压强,平衡正向移动,则平衡时2cp ,A、C错误;增大
2 3 2 3
压强,不利于NH 的分解,则α>α,故α+α<1,D错误。
3 2 3 1 3
6.有甲、乙两容器,甲容器容积固定,乙容器容积可变。一定温度下,在甲中加入 2 mol
N、3 mol H ,反应N(g)+3H(g)2NH (g)达到平衡时生成NH 的物质的量为m mol。
2 2 2 2 3 3
(1)相同温度下,在乙中加入4 mol N 、6 mol H ,若乙的压强始终与甲的压强相等,乙中反
2 2
应达到平衡时,生成NH 的物质的量________(填字母,下同);若乙的容积与甲的容积始终
3
相等,乙中反应达到平衡时,生成NH 的物质的量________。
3
A.小于m mol
B.等于m mol
C.在m~2m mol之间
D.等于2m mol
E.大于2m mol
(2)相同温度下,保持乙的容积为甲的一半,并加入1 mol NH ,要使乙中反应达到平衡时,
3
各物质的体积分数与上述甲容器中达到平衡时相同,则起始时应加入________mol N 和
2
________mol H。
2
答案 (1)D E (2)0.5 0
解析 (1)由于甲容器恒容,而乙容器恒压,若它们的压强相等,达到平衡时,乙的容积应
该为甲的两倍,生成的NH 的物质的量应该等于2m mol。当甲、乙两容器的容积相等时,
3相当于将建立等效平衡后的乙容器压缩,故乙中 NH 的物质的量大于2m mol。(2)乙的容积
3
为甲的一半时,要建立与甲一样的平衡,则乙中的投入量是甲的一半,故乙中应该投入 N
2
为(1-0.5)mol=0.5 mol,H 为(1.5-1.5) mol=0 mol。
2