文档内容
热点强化 13 控制变量探究影响化学反应速率的因素
在研究影响化学反应速率的因素时,由于外界影响因素较多,故为搞清楚某个因素的影响,
需控制其他因素相同或不变,再进行实验。因此,常用控制变量思想解决该类问题。
1.常见考查形式
(1)以表格的形式给出多组实验数据,让学生找出每组数据的变化对化学反应速率的影响。
(2)给出影响化学反应速率的几种因素,让学生设计实验,分析各因素对化学反应速率的影
响。
2.解题策略
(1)确定变量
解答这类题目时首先要认真审题,理清影响实验探究结果的因素有哪些。
(2)定多变一
在探究时,应该先确定其他因素不变,只变化一种因素,看这种因素与探究的问题存在怎样
的关系;这样确定一种以后,再确定另一种,通过分析每种因素与所探究问题之间的关系,
得出所有影响因素与所探究问题之间的关系。
(3)数据有效
解答时注意选择数据(或设置实验)要有效,且变量统一,否则无法作出正确判断。
3.实例分析
探究温度、催化剂对反应:2HO===2HO+O↑的影响,可以确定催化剂(是否加入MnO )
2 2 2 2 2
和温度(加热、常温)作为可变量,其他的则控制为不变量。
探究对象的反应 2HO===2HO+O↑
2 2 2 2
控制的可变量 催化剂 温度
控制的不变量 浓度、温度等 浓度、催化剂等
取相同量的5%H O 溶液于两 取相同量的5%H O 溶液于
2 2 2 2
支规格相同的试管中,向其中 两支规格相同的试管中,
实验方案
一支试管中加入少量MnO , 给其中一支试管加热,另
2
另一支不加,在常温下观察 一支不加热,观察
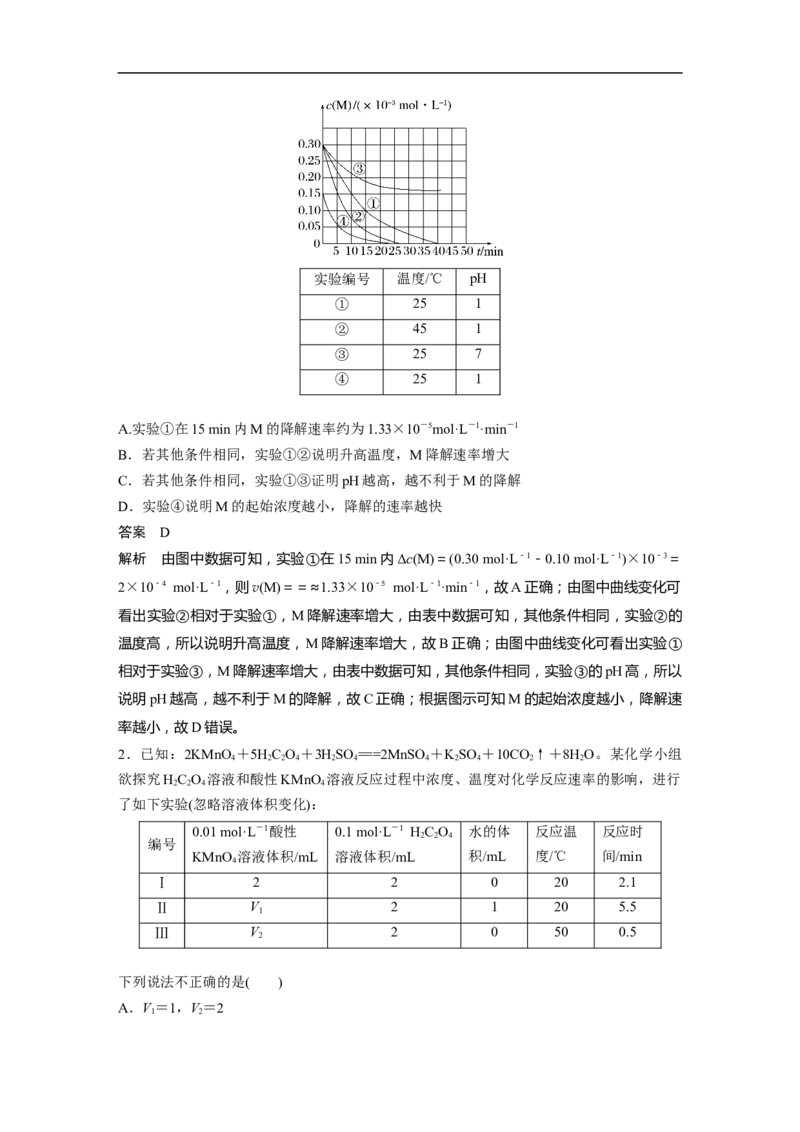
1.用NaFeO 溶液氧化废水中的还原性污染物M,为研究降解效果,设计如下对比实验探
2 4
究温度、浓度、pH对降解速率和效果的影响,实验测得M的浓度与时间关系如图所示,下
列说法不正确的是( )实验编号 温度/℃ pH
① 25 1
② 45 1
③ 25 7
④ 25 1
A.实验①在15 min内M的降解速率约为1.33×10-5mol·L-1·min-1
B.若其他条件相同,实验①②说明升高温度,M降解速率增大
C.若其他条件相同,实验①③证明pH越高,越不利于M的降解
D.实验④说明M的起始浓度越小,降解的速率越快
答案 D
解析 由图中数据可知,实验①在15 min内Δc(M)=(0.30 mol·L-1-0.10 mol·L-1)×10-3=
2×10-4 mol·L-1,则v(M)==≈1.33×10-5 mol·L-1·min-1,故A正确;由图中曲线变化可
看出实验②相对于实验①,M降解速率增大,由表中数据可知,其他条件相同,实验②的
温度高,所以说明升高温度,M降解速率增大,故B正确;由图中曲线变化可看出实验①
相对于实验③,M降解速率增大,由表中数据可知,其他条件相同,实验③的pH高,所以
说明pH越高,越不利于M的降解,故C正确;根据图示可知M的起始浓度越小,降解速
率越小,故D错误。
2.已知:2KMnO +5HC O +3HSO ===2MnSO +KSO +10CO↑+8HO。某化学小组
4 2 2 4 2 4 4 2 4 2 2
欲探究HC O 溶液和酸性KMnO 溶液反应过程中浓度、温度对化学反应速率的影响,进行
2 2 4 4
了如下实验(忽略溶液体积变化):
0.01 mol·L-1酸性 0.1 mol·L-1 HC O 水的体 反应温 反应时
2 2 4
编号
KMnO 溶液体积/mL 溶液体积/mL 积/mL 度/℃ 间/min
4
Ⅰ 2 2 0 20 2.1
Ⅱ V 2 1 20 5.5
1
Ⅲ V 2 0 50 0.5
2
下列说法不正确的是( )
A.V=1,V=2
1 2B.设计实验Ⅰ、Ⅲ的目的是探究温度对反应速率的影响
C.实验计时是从溶液混合开始,溶液呈紫红色时结束
D.实验Ⅲ中用酸性KMnO 溶液的浓度变化表示的反应速率v(KMnO)=0.01 mol·L-1·min-1
4 4
答案 C
解析 实验Ⅰ和实验Ⅱ反应温度相同,实验Ⅱ中加入了1 mL水,根据控制变量的原则,溶
液总体积应保持不变,因而V =1,类比分析可得V =2,A正确;实验Ⅰ、Ⅲ的温度不同,
1 2
其他条件相同,因而可知设计实验Ⅰ、Ⅲ的目的是探究温度对反应速率的影响,B正确;酸
性KMnO 溶液呈紫红色,由表中数据可知,草酸溶液过量,KMnO 可反应完全,因而可以
4 4
用颜色变化来判断反应终点,即实验计时是从溶液混合开始,溶液紫红色刚好褪去时结束,
C错误;根据实验Ⅲ中有关数据可知,Δc(KMnO)==0.005 mol·L-1,v(KMnO)===0.01
4 4
mol·L-1·min-1,D正确。
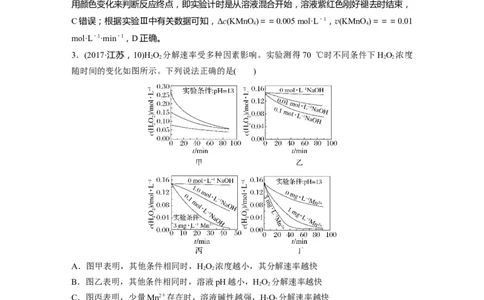
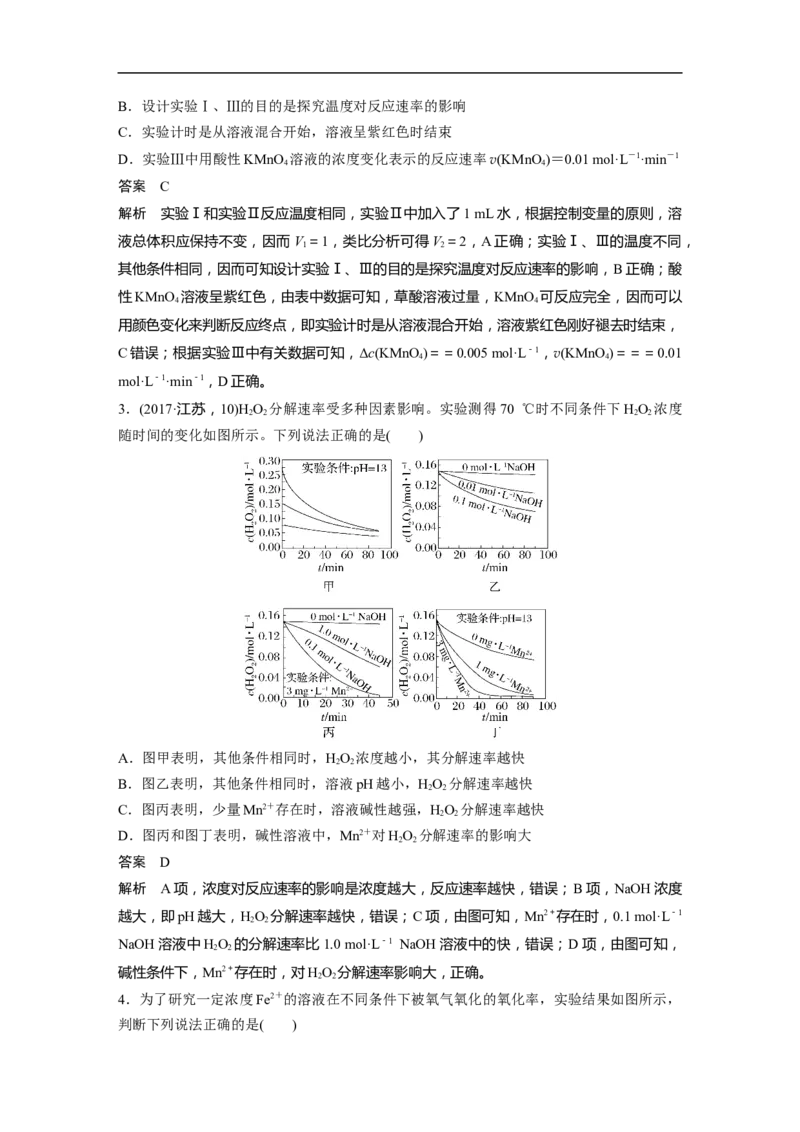
3.(2017·江苏,10)HO 分解速率受多种因素影响。实验测得70 ℃时不同条件下HO 浓度
2 2 2 2
随时间的变化如图所示。下列说法正确的是( )
A.图甲表明,其他条件相同时,HO 浓度越小,其分解速率越快
2 2
B.图乙表明,其他条件相同时,溶液pH越小,HO 分解速率越快
2 2
C.图丙表明,少量Mn2+存在时,溶液碱性越强,HO 分解速率越快
2 2
D.图丙和图丁表明,碱性溶液中,Mn2+对HO 分解速率的影响大
2 2
答案 D
解析 A项,浓度对反应速率的影响是浓度越大,反应速率越快,错误;B项,NaOH浓度
越大,即pH越大,HO 分解速率越快,错误;C项,由图可知,Mn2+存在时,0.1 mol·L-1
2 2
NaOH溶液中HO 的分解速率比1.0 mol·L-1 NaOH溶液中的快,错误;D项,由图可知,
2 2
碱性条件下,Mn2+存在时,对HO 分解速率影响大,正确。
2 2
4.为了研究一定浓度Fe2+的溶液在不同条件下被氧气氧化的氧化率,实验结果如图所示,
判断下列说法正确的是( )A.pH越小,氧化率越小
B.温度越高,氧化率越小
C.Fe2+的氧化率仅与溶液的pH和温度有关
D.实验说明降低pH、升高温度有利于提高Fe2+的氧化率
答案 D
解析 由②③可知,温度相同时,pH越小,氧化率越大,由①②可知,pH相同时,温度越
高,氧化率越大;Fe2+的氧化率除受pH、温度影响外,还受其他因素影响,如浓度等。
5.(1)某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:
序 纯锌 2.0 mol·L-1 硫酸铜 加入蒸
温度/℃
号 粉/g 硫酸溶液/mL 固体/g 馏水/mL
Ⅰ 2.0 50.0 25 0 0
Ⅱ 2.0 40.0 25 0 10.0
Ⅲ 2.0 50.0 25 0.2 0
Ⅳ 2.0 50.0 25 4.0 0
①本实验待测数据可以是________________________________________________________,
实验Ⅰ和实验Ⅱ可以探究__________对锌与稀硫酸反应速率的影响。
②实验Ⅲ和实验Ⅳ的目的是______________________________________________________,
写出有关反应的离子方程式:_____________________________________________________。
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
实验 体积V/mL
序号 KSO 溶液 水 KI溶液 NaSO 溶液 淀粉溶液
2 2 8 2 2 3
① 10.0 0.0 4.0 4.0 2.0
② 9.0 1.0 4.0 4.0 2.0
③ 8.0 V 4.0 4.0 2.0
x
表中V=________,理由是___________________________________________________。
x
答案 (1)①反应结束所需要的时间(或相同条件下产生等体积的氢气所需要的时间) 硫酸
浓度 ②探究硫酸铜的质量对反应速率的影响 Zn+Cu2+===Zn2++Cu,Zn+2H+===Zn2+
+H↑
2(2)2.0 保证反应物KSO 浓度的改变,而其他物质的浓度不变
2 2 8
解析 (1)实验Ⅰ和实验Ⅱ中,锌的质量和状态相同,硫酸的浓度不同,实验Ⅲ和实验Ⅳ中
加入硫酸铜,Cu2+的氧化性强于H+,首先发生反应Zn+Cu2+===Zn2++Cu,生成的铜附着
在锌表面,在稀硫酸溶液中构成原电池,加快锌失电子。但是加入的硫酸铜过多,生成的铜
会覆盖在锌表面,阻止锌与稀硫酸进一步反应,产生氢气的速率会减慢。
(2)实验的目的是探究KSO 溶液的浓度对化学反应速率的影响,故应保证每组实验中其他
2 2 8
物质的浓度相等,即溶液的总体积相等(为20.0 mL),从而可知V=2.0。
x
控制变量法解决问题的基本思路[以第5题(1)为例]