文档内容
第 37 讲 化学反应速率
复习目标 1.了解化学反应速率的概念和定量表示方法。2.了解反应活化能的概念,了解
催化剂的重要作用。3.理解外界条件(浓度、温度、压强、催化剂等)对反应速率的影响,能
用相关理论解释其一般规律。4.了解化学反应速率的调控在生活、生产和科学研究领域中的
重要作用。
考点一 化学反应速率的概念及计算
1.化学反应速率
2.化学反应中各物质浓度的计算模式——“三段式”
(1)写出有关反应的化学方程式。
(2)找出各物质的起始量、转化量、某时刻量。
(3)根据已知条件列方程式计算。例如:反应 mA + nB===pC
t s/(mol·L-1) a b 0
0
转化/(mol·L-1) x
t s/(mol·L-1) a-x b-
1
则v(A)= mol·L-1·s-1,
v(B)= mol·L-1·s-1,
v(C)= mol·L-1·s-1。
3.比较化学反应速率大小的常用方法
(1)先换算成同一物质、同一单位表示,再比较数值的大小。
(2)比较化学反应速率与化学计量数的比值,即对于一般反应 aA(g)+bB(g)===cC(g)+
dD(g),比较与,若>,则不同情况下,用A表示的反应速率比用B表示的大。
(3)应用举例
已知反应4CO+2NO =====N+4CO 在不同条件下的化学反应速率如下:
2 2 2
①v(CO)=1.5 mol·L-1·min-1
②v(NO )=0.7 mol·L-1·min-1
2
③v(N )=0.4 mol·L-1·min-1
2
④v(CO)=1.1 mol·L-1·min-1
2
⑤v(NO )=0.01 mol·L-1·s-1
2
请比较上述5种情况反应的快慢:________________(由大到小的顺序)。
答案 ③>①>②>⑤>④
解析 ②v(CO)=2v(NO )=1.4 mol·L-1·min-1;③v(CO)=4v(N )=1.6 mol·L-1·min-1;
2 2
④v(CO)=v(CO)=1.1 mol·L-1·min-1;⑤v(CO)=2v(NO )=0.02 mol·L-1·s-1=1.2 mol·L-
2 2
1·min-1,故反应的快慢为③>①>②>⑤>④。
1.由v=计算平均速率,用反应物表示为正值,用生成物表示为负值( )
2.单位时间内反应物浓度的变化量表示正反应速率,生成物浓度的变化量表示逆反应速率(
)
3.对于任何化学反应来说,都必须用单位时间内反应物或生成物浓度的变化量来表示化学
反应速率( )
4.化学反应速率为0.8 mol·L-1·s-1是指1 s时某物质的浓度为0.8 mol·L-1( )
5.同一化学反应,相同条件下用不同物质表示的反应速率,数值越大,表示化学反应速率
越快( )
答案 1.× 2.× 3.× 4.× 5.×一、化学反应速率的计算
1.(2021·浙江6月选考,20改编)一定温度下,在NO 的四氯化碳溶液(100 mL)中发生分解
2 5
反应:2NO4NO +O。在不同时刻测量放出的O 体积,换算成NO 浓度如下表:
2 5 2 2 2 2 5
t/s 0 600 1 200 1 710 2 220 2 820 x
c(N O)/ (mol·L-1) 1.40 0.96 0.66 0.48 0.35 0.24 0.12
2 5
(1)计算600~1 200 s,生成NO 的平均速率。
2
(2)计算反应2 220 s时,放出标准状况下的O 体积。
2
(3)分析上表的变化规律,推测表中x值。
答案 (1)600~1 200 s内平均速率v(N O)==5.0×10-4 mol·L-1·s-1,则生成NO 的平均速
2 5 2
率
v(NO )=2v(N O)=2×5.0×10-4 mol·L-1·s-1=1.0×10-3 mol·L-1·s-1。
2 2 5
(2)0~2 220 s内NO 的浓度变化为1.40 mol·L-1-0.35 mol·L-1=1.05 mol·L-1,
2 5
Δn(N O)=1.05 mol·L-1×0.1 L=0.105 mol,
2 5
由反应方程式计量数关系得:
Δn(O )=Δn(N O)=0.052 5 mol,
2 2 5
则标准状况下的V(O )=0.052 5 mol×22.4 L·mol-1=1.176 L。
2
(3)3 930
解析 (3)分析表中数据可知,该反应经过1 110 s(600~1 710,1 710~2 820)后NO 的浓度会
2 5
变为原来的,因此,NO 的浓度由0.24 mol·L-1变为0.12 mol·L-1时,可以推测上表中的x
2 5
为2 820+1 110=3 930。
2.在新型RuO 催化剂作用下,使HCl转化为Cl 的反应2HCl(g)+O(g)HO(g)+Cl(g)具
2 2 2 2 2
有更好的催化活性。一定条件下测得反应过程中n(Cl )的数据如下:
2
t/min 0 2 4 6 8
n(Cl )/10-3 mol 0 1.8 3.7 5.4 7.2
2
计算2~6 min内以HCl的物质的量变化表示的反应速率(以mol·min-1为单位,写出计算过
程)。
答案 解法一 2~6 min内,Δn(Cl )=5.4×10-3 mol-1.8×10-3 mol=3.6×10-3 mol,
2
v(Cl )==9.0×10-4 mol·min-1,
2
所以v(HCl)=2v(Cl )=2×9.0×10-4 mol·min-1=1.8×10-3 mol·min-1。
2
解法二 HCl转化的物质的量为n,则
2HCl(g)+O(g)HO(g)+Cl(g)
2 2 2
2 1n (5.4-1.8)×10-3 mol
解得n=7.2×10-3 mol,所以v(HCl)==1.8×10-3 mol·min-1。
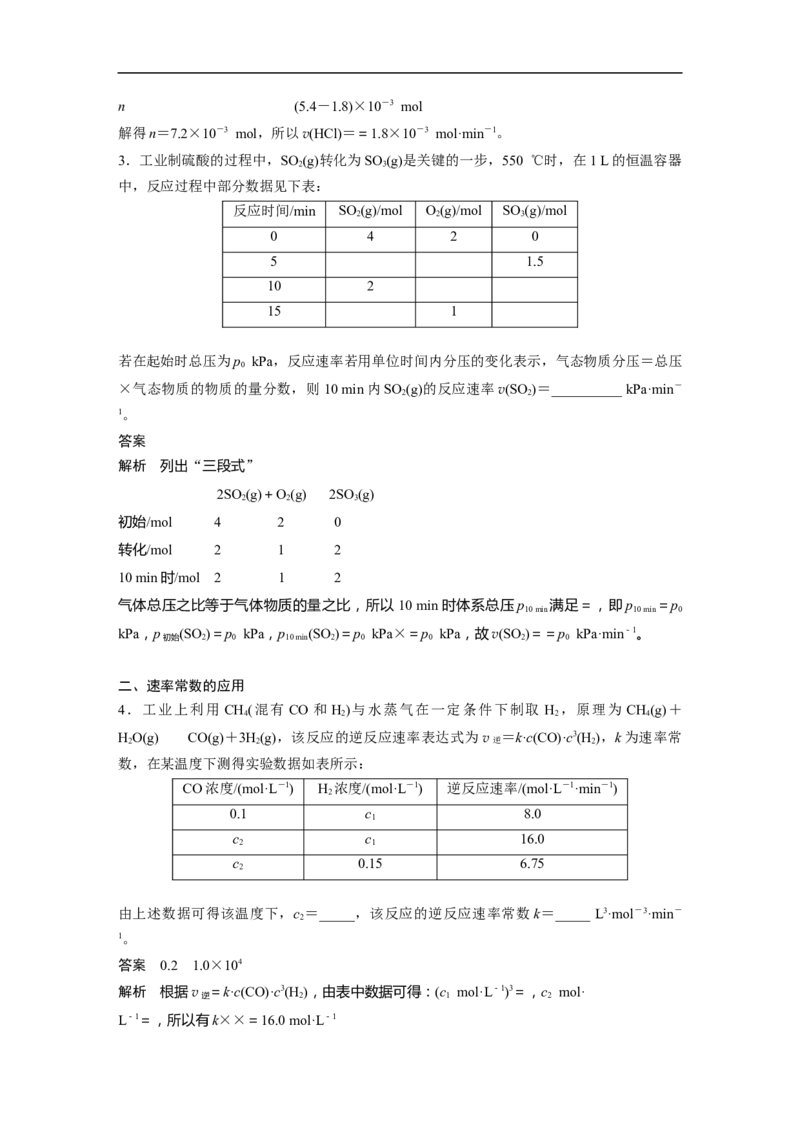
3.工业制硫酸的过程中,SO (g)转化为SO (g)是关键的一步,550 ℃时,在1 L的恒温容器
2 3
中,反应过程中部分数据见下表:
反应时间/min SO (g)/mol O(g)/mol SO (g)/mol
2 2 3
0 4 2 0
5 1.5
10 2
15 1
若在起始时总压为p kPa,反应速率若用单位时间内分压的变化表示,气态物质分压=总压
0
×气态物质的物质的量分数,则10 min内SO (g)的反应速率v(SO )=__________ kPa·min-
2 2
1。
答案
解析 列出“三段式”
2SO (g)+O(g)2SO (g)
2 2 3
初始/mol 4 2 0
转化/mol 2 1 2
10 min时/mol 2 1 2
气体总压之比等于气体物质的量之比,所以 10 min时体系总压p 满足=,即p =p
10 min 10 min 0
kPa,p (SO )=p kPa,p (SO )=p kPa×=p kPa,故v(SO )==p kPa·min-1。
初始 2 0 10 min 2 0 0 2 0
二、速率常数的应用
4.工业上利用 CH(混有 CO 和 H)与水蒸气在一定条件下制取 H ,原理为 CH(g)+
4 2 2 4
H
2
O(g) CO(g)+3H
2
(g),该反应的逆反应速率表达式为v逆 =k·c(CO)·c3(H
2
),k为速率常
数,在某温度下测得实验数据如表所示:
CO浓度/(mol·L-1) H 浓度/(mol·L-1) 逆反应速率/(mol·L-1·min-1)
2
0.1 c 8.0
1
c c 16.0
2 1
c 0.15 6.75
2
由上述数据可得该温度下,c =_____,该反应的逆反应速率常数k=_____ L3·mol-3·min-
2
1。
答案 0.2 1.0×104
解析 根据v =k·c(CO)·c3(H ),由表中数据可得:(c mol·L-1)3=,c mol·
逆 2 1 2
L-1=,所以有k××=16.0 mol·L-1·min-1,解得k=1.0×104 L3·mol-3·min-1,带入c 的等式可得c=0.2。
2 2
5.300 ℃时,2NO(g)+Cl
2
(g)2ClNO(g)的正反应速率表达式为v正 =k·cn(ClNO),测得速
率和浓度的关系如下表:
序号 c(ClNO)/(mol·L-1) v/(mol·L-1·s-1)
① 0.30 3.60×10-9
② 0.60 1.44×10-8
③ 0.90 3.24×10-8
n=________;k=________________。
答案 2 4.0×10-8 L·mol-1·s-1
解析 根据表格①②中的数据,代入速率表达式然后做比:=,解得n=2,k=4×10-8
L·mol-1·s-1。
1.速率常数的含义
速率常数(k)是指在给定温度下,反应物浓度皆为1 mol·L-1时的反应速率。在相同浓度的条
件下,可用速率常数大小来比较化学反应的反应速率。
化学反应速率与反应物浓度(或浓度的次方)成正比,而速率常数是其比例常数,在恒温条件
下,速率常数不随反应物浓度的变化而改变。因此,可以应用速率方程求出该温度下任意浓
度时的反应速率。
2.速率方程
一定温度下,化学反应速率与反应物浓度以其计量数为指数的幂的乘积成正比。
对于反应:aA+bB===gG+hH
则v=k·ca(A)·cb(B)(其中k为速率常数)。
如:①SO ClSO +Cl
2 2 2 2
v=k·c(SO Cl)
1 2 2
②2NO 2NO+O v=k·c2(NO )
2 2 2 2
③2H+2NON+2HO
2 2 2
v=k·c2(H )·c2(NO)
3 2
3.速率常数的影响因素
温度对化学反应速率的影响是显著的,速率常数是温度的函数。同一反应,温度不同,速率
常数将有不同的值,但浓度不影响速率常数。考点二 影响化学反应速率的因素
1.内因
反应物本身的性质是主要因素。如相同条件下 Mg、Al与稀盐酸反应的速率大小关系为Mg
> A l。
2.外因
3.理论解释——有效碰撞理论
(1)活化分子、活化能、有效碰撞
①活化分子:能够发生有效碰撞的分子(必须具有足够的能量)。
②活化能:如图
图中:E 表示反应的活化能,使用催化剂时的活化能为E ,反应热为E - E (注:E 表示活
1 3 1 2 2
化分子变成生成物分子放出的能量)。
③有效碰撞:活化分子之间能够引发化学反应的碰撞。
(2)活化分子、有效碰撞与反应速率的关系4.稀有气体对反应速率的影响
A(g)+B(g)C(g),恒温恒容,充入氦气,对反应速率有何影响?恒温恒压,充入氦气,
对反应速率又有何影响?
1.催化剂参与化学反应,改变了活化能,但反应前后的性质保持不变( )
2.升温时吸热反应速率增大,放热反应速率减小( )
3.对于反应:A+BC,改变容器容积,化学反应速率一定发生变化( )
4.碳酸钙与盐酸反应的过程中,再增加CaCO 固体,可以加快反应速率( )
3
5.增大反应物的浓度,能够增大活化分子的百分数,所以反应速率增大( )
6.100 mL 2 mol·L-1盐酸与锌片反应,加入适量的氯化钠溶液,反应速率不变( )
答案 1.× 2.× 3.× 4.× 5.× 6.×
影响化学反应速率的因素
1.某温度下,在容积一定的密闭容器中进行如下反应 2X(g)+Y(g)Z(g)+W(s) ΔH>0。
下列叙述正确的是( )
A.向容器中充入氩气,反应速率不变
B.加入少量W,逆反应速率增大
C.升高温度,正反应速率增大,逆反应速率减小
D.将容器的容积压缩,可增大单位体积内活化分子的百分数,有效碰撞次数增大
答案 A解析 向恒容容器中充入氩气,各反应组分的浓度不变,反应速率不变,A项正确;W为
固态,加入少量W,反应速率不变,B项错误;升高温度,正、逆反应速率均增大,C项错
误;将容器的容积压缩,可增大单位体积内活化分子数和有效碰撞次数,但活化分子百分数
不变,D项错误。
2.一定温度下,反应N(g)+O(g)2NO(g)在密闭容器中进行,回答下列措施对化学反应
2 2
速率的影响(填“增大”“减小”或“不变”)。
(1) 缩 小 体 积 使 压 强 增 大 : __________ , 原 因 是
________________________________________。
(2)恒容充入N:__________。
2
(3) 恒 容 充 入 He : __________ , 原 因 是
_______________________________________________。
(4)恒压充入He:__________。
答案 (1)增大 单位体积内,活化分子数目增加,有效碰撞的次数增多 (2)增大 (3)不变
单位体积内活化分子数不变 (4)减小
3.(2022·潍坊模拟)“接触法制硫酸”的主要反应是2SO +O2SO ,在催化剂表面的
2 2 3
反应历程如下:
下列说法正确的是( )
A.使用催化剂只能加快正反应速率
B.反应②的活化能比反应①大
C.该反应的催化剂是VO
2 4
D.过程中既有V—O的断裂,又有V—O的形成
答案 D
解析 催化剂能同等幅度地改变正、逆反应速率,加快正反应速率的同时也加快逆反应速率,
故A错误;一般情况下,反应的活化能越小,反应速率越快,故反应②的活化能比反应①
的小,故B错误;催化剂是反应前后质量和化学性质都没有发生变化的物质,从反应历程
图中可知,该反应的催化剂为VO,故C错误;历程中反应①有V—O的断裂,反应②有
2 5
V—O的形成,故D正确。
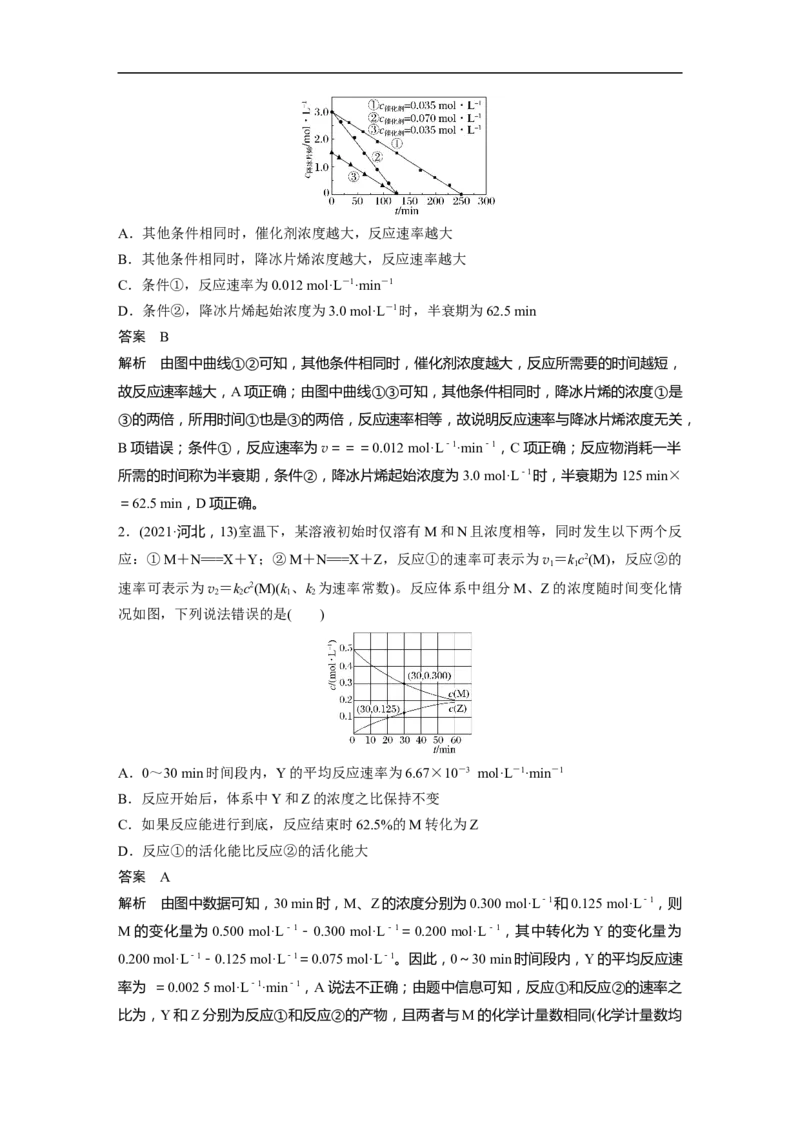
1.(2021·辽宁,12)某温度下,降冰片烯在钛杂环丁烷催化下聚合,反应物浓度与催化剂浓
度及时间关系如图。已知反应物消耗一半所需的时间称为半衰期,下列说法错误的是( )A.其他条件相同时,催化剂浓度越大,反应速率越大
B.其他条件相同时,降冰片烯浓度越大,反应速率越大
C.条件①,反应速率为0.012 mol·L-1·min-1
D.条件②,降冰片烯起始浓度为3.0 mol·L-1时,半衰期为62.5 min
答案 B
解析 由图中曲线①②可知,其他条件相同时,催化剂浓度越大,反应所需要的时间越短,
故反应速率越大,A项正确;由图中曲线①③可知,其他条件相同时,降冰片烯的浓度①是
③的两倍,所用时间①也是③的两倍,反应速率相等,故说明反应速率与降冰片烯浓度无关,
B项错误;条件①,反应速率为v===0.012 mol·L-1·min-1,C项正确;反应物消耗一半
所需的时间称为半衰期,条件②,降冰片烯起始浓度为3.0 mol·L-1时,半衰期为125 min×
=62.5 min,D项正确。
2.(2021·河北,13)室温下,某溶液初始时仅溶有M和N且浓度相等,同时发生以下两个反
应:①M+N===X+Y;②M+N===X+Z,反应①的速率可表示为v =kc2(M),反应②的
1 1
速率可表示为v =kc2(M)(k 、k 为速率常数)。反应体系中组分M、Z的浓度随时间变化情
2 2 1 2
况如图,下列说法错误的是( )
A.0~30 min时间段内,Y的平均反应速率为6.67×10-3 mol·L-1·min-1
B.反应开始后,体系中Y和Z的浓度之比保持不变
C.如果反应能进行到底,反应结束时62.5%的M转化为Z
D.反应①的活化能比反应②的活化能大
答案 A
解析 由图中数据可知,30 min时,M、Z的浓度分别为0.300 mol·L-1和0.125 mol·L-1,则
M的变化量为0.500 mol·L-1-0.300 mol·L-1=0.200 mol·L-1,其中转化为Y的变化量为
0.200 mol·L-1-0.125 mol·L-1=0.075 mol·L-1。因此,0~30 min时间段内,Y的平均反应速
率为 =0.002 5 mol·L-1·min-1,A说法不正确;由题中信息可知,反应①和反应②的速率之
比为,Y和Z分别为反应①和反应②的产物,且两者与M的化学计量数相同(化学计量数均为1),因此反应开始后,体系中Y和Z的浓度之比等于 ,由于k 、k 为速率常数,故该比
1 2
值保持不变,B说法正确; 结合A、B的分析可知,此反应开始后,在相同的时间内体系
中Y和Z的浓度之比等于==,因此,如果反应能进行到底,反应结束时有的M转化为
Z,即62.5%的M转化为Z,C说法正确;由以上分析可知,在相同的时间内生成 Z较多、
生成Y较少,因此,反应①的化学反应速率较小,在同一体系中,活化能较小的化学反应
速率较快,故反应①的活化能比反应②的活化能大,D说法正确。
3.[2020·全国卷Ⅱ,28(2)]高温下,甲烷生成乙烷的反应如下:2CH――→C H +H 。反应在
4 2 6 2
初期阶段的速率方程为r=k× ,其中k为反应速率常数。
①设反应开始时的反应速率为 r ,甲烷的转化率为α时的反应速率为r ,则r =________
1 2 2
r。
1
②对于处于初期阶段的该反应,下列说法正确的是________。
A.增加甲烷浓度,r增大
B.增加H 浓度,r增大
2
C.乙烷的生成速率逐渐增大
D.降低反应温度,k减小
答案 ①(1-α) ②AD
解析 ①甲烷的转化率为α时, 则 即r =(1-
2
α)r 。②A对,由速率方程知,甲烷的浓度越大,反应越快;B错,H 的浓度大小不影响反
1 2
应速率;C错,反应过程中 逐渐减小,故C H 的生成速率逐渐减小;D对,降低反应
2 6
温度,反应速率减小,故k减小。
课时精练
1.下列说法正确的是( )
A.活化分子的每一次碰撞都能发生化学反应
B.能发生有效碰撞的分子一定是活化分子
C.反应物用量增加后,有效碰撞次数增多,反应速率增大
D.催化剂能提高活化分子的活化能,从而加快反应速率
答案 B
解析 活化分子只有发生有效碰撞时才能发生化学反应,A项错误;增加固体或纯液体的量,
反应速率不变,C项错误;催化剂能降低反应的活化能,使原来不是活化分子的分子变成活
化分子,提高了活化分子的百分数,加快了化学反应速率,D项错误。2.反应3Fe(s)+4HO(g)Fe O(s)+4H(g)在一容积可变的密闭容器中进行,下列条件的
2 3 4 2
改变对其化学反应速率几乎无影响的是( )
A.保持容积不变,增加HO(g)的物质的量
2
B.将容器的容积缩小一半
C.保持容积不变,充入Ar使压强增大
D.保持压强不变,充入Ar使容积增大
答案 C
解析 容积不变,增加HO(g)的物质的量,反应物浓度增大,化学反应速率加快,A不符
2
合题意;将容器的容积缩小一半,反应物的浓度增大,化学反应速率加快,B不符合题意;
保持容积不变,充入Ar,Ar不参与反应,反应体系中各物质的浓度不变,化学反应速率不
变,C符合题意;保持压强不变,充入Ar,容器的容积变大,反应物的浓度减小,化学反
应速率减小,D不符合题意。
3.如图安装好实验装置(装置气密性良好),在锥形瓶内盛有6.5 g锌粒(Zn的相对原子质量
为65),通过分液漏斗加入40 mL 2.5 mol·L-1的稀硫酸,将产生的H 收集在注射器中,10 s
2
时恰好收集到标准状况下的H 44.8 mL。下列说法不正确的是( )
2
A.忽略锥形瓶内溶液体积的变化,用H+表示10 s内该反应的速率为0.01 mol·L-1·s-1
B.忽略锥形瓶内溶液体积的变化,用Zn2+表示10 s内该反应的速率为0.01 mol·L-1·s-1
C.用锌粒表示10 s内该反应的速率为0.013 g·s-1
D.用H 表示10 s内该反应的速率为0.000 2 mol·s-1
2
答案 B
解析 Zn+ 2H+=== Zn2++ H↑
2
65 g 2 mol 1 mol 22.4 L
0.13 g 0.004 mol 0.002 mol 0.044 8 L
v(H+)==0.01 mol·L-1·s-1,A正确;
v(Zn2+)=v(H+)=0.005 mol·L-1·s-1,B错误;用锌粒表示10 s内该反应的速率为=
0.013 g·s-1,C正确;用H 表示10 s内该反应的速率为=0.000 2 mol·s-1,D正确。
2
4.一定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应,反应中各物质的
物质的量变化如图所示,对该反应的推断合理的是( )A.该反应的化学方程式为3B+4D6A+2C
B.反应进行到1 s时,v(A)=v(C)
C.反应进行到6 s时,B的平均反应速率为0.05 mol·L-1·s-1
D.反应进行到6 s时,各物质的反应速率相等
答案 C
解析 由图像可知,B、C的物质的量减小,是反应物,A、D的物质的量增大,是生成物,
前 6 s 内,Δn(B)∶Δn(C)∶Δn(A)∶Δn(D)=(1.0-0.4)∶(1.0-0.2)∶(1.2-0)∶(0.4-0)=
3∶4∶6∶2,故反应的化学方程式为3B+4C6A+2D,A项错误;v(A)∶v(C)=3∶2,B
项错误;反应进行到6 s时,v(B)==0.05 mol·L-1·s-1,C项正确;反应进行到6 s时,反应
达到平衡状态,但各物质的反应速率并不相等,D错误。
5.O 在水中易分解,一定条件下,相同浓度的O 的浓度减小一半所需的时间(t)如下表。
3 3
pH
t/min 3.0 4.0 5.0 6.0
T/℃
20 301 231 169 58
30 158 108 48 15
50 31 26 15 7
根据表中的递变规律,推测O 分别在以下条件下反应:①40 ℃、pH=3.0;②10 ℃、pH
3
=5.0;③30 ℃、pH=7.0,分解速率依次增大的顺序为( )
A.①②③ B.③②①
C.②①③ D.③①②
答案 C
解析 分析题表中数据,温度一定时,pH越大,c(O )减小一半所需时间越短;pH一定时,
3
温度越高,c(O )减小一半所需时间越短。c(O )减小一半,在①40 ℃、pH=3.0时,所需时
3 3
间在31~158 min之间;在②10 ℃、pH=5.0时,所需时间大于169 min;在③30 ℃、pH
=7.0时,所需时间小于15 min,则分解速率依次增大的顺序为②<①<③。
6.一定温度下反应:4A(s)+3B(g)2C(g)+D(g),经2 min,B的浓度减少0.6 mol·L-1,
对此反应速率的表示正确的是( )
A.用A表示的反应速率是0.4 mol·L-1·min-1
B.分别用B、C、D表示反应速率,其比值是1∶2∶3C.在2 min末的反应速率,用B表示为0.3 mol·L-1·min-1
D.在这2 min内用B和C表示的瞬时速率的值都是逐渐减小的
答案 D
解析 A是固体,不能用其浓度的变化来表示反应速率;v =0.3 mol·L-1·min-1,表示2 min
B
内的平均反应速率,在2 min末的速率为瞬时速率,不等于0.3 mol·L-1·min-1;在反应过程
中B的浓度逐渐减小,故A、B反应生成C、D的瞬时速率也逐渐减小。
7.2SO (g)+O(g)2SO (g) ΔH=-198 kJ·mol-1,在VO 存在时,该反应的机理为VO
2 2 3 2 5 2 5
+SO ―→2VO +SO (快),4VO +O―→2VO(慢)。下列说法正确的是( )
2 2 3 2 2 2 5
A.反应速率主要取决于VO 的质量
2 5
B.VO 是该反应的催化剂
2
C.逆反应的活化能大于198 kJ·mol-1
D.增大SO 的浓度可显著提高反应速率
2
答案 C
解析 由反应机理可得,VO 是该反应的催化剂,反应速率与催化剂VO 的质量有一定关
2 5 2 5
系,但主要取决于催化剂VO 的表面积,A、B项错误;ΔH=正反应的活化能-逆反应的
2 5
活化能=-198 kJ·mol-1,所以逆反应的活化能大于198 kJ·mol-1,C项正确;使用催化剂可
以显著提高反应速率,增大SO 的浓度可以提高反应速率(不是显著提高),D项错误。
2
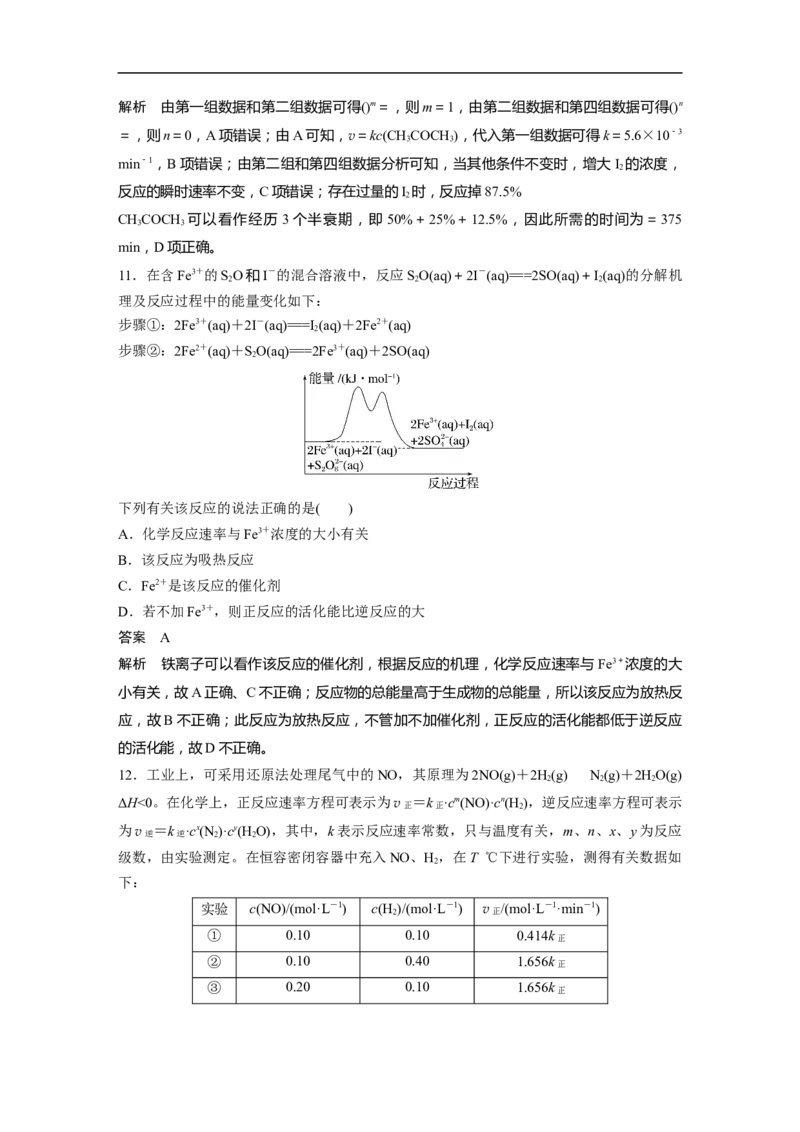
8.研究表明NO与CO在Fe+作用下发生可逆反应的能量变化及反应历程如图所示。下列
2
说法不正确的是( )
A.反应中Fe+是催化剂,FeO+是中间产物
B.总反应速率由反应②的速率决定
C.升高温度,总反应的平衡常数K减小
D.当有14 g N 生成时,转移1 mol e-
2
答案 B
解析 由图可知,Fe+先转化为FeO+,FeO+后续又转化为Fe+,因此Fe+是催化剂,FeO+
是中间产物,A不符合题意;由图可知,反应①的能垒高于反应②,因此反应①的速率较慢,
总反应速率由反应①的速率决定,B符合题意;由图可知,反应物的总能量高于生成物的总
能量,该反应的正反应为放热反应,升高温度,平衡逆向移动,总反应的平衡常数K减小,
C不符合题意;由图可知,总反应的化学方程式为 NO+COCO +N ,N元素化合价
2 2 2
从+1降低至0,当有14 g N 即0.5 mol N 生成时,转移电子的物质的量为 0.5 mol×2=1
2 2mol,D不符合题意。
9.下列表格中的各种情况,可以用对应选项中的图像表示的是( )
选项 反应 甲 乙
A 外形、大小相近的金属和水反应 Na K
4 mL 0.01 mol·L-1 KMnO 溶液分别和 0.1 mol·L-1的 0.2 mol·L-1的
4
B
不同浓度的2 mL H C O(草酸)溶液反应 HC O 溶液 HC O 溶液
2 2 4 2 2 4 2 2 4
5 mL 0.1 mol·L-1 Na SO 溶液和5 mL
2 2 3
C 热水 冷水
0.1 mol·L-1 HSO 溶液反应
2 4
D 5 mL 4%的过氧化氢溶液分解放出O 无MnO 粉末 加MnO 粉末
2 2 2
答案 C
解析 由于K比Na活泼,故大小相近的金属K和Na与水反应,K的反应速率更快,又由
于Na、K与HO反应均为放热反应,随着反应的进行,放出大量的热,反应速率逐渐加快,
2
A项不正确;由于起始时乙中HC O 浓度大,故其反应速率比甲快,B项不正确;由于甲
2 2 4
反应是在热水中进行的,温度高,故甲的反应速率大于乙,随着反应的进行,反应物浓度逐
渐减小,故甲、乙中反应速率逐渐减小,C项正确;MnO 在HO 的分解过程中起催化作用,
2 2 2
故乙的反应速率大于甲,D项不正确。
10.丙酮的碘代反应CHCOCH +I―→CHCOCH I+HI的速率方程为v=kcm(CHCOCH )·
3 3 2 3 2 3 3
cn(I),其半衰期(当剩余反应物恰好是起始的一半时所需的时间)为,改变反应物浓度时,反
2
应的瞬时速率如表所示。
c(CHCOCH )/ (mol·L-1) c(I)/ (mol·L-1) v/(×10-3mol·L-1·min-1)
3 3 2
0.25 0.050 1.4
0.50 0.050 2.8
1.00 0.050 5.6
0.50 0.100 2.8
下列说法正确的是( )
A.速率方程中的m=1、n=1
B.该反应的速率常数k=2.8×10-2min-1
C.增大I 的浓度,反应的瞬时速率加快
2
D.当过量的I 存在时,反应掉87.5%的CHCOCH 所需的时间是375 min
2 3 3
答案 D解析 由第一组数据和第二组数据可得()m=,则m=1,由第二组数据和第四组数据可得()n
=,则n=0,A项错误;由A可知,v=kc(CHCOCH ),代入第一组数据可得k=5.6×10-3
3 3
min-1,B项错误;由第二组和第四组数据分析可知,当其他条件不变时,增大I 的浓度,
2
反应的瞬时速率不变,C项错误;存在过量的I 时,反应掉87.5%
2
CHCOCH 可以看作经历 3个半衰期,即 50%+25%+12.5%,因此所需的时间为=375
3 3
min,D项正确。
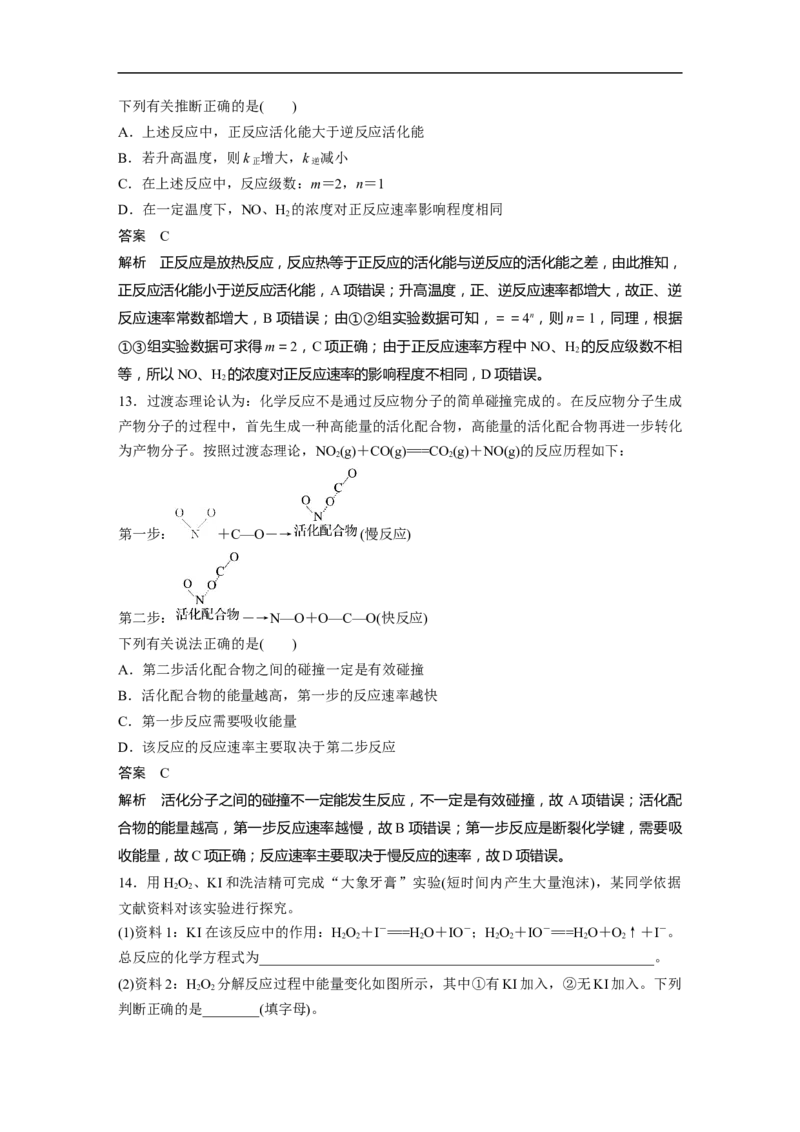
11.在含Fe3+的SO和I-的混合溶液中,反应SO(aq)+2I-(aq)===2SO(aq)+I(aq)的分解机
2 2 2
理及反应过程中的能量变化如下:
步骤①:2Fe3+(aq)+2I-(aq)===I(aq)+2Fe2+(aq)
2
步骤②:2Fe2+(aq)+SO(aq)===2Fe3+(aq)+2SO(aq)
2
下列有关该反应的说法正确的是( )
A.化学反应速率与Fe3+浓度的大小有关
B.该反应为吸热反应
C.Fe2+是该反应的催化剂
D.若不加Fe3+,则正反应的活化能比逆反应的大
答案 A
解析 铁离子可以看作该反应的催化剂,根据反应的机理,化学反应速率与Fe3+浓度的大
小有关,故A正确、C不正确;反应物的总能量高于生成物的总能量,所以该反应为放热反
应,故B不正确;此反应为放热反应,不管加不加催化剂,正反应的活化能都低于逆反应
的活化能,故D不正确。
12.工业上,可采用还原法处理尾气中的NO,其原理为2NO(g)+2H(g)N(g)+2HO(g)
2 2 2
ΔH<0。在化学上,正反应速率方程可表示为v正 =k
正
·cm(NO)·cn(H
2
),逆反应速率方程可表示
为v逆 =k
逆
·cx(N
2
)·cy(H
2
O),其中,k表示反应速率常数,只与温度有关,m、n、x、y为反应
级数,由实验测定。在恒容密闭容器中充入NO、H ,在T ℃下进行实验,测得有关数据如
2
下:
实验 c(NO)/(mol·L-1) c(H
2
)/(mol·L-1) v正 /(mol·L-1·min-1)
① 0.10 0.10 0.414k
正
② 0.10 0.40 1.656k
正
③ 0.20 0.10 1.656k
正下列有关推断正确的是( )
A.上述反应中,正反应活化能大于逆反应活化能
B.若升高温度,则k 增大,k 减小
正 逆
C.在上述反应中,反应级数:m=2,n=1
D.在一定温度下,NO、H 的浓度对正反应速率影响程度相同
2
答案 C
解析 正反应是放热反应,反应热等于正反应的活化能与逆反应的活化能之差,由此推知,
正反应活化能小于逆反应活化能,A项错误;升高温度,正、逆反应速率都增大,故正、逆
反应速率常数都增大,B项错误;由①②组实验数据可知,==4n,则n=1,同理,根据
①③组实验数据可求得m=2,C项正确;由于正反应速率方程中NO、H 的反应级数不相
2
等,所以NO、H 的浓度对正反应速率的影响程度不相同,D项错误。
2
13.过渡态理论认为:化学反应不是通过反应物分子的简单碰撞完成的。在反应物分子生成
产物分子的过程中,首先生成一种高能量的活化配合物,高能量的活化配合物再进一步转化
为产物分子。按照过渡态理论,NO (g)+CO(g)===CO(g)+NO(g)的反应历程如下:
2 2
第一步: +C—O―→ (慢反应)
第二步: ―→N—O+O—C—O(快反应)
下列有关说法正确的是( )
A.第二步活化配合物之间的碰撞一定是有效碰撞
B.活化配合物的能量越高,第一步的反应速率越快
C.第一步反应需要吸收能量
D.该反应的反应速率主要取决于第二步反应
答案 C
解析 活化分子之间的碰撞不一定能发生反应,不一定是有效碰撞,故 A项错误;活化配
合物的能量越高,第一步反应速率越慢,故B项错误;第一步反应是断裂化学键,需要吸
收能量,故C项正确;反应速率主要取决于慢反应的速率,故D项错误。
14.用HO 、KI和洗洁精可完成“大象牙膏”实验(短时间内产生大量泡沫),某同学依据
2 2
文献资料对该实验进行探究。
(1)资料1:KI在该反应中的作用:HO+I-===HO+IO-;HO+IO-===HO+O↑+I-。
2 2 2 2 2 2 2
总反应的化学方程式为________________________________________________________。
(2)资料2:HO 分解反应过程中能量变化如图所示,其中①有KI加入,②无KI加入。下列
2 2
判断正确的是________(填字母)。a.加入KI后改变了反应的路径
b.加入KI后改变了总反应的能量变化
c.HO+I-===HO+IO-是放热反应
2 2 2
(3)实验中发现,HO 与KI溶液混合后,产生大量气泡,溶液颜色变黄。再加入 CCl ,振荡、
2 2 4
静置,气泡明显减少。
资料3:I 也可催化HO 的分解反应。
2 2 2
①加CCl 并振荡、静置后还可观察到__________,说明有I 生成。
4 2
②气泡明显减少的原因可能是:i.H O 浓度降低;
2 2
ii.__________________________。以下对照实验说明i不是主要原因:向HO 溶液中加入
2 2
KI溶液,待溶液变黄后,分成两等份于A、B两试管中。A试管中加入CCl ,B试管中不加
4
CCl ,分别振荡、静置。观察到的现象是___________________________________________。
4
(4)资料4:I-(aq)+I(aq)I(aq) K=640。
2
为了探究体系中含碘微粒的存在形式,进行实验:向20 mL一定浓度的HO 溶液中加入10
2 2
mL 0.10 mol·L-1 KI溶液,达平衡后,相关微粒浓度如下:
微粒 I- I I
2
浓度/(mol·L-1) 2.5×10-3 a 4.0×10-3
①a=________。
②该平衡体系中除了含有 I-、I 、I 外,一定还含有其他含碘微粒,理由是
2
__________________
_______________________________________________________________________________
。
答案 (1)2H O=====2HO+O↑ (2)a (3)①下层溶液呈紫红色 ②在水溶液中I 的浓度
2 2 2 2 2
降低 A试管中产生气泡明显变少;B试管中产生气泡速率没有明显减小 (4)①2.5×10-3
②2c(I)+c(I-)+3c(I)<0.033 mol·L-1
2
解析 (2)加入KI后,一步反应分为两步进行,也就是改变了反应的路径,a正确;加入KI
后,反应物和生成物的能量都没有改变,b不正确;由图可知,反应物的总能量小于生成物
的总能量,所以该反应是吸热反应,c不正确。
(4)①K==640,由此可求出a=2.5×10-3。②原溶液中,c(I-)=≈0.033 mol·L-1;现在溶液
中I-、I 、I中所含I元素的浓度和为 2c(I)+c(I-)+3c(I)=(2×2.5×10-3+2.5×10-3+
2 2
3×4.0×10-3)mol·L-1=0.019 5 mol·L-1<0.033 mol·L-1,I元素不守恒,说明产物中还有其他含碘微粒。