文档内容
第 43 讲 弱电解质的电离平衡
复习目标 1.理解弱电解质在水溶液中的电离平衡。2.理解电离平衡常数,掌握电离平衡常
数的相关计算。3.理解电离平衡常数的相关应用。
考点一 弱电解质的电离平衡及影响因素
1.弱电解质的电离平衡概念
(1)电离平衡的建立
在一定条件下(如温度、压强等),当弱电解质分子电离产生离子的速率和离子结合成分子的
速率相等时,电离过程达到了平衡。
(2)电离平衡的建立与特征
①开始时,v(电离)最大,而v(结合)为0。
②平衡的建立过程中,v(电离)>v(结合)。
③当v(电离)=v(结合)时,电离过程达到平衡状态。
2.影响电离平衡的因素
以0.1 mol·L-1 CHCOOH溶液为例,填写外界条件对CHCOOH(aq)CHCOO-(aq)+H+
3 3 3
(aq) ΔH>0的影响。
改变条件 平衡移动方向 n(H+) c(H+) 导电能力
加水稀释 向右 增大 减小 减弱
加入少量冰醋酸 向右 增大 增大 增强通入HCl(g) 向左 增大 增大 增强
加NaOH(s) 向右 减小 减小 增强
加CHCOONa(s) 向左 减小 减小 增强
3
升高温度 向右 增大 增大 增强
1.弱电解质溶液中至少存在两种共价化合物分子( )
2.氨气溶于水,当NH ·H O电离出的c(OH-)=c(NH)时,表明NH ·H O电离处于平衡状态
3 2 3 2
( )
3.电离平衡右移,电解质分子的浓度一定减小,离子浓度一定增大( )
4.25 ℃时,0.1 mol·L-1 CHCOOH加水稀释,各离子浓度均减小( )
3
5.电离平衡向右移动,弱电解质的电离度一定增大( )
6.电离平衡向右移动,电解质分子的浓度一定减小( )
答案 1.√ 2.× 3.× 4.× 5.× 6.×
电离平衡移动结果的分析
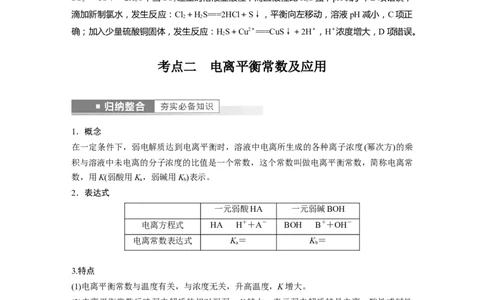
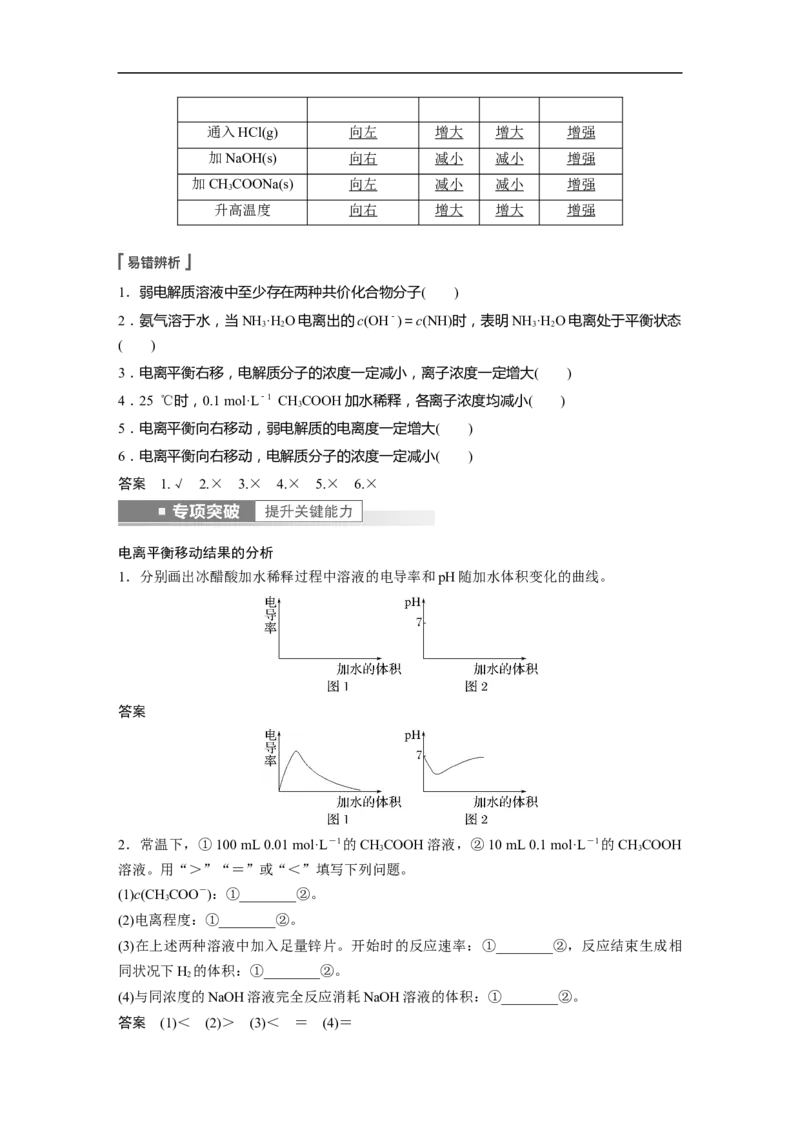
1.分别画出冰醋酸加水稀释过程中溶液的电导率和pH随加水体积变化的曲线。
答案
2.常温下,①100 mL 0.01 mol·L-1的CHCOOH溶液,②10 mL 0.1 mol·L-1的CHCOOH
3 3
溶液。用“>”“=”或“<”填写下列问题。
(1)c(CHCOO-):①________②。
3
(2)电离程度:①________②。
(3)在上述两种溶液中加入足量锌片。开始时的反应速率:①________②,反应结束生成相
同状况下H 的体积:①________②。
2
(4)与同浓度的NaOH溶液完全反应消耗NaOH溶液的体积:①________②。
答案 (1)< (2)> (3)< = (4)=3.HS水溶液中存在电离平衡:HSH++HS-和HS-H++S2-。若向HS溶液中 (
2 2 2
)
A.加水,平衡向右移动,溶液中氢离子浓度增大
B.通入过量SO 气体,平衡向左移动,溶液pH增大
2
C.滴加新制氯水,平衡向左移动,溶液pH减小
D.加入少量硫酸铜固体(忽略体积变化),溶液中所有离子浓度都减小
答案 C
解析 加水促进电离,但氢离子浓度减小,A项错误;通入过量SO 气体发生反应:2HS+
2 2
SO ===3S↓+2HO,当SO 过量时溶液显酸性,而且酸性比HS强,pH减小,B项错误;
2 2 2 2
滴加新制氯水,发生反应:Cl +HS===2HCl+S↓,平衡向左移动,溶液pH减小,C项正
2 2
确;加入少量硫酸铜固体,发生反应:HS+Cu2+===CuS↓+2H+,H+浓度增大,D项错误。
2
考点二 电离平衡常数及应用
1.概念
在一定条件下,弱电解质达到电离平衡时,溶液中电离所生成的各种离子浓度(幂次方)的乘
积与溶液中未电离的分子浓度的比值是一个常数,这个常数叫做电离平衡常数,简称电离常
数,用K(弱酸用K,弱碱用K )表示。
a b
2.表达式
一元弱酸HA 一元弱碱BOH
电离方程式 HAH++A- BOHB++OH-
电离常数表达式 K= K =
a b
3.特点
(1)电离平衡常数与温度有关,与浓度无关,升高温度,K增大。
(2)电离平衡常数反映弱电解质的相对强弱,K越大,表示弱电解质越易电离,酸性或碱性
越强。
(3)多元弱酸的各步电离常数的大小关系是K ≫K ≫K ……,故其酸性取决于第一步的电离。
1 2 3
4.电离度
(1)概念
在一定条件下的弱电解质达到电离平衡时,已经电离的电解质分子数占原电解质分子总数的
百分比。
(2)表示方法
α=×100%,也可表示为α=×100%。(3)影响因素
①相同温度下,同一弱电解质,浓度越大,其电离度(α)越小。
②相同浓度下,同一弱电解质,温度越高,其电离度(α)越大。
1.弱电解质的电离平衡右移,电离常数一定增大( )
2.电离常数大的酸溶液中的c(H+)一定比电离常数小的酸溶液中的c(H+)大( )
3.某一弱电解质,电离度越大,电离常数就越大( )
4.相同温度下,向1 mol·L-1的醋酸溶液中加入少量冰醋酸,其电离度变小( )
5.稀醋酸中加入少量醋酸钠能增大醋酸的电离程度( )
答案 1.× 2.× 3.× 4.√ 5.×
一、利用电离常数判断弱电解质的相对强弱
1.部分弱酸的电离平衡常数如下表:
弱酸 HCOOH HS HCO HClO
2 2 3
电离平衡常 K= K =1.1×10-7 K =4.5×10-7 K=
a a1 a1 a
数(25℃) 1.77×10-4 K =1.3×10-13 K =4.7×10-11 4.0×10-8
a2 a2
按要求回答下列问题:
(1)HCOOH、HS、HCO、HClO的酸性由强到弱的顺序为___________________________。
2 2 3
(2)相同浓度的HCOO-、HS-、S2-、HCO、CO、ClO-结合H+的能力由强到弱的顺序为
______________________________________________________________________________。
(3)运用上述电离常数及物质的特性判断下列化学方程式不正确的是________(填序号)。
①次氯酸与NaHCO 溶液的反应:HClO+HCO===ClO-+HO+CO↑
3 2 2
②少量CO 通入NaClO溶液中:CO+HO+2ClO-===CO+2HClO
2 2 2
③少量CO 通入NaClO溶液中:CO+HO+ClO-===HCO+HClO
2 2 2
④硫化氢通入NaClO溶液中:HS+ClO-===HS-+HClO
2
⑤碳酸钠滴入足量甲酸溶液中:2HCOOH+CO===2HCOO-+CO↑+HO
2 2
答案 (1)HCOOH>HCO>HS>HClO
2 3 2
(2)S2->CO>ClO->HS->HCO>HCOO-
(3)①②④二、判断微粒浓度比值的大小
2.下列关于电解质的说法正确的是______________(填字母)。
A.向0.1 mol·L-1 CHCOOH溶液中加入少量水,溶液中减小
3
B.室温下向10 mL 0.1 mol·L-1的氨水中加水稀释后,溶液中不变
C.等体积、等物质的量浓度的NaCO 和NaHCO 溶液混合:<
2 3 3
D.将浓度为0.1 mol·L-1 HF溶液加水不断稀释过程中,电离平衡常数K(HF)保持不变,始
a
终增大
答案 B
解析 B项,NH ·H O的电离常数K =,温度不变,K 不变,正确;C项,等体积、等物质
3 2 b b
的量浓度的NaCO 和NaHCO 溶液混合,根据电离常数有K =、K =,同一溶液中c(H+)
2 3 3 a1 a2
相等,则c(H+)=K ·=K ·,而K >K ,则>,错误;D项,0.1 mol·L-1的HF加水稀释,
a1 a2 a1 a2
c(F-)趋近于0,而c(H+)趋于不变(10-7 mol·L-1),故变小,错误。
3.常温下,将0.1 mol·L-1的CHCOOH溶液加水稀释,请填写下列表达式中的数据变化情
3
况(填“变大”“变小”或“不变”)。
(1)________;
(2)________;
(3)________;
(4)________;
(5)________。
答案 (1)变小 (2)变大 (3)变小 (4)不变
(5)不变
解析 (1)将该式变为=或稀释时醋酸的电离平衡正向移动,n(CHCOOH)减小,n(H+)增大
3
因而其比值变小。
(2)将该式变为=或稀释时醋酸的电离平衡正向移动,n(CHCOOH)减小,n(CHCOO-)增大
3 3
因而其比值变大。
(5)将该式变为=,故比值不变。
判断溶液中微粒浓度比值的三种方法
(1)将浓度之比转化为物质的量之比进行比较,这样分析起来可以忽略溶液体积的变化,只
需分析微粒数目的变化即可。
(2)“假设法”,如上述问题(3),假设无限稀释,c(CHCOO-)趋近于0,c(H+)趋于10-
3
7mol·L-1,故比值变小。
(3)“凑常数”,解题时将某些粒子的浓度比值乘以或除以某种粒子的浓度,转化为一个常
数与某种粒子浓度的乘积或相除的关系。三、根据电离度求电离常数
4.已知25 ℃时,某浓度为c的一元弱酸HA的电离度为α,求该温度下的HA的电离常数
(K)。
a
答案 HA H+ + A-
起始 c 0 0
转化 c·α c·α c·α
平衡 c·(1-α) c·α c·α
K==,α很小,可认为1-α≈1,则K=c·α2。
a a
1.(2020·北京,11)室温下,对于1 L 0.1 mol·L-1醋酸溶液。下列判断正确的是( )
A.该溶液中CHCOO-的粒子数为6.02×1022
3
B.加入少量CHCOONa固体后,溶液的pH降低
3
C.滴加NaOH溶液过程中,n(CHCOO-)与n(CHCOOH)之和始终为0.1 mol
3 3
D.与NaCO 溶液反应的离子方程式为CO+2H+===HO+CO↑
2 3 2 2
答案 C
解析 醋酸属于弱电解质,则 CHCOO-的粒子数小于 6.02×1022,A 错误;加入少量
3
CHCOONa固体,抑制醋酸的电离,溶液的pH升高,故B错误;根据物料守恒,
3
n(CHCOO-)+n(CHCOOH)=0.1 mol,故C正确;醋酸的酸性强于碳酸,则根据强酸制取
3 3
弱酸,醋酸与NaCO 溶液反应生成醋酸钠、二氧化碳和水,醋酸是弱电解质,离子反应中
2 3
不能拆写,故D错误。
2.(2021·河北1月选考模拟,14)HPO 的电离是分步进行的,常温下K =7.6×10-3,K =
3 4 a1 a2
6.3×10-8,K =4.4×10-13。下列说法正确的是( )
a3
A.浓度均为0.1 mol·L-1的NaOH溶液和HPO 溶液按照体积比2∶1混合,混合液的pH<7
3 4
B.NaHPO 溶液中,c(H+)+c(H PO)+c(H PO )=c(PO)+c(OH-)
2 4 2 3 4
C.向0.1 mol·L-1的HPO 溶液中通入HCl气体(忽略溶液体积的变化),溶液pH=1时,溶
3 4
液中大约有7.1%的HPO 电离
3 4
D.在HPO 溶液中加入NaOH溶液,随着NaOH的加入,溶液的pH增大,当溶液的pH=
3 4
11时,c(PO)>c(HPO)
答案 C
解析 NaOH和HPO 按物质的量之比2∶1混合,恰好反应产生NaHPO ,在HPO溶液中,
3 4 2 4
存在HPO的电离平衡和水解平衡,电离平衡常数K =4.4×10-13,水解平衡常数K ==
a3 h2
≈1.59×10-7,K >K ,水解程度大于电离程度,因此溶液显碱性,pH>7,A错误;在
h2 a3
NaHPO 溶液中,根据质子守恒可得c(H+)+c(H PO)+2c(H PO )=c(PO)+c(OH-),B错误;
2 4 2 3 4
设电离出的c(H PO)=x,K ===7.6×10-3,x≈
2 a10.007 1 mol·L-1,溶液中大约电离的HPO 有×100%=7.1%,C正确;当溶液的pH=11时,
3 4
c(H+)=10-11 mol·L-1,K ===4.4×10-13,则 =4.4×10-2,则c(PO)<c(HPO),D错误。
a3
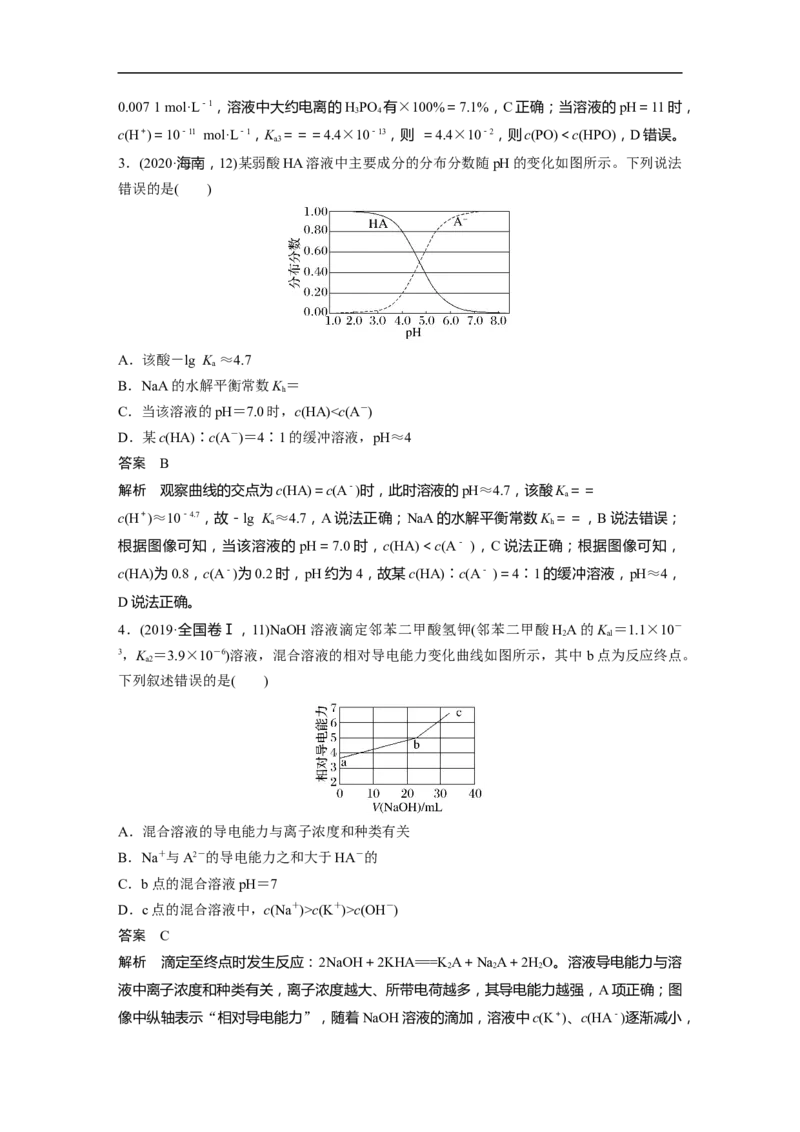
3.(2020·海南,12)某弱酸HA溶液中主要成分的分布分数随pH的变化如图所示。下列说法
错误的是( )
A.该酸-lg K ≈4.7
a
B.NaA的水解平衡常数K =
h
C.当该溶液的pH=7.0时,c(HA)c(K+)>c(OH-)
答案 C
解析 滴定至终点时发生反应:2NaOH+2KHA===KA+NaA+2HO。溶液导电能力与溶
2 2 2
液中离子浓度和种类有关,离子浓度越大、所带电荷越多,其导电能力越强,A项正确;图
像中纵轴表示“相对导电能力”,随着NaOH溶液的滴加,溶液中c(K+)、c(HA-)逐渐减小,而Na+、A2-的物质的量逐渐增大,由题图可知,溶液的相对导电能力逐渐增强,说明 Na+
与A2-的导电能力之和大于HA-的,B项正确;本实验默认在常温下进行,滴定终点时,溶
液中的溶质为邻苯二甲酸钠和邻苯二甲酸钾,由于邻苯二甲酸是弱酸,所以溶液呈碱性,
pH>7,C项错误;滴定终点时,c(K+)=c(Na+),a点到b点加入NaOH溶液的体积大于b点
到c点的,故c点时c(K+)>c(OH-),所以c(Na+)>c(K+)>c(OH-),D项正确。
课时精练
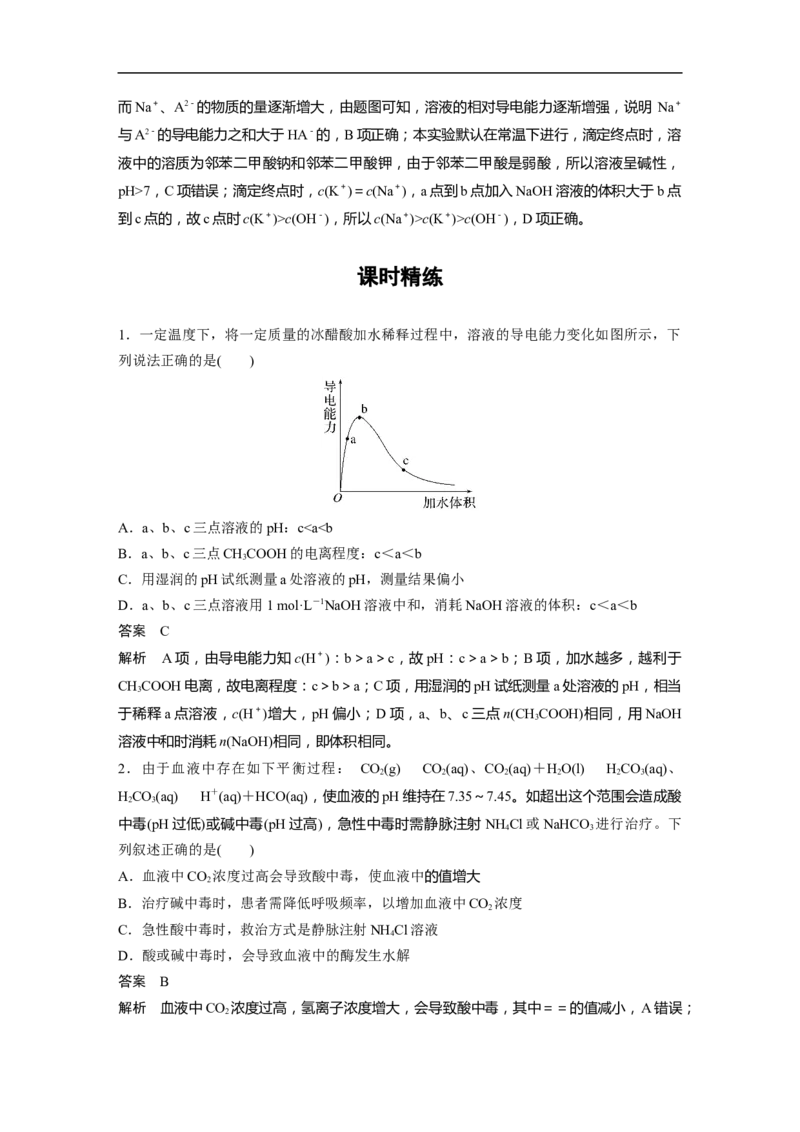
1.一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,下
列说法正确的是( )
A.a、b、c三点溶液的pH:cNaB(OH)
3 4
D.NaOH溶液溅到皮肤时,可用大量清水冲洗,再涂上硼酸溶液
答案 C
解析 根据题意可知HBO 只存在一步电离,产生一个氢离子,所以为一元酸,A正确;设
3 3
0.01 mol·L-1 HBO 溶液中c(H+)=x,则c[B(OH)]也可近似认为等于x,则有K(H BO)==
3 3 a 3 3
5.4×10-10,解得x≈2.3×10-6 mol·L-1,所以pH≈6,B正确;K(H BO)<
a 3 3
K(CHCOOH),所以B(OH)的水解程度更大,浓度相同时硼酸钠碱性更强,则等浓度溶液
a 3
的pH:CHCOONa<NaB(OH) ,C错误;NaOH溶液溅到皮肤上,用水冲洗后涂上酸性较
3 4
弱的硼酸溶液,可中和残留的碱,D正确。
8.常温下,CHCOOH、HCOOH(甲酸)的电离常数分别为1.7×10-5、1.8×10-4,以下关于
3
0.1 mol·L-1 CHCOOH溶液、0.1 mol·L-1 HCOOH溶液的说法正确的是( )
3
A.c(H+):CHCOOH>HCOOH
3
B.等体积的两溶液中,分别加入过量的镁,产生氢气的体积:HCOOH>CHCOOH
3
C.HCOOH可能与NaOH发生反应:H++OH-===HO
2
D.将CHCOOH溶液稀释100倍过程中,保持不变
3
答案 D
解析 等浓度的甲酸和乙酸溶液,甲酸酸性强,电离程度大,所以溶液中的 c(H+):
CHCOOH<HCOOH,故A错误;等浓度等体积的甲酸和乙酸溶液中,甲酸和乙酸的物质
3
的量相等,分别加入过量的镁,产生氢气的体积相等,故 B错误;HCOOH是弱酸,与
NaOH发生反应:HCOOH+OH-===HCOO-+HO,故C错误。
29.将浓度为0.1 mol·L-1 HF溶液加水稀释,下列各量保持增大的是( )
①c(H+) ②c(F-) ③c(OH-) ④K(HF) ⑤K ⑥ ⑦
a w
A.①⑥ B.②④ C.③⑦ D.④⑤
答案 C
解析 HF溶液中存在电离平衡:HFF-+H+,加水稀释时,平衡正向移动,由于溶液体
积的增大程度大于n(F-)、n(H+)的增大程度,则溶液中c(F-)、c(H+)均减小,①②错误;由
于溶液的温度不变,则K 、K(HF)不变,④⑤错误;由于K =c(H+)·c(OH-),c(H+)减小且
w a w
K 不变,则c(OH-)增大,③正确;K(HF)=,=,K(HF)不变,
w a a
c(F-)减小,则的值增大,⑦正确。
10.25 ℃时,用0.1 mol·L-1的CHCOOH溶液滴定20 mL 0.1 mol·L-1的NaOH溶液,当滴
3
加V mL CH COOH溶液时,混合溶液的pH=7。已知CHCOOH的电离常数为K,忽略混
3 3 a
合时引起的溶液体积的变化,下列关系式正确的是( )
A.K= B.V= C.K= D.K=
a a a
答案 A
解析 混合溶液的pH=7,说明醋酸过量,c(CHCOOH)≈ mol·L-1,根据电荷守恒:c(Na
3
+)+c(H+)=c(CHCOO-)+c(OH-)及c(H+)=c(OH-)可得,c(Na+)=c(CHCOO-)= mol·L-
3 3
1,则K==,A项正确。
a
11.(2022·临汾模拟)现取20 mL c(H+)=1×10-3 mol·L-1的CHCOOH溶液,加入0.2 mol·
3
L-1的氨水,测得溶液导电能力的变化如图所示,则加入氨水前 CHCOOH的电离度为(
3
)
A.0.5% B.1.5% C.0.1% D.1%
答案 D
解析 由题图可知,当加入10 mL氨水时,溶液的导电能力最强,即此时二者恰好完全反
应,则有20 mL×c(CHCOOH)=0.2 mol·L-1×10 mL,则c(CHCOOH)=0.1 mol·L-1,故
3 3
CHCOOH的电离度为×100%=1%。
3
12.下表是几种弱酸常温下的电离平衡常数:
CHCOOH HCO HS
3 2 3 2
K =4.3×10-7 K =9.1×10-8
a1 a1
K=1.8×10-5
a
K =5.6×10-11 K =1.1×10-12
a2 a2
则下列说法不正确的是( )A.碳酸的酸性强于氢硫酸
B.多元弱酸的酸性主要由第一步电离决定
C.常温下,加水稀释醋酸,增大
D.向弱酸溶液中加少量NaOH溶液,电离常数不变
答案 C
解析 由表中HCO 和HS的电离平衡常数可知,HCO 的K 大于HS的K ,则碳酸的酸
2 3 2 2 3 a1 2 a1
性强于氢硫酸,A正确;多元弱酸分步发生电离,第一步电离产生的H+抑制第二步、第三
步的电离,故多元弱酸的酸性主要由第一步电离决定,B正确;电离平衡常数只与温度有关,
向弱酸溶液中加少量NaOH溶液,溶液温度不变,则电离平衡常数不变,D正确。
13.(2022·河南罗山模拟)磷是重要的元素,能形成多种含氧酸和含氧酸盐。回答下列问题:
Ⅰ. 亚磷酸(H PO )是二元酸,HPO 溶液存在电离平衡:HPO H++HPO。亚磷酸与足
3 3 3 3 3 3 2
量NaOH溶液反应,生成水和NaHPO 。
2 3
(1)写出亚磷酸钠(Na HPO )中磷的化合价:_______________________________________。
2 3
(2)亚磷酸与少量NaOH溶液反应的离子方程式为__________________________________。
(3)亚磷酸具有强还原性,可使碘水褪色,该反应的化学方程式为_____________。
Ⅱ.已知:①次磷酸(H PO )是一种一元弱酸;②常温下,电离平衡常数K(H PO )=5.9×10-
3 2 a 3 2
2,K(CHCOOH)=1.8×10-5。
a 3
(4)下列说法正确的是__________(填字母)。
A.次磷酸的电离方程式为HPO H++HPO
3 2 2
B.NaH PO 属于酸式盐
2 2
C.浓度均为0.1 mol·L-1的次磷酸(H PO )与盐酸相比前者导电能力强
3 2
D.0.1 mol·L-1 NaH PO 溶液的pH比0.1 mol·L-1 CHCOONa溶液的pH小
2 2 3
答案 (1)+3 (2)H PO +OH-===HPO+HO (3)H PO +I+HO===2HI+HPO (4)AD
3 3 2 2 3 3 2 2 3 4
解析 (4)次磷酸为一元弱酸,则电离方程式为HPO H++HPO,A正确;NaH PO 属于
3 2 2 2 2
正盐,B错误;次磷酸为一元弱酸,则浓度均为0.1 mol·L-1的次磷酸(H PO )与盐酸相比前
3 2
者导电能力弱,C错误;由信息②可知HPO 的酸性比醋酸强,则0.1 mol·L-1 NaH PO 溶
3 2 2 2
液的pH比0.1 mol·L-1 CHCOONa溶液的pH小,D正确。
3
14.(1)已知酸性:HSO > >HSO> ,水杨酸( )与
2 3
NaSO 溶液反应,生成物为________(填字母)。
2 3
A. B.SO
2
C.NaHCO D.
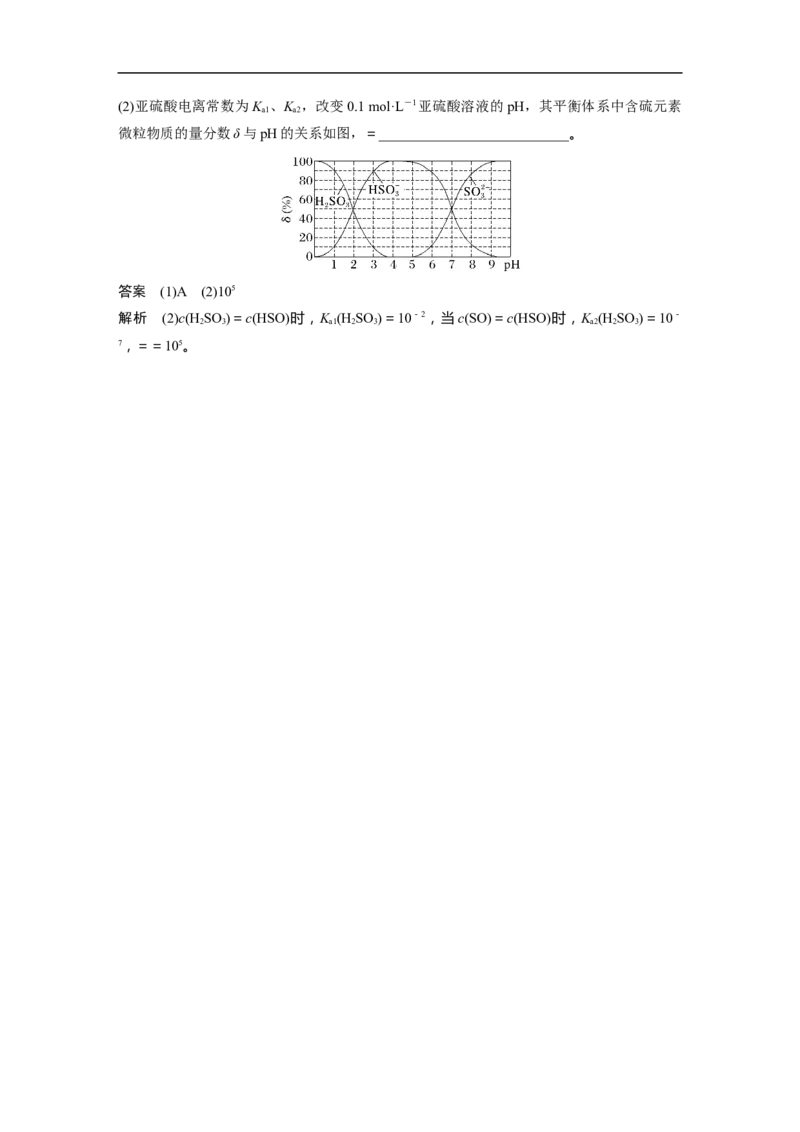
3(2)亚硫酸电离常数为K 、K ,改变0.1 mol·L-1亚硫酸溶液的pH,其平衡体系中含硫元素
a1 a2
微粒物质的量分数δ与pH的关系如图,=___________________________。
答案 (1)A (2)105
解析 (2)c(H SO )=c(HSO)时,K (H SO )=10-2,当c(SO)=c(HSO)时,K (H SO )=10-
2 3 a1 2 3 a2 2 3
7,==105。