文档内容
第 69 讲 以物质制备为主的综合实验
[复习目标] 1.掌握物质制备型实验方案设计的原则。2.掌握解答物质制备型实验综合题的
思维模型。
类型一 无机物的制备
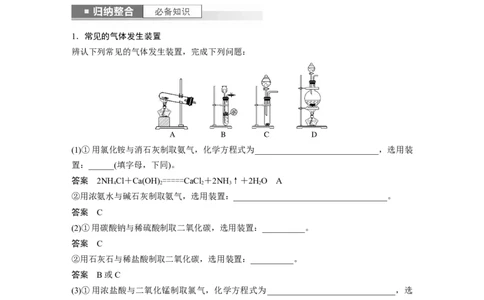
1.常见的气体发生装置
辨认下列常见的气体发生装置,完成下列问题:
(1)①用氯化铵与消石灰制取氨气,化学方程式为_____________________________,选用装
置:______(填字母,下同)。
答案 2NH Cl+Ca(OH) =====CaCl +2NH ↑+2HO A
4 2 2 3 2
②用浓氨水与碱石灰制取氨气,选用装置:____________________________________。
答案 C
(2)①用碳酸钠与稀硫酸制取二氧化碳,选用装置:__________。
答案 C
②用石灰石与稀盐酸制取二氧化碳,选用装置:__________。
答案 B或C
(3)①用浓盐酸与二氧化锰制取氯气,化学方程式为______________________________,选
用装置:______。
答案 MnO +4HCl(浓)=====MnCl +Cl↑+2HO D
2 2 2 2
②用漂白粉与浓盐酸制取少量氯气,化学方程式为___________________________________,
选用装置:______。
答案 Ca(ClO) +4HCl(浓)===CaCl +2Cl↑+2HO C
2 2 2 2
(4)铜与浓硝酸反应制取二氧化氮,选用装置:__________。
答案 C
(5)实验室制取乙烯的装置,可以通过选用上面哪个装置进行改进?若橡皮塞最多只允许打两个孔,应如何改进所选实验装置: _____________________________________。
答案 D,将分液漏斗换成温度计(或将烧瓶换成蒸馏烧瓶,将导气管换成温度计)
(6)上述B装置还能制取的气体有:__________________________________________。
答案 H 或HS
2 2
2.气体的净化
(1)设计原则:根据主要气体及杂质气体的性质差异来选择除杂试剂及除杂装置。
(2)吸收剂的选择
吸收剂的选择应根据被提纯气体的性质和杂质的性质来确定,一般情况如下:
①易溶于水的气体杂质可用水吸收;
②酸性杂质可用碱性物质吸收;
③碱性杂质可用酸性物质吸收;
④水为杂质时,可用干燥剂吸收;
⑤能与杂质发生反应生成沉淀(或可溶物)的物质也可作为吸收剂。
3.尾气处理装置的选择
a装置用于吸收或溶解反应速率不是很快的气体,如用NaOH溶液吸收Cl、CO 等。
2 2
b装置用于收集少量气体。
c、d装置用于吸收极易溶且溶解很快的气体,如HCl、HBr、NH 等,其中d装置吸收量较
3
少。
e装置用于处理难以吸收的可燃性气体,如H、CO等。
2
4.实验条件的控制
(1)排气方法
为了防止空气中的O 、CO 、水蒸气等干扰实验,常用其他稳定的气体(如氮气)排尽装置中
2 2
的空气;有时也可充分利用反应产物气体(如氨气、氯气、二氧化硫等)排尽装置中的空气。
(2)控制气体的流速及用量
①用分液漏斗控制液体滴加的速度和用量。
②观察气泡,控制气流速度,如图甲,可通过观察气泡得到 N 、H 的体积比约为1∶3的混
2 2
合气体。
③平衡气压,如图乙,用长玻璃管平衡气压,防堵塞。
(3)压送液体根据装置的密封性,让反应生成气体或消耗气体,产生压强差,将液体压入或倒流入另一反
应容器。
(4)温度控制
①控制低温的目的:减少某些反应物或产物分解,如HO 、NH HCO 等;减少某些反应物
2 2 4 3
或产物挥发,如盐酸、氨水等;防止某些物质水解,避免副反应发生等。
②采取加热的目的:加快反应速率或使平衡移动,加速溶解等。
③常考的温度控制方式
a.水浴加热:均匀加热,反应温度在100 ℃以下。
b.油浴加热:均匀加热,反应温度在100~260 ℃之间。
c.冰水冷却:使某物质液化、降低产物的溶解度;减少其他副反应,提高产品纯度等。
d.保温:如真空双层玻璃容器等。
5.解答物质制备综合实验题的一般程序
(1)认真阅读题干,提取有用信息,包括实验目的、反应条件、陌生物质的性质、陌生反应
原理等。
(2)仔细观察装置图(或框图),联想熟悉的实验,找出每件仪器(或步骤)与熟悉的某一实验相
似的地方,分析每件仪器中所装药品的作用。
(3)通读问题,整合信息,把所有的问题进行综合分析,运用题给信息和化学基础知识做出
正确解答。
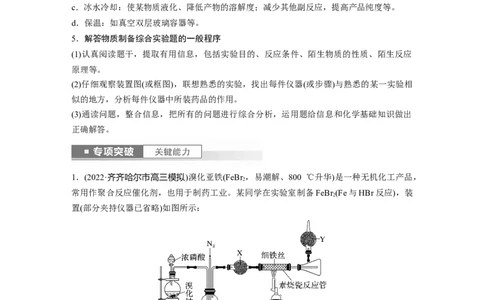
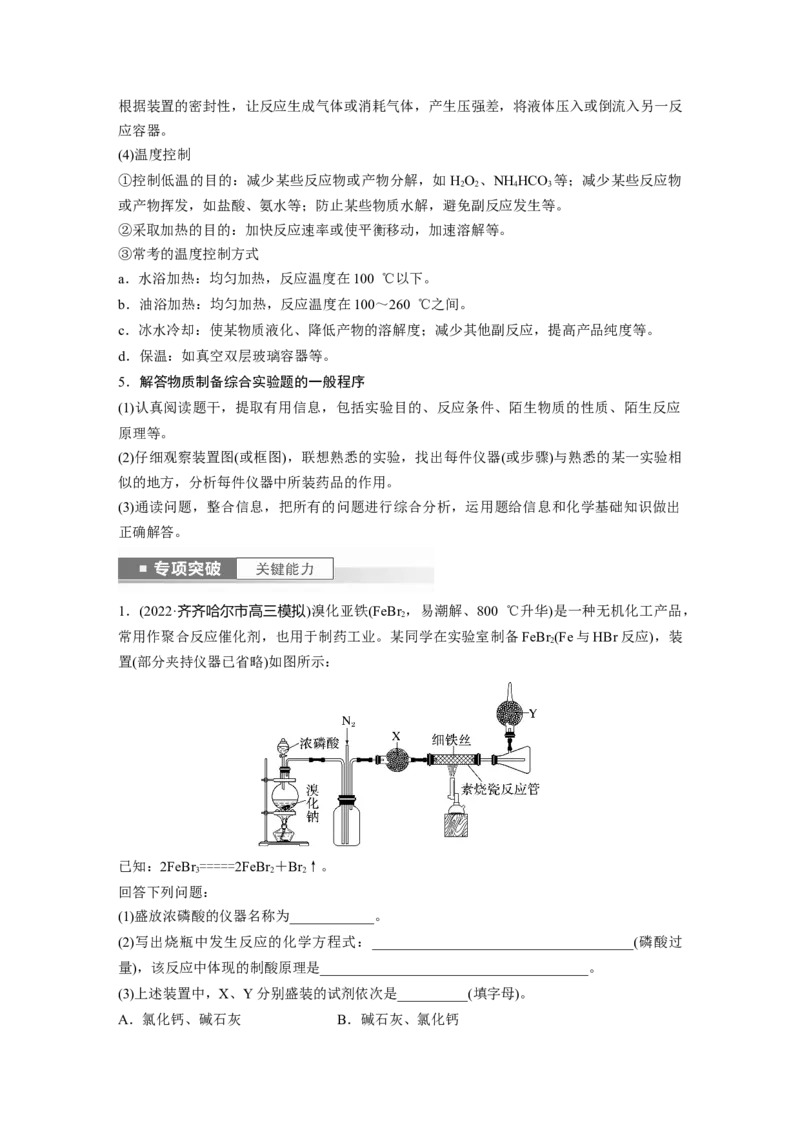
1.(2022·齐齐哈尔市高三模拟)溴化亚铁(FeBr ,易潮解、800 ℃升华)是一种无机化工产品,
2
常用作聚合反应催化剂,也用于制药工业。某同学在实验室制备FeBr (Fe与HBr反应),装
2
置(部分夹持仪器已省略)如图所示:
已知:2FeBr =====2FeBr +Br ↑。
3 2 2
回答下列问题:
(1)盛放浓磷酸的仪器名称为____________。
(2)写出烧瓶中发生反应的化学方程式:_____________________________________(磷酸过
量),该反应中体现的制酸原理是______________________________________。
(3)上述装置中,X、Y分别盛装的试剂依次是__________(填字母)。
A.氯化钙、碱石灰 B.碱石灰、氯化钙C.氯化钙、硫酸铜 D.氢氧化钠、硫酸铜
(4) 实 验 结 束 后 , 关 闭 热 源 , 仍 需 要 通 入 一 段 时 间 N , 其 目 的 是
2
__________________________。
(5)若用浓硫酸(生成 SO 和 Br )代替浓磷酸,同样可以制备 FeBr ,请简述原因:
2 2 2
________________________________________________________________________。
答案 (1)分液漏斗 (2)NaBr+HPO (浓)=====NaH PO +HBr↑ 难挥发性酸制取挥发性酸
3 4 2 4
(或高沸点酸制取低沸点酸) (3)A (4)将装置中的HBr全部排到干燥管中,被试剂Y完全吸
收,避免污染环境 (5) 浓硫酸代替浓磷酸,生成SO 和Br ,SO 不与铁反应,Br 和铁反
2 2 2 2
应生成FeBr ,FeBr 在高温下又分解为FeBr 和Br
3 3 2 2
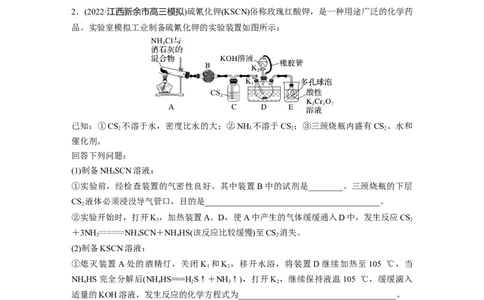
2.(2022·江西新余市高三模拟)硫氰化钾(KSCN)俗称玫瑰红酸钾,是一种用途广泛的化学药
品。实验室模拟工业制备硫氰化钾的实验装置如图所示:
已知:①CS 不溶于水,密度比水的大;②NH 不溶于CS ;③三颈烧瓶内盛有CS 、水和
2 3 2 2
催化剂。
回答下列问题:
(1)制备NH SCN溶液:
4
①实验前,经检查装置的气密性良好。其中装置B中的试剂是________。三颈烧瓶的下层
CS 液体必须浸没导气管口,目的是_________________________________________。
2
②实验开始时,打开K ,加热装置A、D,使A中产生的气体缓缓通入D中,发生反应CS
1 2
+3NH ======NH SCN+NH HS(该反应比较缓慢)至CS 消失。
3 4 4 2
(2)制备KSCN溶液:
①熄灭装置A处的酒精灯,关闭K 和K ,移开水浴,将装置D继续加热至105 ℃,当
1 2
NH HS完全分解后(NH HS===HS↑+NH ↑),打开K ,继续保持液温105 ℃,缓缓滴入
4 4 2 3 2
适量的KOH溶液,发生反应的化学方程式为_____________________________________。
②使用KOH溶液会使产品KSCN固体中混有较多的KS,工业上用相同浓度的KCO 溶液
2 2 3
替换KOH溶液,除了原料成本因素外,优点是_____________________________________。
③装置E的作用是______________________________________________________。
(3)制备KSCN晶体:先滤去三颈烧瓶中的固体催化剂,再减压、________、________、过
滤、洗涤、干燥,得到硫氰化钾晶体。
答案 (1)①碱石灰 使反应物NH 和CS 充分接触,并防止发生倒吸
3 2
(2)①NH SCN+KOH=====KSCN+NH ↑+HO
4 3 2
②KCO 能与NH SCN反应产生更多CO 和NH ,有利于残留在装置中的HS逸出 ③除去
2 3 4 2 3 2反应过程中产生的HS和NH ,以免污染环境
2 3
(3)蒸发浓缩 冷却结晶
类型二 有机物的制备
1.有机物制备的注意要点
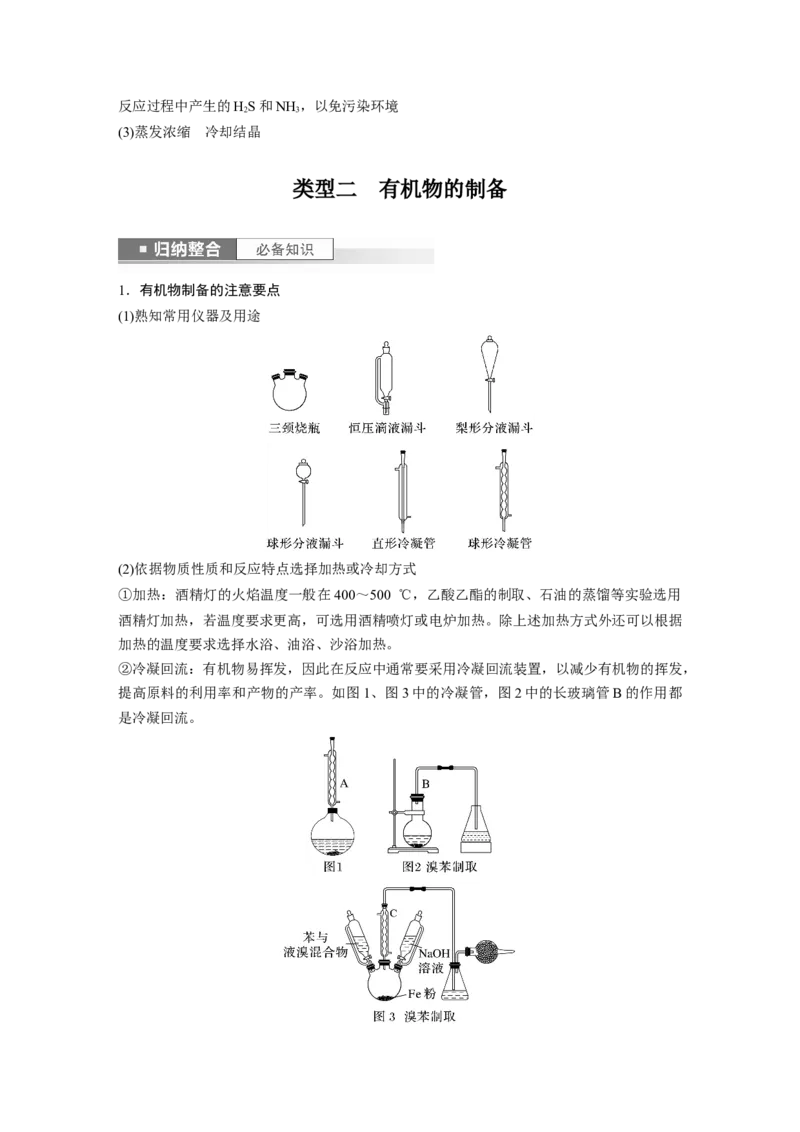
(1)熟知常用仪器及用途
(2)依据物质性质和反应特点选择加热或冷却方式
①加热:酒精灯的火焰温度一般在400~500 ℃,乙酸乙酯的制取、石油的蒸馏等实验选用
酒精灯加热,若温度要求更高,可选用酒精喷灯或电炉加热。除上述加热方式外还可以根据
加热的温度要求选择水浴、油浴、沙浴加热。
②冷凝回流:有机物易挥发,因此在反应中通常要采用冷凝回流装置,以减少有机物的挥发,
提高原料的利用率和产物的产率。如图1、图3中的冷凝管,图2中的长玻璃管B的作用都
是冷凝回流。③防暴沸:加沸石(或碎瓷片),防止溶液暴沸;若开始忘加沸石(或碎瓷片),需冷却后补加。
2.常见有机物分离提纯的方法
(1)分液:用于分离两种互不相溶(密度也不同)的液体。
(2)蒸馏:用于分离沸点不同的互溶液体。分馏的原理与此相同。
(3)洗气:用于除去气体混合物中的杂质,如乙烷中的乙烯可通过溴水洗气除去。
(4)萃取分液:如分离溴水中的溴和水,可用四氯化碳或苯进行萃取,然后分液。
3.有机物制备实验题的答题思路
有机物制备一般会给出相应的信息,通常会以表格的形式给出,表格
根据题给信 中的数据主要是有机化合物的密度、沸点和在水中的溶解性,在分析
息,初步判定 这些数据时要多进行横向和纵向地比较,密度主要是与水比较,沸点
物质性质 主要是表中各物质的比较,溶解性主要是判断溶还是不溶。主要根据
这些数据选择分离、提纯的方法
注意仪器名称
所给的装置图中有一些不常见的仪器,要明确这些仪器的作用
和作用
大多数有机反应副反应较多,且为可逆反应,因此设计有机物制备实
验方案时,要注意控制反应条件,尽可能选择步骤少、副产物少的反
关注有机反应
应;由于副产物多,所以需要进行除杂、净化。另外,若为两种有机
条件
物参加的可逆反应,应考虑多加一些价廉的有机物,以提高另一种有
机物的转化率和生成物的产率
1.(2022·日照模拟)乙醇酸钠(HOCHCOONa)又称羟基乙酸钠,它是一种有机原料,其相对
2
分子质量为98。羟基乙酸钠易溶于热水,微溶于冷水,不溶于醇、醚等有机溶剂。实验室
拟用氯乙酸(ClCH COOH)和NaOH溶液制备少量羟基乙酸钠,此反应为剧烈的放热反应。
2
具体实验步骤如下:
步骤1:向如图所示装置的三颈烧瓶中,加入132.3 g氯乙酸、50 mL水,搅拌。逐步加入
40% NaOH溶液,在95 ℃继续搅拌反应2小时,反应过程控制 pH约为9至10之间。步骤2:蒸出部分水至液面有薄膜,加少量热水,操作1,滤液冷却至15 ℃,过滤得粗产
品。
步骤3:粗产品溶解于适量热水中,加活性炭脱色,操作2,分离掉活性炭。
步骤4:将去除活性炭后的溶液加入适量乙醇中,操作3,过滤,干燥,得到羟基乙酸钠。
请回答下列问题:
(1)步骤1中,发生反应的化学方程式是____________________________________________。
(2)如图所示的装置中仪器B为球形冷凝管,下列说法不正确的是________(填字母)。
A.球形冷凝管与直形冷凝管相比,冷却面积更大,效果更好
B.球形冷凝管既可以作倾斜式蒸馏装置,也可用于垂直回流装置
C.在使用冷凝管进行蒸馏操作时,一般蒸馏物的沸点越高,蒸气越不易冷凝
(3) 步 骤 2 中 , 三 颈 烧 瓶 中 如 果 忘 加 磁 转 子 该 如 何 操 作 :
________________________________。
(4)上述步骤中,操作1、2、3的名称分别是________(填字母)。
A.过滤,过滤,冷却结晶
B.趁热过滤,过滤,蒸发结晶
C.趁热过滤,趁热过滤,冷却结晶
(5)步骤4中,得到纯净羟基乙酸钠1.1 mol,则实验产率为________%(结果保留1位小数)。
答案 (1)ClCH COOH+2NaOH――→HOCH COONa+NaCl+HO (2)BC
2 2 2
(3)待溶液冷却后补加磁转子 (4)C (5)78.6
解析 (2)球形冷凝管内芯管为球泡状,容易积留蒸馏液,故不适宜作倾斜式蒸馏装置,多
用于垂直回馏装置,故B错误;在使用冷凝管进行蒸馏操作时,一般蒸馏物的沸点越高,
蒸气越易冷凝,故C错误。(4)蒸出部分水至液面有薄膜,说明有固体开始析出,加少量热
水趁热过滤;粗产品溶解于适量热水中,加活性炭脱色,需要趁热过滤分离掉活性炭固体;
将去除活性炭后的溶液加到适量乙醇中,冷却结晶,过滤,干燥,得到羟基乙酸钠。
(5)132.3 g氯乙酸(ClCH COOH)的物质的量为=1.4 mol,根据ClCH COOH~HOCH COONa
2 2 2
可知,理论上可以生成1.4 mol羟基乙酸钠,步骤4中,得到纯净羟基乙酸钠1.1 mol,则实
验产率为×100%≈78.6%。
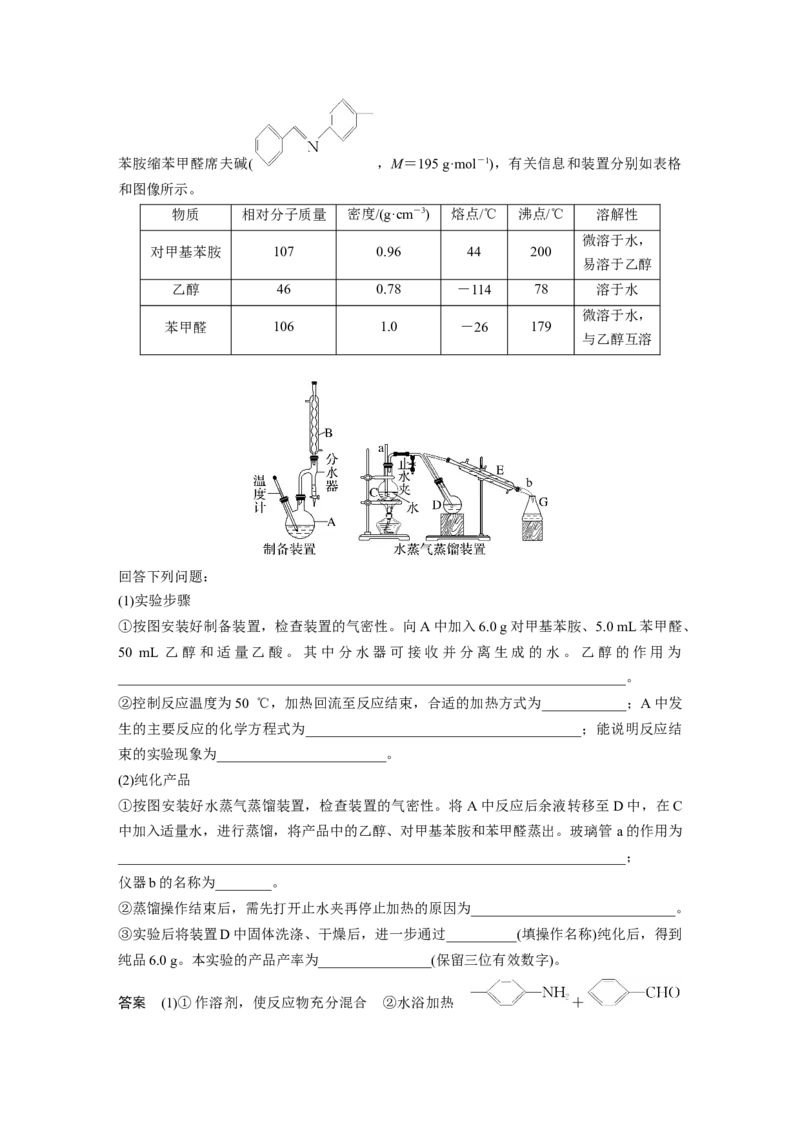
2.席夫碱在有机合成、液晶材料、植物生长调节等多个领域有重要用途。学习小组在实验
室中探究由对甲基苯胺( )与苯甲醛( )在酸催化下制备对甲基苯胺缩苯甲醛席夫碱( ,M=195 g·mol-1),有关信息和装置分别如表格
和图像所示。
物质 相对分子质量 密度/(g·cm-3) 熔点/℃ 沸点/℃ 溶解性
微溶于水,
对甲基苯胺 107 0.96 44 200
易溶于乙醇
乙醇 46 0.78 -114 78 溶于水
微溶于水,
苯甲醛 106 1.0 -26 179
与乙醇互溶
回答下列问题:
(1)实验步骤
①按图安装好制备装置,检查装置的气密性。向A中加入6.0 g对甲基苯胺、5.0 mL苯甲醛、
50 mL 乙醇和适量乙酸。其中分水器可接收并分离生成的水。乙醇的作用为
________________________________________________________________________。
②控制反应温度为50 ℃,加热回流至反应结束,合适的加热方式为____________;A中发
生的主要反应的化学方程式为_______________________________________;能说明反应结
束的实验现象为________________________。
(2)纯化产品
①按图安装好水蒸气蒸馏装置,检查装置的气密性。将 A中反应后余液转移至D中,在C
中加入适量水,进行蒸馏,将产品中的乙醇、对甲基苯胺和苯甲醛蒸出。玻璃管 a的作用为
________________________________________________________________________;
仪器b的名称为________。
②蒸馏操作结束后,需先打开止水夹再停止加热的原因为_____________________________。
③实验后将装置D中固体洗涤、干燥后,进一步通过__________(填操作名称)纯化后,得到
纯品6.0 g。本实验的产品产率为________________(保留三位有效数字)。
答案 (1)①作溶剂,使反应物充分混合 ②水浴加热 +―――――→ +HO 分水器中水不再增加
2
(2)①平衡压强,检验固体产品是否堵塞导管 牛角管 ②防止装置D中液体倒吸入装置C
中 ③重结晶 65.2%
解析 (2)③晶体经重结晶后可进一步纯化;5.0 mL 苯甲醛的质量为1.0×5.0 g=5 g,由关
系式:
苯甲醛 ~ 对甲基苯胺缩苯甲醛席夫碱
106 g 195 g
5 g m
可知理论上制得产品的质量为m≈9.198 g,产率为×100%≈65.2%。
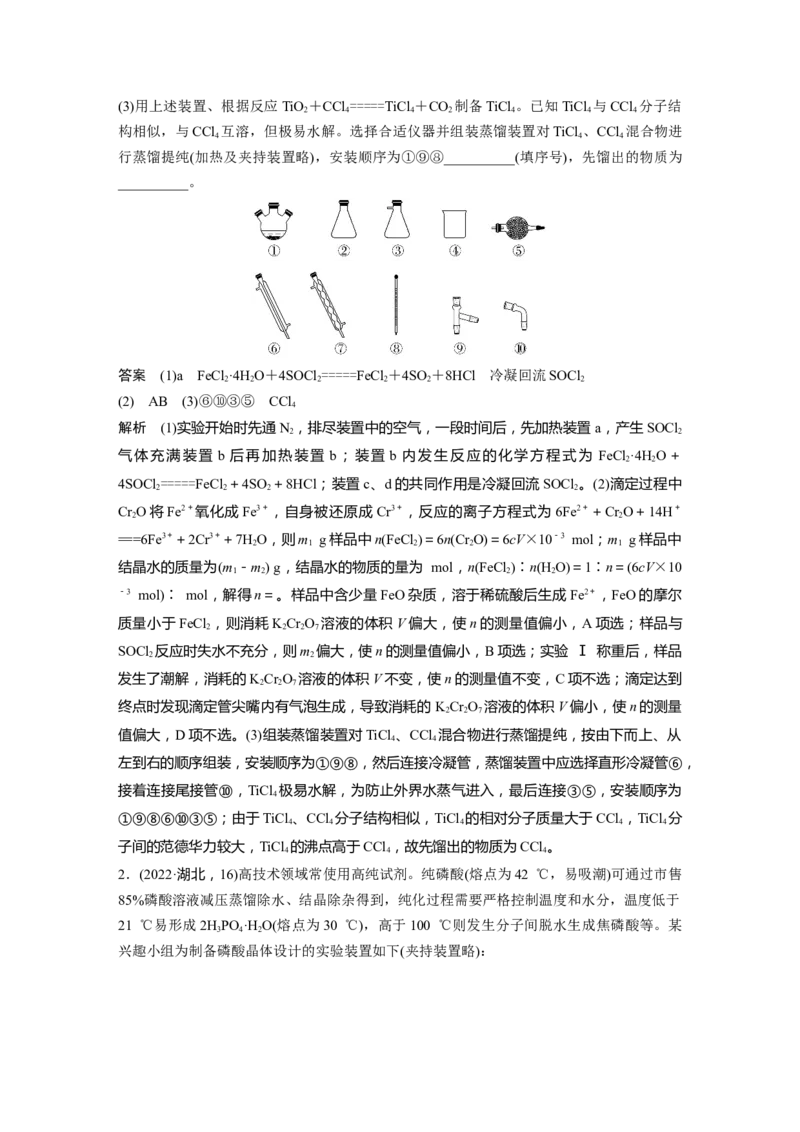
1.(2022·山东,18)实验室利用FeCl ·4H O和亚硫酰氯(SOCl )制备无水FeCl 的装置如图所
2 2 2 2
示(加热及夹持装置略)。已知SOCl 沸点为76 ℃,遇水极易反应生成两种酸性气体。回答
2
下列问题:
(1)实验开始先通N。一段时间后,先加热装置________(填“a”或“b”)。装置b内发生反
2
应的化学方程式为___________________________________________________________。
装置c、d共同起到的作用是_______________________________________________________。
(2)现有含少量杂质的FeCl ·nHO,为测定n值进行如下实验:
2 2
实验Ⅰ:称取m g样品,用足量稀硫酸溶解后,用c mol·L-1 KCr O 标准溶液滴定Fe2+达
1 2 2 7
终点时消耗V mL(滴定过程中Cr O转化为Cr3+,Cl-不反应)。
2
实验 Ⅱ:另取m g样品,利用上述装置与足量SOCl 反应后,固体质量为m g。
1 2 2
则n=__________;下列情况会导致n测量值偏小的是__________(填字母)。
A.样品中含少量FeO杂质
B.样品与SOCl 反应时失水不充分
2
C.实验Ⅰ中,称重后样品发生了潮解
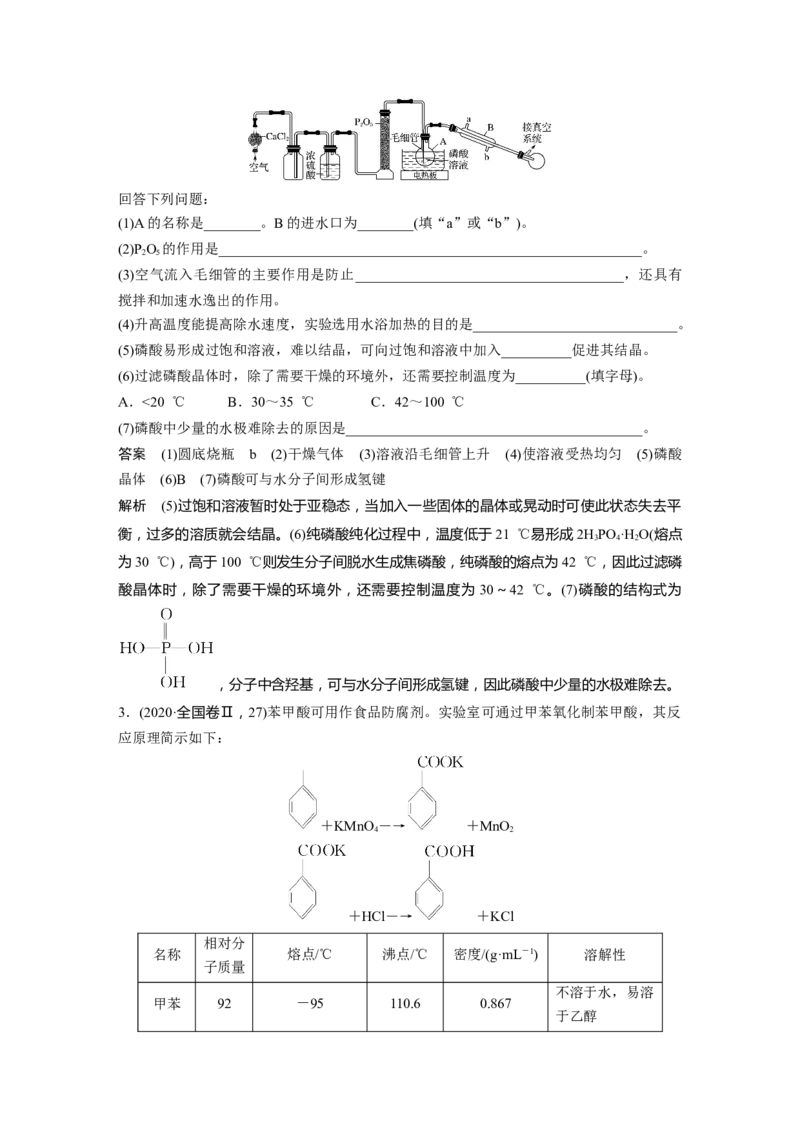
D.滴定达终点时发现滴定管尖嘴内有气泡生成(3)用上述装置、根据反应TiO +CCl =====TiCl +CO 制备TiCl 。已知TiCl 与CCl 分子结
2 4 4 2 4 4 4
构相似,与CCl 互溶,但极易水解。选择合适仪器并组装蒸馏装置对TiCl 、CCl 混合物进
4 4 4
行蒸馏提纯(加热及夹持装置略),安装顺序为①⑨⑧__________(填序号),先馏出的物质为
__________。
答案 (1)a FeCl ·4H O+4SOCl =====FeCl +4SO +8HCl 冷凝回流SOCl
2 2 2 2 2 2
(2) AB (3)⑥⑩③⑤ CCl
4
解析 (1)实验开始时先通N ,排尽装置中的空气,一段时间后,先加热装置a,产生SOCl
2 2
气体充满装置 b 后再加热装置 b;装置 b 内发生反应的化学方程式为 FeCl ·4H O+
2 2
4SOCl =====FeCl +4SO +8HCl;装置c、d的共同作用是冷凝回流SOCl 。(2)滴定过程中
2 2 2 2
Cr O将Fe2+氧化成Fe3+,自身被还原成Cr3+,反应的离子方程式为 6Fe2++Cr O+14H+
2 2
===6Fe3++2Cr3++7HO,则m g样品中n(FeCl )=6n(CrO)=6cV×10-3 mol;m g样品中
2 1 2 2 1
结晶水的质量为(m -m) g,结晶水的物质的量为 mol,n(FeCl )∶n(H O)=1∶n=(6cV×10
1 2 2 2
-3 mol)∶ mol,解得n=。样品中含少量FeO杂质,溶于稀硫酸后生成Fe2+,FeO的摩尔
质量小于FeCl ,则消耗KCr O 溶液的体积V偏大,使n的测量值偏小,A项选;样品与
2 2 2 7
SOCl 反应时失水不充分,则m 偏大,使n的测量值偏小,B项选;实验 Ⅰ 称重后,样品
2 2
发生了潮解,消耗的KCr O 溶液的体积V不变,使n的测量值不变,C项不选;滴定达到
2 2 7
终点时发现滴定管尖嘴内有气泡生成,导致消耗的 KCr O 溶液的体积V偏小,使n的测量
2 2 7
值偏大,D项不选。(3)组装蒸馏装置对TiCl 、CCl 混合物进行蒸馏提纯,按由下而上、从
4 4
左到右的顺序组装,安装顺序为①⑨⑧,然后连接冷凝管,蒸馏装置中应选择直形冷凝管⑥,
接着连接尾接管⑩,TiCl 极易水解,为防止外界水蒸气进入,最后连接③⑤,安装顺序为
4
①⑨⑧⑥⑩③⑤;由于TiCl 、CCl 分子结构相似,TiCl 的相对分子质量大于CCl ,TiCl 分
4 4 4 4 4
子间的范德华力较大,TiCl 的沸点高于CCl ,故先馏出的物质为CCl 。
4 4 4
2.(2022·湖北,16)高技术领域常使用高纯试剂。纯磷酸(熔点为42 ℃,易吸潮)可通过市售
85%磷酸溶液减压蒸馏除水、结晶除杂得到,纯化过程需要严格控制温度和水分,温度低于
21 ℃易形成2HPO ·H O(熔点为30 ℃),高于100 ℃则发生分子间脱水生成焦磷酸等。某
3 4 2
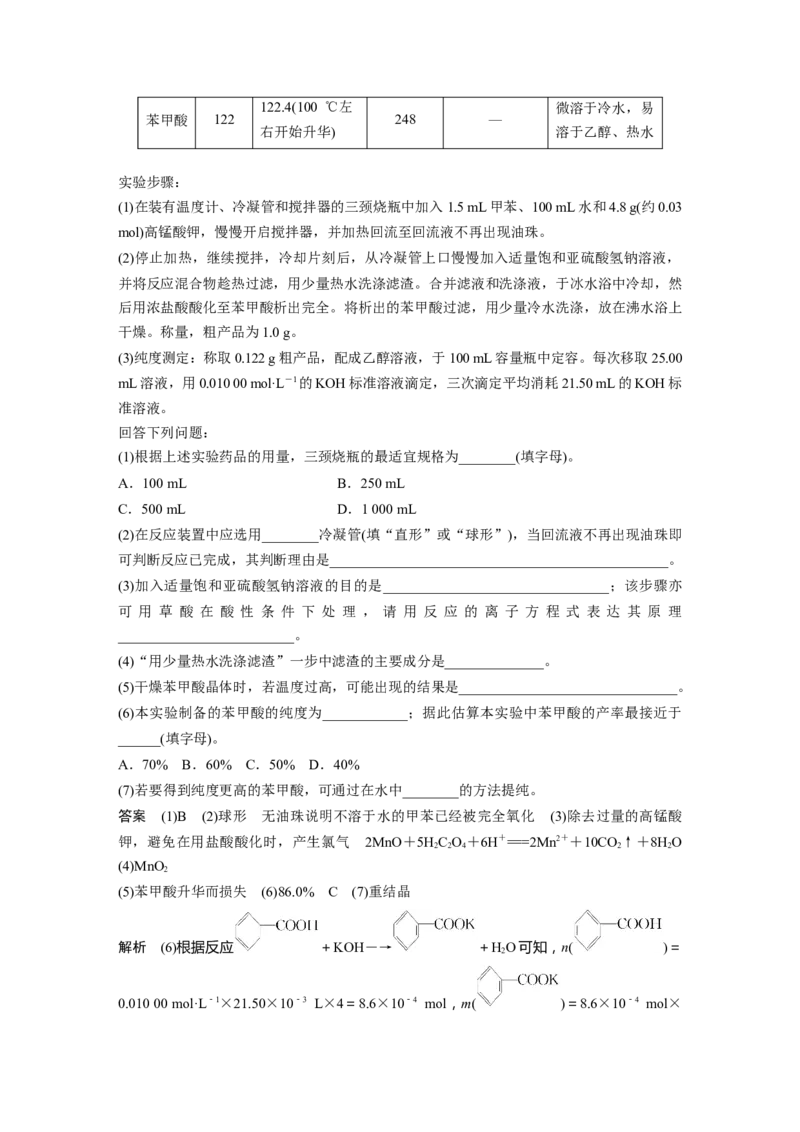
兴趣小组为制备磷酸晶体设计的实验装置如下(夹持装置略):回答下列问题:
(1)A的名称是________。B的进水口为________(填“a”或“b”)。
(2)P O 的作用是____________________________________________________________。
2 5
(3)空气流入毛细管的主要作用是防止______________________________________,还具有
搅拌和加速水逸出的作用。
(4)升高温度能提高除水速度,实验选用水浴加热的目的是_____________________________。
(5)磷酸易形成过饱和溶液,难以结晶,可向过饱和溶液中加入__________促进其结晶。
(6)过滤磷酸晶体时,除了需要干燥的环境外,还需要控制温度为__________(填字母)。
A.<20 ℃ B.30~35 ℃ C.42~100 ℃
(7)磷酸中少量的水极难除去的原因是__________________________________________。
答案 (1)圆底烧瓶 b (2)干燥气体 (3)溶液沿毛细管上升 (4)使溶液受热均匀 (5)磷酸
晶体 (6)B (7)磷酸可与水分子间形成氢键
解析 (5)过饱和溶液暂时处于亚稳态,当加入一些固体的晶体或晃动时可使此状态失去平
衡,过多的溶质就会结晶。(6)纯磷酸纯化过程中,温度低于21 ℃易形成2HPO ·H O(熔点
3 4 2
为30 ℃),高于100 ℃则发生分子间脱水生成焦磷酸,纯磷酸的熔点为42 ℃,因此过滤磷
酸晶体时,除了需要干燥的环境外,还需要控制温度为 30~42 ℃。(7)磷酸的结构式为
,分子中含羟基,可与水分子间形成氢键,因此磷酸中少量的水极难除去。
3.(2020·全国卷Ⅱ,27)苯甲酸可用作食品防腐剂。实验室可通过甲苯氧化制苯甲酸,其反
应原理简示如下:
+KMnO ―→ +MnO
4 2
+HCl―→ +KCl
相对分
名称 熔点/℃ 沸点/℃ 密度/(g·mL-1) 溶解性
子质量
不溶于水,易溶
甲苯 92 -95 110.6 0.867
于乙醇122.4(100 ℃左 微溶于冷水,易
苯甲酸 122 248 —
右开始升华) 溶于乙醇、热水
实验步骤:
(1)在装有温度计、冷凝管和搅拌器的三颈烧瓶中加入1.5 mL甲苯、100 mL水和4.8 g(约0.03
mol)高锰酸钾,慢慢开启搅拌器,并加热回流至回流液不再出现油珠。
(2)停止加热,继续搅拌,冷却片刻后,从冷凝管上口慢慢加入适量饱和亚硫酸氢钠溶液,
并将反应混合物趁热过滤,用少量热水洗涤滤渣。合并滤液和洗涤液,于冰水浴中冷却,然
后用浓盐酸酸化至苯甲酸析出完全。将析出的苯甲酸过滤,用少量冷水洗涤,放在沸水浴上
干燥。称量,粗产品为1.0 g。
(3)纯度测定:称取0.122 g粗产品,配成乙醇溶液,于100 mL容量瓶中定容。每次移取25.00
mL溶液,用0.010 00 mol·L-1的KOH标准溶液滴定,三次滴定平均消耗21.50 mL的KOH标
准溶液。
回答下列问题:
(1)根据上述实验药品的用量,三颈烧瓶的最适宜规格为________(填字母)。
A.100 mL B.250 mL
C.500 mL D.1 000 mL
(2)在反应装置中应选用________冷凝管(填“直形”或“球形”),当回流液不再出现油珠即
可判断反应已完成,其判断理由是________________________________________________。
(3)加入适量饱和亚硫酸氢钠溶液的目的是________________________________;该步骤亦
可 用 草 酸 在 酸 性 条 件 下 处 理 , 请 用 反 应 的 离 子 方 程 式 表 达 其 原 理
_________________________。
(4)“用少量热水洗涤滤渣”一步中滤渣的主要成分是______________。
(5)干燥苯甲酸晶体时,若温度过高,可能出现的结果是_______________________________。
(6)本实验制备的苯甲酸的纯度为____________;据此估算本实验中苯甲酸的产率最接近于
______(填字母)。
A.70% B.60% C.50% D.40%
(7)若要得到纯度更高的苯甲酸,可通过在水中________的方法提纯。
答案 (1)B (2)球形 无油珠说明不溶于水的甲苯已经被完全氧化 (3)除去过量的高锰酸
钾,避免在用盐酸酸化时,产生氯气 2MnO+5HC O +6H+===2Mn2++10CO↑+8HO
2 2 4 2 2
(4)MnO
2
(5)苯甲酸升华而损失 (6)86.0% C (7)重结晶
解析 (6)根据反应 +KOH―→ +HO可知,n( )=
2
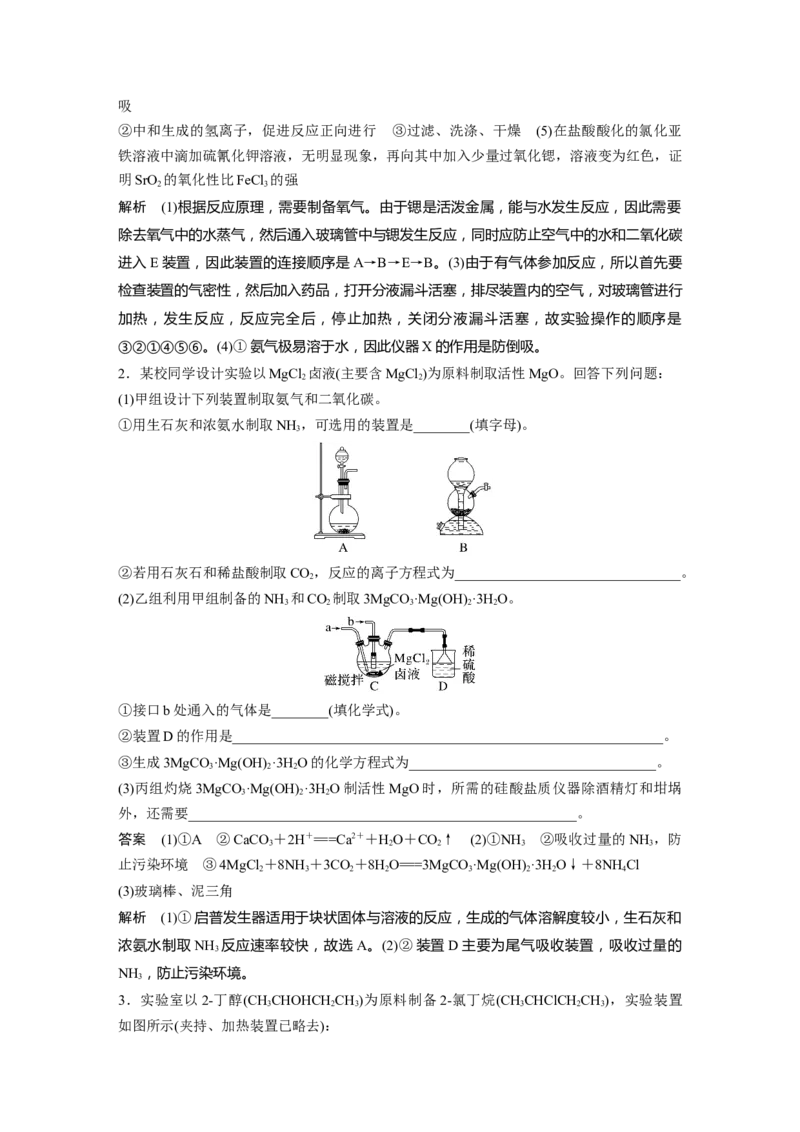
0.010 00 mol·L-1×21.50×10-3 L×4=8.6×10-4 mol,m( )=8.6×10-4 mol×122 g·mol-1=0.104 92 g,制备的苯甲酸的纯度为×100%=86.0%。在理论上,1 mol甲苯反
应后生成1 mol苯甲酸,则:
~
92 122
1.5 mL×0.867 g·mL-1 m
苯甲酸的理论产量m≈1.72 g,苯甲酸的产率为×100%=50%。(7)根据苯甲酸的水溶性可知,
若要得到纯度更高的苯甲酸,需要利用重结晶的方法进行提纯。
课时精练
1.过氧化锶(SrO )通常用作分析试剂、氧化剂、漂白剂等。制备原理为 Sr+O=====SrO 。
2 2 2
某兴趣小组利用下列装置在实验室中模拟制备过氧化锶。
(1) 选 择 必 要 仪 器 制 备 过 氧 化 锶 ( 气 流 按 从 左 到 右 的 流 向 ) :
____________________________(填字母)。
(2)该实验制备氧气的化学方程式为______________________________________________。
(3) 连 接 好 装 置 进 行 实 验 , 实 验 步 骤 如 下 , 正 确 的 操 作 顺 序 为
___________________________(填序号)。
①打开分液漏斗活塞,将水滴入烧瓶中 ②在相应装置中装入药品 ③检查装置气密性 ④
加热 ⑤停止加热 ⑥关闭分液漏斗活塞
(4)利用反应Sr2++HO+2NH +8HO===SrO ·8H O↓+2NH制备过氧化锶,装置如下:
2 2 3 2 2 2
①仪器X的作用是____________。
②氨气在该反应中所起的作用是_________________________________________。
③实验结束后,得到SrO ·8H O的操作为___________________________________________。
2 2
(5)设计实验证明SrO 的氧化性比FeCl 的氧化性强:_________________________________。
2 3
答案 (1)A→B→E→B (2)2Na O +2HO===4NaOH+O↑ (3)③②①④⑤⑥ (4)①防倒
2 2 2 2吸
②中和生成的氢离子,促进反应正向进行 ③过滤、洗涤、干燥 (5)在盐酸酸化的氯化亚
铁溶液中滴加硫氰化钾溶液,无明显现象,再向其中加入少量过氧化锶,溶液变为红色,证
明SrO 的氧化性比FeCl 的强
2 3
解析 (1)根据反应原理,需要制备氧气。由于锶是活泼金属,能与水发生反应,因此需要
除去氧气中的水蒸气,然后通入玻璃管中与锶发生反应,同时应防止空气中的水和二氧化碳
进入E装置,因此装置的连接顺序是A→B→E→B。(3)由于有气体参加反应,所以首先要
检查装置的气密性,然后加入药品,打开分液漏斗活塞,排尽装置内的空气,对玻璃管进行
加热,发生反应,反应完全后,停止加热,关闭分液漏斗活塞,故实验操作的顺序是
③②①④⑤⑥。(4)①氨气极易溶于水,因此仪器X的作用是防倒吸。
2.某校同学设计实验以MgCl 卤液(主要含MgCl )为原料制取活性MgO。回答下列问题:
2 2
(1)甲组设计下列装置制取氨气和二氧化碳。
①用生石灰和浓氨水制取NH ,可选用的装置是________(填字母)。
3
②若用石灰石和稀盐酸制取CO,反应的离子方程式为________________________________。
2
(2)乙组利用甲组制备的NH 和CO 制取3MgCO ·Mg(OH) ·3H O。
3 2 3 2 2
①接口b处通入的气体是________(填化学式)。
②装置D的作用是_____________________________________________________________。
③生成3MgCO ·Mg(OH) ·3H O的化学方程式为___________________________________。
3 2 2
(3)丙组灼烧3MgCO ·Mg(OH) ·3H O制活性MgO时,所需的硅酸盐质仪器除酒精灯和坩埚
3 2 2
外,还需要_______________________________________________________。
答案 (1)①A ②CaCO +2H+===Ca2++HO+CO↑ (2)①NH ②吸收过量的NH ,防
3 2 2 3 3
止污染环境 ③4MgCl +8NH +3CO+8HO===3MgCO ·Mg(OH) ·3H O↓+8NH Cl
2 3 2 2 3 2 2 4
(3)玻璃棒、泥三角
解析 (1)①启普发生器适用于块状固体与溶液的反应,生成的气体溶解度较小,生石灰和
浓氨水制取NH 反应速率较快,故选A。(2)②装置D主要为尾气吸收装置,吸收过量的
3
NH ,防止污染环境。
3
3.实验室以2-丁醇(CHCHOHCH CH)为原料制备2-氯丁烷(CHCHClCH CH),实验装置
3 2 3 3 2 3
如图所示(夹持、加热装置已略去):相关信息如表所示:
物质 熔点/℃ 沸点/℃ 密度/(g·cm-3) 其他
2-丁醇 -114.7 99.5 0.81 与水互溶
2-氯丁烷 -131.3 68.2 0.87 微溶于水,碱性水解
[实验步骤]
步骤1:在甲装置中的圆底烧瓶内加入无水ZnCl 和100 mL 12 mol·L-1浓盐酸,充分溶解、
2
冷却,再加入45.68 mL 2-丁醇,加热一段时间。
步骤2:将反应混合物移至乙装置的蒸馏烧瓶内,蒸馏并收集115 ℃以下的馏分。
步骤3:从馏分中分离出有机相,进行系列操作,放置一段时间后过滤。
步骤4:滤液经进一步精制得产品。
回答下列问题:
(1)Ⅰ中应放的仪器是________(填“A”或“B”,下同), Ⅱ 中应放的仪器是____________。
(2)步骤1中加入的无水ZnCl 的作用是_______________________________________。
2
(3)步骤3进行系列操作的顺序是____________(填序号,可重复使用)。
①10%Na CO 溶液洗涤 ②加入CaCl 固体 ③蒸馏水洗涤
2 3 2
用NaCO 溶液洗涤时操作要迅速,其原因是________________________________________。
2 3
(4)步骤4进一步精制得产品所采用的操作方法是____________(填名称)。
(5)测定实验中生成2-氯丁烷的产率。将全部产品加入足量NaOH溶液中,加热,冷却后,
滴入硝酸溶液至溶液呈酸性,再滴入足量的硝酸银溶液,得到57.40 g沉淀,则2-氯丁烷的
产率是____________。
答案 (1)A B (2)作催化剂 (3)③①③②
防止2-氯丁烷水解,减少2-氯丁烷挥发
(4)蒸馏 (5)80%
解析 (1)A为球形冷凝管,一般竖直放置,用于冷凝回流;B为直形冷凝管,倾斜放置,用
于 冷 凝 馏 分 。 (2) 甲 装 置 中 圆 底 烧 瓶 中 发 生 的 反 应 是 CHCHOHCH CH +
3 2 3
HCl―→CHCHClCH CH +HO,步骤1中加入的无水ZnCl 不作反应物,故其作催化剂,
3 2 3 2 2
加快化学反应速率。(3)步骤3进行系列操作的顺序是用蒸馏水洗去产品中含有的HCl、
ZnCl―→用10%Na CO 溶液洗去少量的HCl―→用蒸馏水洗去少量的NaCO―→用CaCl
2 2 3 2 3 2
固体干燥产品,放置一段时间后过滤;因为2-氯丁烷在碱性溶液中水解,为了防止2-氯丁
烷水解,同时减少2-氯丁烷(沸点较低)挥发,故用NaCO 溶液洗涤时操作要迅速。(4)蒸馏
2 3可分离互溶的、有一定沸点差异的液体混合物,故步骤4进一步精制得产品所采用的操作方
法是蒸馏。(5)45.68 mL 2-丁醇的物质的量为≈0.50 mol,则理论上可得到0.50 mol 2-氯丁烷;
由 2-氯丁烷在测定实验中的反应可得关系式为 CHCHClCH CH ~NaCl~AgCl,
3 2 3
n(CHCHClCH CH)=n(AgCl)==0.40 mol,则2-氯丁烷的产率是×100%=80%。
3 2 3
4.(2022·河南洛阳模拟)Cl(三氯六氨合钴)是一种重要的化工产品,常用于合成其他Co(Ⅱ)
3
配合物。以下是一种制备三氯六氨合钴的实验方法,回答下列问题:
Ⅰ.氯化钴的制备
已知氯化钴(CoCl )易潮解,Co(Ⅲ)的氧化性强于Cl ,可用高熔点金属钴与氯气反应制取。
2 2
实验室提供下列装置进行组合(连接用橡胶管省略):
(1)仪器 a 的名称是________,用上图中的装置组合制备氯化钴,连接顺序为
A→________________。
(2)装置A产生氯气的化学方程式为_______________________________________________。
(3)用正确的方式连接装置进行实验,装置B的作用是________________________________。
Ⅱ.三氯六氨合钴晶体的制备
(4)“氧化”的目的是___________________________________________________________。
“操作X”包括冷却结晶、过滤,并依次用少量冷的稀盐酸和无水乙醇对晶体进行洗涤,用
无水乙醇洗涤的目的是________________________________________________。
(5)制备Cl 总反应的化学方程式为________________________________________。
3
反应中活性炭的作用是________(填字母)。
a.脱色剂 b.氧化剂
c.还原剂 d.催化剂
答案 (1)分液漏斗 D→C→E→B(2)2KMnO+16HCl(浓)===2KCl+2MnCl +5Cl↑+8HO
4 2 2 2
(3)防止多余的Cl 污染空气、防止空气中的水蒸气进入装置E
2
(4)把+2价钴氧化成+3价钴 减少晶体表面水分,加快晶体干燥
(5)2CoCl +10NH +2NH Cl+HO===2[Co(NH )]Cl +2HO d
2 3 4 2 2 3 6 3 2
解析 (5)CoCl 与NH Cl固体混合物用水溶解后,加入浓氨水、活性炭配合,再用HO 氧
2 4 2 2
化,后经多步操作得到Cl ,总反应的化学方程式为2CoCl +10NH +2NH Cl+HO===2Cl
3 2 3 4 2 2 3
+2HO;活性炭可分散反应物,增大反应物的接触面积,加快反应速率,起到催化剂作用,
2
故选d。