文档内容
第 30 讲 原子结构 核外电子排布规律
[复习目标] 1.掌握原子结构中微粒数目的关系。2.了解原子核外电子的运动状态、能级分
布和排布原理。3.能正确书写1~36号元素原子核外电子排布式、价层电子排布式和轨道表
示式。
考点一 原子结构、核素、同位素
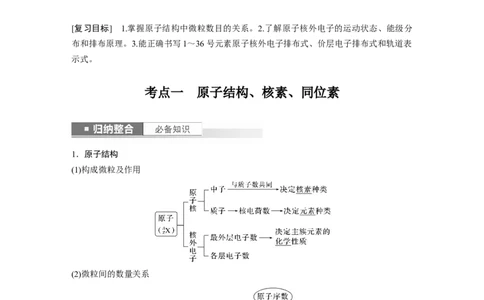
1.原子结构
(1)构成微粒及作用
(2)微粒间的数量关系
①阳离子的核外电子数=质子数-所带电荷数。
②阴离子的核外电子数=质子数+所带电荷数。
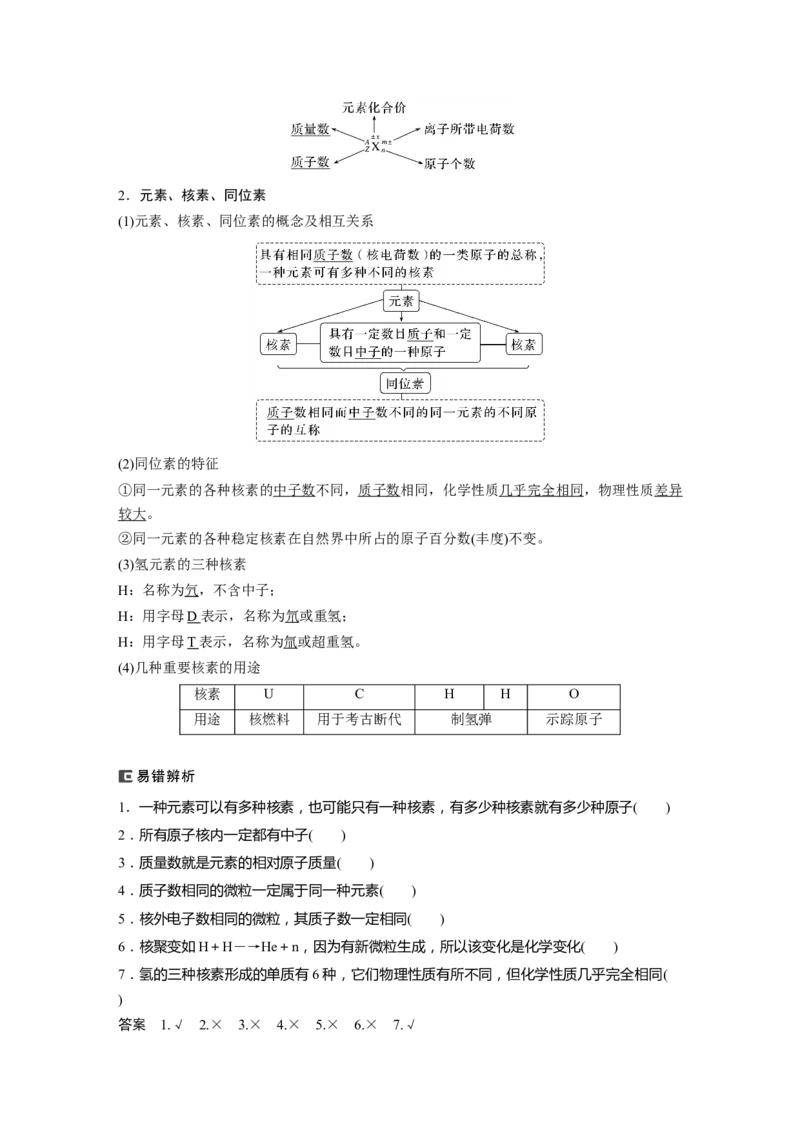
(3)微粒符号周围数字代表的信息2.元素、核素、同位素
(1)元素、核素、同位素的概念及相互关系
(2)同位素的特征
①同一元素的各种核素的中子数不同,质子数相同,化学性质几乎完全相同,物理性质差异
较大。
②同一元素的各种稳定核素在自然界中所占的原子百分数(丰度)不变。
(3)氢元素的三种核素
H:名称为氕,不含中子;
H:用字母D 表示,名称为氘或重氢;
H:用字母T 表示,名称为氚或超重氢。
(4)几种重要核素的用途
核素 U C H H O
用途 核燃料 用于考古断代 制氢弹 示踪原子
1.一种元素可以有多种核素,也可能只有一种核素,有多少种核素就有多少种原子( )
2.所有原子核内一定都有中子( )
3.质量数就是元素的相对原子质量( )
4.质子数相同的微粒一定属于同一种元素( )
5.核外电子数相同的微粒,其质子数一定相同( )
6.核聚变如H+H―→He+n,因为有新微粒生成,所以该变化是化学变化( )
7.氢的三种核素形成的单质有6种,它们物理性质有所不同,但化学性质几乎完全相同(
)
答案 1.√ 2.× 3.× 4.× 5.× 6.× 7.√一、微粒中“粒子数”的确定
1.月球上的每百吨He聚变所释放出的能量相当于目前人类一年消耗的能量,地球上氦元
素主要以He的形式存在。已知一个 12C原子的质量为a g,一个He原子的质量为b g,N
A
为阿伏加德罗常数。下列说法正确的是( )
A.He比He多一个中子
B.氦元素的近似相对原子质量为3.5
C.He的相对原子质量为
D.He的摩尔质量为bN
A
答案 C
解析 He比He少一个中子,A错误;不能确定核素的原子百分含量,因此不能计算氦元素
的近似相对原子质量,B错误;一个原子的真实质量与一个C原子质量的的比值是该核素的
相对原子质量,因此He的相对原子质量为,C正确;He的摩尔质量为bN g·
A
mol-1,D错误。
2.(1)1 mol H 18O与1 mol D 16O的中子数之比为________。
2 2
(2)已知阴离子R2-的原子核内有n个中子,R原子的质量数为m,则w g R原子完全转化为
R2-时,含有电子的物质的量是_________________________________________。
答案 (1)1∶1 (2) mol
解析 (2)质量数=质子数+中子数,则R的质子数为m-n,故R2-的核外电子数为m-n+
2,w g R原子的物质的量为 mol,所以w g R2-含有电子的物质的量为 mol×(m-n+2)=
mol。
二、元素、核素、同位素的概念辨析
3.汤姆孙(J.J.Thomson)和阿斯通(F.W.Aston)在1913年发现了Ne。下列有关说法正确的是(
)
A.Ne和Ne属于同素异形体
B.Ne和 Ne属于不同的核素
C.Ne和Ne的中子数相同
D.Ne转变为Ne为化学变化
答案 B
解析 Ne和Ne的质子数相同,中子数不同,属于不同的核素,互为同位素,不互为同素异
形体,A、C项错误,B项正确;Ne转变为Ne,没有新物质生成,不是化学变化,D项错
误。
4.现有下列9种微粒:H、H、C、C、N、Fe2+、Fe3+、O、O。按要求完成以下各题:
2 3
(1)H、H分别是氢元素的一种________,它们互称为________。(2)互为同素异形体的微粒是________。
(3)Fe2+的中子数为________,核外电子数为____________________________________。
(4)上述9种微粒中有________种核素,含有________种元素。
答案 (1)核素 同位素 (2)O、O
2 3
(3)30 24 (4)7 5
解析 (1)H、H分别是氢元素的一种核素;H、H是质子数相同而中子数不同的氢元素的不
同原子,它们互称为同位素。
(2)O 和O 是同种元素组成的不同单质,互为同素异形体。
2 3
(3)Fe2+的中子数为56-26=30,核外电子数为26-2=24。
考点二 核外电子运动状态与排布原理
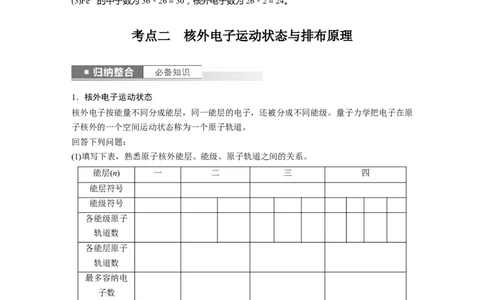
1.核外电子运动状态
核外电子按能量不同分成能层,同一能层的电子,还被分成不同能级。量子力学把电子在原
子核外的一个空间运动状态称为一个原子轨道。
回答下列问题:
(1)填写下表,熟悉原子核外能层、能级、原子轨道之间的关系。
能层(n) 一 二 三 四
能层符号
能级符号
各能级原子
轨道数
各能层原子
轨道数
最多容纳电
子数
(2)常用电子云轮廓图的形状和取向来表示原子轨道的形状和取向。s 电子云轮廓图呈
________形、p电子云轮廓图呈________形。p电子云有________种伸展方向。
(3)预测第五电子层上原子轨道总数是多少?最多能容纳的电子数是多少?
(4)比较下列基态原子能级或原子轨道的能量高低。
①1s、2s、2p、3s、3p、3d ②2s、2p、2p、2p
x y z
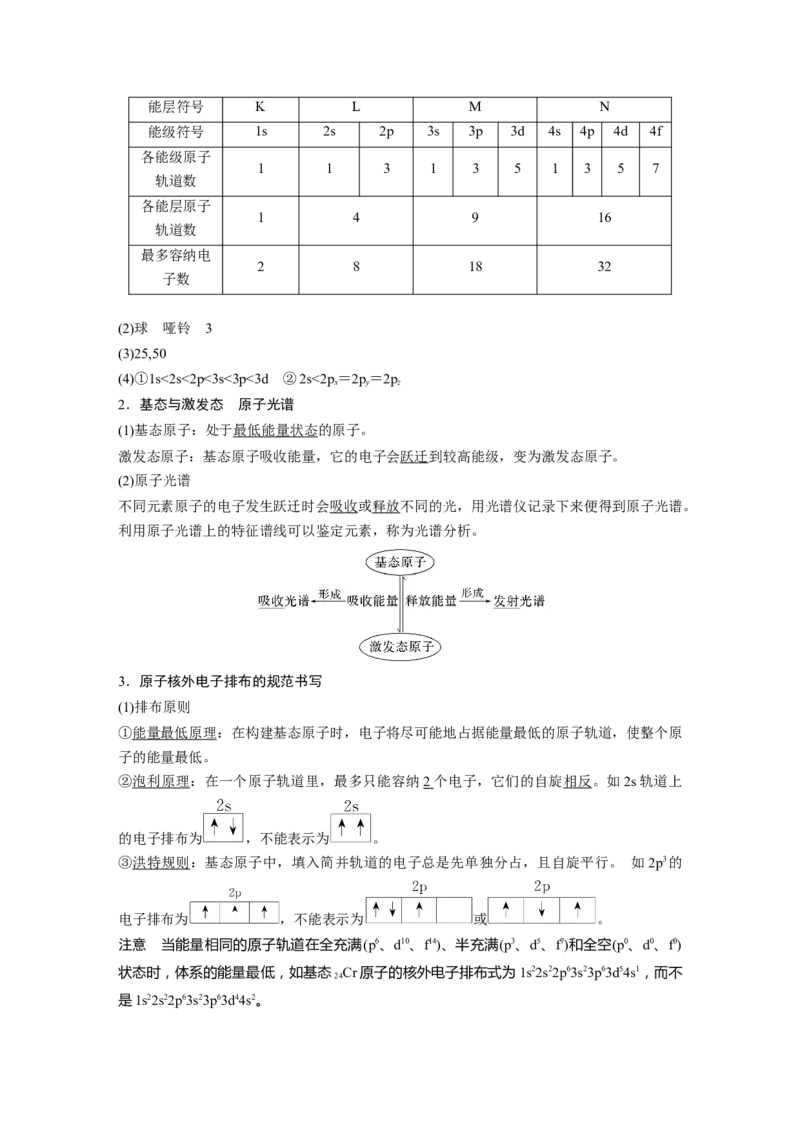
答案 (1)
能层(n) 一 二 三 四能层符号 K L M N
能级符号 1s 2s 2p 3s 3p 3d 4s 4p 4d 4f
各能级原子
1 1 3 1 3 5 1 3 5 7
轨道数
各能层原子
1 4 9 16
轨道数
最多容纳电
2 8 18 32
子数
(2)球 哑铃 3
(3)25,50
(4)①1s<2s<2p<3s<3p<3d ②2s<2p=2p=2p
x y z
2.基态与激发态 原子光谱
(1)基态原子:处于最低能量状态的原子。
激发态原子:基态原子吸收能量,它的电子会跃迁到较高能级,变为激发态原子。
(2)原子光谱
不同元素原子的电子发生跃迁时会吸收或释放不同的光,用光谱仪记录下来便得到原子光谱。
利用原子光谱上的特征谱线可以鉴定元素,称为光谱分析。
3.原子核外电子排布的规范书写
(1)排布原则
①能量最低原理:在构建基态原子时,电子将尽可能地占据能量最低的原子轨道,使整个原
子的能量最低。
②泡利原理:在一个原子轨道里,最多只能容纳2 个电子,它们的自旋相反。如2s轨道上
的电子排布为 ,不能表示为 。
③洪特规则:基态原子中,填入简并轨道的电子总是先单独分占,且自旋平行。 如2p3的
电子排布为 ,不能表示为 或 。
注意 当能量相同的原子轨道在全充满(p6、d10、f14)、半充满(p3、d5、f7)和全空(p0、d0、f0)
状态时,体系的能量最低,如基态 Cr原子的核外电子排布式为1s22s22p63s23p63d54s1,而不
24
是1s22s22p63s23p63d44s2。(2)填充顺序——构造原理
(3)基态原子核外电子排布表示方法(以硫原子为例)
电子排布式 1s22s22p63s23p4
简化电子排布式 [Ne]3s23p4
价层电子排布式 3s23p4
价层电子轨道表示式(电子排布图)
1.p能级能量不一定比s能级的能量高( )
2.Fe的基态原子的电子排布式为1s22s22p63s23p64s23d6( )
3. Ti的电子排布式1s22s22p63s23p10违反了能量最低原理( )
22
4. 表示的原子能量处于最低状态( )
5.1s22s12p1表示的是激发态原子的电子排布( )
6.某些金属及其化合物在燃烧时会产生特殊的颜色,是由于电子跃迁时能量以一定频率的光
释放出来( )
答案 1.√ 2.× 3.× 4.× 5.√ 6.√
一、核外电子的运动状态及排布式的书写
1.完成下列各小题:
(1)基态硅原子最外层电子的轨道表示式为____________________________________
________________________________________________________________________。
(2)在KH PO 的四种组成元素各自所能形成的简单离子中,核外电子排布相同的是
2 4
________(填离子符号)。(3)铜或铜盐的焰色试验为绿色,该光谱是________________(填“吸收光谱”或“发射光
谱”)。
答案 (1)
(2)K+和P3- (3)发射光谱
2.下列Li原子轨道表示式表示的状态中,能量最低和最高的分别为________、________(填
字母)。
A.
B.
C.
D.
答案 D C
解析 根据核外电子排布规律可知Li的基态原子核外电子排布式为1s22s1,则D中能量最低;
选项C中有2个电子处于2p能级上,能量最高。
3.钾发生焰色试验的原因是_____________________________________________________
________________________________________________________________________。
答案 电子由较高能量的激发态跃迁到较低能量的激发态或基态时,以光的形式释放能量
核外电子排布常见错误
(1)在书写基态原子的轨道表示式时,常出现以下错误:
① (违反能量最低原理);
② (违反泡利原理);
③ (违反洪特规则);
④ (违反洪特规则)。
(2)当出现d轨道时,虽然电子按ns、(n-1)d、np的顺序填充,但在书写电子排布式时,仍
把(n-1)d放在ns前,如Fe:1s22s22p63s23p63d64s2,而失电子时,却先失4s轨道上的电子,
如Fe3+:1s22s22p63s23p63d5。二、核外电子排布规律的应用
4.判断电子的运动状态
按要求填空:
(1)基态F原子核外电子的运动状态有______种。
(2)基态钛原子的价层电子排布式为________,其原子核外电子的空间运动状态有________
种,共有________种运动状态不同的电子。
(3)基态Si原子价层电子的运动状态有________种,若其电子排布式表示为[Ne]3s23p违背了
________。
(4)基态Cu原子核外电子的空间运动状态有________种。
答案 (1) 9
(2)3d24s2 12 22
(3)4 洪特规则
(4)15
解析 (1)基态F原子共有9个核外电子,则每个电子都有对应的轨道和自旋状态,所以核
外电子的运动状态有9种。
(2)基态Ti原子核外电子排布式为1s22s22p63s23p63d24s2,价层电子排布式为3d24s2;s轨道有
一种空间运动状态,p轨道有三种空间运动状态,d轨道有五种空间运动状态,3d轨道只有
两个电子,有两种空间运动状态,因此基态Ti原子的核外电子的空间运动状态有12种;核
外有22个电子,就有22种运动状态。
(4)基态Cu原子核外电子排布式为[Ar]3d104s1,基态Cu原子核外有几个轨道,其核外电子就
有几种空间运动状态,则基态Cu原子核外电子的空间运动状态有1+1+3+1+3+5+1=
15种。
核外电子运动状态的判断
电子的运动状态与原子核外电子数目相等;空间运动状态与核外电子填充原子轨道的数目相
等。
5.判断原子中未成对电子数目
按要求填空:
(1)基态Ti3+中未成对电子数有________个;与Ti同族相邻的元素Zr的基态原子价层电子排
布式为________。与钛同周期元素的基态原子中,未成对电子数与钛相同的元素有________
种。
(2)血红蛋白中的铁处于基态时,其最高能级中的单电子数为________。
(3)Cr与Ni的基态原子核外未成对电子数之比为________。
(4)第四周期中未成对电子数最多的基态原子的价层电子轨道表示式为________。
(5)2020年12月17日,“嫦娥五号”首次成功实现地外天体采样返回,标志着我国航天向前迈出了一大步。其制作材料中包含了Al、Cr、Cu、C、N、O、Si等多种元素。上述元素
中基态原子未成对电子数与Al相同的有________。
(6)氨硼烷(NH BH)的制备是当今科学研究的重要课题,可用反应B(OCH )+NH Cl+
3 3 3 3 4
LiAlH ===NH BH+Al (OCH)+LiCl+H↑进行制备。反应中涉及元素的基态原子中含1
4 3 3 3 3 2
个未成对电子的有________种。
答案 (1)1 4d25s2 3 (2)4 (3)3∶1
(4)
(5)Cu (6)5
解析 (1)Ti位于第四周期,Ti基态原子未成对电子数是2,与钛同周期的所有元素的基态原
子中,未成对电子数与钛相同的元素有Ni、Ge、Se。
(3)基态铬原子价层电子排布式为3d54s1,核外有6个未成对电子,基态镍原子价层电子排布
式为3d84s2,核外有2个未成对电子,则铬与镍的基态原子核外未成对电子数之比为3∶1。
(5)Al的核外电子排布式为1s22s22p63s23p1,有1个未成对电子,Cr、Cu、C、N、O、Si中只
有Cu(价层电子排布:3d104s1)基态原子未成对电子数与Al相同。
6.元素推断
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为________;
其基态原子价层电子的轨道表示式为
________________________________________________________________________。
(2)E元素基态原子的M层全充满,N层没有成对电子且只有一个未成对电子,E的元素符号
为________,其基态原子的核外电子排布式为
________________________________________________________________________。
(3)元素D的正三价离子的3d能级为半充满,D的元素符号为________,其基态原子的核外
电子排布式为________。
答案 (1)N
(2)Cu 1s22s22p63s23p63d104s1(或[Ar]3d104s1)
(3)Fe 1s22s22p63s23p63d64s2(或[Ar]3d64s2)
1.(2021·北京,2)下列有关放射性核素氚(H)的表述不正确的是( )
A.H原子核外电子数为1
B.H原子核内中子数为3
C.H 与H 化学性质基本相同
2 2
D.HO具有放射性
2答案 B
2.(2021·辽宁,2)下列化学用语使用正确的是( )
A.基态C原子价层电子排布图:
B.Cl-结构示意图:
C.KCl形成过程:
D.质量数为2的氢核素:H
答案 D
解析 基态C原子价层电子排布图为 ,A错误;Cl-结构示意图为 ,B
错误;KCl形成过程为 ,C错误。
3.(2020·山东等级模拟考,4)某元素基态原子4s轨道上有1个电子,则该基态原子价层电子
排布不可能是( )
A.3p64s1 B.4s1 C.3d54s1 D.3d104s1
答案 A
解析 基态原子4s轨道上有1个电子,在s区价层电子排布式为4s1,在d区价层电子排布
式为3d54s1,在ds区价层电子排布式为3d104s1,在p区不存在4s轨道上有1个电子,故A
符合题意。
4.(2022·山东,3)O、O的半衰期很短,自然界中不能稳定存在。人工合成反应如下:O+
He―→O+X;O+He―→O+Y。下列说法正确的是( )
A.X的中子数为2
B.X、Y互为同位素
C.O、O可用作示踪原子研究化学反应历程
D.自然界不存在O、O 分子是因其化学键不稳定
2 2
答案 B
解析 根据质量守恒可知,X微粒为He,Y微粒为He,据此分析解题。X微粒为He,根据
质量数等于质子数加中子数可知,该微粒的中子数为4,A错误;X微粒为He,Y微粒为
He,二者为具有相同的质子数和不同的中子数的原子,故互为同位素,B正确;由题干信
息可知,O与O的半衰期很短,故不适宜用作示踪原子研究化学反应历程,C错误;自然界
中不存在O 与O 分子并不是因其化学键不稳定,而是由于O与O的半衰期很短,很容易发
2 2
生核变化,转化为其他原子,D错误。
5.按要求解答下列问题。(1)[2020·全国卷Ⅱ,35(1)]基态Ti原子的核外电子排布式为________。
(2)[2019·全国卷Ⅰ,35(1)]下列状态的镁中,电离最外层一个电子所需能量最大的是
__________(填字母)。
A.[Ne] B.[Ne]
C.[Ne] D.[Ne]
(3)[2020·全国卷Ⅰ,35(1)]基态Fe2+与Fe3+离子中未成对的电子数之比为________。
答案 (1)1s22s22p63s23p63d24s2(或[Ar]3d24s2)
(2)A (3)4∶5
课时精练
1.三星堆见证了中华文明起源的多样性,通过“14C测定法”初步确定其年代区间。下列有
关说法正确的是( )
A.14C与12C互为同位素
B.14C的核外电子数是14
C.14C可由中子轰击14N产生,14C与14N的化学性质相同
D.青铜器皿、骨头、纺织品、灰烬等都可作为检测的样品
答案 A
2.钍是一种放射性金属元素,有钢灰色光泽,质地柔软,化学性质较活泼,广泛分布在地壳
中。230Th和232Th是钍的两种同位素,232Th可以转化成233U,因此它是潜在的核燃料。下列
有关Th的说法正确的是( )
A.Th元素的质量数是232
B.Th元素的相对原子质量是231
C.232Th转换成233U是化学变化
D.230Th和232Th的化学性质相同
答案 D
解析 Th有质量数为230、232的两种核素,不能说Th元素的质量数为232,A项错误;元
素的相对原子质量是由各种同位素的相对原子质量与其在自然界中的百分含量求得的平均值,
B项错误;232Th转换成233U,不是化学变化,C项错误;同位素的物理性质差异较大,但化
学性质几乎完全相同,D项正确。
3.在宾馆、办公楼等公共场所,常使用一种电离式烟雾报警器,其主体是一个放有
镅-241(Am)放射源的电离室。 Am原子核内中子数与核外电子数之差是( )
A.241 B.146 C.95 D.51答案 D
解析 Am的质子数为95,质量数为241,中子数=241-95=146,核外电子数=质子数=
95,中子数与核外电子数之差为146-95=51。
4.某元素的一种核素X的原子质量数为A,含N个中子,它与1H原子组成H X分子,a g
m
H X中所含质子的物质的量是( )
m
A. mol B. mol
C. mol D. mol
答案 A
解析 H X的摩尔质量为(A+m) g·mol-1,a g H X的物质的量为 mol;X原子的质量数为
m m
A,含N个中子,则质子数为A-N,所以a g H X中含质子的物质的量为 mol×(A-N+m)
m
= mol,A正确。
5.下列有关构造原理的说法错误的是( )
A.原子核外电子填充3p、3d、4s能级的顺序为3p→4s→3d
B.某基态原子部分核外电子的排布式为3d64s2
C.所有基态原子的核外电子排布都遵循构造原理
D.构造原理中的电子排布能级顺序,实质是各能级能量由低到高的顺序
答案 C
解析 绝大多数基态原子的核外电子排布都遵循构造原理,但也有少数例外,如Cu,故C
错误;构造原理中电子填入能级的顺序即各能级能量由低到高的顺序,故D正确。
6.下列关于原子结构、原子轨道的说法正确的是( )
A.N能层中有4s、4p、4d、4f四个能级,共16个轨道,可容纳32种运动状态的电子
B.在K能层中,有自旋相反的两条轨道
C.s电子绕核运动,其轨道为球面,而p电子在哑铃形曲面上运动
D.电子云通常是用小黑点来表示电子的多少
答案 A
解析 N能层中有4s、4p、4d、4f四个能级,各具有1、3、5、7个轨道,每个轨道最多可
容纳2个电子,故可容纳32个电子,所以有32种运动状态,A正确;在K能层中,只有1
个轨道,能容纳自旋相反的2个电子,B不正确;电子云通常是用小黑点来表示电子出现的
机会多少,但小黑点不表示电子,D不正确。
7.第四周期元素中基态原子核外有3个未成对电子的共有( )
A.2种 B.3种 C.4种 D.5种
答案 B
解析 第四周期元素中基态原子核外有3个未成对电子的共有3种,分别是V(3d34s2)、
Co(3d74s2)、As(4s24p3),故选B。
8.下列轨道表示式所表示的元素原子中,其能量处于最低状态的是( )A.
B.
C.
D.
答案 D
解析 原子处于基态时能量最低,A项,Be原子的2s轨道未排满电子,2p轨道排布1个电
子,应为激发态,错误;B项,N原子核外电子排布不符合洪特规则,错误;C项,B原子
的2s轨道未排满电子,2p轨道排布2个电子,应为激发态,错误;D项,碳原子的1s和2s
轨道全部排满电子后,2p轨道排布2个电子,核外电子排布符合能量最低原理,应是基态
碳原子,正确。
9.下列说法正确的是( )
A.最外层电子排布式为ns2的基态原子所对应元素一定位于第ⅡA族
B.d区元素的原子一定都有d轨道电子
C.最外层电子排布式为ns1的基态原子所对应元素一定是金属元素
D.基态原子价层电子排布式为nsnnpn的元素一定是金属元素
答案 B
解析 最外层电子排布式为ns2的基态原子所对应元素不一定位于第ⅡA族,可能位于副族
或0族,如副族的Zn或0族的He,故A错误;d区元素的基态原子都含有d轨道电子,故
B正确;最外层电子排布式为ns1的基态原子所对应元素不一定是金属元素,如 H,故C错
误;基态原子价层电子排布式为nsnnpn的元素,s能级上最多排列2个电子,则n=2,所以
该原子价层电子排布式为2s22p2,为C元素,是非金属元素,故D错误。
10.人们通常将在同一原子轨道上运动、自旋相反的2个电子,称为“电子对”,将在某一
原子轨道上运动的单个电子,称为“未成对电子”。下列基态原子的电子排布式中,未成对
电子数最多的是( )
A.1s22s22p63s23p6
B.1s22s22p63s23p63d54s2
C.1s22s22p63s23p63d54s1
D.1s22s22p63s23p63d104s1
答案 C
解析 1s22s22p63s23p6中未成对电子数为 0;1s22s22p63s23p63d54s2中未成对电子数为 5;
1s22s22p63s23p63d54s1中未成对电子数为6;1s22s22p63s23p63d104s1中未成对电子数为1。11.1934年约里奥-居里夫妇在核反应中用α粒子(即氦核He)轰击金属原子X,得到核素
Y,开创了人造放射性核素的先河:
X+He―→Y+n。
其中元素X、Y的最外层电子数之和为8。下列叙述正确的是( )
A.X的相对原子质量为26
B.X、Y均可形成三氯化物
C.X的质子数大于Y的
D.Y仅有一种含氧酸
答案 B
解析 由守恒关系可知元素X的质量数为27,X与Y最外层电子数之和为8,质子数相差
2,且X为金属元素,可推知X为Al元素,Y为P元素,二者都有+3价,都可以形成三氯
化物,A项错误,B项正确;Al原子质子数为13,P原子质子数为15,故质子数:X