文档内容
2025届高三化学一轮专题复习讲义(06)
专题二 物质结构
2-2 原子、分子结构与性质(1课时)
【复习目标】
1.能结合能量最低原理、泡利不相容原理、洪特规则书写1~36号元素基态原子的核外
电子排布式和轨道表达式,并说明含义。
2.能利用电负性判断共价键的极性,能根据共价分子的结构特点说明简单分子的某些
性质;能说明分子间作用力(含氢键)对物质熔、沸点等性质的影响 ,能列举含有氢键的物质
及其性质特点 。
3.能根据给定的信息分析常见简单分子的空间结构,能利用相关理论解释简单的共价
分子的空间结构;能根据分子结构特点和键的极性来判断分子的极性,并据此对分子的一些
典型性质及其应用作出解释。
【重点突破】
1.1~36号元素基态原子核外电子排布的表示。
2.简单分子空间构型的判断及解释(杂化轨道、价层电子对互斥模型)。
3.分子的性质与应用。
【真题再现】
例1.(2023·江苏卷节选)阅读下列材料,回答下列问题:
氢元素及其化合物在自然界广泛存在且具有重要应用。H、H、H是氢元素的3种核素,
基态H原子1s1的核外电子排布,使得H既可以形成H+又可以形成H-,还能形成HO、HO、
2 2 2
NH 、NH、CaH 等重要化合物;水煤气法、电解水、光催化分解水都能获得H,如水煤气法
3 2 4 2 2
制氢反应中,HO(g)与足量C(s)反应生成1molH (g)和1molCO(g)吸收131.3kJ的热量。H 在
2 2 2
金属冶炼、新能源开发、碳中和等方面具有重要应用,如HCO在催化剂作用下与H 反应可得
2
到HCOO-。我国科学家在氢气的制备和应用等方面都取得了重大成果。
下列说法正确的是
A.H、H、H都属于氢元素
B.NH和HO的中心原子轨道杂化类型均为sp2
2
C.HO 分子中的化学键均为极性共价键
2 2
D.CaH 晶体中存在Ca与H 之间的强烈相互作用
2 2
解析:A项,H、H、H都属于氢元素,三者互为同位素,统称为氢元素,正确;B项,NH和HO
2
的中心原子轨道杂化类型均为sp3,错误;C项,HO 分子中的化学键既存在O—H极性
2 2
共价键,也存在O—O非极性共价键,错误;D项,CaH 晶体中存在Ca2+与H-之间的离子
2
键,阴阳离子间强烈的相互作用,错误。
答案:A
例2.(2022·全国甲卷)2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为
“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯(CH=CH )与四
2 2
氟乙烯(CF=CF )的共聚物(ETFE)制成。回答下列问题:
2 2
(1)基态F原子的价电子排布图(轨道表示式)为_______。
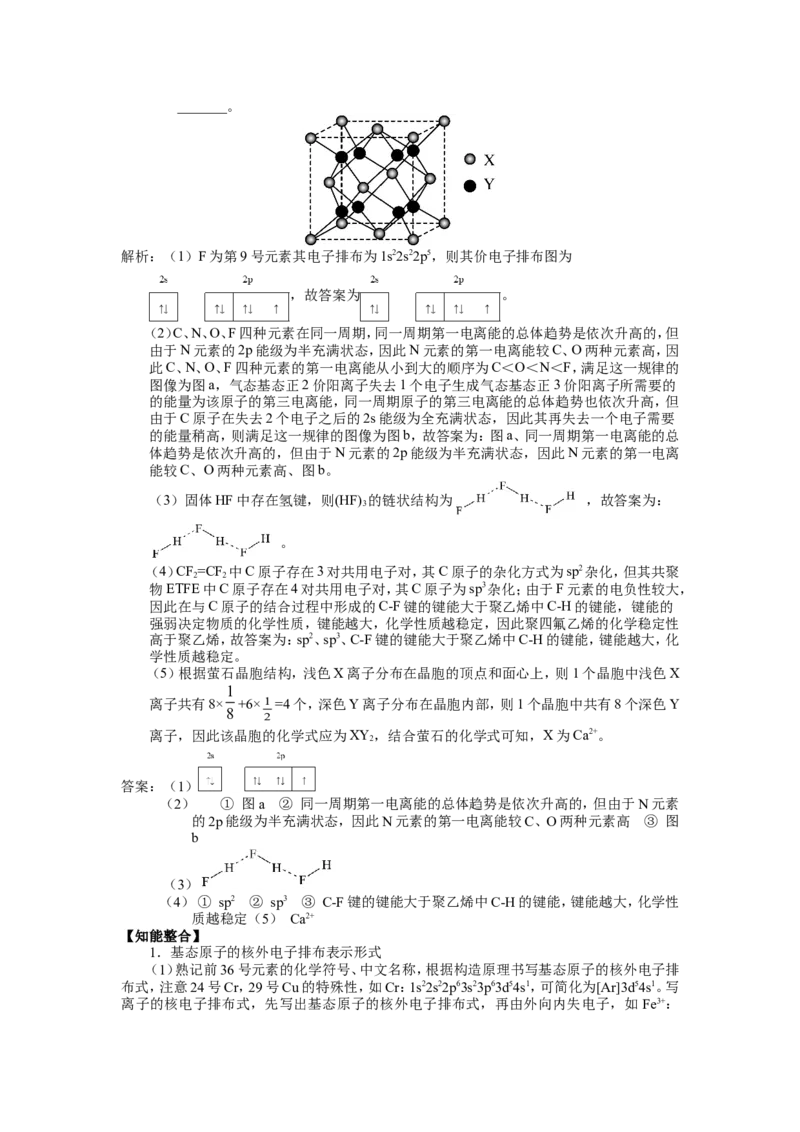
(2)图a、b、c分别表示C、N、O和F的逐级电离能Ⅰ 数值变化趋势(纵坐标的标度不
同)。第一电离能的变化图是______(填标号),判断的根据是 ;第三电离
能的变化图是_______(填标号)。
(3)固态氟化氢中存在(HF) 形式,画出(HF) 的链状结构_______。
n 3
(4) CF=CF 和ETFE分子中C的杂化轨道类型分别为_______和_______;聚四氟乙烯
2 2
的化学稳定性高于聚乙烯,从化学键的角度解释原因_______。
(5)萤石(CaF )是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是
2_______。
解析:(1)F为第9号元素其电子排布为1s22s22p5,则其价电子排布图为
,故答案为 。
(2)C、N、O、F四种元素在同一周期,同一周期第一电离能的总体趋势是依次升高的,但
由于N元素的2p能级为半充满状态,因此N元素的第一电离能较C、O两种元素高,因
此C、N、O、F四种元素的第一电离能从小到大的顺序为C<O<N<F,满足这一规律的
图像为图a,气态基态正2价阳离子失去1个电子生成气态基态正3价阳离子所需要的
的能量为该原子的第三电离能,同一周期原子的第三电离能的总体趋势也依次升高,但
由于C原子在失去2个电子之后的2s能级为全充满状态,因此其再失去一个电子需要
的能量稍高,则满足这一规律的图像为图b,故答案为:图a、同一周期第一电离能的总
体趋势是依次升高的,但由于N元素的2p能级为半充满状态,因此N元素的第一电离
能较C、O两种元素高、图b。
(3)固体HF中存在氢键,则(HF) 的链状结构为 ,故答案为:
3
。
(4)CF=CF 中C原子存在3对共用电子对,其C原子的杂化方式为sp2杂化,但其共聚
2 2
物ETFE中C原子存在4对共用电子对,其C原子为sp3杂化;由于F元素的电负性较大,
因此在与C原子的结合过程中形成的C-F键的键能大于聚乙烯中C-H的键能,键能的
强弱决定物质的化学性质,键能越大,化学性质越稳定,因此聚四氟乙烯的化学稳定性
高于聚乙烯,故答案为:sp2、sp3、C-F键的键能大于聚乙烯中C-H的键能,键能越大,化
学性质越稳定。
(5)根据萤石晶胞结构,浅色X离子分布在晶胞的顶点和面心上,则1个晶胞中浅色X
1
离子共有8× +6×1 =4个,深色Y离子分布在晶胞内部,则1个晶胞中共有8个深色Y
8
2
离子,因此该晶胞的化学式应为XY ,结合萤石的化学式可知,X为Ca2+。
2
答案:(1)
(2) ① 图a ② 同一周期第一电离能的总体趋势是依次升高的,但由于N元素
的2p能级为半充满状态,因此N元素的第一电离能较C、O两种元素高 ③ 图
b
(3)
(4) ① sp2 ② sp3 ③ C-F键的键能大于聚乙烯中C-H的键能,键能越大,化学性
质越稳定(5) Ca2+
【知能整合】
1.基态原子的核外电子排布表示形式
(1)熟记前36号元素的化学符号、中文名称,根据构造原理书写基态原子的核外电子排
布式,注意24号Cr,29号Cu的特殊性,如Cr:1s22s22p63s23p63d54s1,可简化为[Ar]3d54s1。写
离子的核电子排布式,先写出基态原子的核外电子排布式,再由外向内失电子,如 Fe3+:[Ar]3d64s2 [Ar]3d5。
(2)价层(外围)电子排布式:主族元素就是最外层电子排布式,如As位于第4周期VA
族,价电子排布式为4s24p3;副族元素去掉原子实剩余部分,如Cu外围电子排布式为3d104s1。
(3)电子排布图又称轨道表示式:如O:
2.第一电离能、电负性
(1)规律:在元素周期表中,元素的第一电离能从左到右有增大的趋势,从上往下逐渐减
小、电负性从左到右逐渐增大,从上往下逐渐减小。
(2)特性:同周期主族元素,第ⅡA族(np0)全空、ⅤA族(np3)半充满,比较稳定,所以其
第一电离能大于同周期相邻的ⅢA和ⅥA族元素。
(3)方法:我们常常应用化合价及物质类别判断电负性的大小。如O与Cl的电负性比较:
a.HClO中Cl为+1价、O为-2价,可知O的电负性大于Cl;
b.Al O 是离子化合物、AlCl 是共价化合物,可知O的电负性大于Cl。
2 3 3
例3.(2022·江苏卷)下列说法正确的是
A.金刚石与石墨烯中的 C—C—C 夹角都为120°
B.SiH、SiCl 都是由极性键构成的非极性分子
4 4
C.锗原子( Ge)基态核外电子排布式为 4s24p2
32
D.IVA 族元素单质的晶体类型相同
解析:A 项,金刚石中C原子为sp3杂化,键角为109°28',石墨中的C为 sp2杂化,键角为
120°,错误;B项,Si—H、Si—Cl 中的共用电子对均偏离 Si,化学键为极性键,SiH、
4
SiCl 都是正四面体结构,正、负电荷中心重合,属于非极性分子,正确;C项,Ge 的基
4
态核外电子排布式为1s22s22p63s23p63d104s24p2,错误;D 项,金刚石和晶体硅为共价晶体,
石墨为混合型晶体,锗、锡、铅等为金属晶体,错误。
答案:B
例4.(2023·全国甲卷)将酞菁—钴钛—三氯化铝复合嵌接在碳纳米管上,制得一种高效催化
还原二氧化碳的催化剂。回答下列问题:
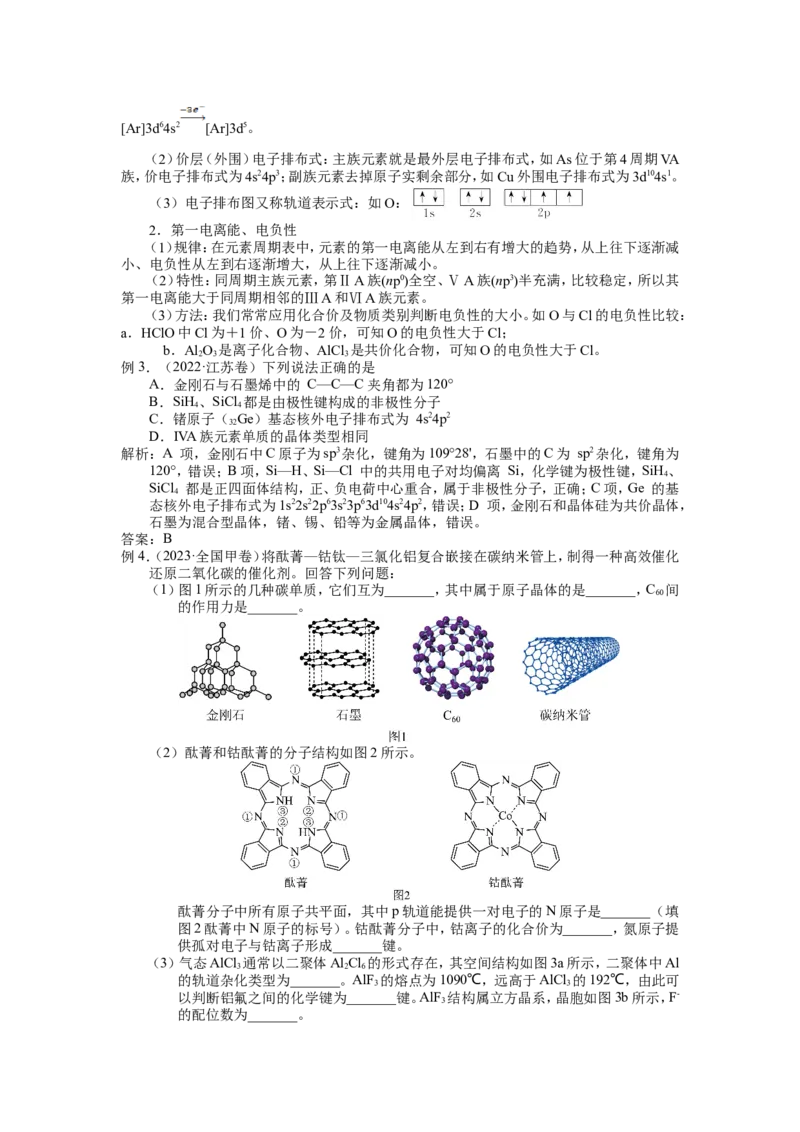
(1)图1所示的几种碳单质,它们互为_______,其中属于原子晶体的是_______,C 间
60
的作用力是_______。
(2)酞菁和钴酞菁的分子结构如图2所示。
酞菁分子中所有原子共平面,其中p轨道能提供一对电子的N原子是_______(填
图2酞菁中N原子的标号)。钴酞菁分子中,钴离子的化合价为_______,氮原子提
供孤对电子与钴离子形成_______键。
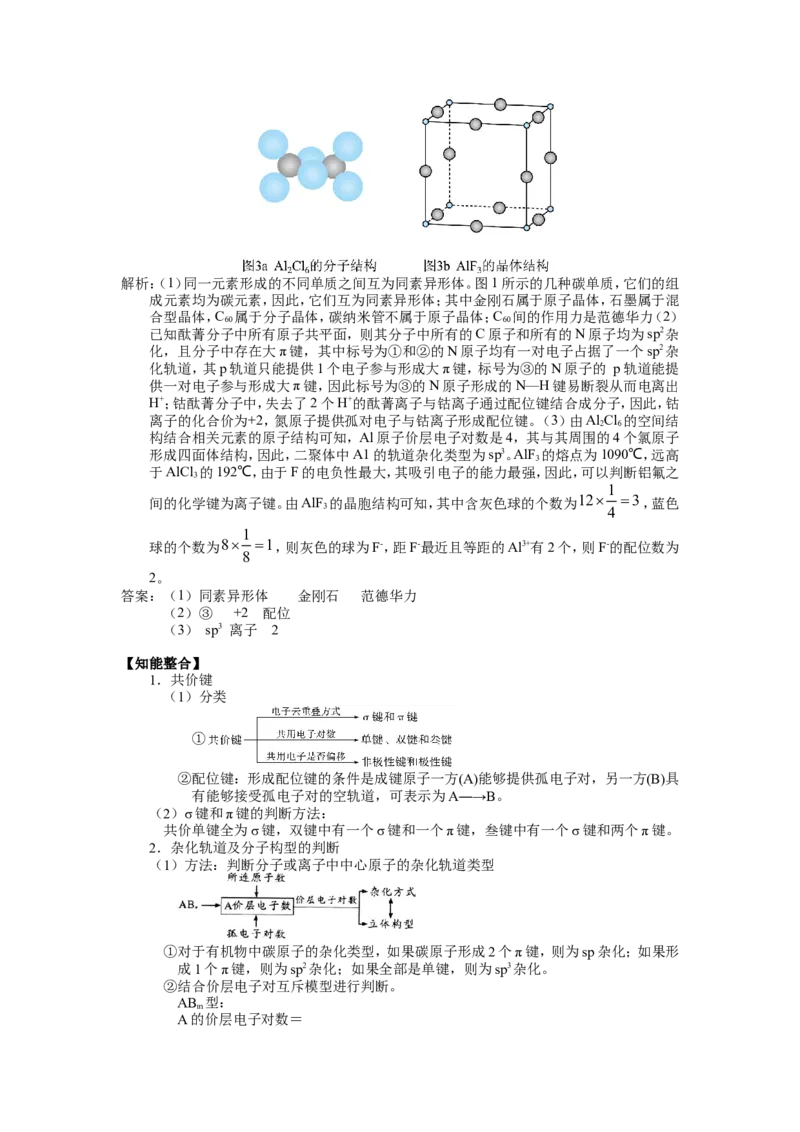
(3)气态AlCl 通常以二聚体Al Cl 的形式存在,其空间结构如图3a所示,二聚体中Al
3 2 6
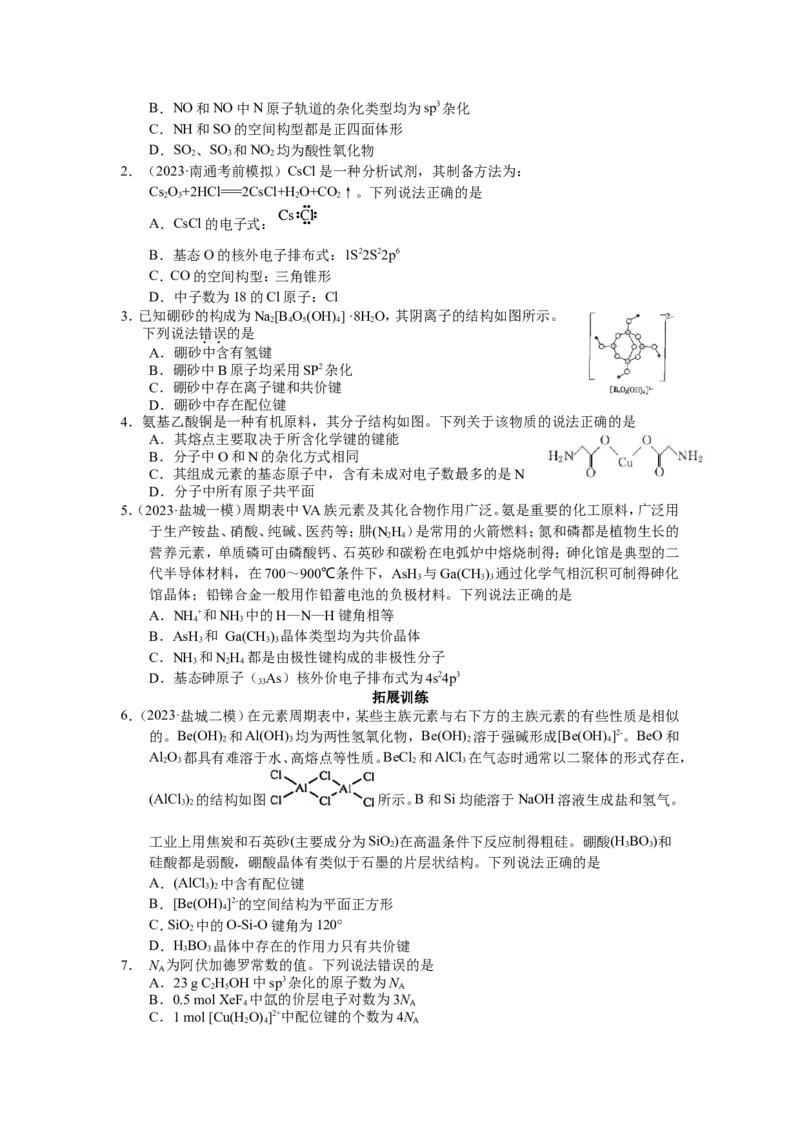
的轨道杂化类型为_______。AlF 的熔点为1090℃,远高于AlCl 的192℃,由此可
3 3
以判断铝氟之间的化学键为_______键。AlF 结构属立方晶系,晶胞如图3b所示,F-
3
的配位数为_______。解析:(1)同一元素形成的不同单质之间互为同素异形体。图1所示的几种碳单质,它们的组
成元素均为碳元素,因此,它们互为同素异形体;其中金刚石属于原子晶体,石墨属于混
合型晶体,C 属于分子晶体,碳纳米管不属于原子晶体;C 间的作用力是范德华力(2)
60 60
已知酞菁分子中所有原子共平面,则其分子中所有的C原子和所有的N原子均为sp2杂
化,且分子中存在大π键,其中标号为①和②的N原子均有一对电子占据了一个sp2杂
化轨道,其p轨道只能提供1个电子参与形成大π键,标号为③的N原子的 p轨道能提
供一对电子参与形成大π键,因此标号为③的N原子形成的N—H键易断裂从而电离出
H+;钴酞菁分子中,失去了2个H+的酞菁离子与钴离子通过配位键结合成分子,因此,钴
离子的化合价为+2,氮原子提供孤对电子与钴离子形成配位键。(3)由Al Cl 的空间结
2 6
构结合相关元素的原子结构可知,Al原子价层电子对数是4,其与其周围的4个氯原子
形成四面体结构,因此,二聚体中A1的轨道杂化类型为sp3。AlF 的熔点为1090℃,远高
3
于AlCl 的192℃,由于F的电负性最大,其吸引电子的能力最强,因此,可以判断铝氟之
3
1
间的化学键为离子键。由AlF 的晶胞结构可知,其中含灰色球的个数为12 3,蓝色
3 4
1
球的个数为8 1,则灰色的球为F-,距F-最近且等距的Al3+有2个,则F-的配位数为
8
2。
答案:(1)同素异形体 金刚石 范德华力
(2)③ +2 配位
(3) sp3 离子 2
【知能整合】
1.共价键
(1)分类
①
②配位键:形成配位键的条件是成键原子一方(A)能够提供孤电子对,另一方(B)具
有能够接受孤电子对的空轨道,可表示为A―→B。
(2)σ键和π键的判断方法:
共价单键全为σ键,双键中有一个σ键和一个π键,叁键中有一个σ键和两个π键。
2.杂化轨道及分子构型的判断
(1)方法:判断分子或离子中中心原子的杂化轨道类型
①对于有机物中碳原子的杂化类型,如果碳原子形成2个π键,则为sp杂化;如果形
成1个π键,则为sp2杂化;如果全部是单键,则为sp3杂化。
②结合价层电子对互斥模型进行判断。
AB 型:
m
A的价层电子对数=配位原子为卤素、氢原子时提供1个电子,氧原子、硫原子作配位原子时按不提供
电子计算或者杂化轨道数=中心原子的孤电子对数+中心原子的σ键个数。孤电子
对数=,如HO的中心原子为O原子,其价电子数为6,H原子的未成对电子数为1,
2
可知氧原子上的孤电子对数= =2。
(2)中心原子杂化类型和分子构型的相互判断:
分子组成
中心原子的 中心原子的
(A为中心 分子空间构型 示例
孤电子对数 杂化方式
原子)
0 sp 直线形 BeCl
2
AB 1 sp2 V形 SO
2 2
2 sp3 V形 HO
2
0 sp2 平面三角形 BF
AB 3
3 1 sp3 三角锥形 NH
3
AB 0 sp3 正四面体形 CH
4 4
3.三种作用力及对物质性质的影响
范德华力 氢键 共价键
作用微粒 分子 H与N、O、F 原子
强度比较 共价键>氢键>范德华力
组成和结构相似的物
形成氢键元素的
影响因素 质,相对分子质量越大, 原子半径
电负性
范德华力越大
分子间氢键使熔、
影响物质的熔、沸点和 键能越大,稳
性质的影响 沸点升高,溶解度
溶解度等物理性质 定性越强
增大
4.等电子体的书写方法
5.配位键与配合物
(1)配位键的表示方法
如A→B,其中A表示提供孤电子对的原子,B表示提供空轨道的原子。如NH可表
示为 ,在NH中,虽然有一个N—H键形成过程与其他3个N—H键形成过程不
同,但是一旦形成之后,4个共价键就完全相同。
(2)配合物组成:以[Cu(NH )]SO 为例
3 4 4
电离方程式:[Cu(NH )]SO ===[Cu(NH)]2++SO
3 4 4 3 4
【体系再构】
【随堂反馈】
基础训练
1.(2023·连云港考前模拟)下列有关含氮、含硫微粒的说法正确的是
A.SO 转化为SO 时,分子的键角变小
2 3B.NO和NO中N原子轨道的杂化类型均为sp3杂化
C.NH和SO的空间构型都是正四面体形
D.SO 、SO 和NO 均为酸性氧化物
2 3 2
2.(2023·南通考前模拟)CsCl是一种分析试剂,其制备方法为:
CsO+2HCl===2CsCl+H O+CO↑。下列说法正确的是
2 3 2 2
A.CsCl的电子式:
B.基态O的核外电子排布式:1S22S22p6
C.CO的空间构型:三角锥形
D.中子数为18的Cl原子:Cl
3.已知硼砂的构成为Na[B O(OH) ] ·8HO,其阴离子的结构如图所示。
2 4 5 4 2
下列说法错误的是
A.硼砂中含有氢键
B.硼砂中B原子均采用SP2杂化
C.硼砂中存在离子键和共价键
D.硼砂中存在配位键
4.氨基乙酸铜是一种有机原料,其分子结构如图。下列关于该物质的说法正确的是
A.其熔点主要取决于所含化学键的键能
B.分子中O和N的杂化方式相同
C.其组成元素的基态原子中,含有未成对电子数最多的是N
D.分子中所有原子共平面
5.(2023·盐城一模)周期表中VA族元素及其化合物作用广泛。氨是重要的化工原料,广泛用
于生产铵盐、硝酸、纯碱、医药等;肼(N H)是常用的火箭燃料;氮和磷都是植物生长的
2 4
营养元素,单质磷可由磷酸钙、石英砂和碳粉在电弧炉中熔烧制得;砷化馆是典型的二
代半导体材料,在700~900℃条件下,AsH 与Ga(CH ) 通过化学气相沉积可制得砷化
3 3 3
馆晶体;铅锑合金一般用作铅蓄电池的负极材料。下列说法正确的是
A.NH +和NH 中的H—N—H键角相等
4 3
B.AsH 和 Ga(CH ) 晶体类型均为共价晶体
3 3 3
C.NH 和NH 都是由极性键构成的非极性分子
3 2 4
D.基态砷原子( As)核外价电子排布式为4s24p3
33
拓展训练
6.(2023·盐城二模)在元素周期表中,某些主族元素与右下方的主族元素的有些性质是相似
的。Be(OH) 和Al(OH) 均为两性氢氧化物,Be(OH) 溶于强碱形成[Be(OH) ]2-。BeO和
2 3 2 4
AlO 都具有难溶于水、高熔点等性质。BeCl 和AlCl 在气态时通常以二聚体的形式存在,
2 3 2 3
(AlCl ) 的结构如图 所示。B和Si均能溶于NaOH溶液生成盐和氢气。
3 2
工业上用焦炭和石英砂(主要成分为SiO )在高温条件下反应制得粗硅。硼酸(H BO)和
2 3 3
硅酸都是弱酸,硼酸晶体有类似于石墨的片层状结构。下列说法正确的是
A.(AlCl ) 中含有配位键
3 2
B.[Be(OH) ]2-的空间结构为平面正方形
4
C.SiO 中的O-Si-O键角为120°
2
D.HBO 晶体中存在的作用力只有共价键
3 3
7. N 为阿伏加德罗常数的值。下列说法错误的是
A
A.23 g C HOH中sp3杂化的原子数为N
2 5 A
B.0.5 mol XeF 中氙的价层电子对数为3N
4 A
C.1 mol [Cu(H O) ]2+中配位键的个数为4N
2 4 AD.标准状况下,11.2 L CO和H 的混合气体中分子数为0.5N
2 A
8.(2023·江苏七市一模)NH 易液化,能与多种物质发生反应。将金属钠投入液氨中有H 产
3 2
生,NH 能与CaCl 结合生成CaCl ·8NH ,加热条件下NH 能将CuO还原成Cu。NH 可
3 2 2 3 3 3
用于制取肼(NH)和尿素[CO(NH)]等,工业上常用浓氨水检验输送氯气的管道是否泄
2 4 2 2
漏,泄漏处有白烟生成。下列说法正确的是
A.NH 分子中的H—N—H键角为120°
2 4
B.NH 与Cl 反应生成的白烟成分为NH Cl
3 2 4
C.金属钠与液氨反应体现了NH 的还原性
3
D.NH 易液化是由于NH 与HO分子间形成氢键
3 3 2
9.(1)乙二胺(H NCH CHNH )是一种有机化合物,分子中氮、碳的杂化类型分别是________、
2 2 2 2
________。乙二胺能与 Mg2+、Cu2+等金属离子形成稳定环状离子,其原因是
______________________________________________________,其中与乙二胺形成的
化合物稳定性相对较高的是________(填“Mg2+”或“Cu2+”)。
(2)元素As与N同族。预测As的氢化物分子的立体结构为________,其沸点比NH 的
3
________(填“高”或“低”),其判断理由是___________________________________。
10.经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。
(1)从结构角度分析,R中两种阳离子的相同之处为________,不同之处为________。
(填标号)
A.中心原子的杂化轨道类型
B.中心原子的价层电子对数
C.立体结构
D.共价键类型
(2)R中阴离子N中的σ键总数为________个。分子中的大π键可用符号Π表示,其中
m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大
π键可表示为Π),则N中的大π键应表示为____________。
(3)图中虚线代表氢键,其表示式为(NH)N—H…Cl、________、________。
【随堂反馈】答案:
1.C 2.B 3.B 4.C 5.D 6.A 7.A 8.B
9.(1)sp3 sp3 乙二胺的两个N提供孤对电子给金属离子形成配位键 Cu2+
(2)三角锥形 低 NH 分子间存在氢键
3
10.(1)ABD C
(2)5 Π (3)(H O+)O—H…N(N) (NH)N—H…N(N)
3
【课后作业】
乙醚
1.(2023·南通三模)乙硼烷(B H)常应用于有机合成领域,可通过反应3NaH +4BF
2 6 4 3
2B H+3NaBF 制得。下列说法正确的是
2 6 4
A.基态B原子的轨道表示式为
B.基态F原子核外电子排布式为2s22p5
C.BF 分子空间构型为三角锥形
3
D.NaBF 中含有配位键
4
2.(2023·苏锡常镇二模)反应2NH +NaClO===NH+NaCl+HO用于合成NH。下列说法不
3 2 4 2 2 4
正确 的是A.NH 的空间构型为正三角形 B.NaClO的电子式为
3
C.NH 含有极性键和非极性键 D.HO和NH 之间可以形成氢键
2 4 2 2 4
3.缺电子化合物是指电子数不符合路易斯结构(一个原子通过共享电子使其价层电子数达
到8,H原子达到2所形成的稳定分子结构)要求的一类化合物。下列说法错误的是
A.NH 、BF、BF-中只有BF 是缺电子化合物
3 3 4 3
B.BF、BF-中心原子的杂化方式分别为sp2、sp3
3 4
C.BF 与NH 反应时有配位键生成
3 3
D.BF-的键角小于NH
4 3
4.(2023·徐州三模)反应CFI+H O===CFH+HIO,下列说法正确的是
3 2 3
A.氧原子的结构示意图为 B.HIO的电子式为
C.CFI中I元素的化合价为+1 D.CFH的空间构型为正四面体
3 3
5.BF 与一定量的水形成(H O) ·BF,一定条件下(H O) ·BF 可发生如图转化,下列说法中正
3 2 2 3 2 2 3
确的是
A.(H O) ·BF 熔化后得到的物质属于离子晶体
2 2 3
B.(H O) ·BF 分子间存在着配位键和氢键
2 2 3
C.BF 是仅含极性共价键的非极性分子
3
D.基态B原子核外电子的空间运动状态有5种
6.(2022·湖北卷)磷酰三叠氮是一种高能分子,结构简式为O==P(N )。下列关于该分子 的说
3 3
法正确的是
A.该分子为非极性分子 B.该分子立体构型为正四面体形
C.加热条件下会分解并放出N D.分解产物NPO的电子式为
2
7.(2023·昆山六校调研)汽车尾气净化装置可将污染物中的CO和NO转化为无害气体,发
生反应为2CO(g)+2NO(g)===N(g)+2CO(g) ΔH=-746.5 kJ·mol-1。汽油抗震添加剂
2 2
四乙基铅(熔点为-136 ℃,极易挥发)的排放严重危害人体中枢神经系统。下列有关说法
正确的是
A.SO 和SO 中的键角相等
2 3
B.丙烯能形成分子间氢键
C.N 中σ键和π键数目之比为1∶2
2
D.固态四乙基铅为离子晶体
8.(1)甲胺(CHNH )极易溶于水,除因为它们都是极性分子外,还因______________。
3 2
(2)乙二胺(H CHCHNH )和三甲胺[N(CH )]均属于胺,相对分子质量相近,但乙二胺比
2 2 2 2 3 3
三甲胺的沸点高得多,原因是_________________________________。
(3)化合物A ( )能与水以任意比例互溶,这是因为_______________________。
(4)1 mol物质B( )中所含σ键的物质的量为________mol。
(5)C H 分子中σ键与π键数目之比为________。
2 2
(6)1 mol草酸(HOOCCOOH)分子中含有σ键的数目为______________。
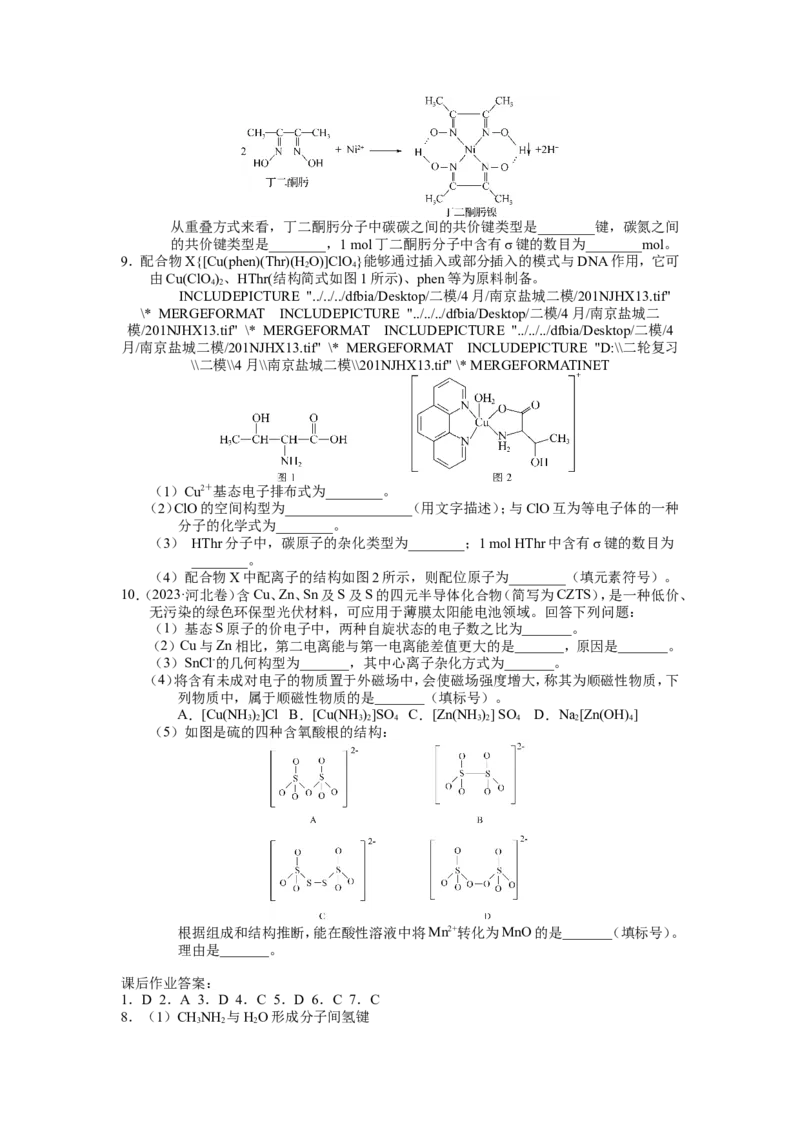
(7)Ni2+与丁二酮肟生成鲜红色丁二酮肟镍沉淀,该反应可用于检验Ni2+。从重叠方式来看,丁二酮肟分子中碳碳之间的共价键类型是________键,碳氮之间
的共价键类型是________,1 mol丁二酮肟分子中含有σ键的数目为________mol。
9.配合物X{[Cu(phen)(Thr)(H O)]ClO }能够通过插入或部分插入的模式与DNA作用,它可
2 4
由Cu(ClO )、HThr(结构简式如图1所示)、phen等为原料制备。
4 2
INCLUDEPICTURE "../../../dfbia/Desktop/二模/4月/南京盐城二模/201NJHX13.tif"
\* MERGEFORMAT INCLUDEPICTURE "../../../dfbia/Desktop/二模/4月/南京盐城二
模/201NJHX13.tif" \* MERGEFORMAT INCLUDEPICTURE "../../../dfbia/Desktop/二模/4
月/南京盐城二模/201NJHX13.tif" \* MERGEFORMAT INCLUDEPICTURE "D:\\二轮复习
\\二模\\4月\\南京盐城二模\\201NJHX13.tif" \* MERGEFORMATINET
(1)Cu2+基态电子排布式为________。
(2)ClO的空间构型为__________________(用文字描述);与ClO互为等电子体的一种
分子的化学式为________。
(3) HThr分子中,碳原子的杂化类型为________;1 mol HThr中含有σ键的数目为
________。
(4)配合物X中配离子的结构如图2所示,则配位原子为________(填元素符号)。
10.(2023·河北卷)含Cu、Zn、Sn及S及S的四元半导体化合物(简写为CZTS),是一种低价、
无污染的绿色环保型光伏材料,可应用于薄膜太阳能电池领域。回答下列问题:
(1)基态S原子的价电子中,两种自旋状态的电子数之比为_______。
(2)Cu与Zn相比,第二电离能与第一电离能差值更大的是_______,原因是_______。
(3)SnCl-的几何构型为_______,其中心离子杂化方式为_______。
(4)将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质,下
列物质中,属于顺磁性物质的是_______(填标号)。
A.[Cu(NH )]Cl B.[Cu(NH )]SO C.[Zn(NH )] SO D.Na[Zn(OH) ]
3 2 3 2 4 3 2 4 2 4
(5)如图是硫的四种含氧酸根的结构:
根据组成和结构推断,能在酸性溶液中将Mn2+转化为MnO的是_______(填标号)。
理由是_______。
课后作业答案:
1.D 2.A 3.D 4.C 5.D 6.C 7.C
8.(1)CHNH 与HO形成分子间氢键
3 2 2(2)乙二胺分子之间可以形成氢键,三甲胺分子间不能形成氢键
(3)化合物A与水分子间存在氢键
(4)16
(5)3∶2
(6)7 mol或7×6.02×1023
(7)σ 1个σ键、1个π键 15
9.(1)1s22s22p63s23p63d9或[Ar]3d9
(2)正四面体形 CCl 等
4
(3) sp2、sp3 16 mol或16×6.02×1023个
(4)O、N
10.
(1)1︰2或2︰1
(2)Cu Cu的第二电离能失去的是3d10的电子,第一电离能失去的是4s1电子,Zn的第二
电离能失去的是4s1的电子,第一电离能失去的是4s2电子,3d10电子处于全充满状态,
其与4s1电子能量差值更大
(3)三角锥形 sp3杂化
(4)B
(5)D D中含有-1价的O,易被还原,具有强氧化性,能将Mn2+转化为MnO