文档内容
课时检测(三十五) 元素“位—构—性”关系相互推断
1.(2023·浙江6月选考)X、Y、Z、W四种短周期主族元素,原子序数依次增大。X、Y与Z位于同一
周期,且只有X、Y元素相邻;X基态原子核外有2个未成对电子;W原子在同周期中原子半径最大。
下列说法不正确的是( )
A.第一电离能:Y>Z>X
B.电负性:Z>Y>X>W
C.Z、W原子形成稀有气体电子构型的简单离子的半径:WM
B.电负性:X>Z
C.简单氢化物沸点:Z>W
D.MXYZW 难溶于水
2 3 2
3.(2023·福建等级考)某含锰着色剂的化学式为XY MnZ Q,
4 2 7
Y、X、Q、Z为原子序数依次增大的短周期元素,其中XY具有正四面体空间结构,Z Q结构如图
2
所示。下列说法正确的是( )
A.键角:XY >XY
3
B.简单氢化物沸点:X>Q>Z
C.第一电离能:X>Q>Mn
D.最高价氧化物对应的水化物酸性:Z>X
4.(2023·四川乐山三模)我国科学家分析月壤成分发现含有X、Y、Z、W、M五种主族元素,X、Y、
Z、W、M的原子序数依次增大且都不大于20,Y、Z、W同周期且Z、M同主族;X与W形成的化合物
是光导纤维的基本原料,在潜水艇中YX 可以用作供氧剂。下列说法正确的是( )
2 2
A.离子半径:Z>Y>X
B.X、Y形成的化合物中可能含有离子键、共价键
C.最高价氧化物对应水化物的碱性:Z>M
D.工业上常用电解熔融ZX来制备Z单质
5.某种净水剂由原子序数依次增大的R、W、X、Y、Z五种主族元素组成。五种元素分处三个短周
期,且包含地壳中含量前三的三种元素。五种元素原子的最外层电子数之和为20。下列说法正确的是(
)
A.简单离子半径:Z>X>W
B.最简单氢化物的稳定性:W>Y>Z
C.R分别与W、Z形成的三原子分子均为V形分子
D.常见单质的熔点:X>Y>Z>W>R
6.如表为元素周期表的一部分,X、Y、Z、W均为短周期元素,其中X的最高化合价与最低化合价
代数和为2。下列判断正确的是( )X
Y Z W
A.第二电离能:I(Z)<I(Y)
2 2
B.含Y元素的盐溶液一定显酸性
C.X的简单气态氢化物分子呈平面三角形
D.Y、Z、W的最高价氧化物对应水化物能两两反应
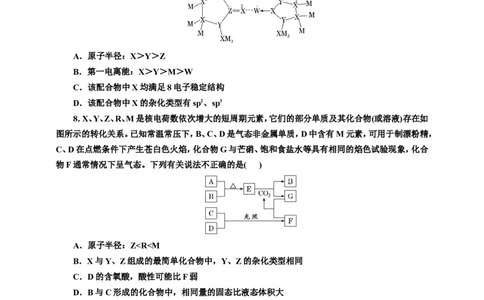
7.某化合物结构如图所示。其中M、X、Y、Z为原子序数依次增大的短周期非金属元素,X是有机
分子的骨架元素,W基态原子的M层为全充满,N层只有一个电子。下列说法正确的是( )
A.原子半径:X>Y>Z
B.第一电离能:X>Y>M>W
C.该配合物中X均满足8电子稳定结构
D.该配合物中X的杂化类型有sp2、sp3
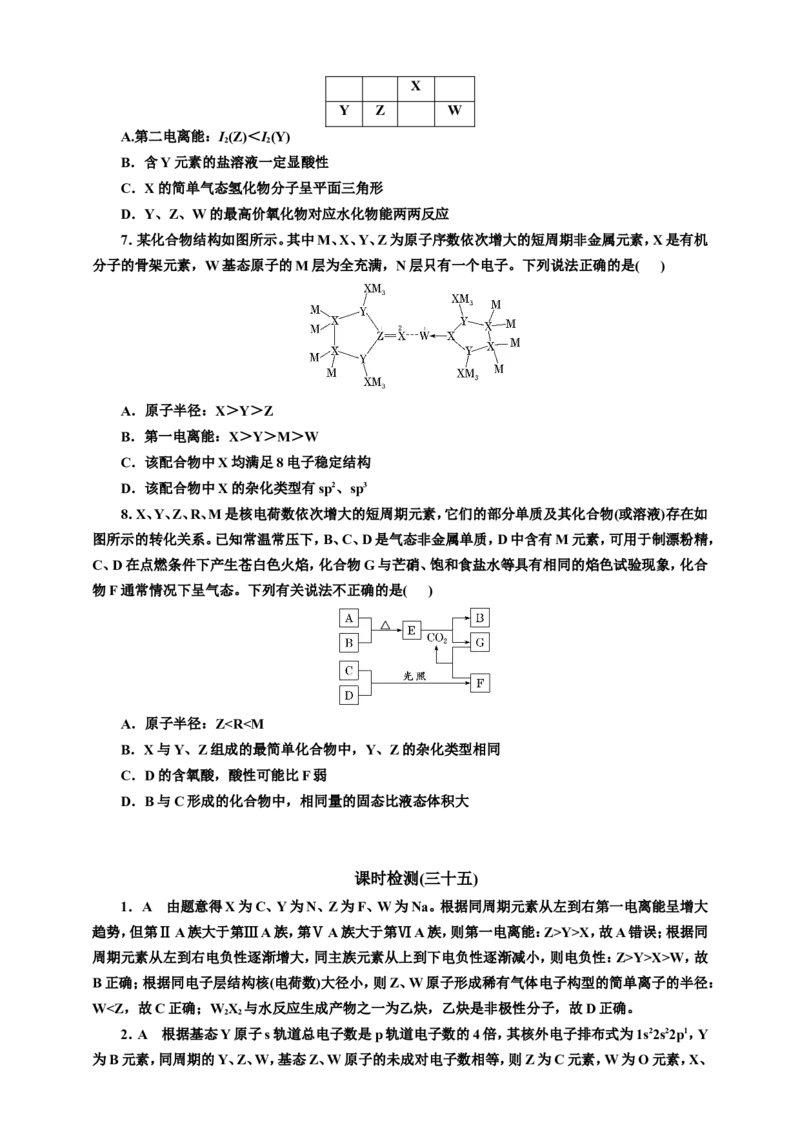
8.X、Y、Z、R、M是核电荷数依次增大的短周期元素,它们的部分单质及其化合物(或溶液)存在如
图所示的转化关系。已知常温常压下,B、C、D是气态非金属单质,D中含有M元素,可用于制漂粉精,
C、D在点燃条件下产生苍白色火焰,化合物G与芒硝、饱和食盐水等具有相同的焰色试验现象,化合
物F通常情况下呈气态。下列有关说法不正确的是( )
A.原子半径:ZY>X,故A错误;根据同
周期元素从左到右电负性逐渐增大,同主族元素从上到下电负性逐渐减小,则电负性:Z>Y>X>W,故
B正确;根据同电子层结构核(电荷数)大径小,则Z、W原子形成稀有气体电子构型的简单离子的半径:
WM,A正确;C的非金属性大于H,元素非金属性越强,电
负性越大,电负性:XNa+>Mg2+,A错误;Na、O形成的Na O 中含有离子键、共价键,B正确;金属性:
2 2
Ca>Mg,则最高价氧化物对应水化物的碱性:Ca(OH) >Mg(OH) ,C错误;工业上常用电解熔融
2 2
MgCl 的方法来制备Mg单质,D错误。
2
5.C R、W、X、Y、Z为原子序数依次增大的五种主族元素,且分处三个短周期,则R一定位于第
一周期,为H,Z一定位于第三周期。五种元素包含地壳中含量前三的元素O、Si、Al,且五种元素原子
的最外层电子数之和为20,则剩余的一种元素最外层电子数为20-1-6-4-3=6,为S,结合原子序
数关系,可知W为O,X为Al,Y为Si,Z为S。电子层结构相同的离子,原子序数越大,半径越小,故
离子半径:Al3+<O2-,A错误;非金属性:O>S>Si,故最简单氢化物的稳定性:HO>HS>SiH ,B
2 2 4
错误;HO和HS的空间结构均为V形,C正确;硅单质为共价晶体,其熔点比铝单质的高,D错误。
2 2
6.A X的最高化合价与最低化合价代数和为2,则X为N,根据周期表结构得出Y为Al,Z为
Si,W为S。A项,Al失去一个电子,价层电子排布式为3s2,为3s能级全充满的稳定结构,Si失去一个
电子,价层电子排布式为3s23p1,故第二电离能:I(Y)>I(Z),正确;B项,四羟基合铝酸钠溶液显碱性,
2 2
错误;C项,氨气分子中,氮原子的价层电子对数为4,有1个孤电子对,故空间结构为三角锥形,错误;
D项,Y、Z、W的最高价氧化物对应水化物分别为氢氧化铝、硅酸、硫酸,氢氧化铝、硫酸均与硅酸不反
应,错误。
7.D X是有机分子的骨架元素,说明X为C元素;W基态原子的M层为全充满,N层只有一个
电子,则W的价层电子排布式为3d104s1,W为Cu元素;M、X、Y、Z为原子序数依次增大的短周期非
金属元素,根据结构式可知,M为H元素,Y为N元素,Z为P元素。电子层数越多,半径越大,电子层
数相同时,核电荷数越小,半径越大,则原子半径:P>C>H,A错误;N的2p轨道为半充满状态,第一
电离能较大,H比C的原子半径小得多,核外电子受到原子核的引力大,电离需要更多的能量,故第一
电离能:H>C,而Cu的电子层数最大,较容易失去一个电子,其第一电离能最小,故第一电离能:N>
H>C>Cu,B错误;该配合物中与W形成配位键的X不满足8电子稳定结构,C错误;该配合物中X
的价层电子对数有3和4,故其杂化类型有sp2、sp3,D正确。8.A 芒硝的化学式为Na SO ,其焰色试验呈黄色,则化合物G的焰色试验也呈黄色,G含有Na
2 4
元素,E能与二氧化碳反应得到G和气体单质B,则E为Na O、B为O、G为Na CO ;A与O 反应得
2 2 2 2 3 2
到Na O,则A为Na,Na CO 与F反应得到CO ,又化合物F通常情况下呈气态,且由非金属气态单
2 2 2 3 2
质C与D在光照条件下得到,则F属于酸,为HCl,C、D分别为H、Cl 中的一种,而D可用于制漂粉
2 2
精,故D为Cl ,C为H,X、Y、Z、R、M依次是H、C、O、Na、Cl元素。原子半径:O