文档内容
课时检测(二十六) 氮及其化合物的基本知能评价
1.下列有关环境保护与绿色化学的叙述错误的是( )
A.形成酸雨的主要物质是硫的氧化物和氮的氧化物
B.汽车尾气中含有大量污染气体,这是汽油不完全燃烧造成的
C.水华、赤潮等水体污染主要是由含氮、磷的生活污水任意排放造成的
D.绿色化学的核心就是利用化学原理从源头上减少和消除工业生产对环境的污染
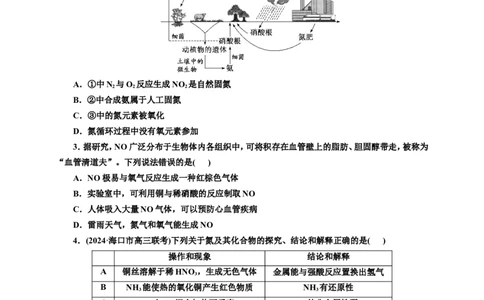
2.自然界的氮循环如图所示,下列说法正确的是( )
A.①中N 与O 反应生成NO 是自然固氮
2 2 2
B.②中合成氨属于人工固氮
C.③中的氮元素被氧化
D.氮循环过程中没有氧元素参加
3.据研究,NO广泛分布于生物体内各组织中,可将积存在血管壁上的脂肪、胆固醇带走,被称为
“血管清道夫”。下列说法错误的是( )
A.NO极易与氧气反应生成一种红棕色气体
B.实验室中,可利用铜与稀硝酸的反应制取NO
C.人体吸入大量NO气体,可以预防心血管疾病
D.雷雨天气,氮气和氧气能生成NO
4.(2024·海口市高三联考)下列关于氮及其化合物的探究、结论和解释正确的是( )
操作和现象 结论和解释
A 铜丝溶解于稀HNO ,生成无色气体 金属能与强酸反应置换出氢气
3
B NH 能使热的氧化铜产生红色物质 NH 有还原性
3 3
C N 与H 混合加热不反应 N的非金属性弱
2 2
D NO 被NaOH溶液吸收 NO 是酸性氧化物
2 2
5.汽车尾气中的氮氧化合物NO 与大气中的NH 发生如下作用,形成烟(一种雾霾)。
x 3
NO ――→NO――→HNO ――→烟
x 2 5 3
下列有关该雾霾的叙述正确的是( )
A.NO 为酸性氧化物,可形成酸雨
x
B.反应②是氧化还原反应
C.NH 是形成该雾霾的催化剂
3
D.NH 可能来自过度施用氮肥
3
6.探究氨及铵盐性质的过程中,下列根据实验现象得出的结论不正确的是( )A.将集有氨的试管倒扣于水槽中,液体迅速充满试管,说明氨极易溶于水
B.向氨水中加入浓氢氧化钠溶液,加热产生使湿润的红色石蕊试纸变蓝的气体,说明氨水中含有
NH
C.加热NH HCO 固体,观察到固体逐渐减少,试管口有液滴产生,说明NH HCO 具有热不稳定
4 3 4 3
性
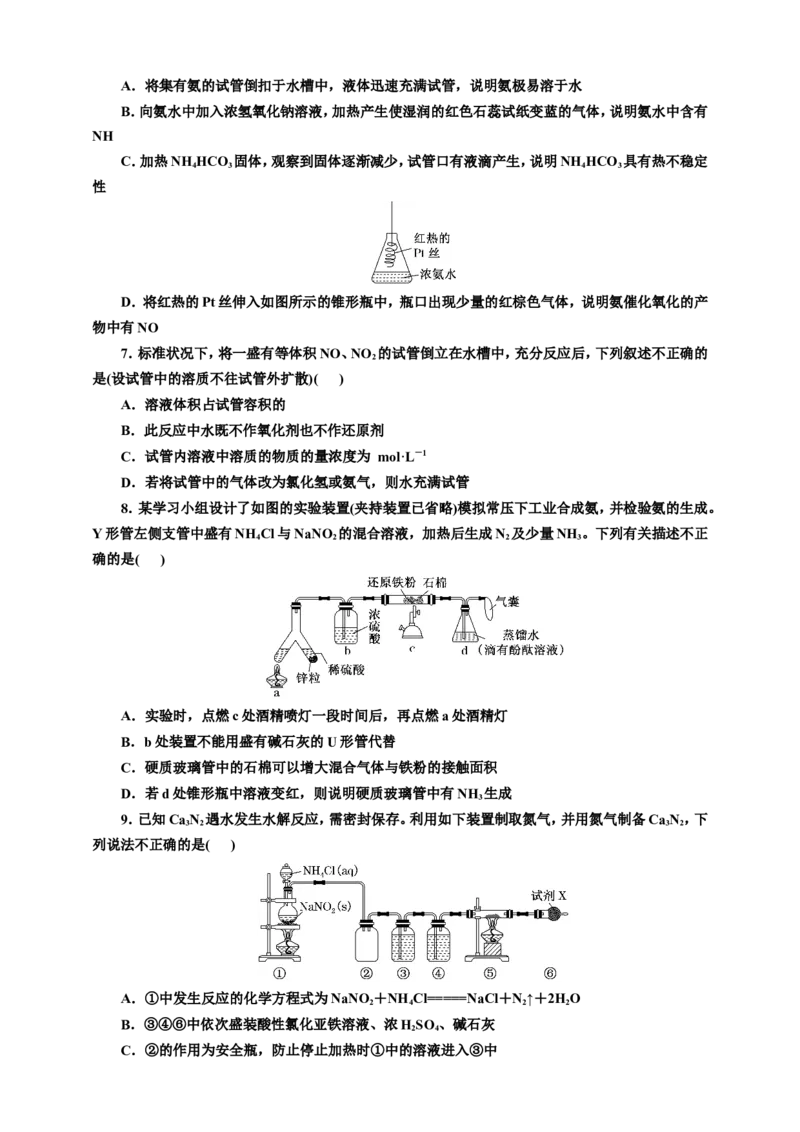
D.将红热的Pt丝伸入如图所示的锥形瓶中,瓶口出现少量的红棕色气体,说明氨催化氧化的产
物中有NO
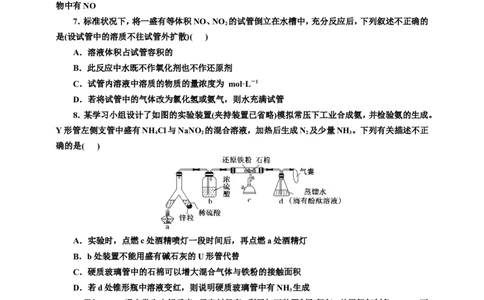
7.标准状况下,将一盛有等体积NO、NO 的试管倒立在水槽中,充分反应后,下列叙述不正确的
2
是(设试管中的溶质不往试管外扩散)( )
A.溶液体积占试管容积的
B.此反应中水既不作氧化剂也不作还原剂
C.试管内溶液中溶质的物质的量浓度为 mol·L-1
D.若将试管中的气体改为氯化氢或氨气,则水充满试管
8.某学习小组设计了如图的实验装置(夹持装置已省略)模拟常压下工业合成氨,并检验氨的生成。
Y形管左侧支管中盛有NH Cl与NaNO 的混合溶液,加热后生成N 及少量NH 。下列有关描述不正
4 2 2 3
确的是( )
A.实验时,点燃c处酒精喷灯一段时间后,再点燃a处酒精灯
B.b处装置不能用盛有碱石灰的U形管代替
C.硬质玻璃管中的石棉可以增大混合气体与铁粉的接触面积
D.若d处锥形瓶中溶液变红,则说明硬质玻璃管中有NH 生成
3
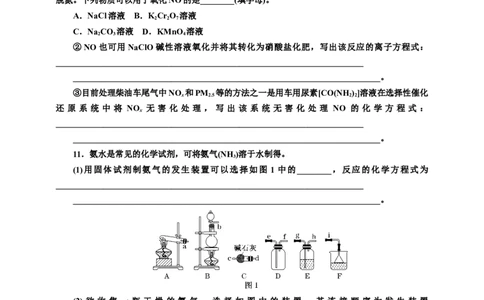
9.已知Ca N 遇水发生水解反应,需密封保存。利用如下装置制取氮气,并用氮气制备Ca N,下
3 2 3 2
列说法不正确的是( )
A.①中发生反应的化学方程式为NaNO +NH Cl=====NaCl+N↑+2HO
2 4 2 2
B.③④⑥中依次盛装酸性氯化亚铁溶液、浓HSO 、碱石灰
2 4
C.②的作用为安全瓶,防止停止加热时①中的溶液进入③中D.实验结束后,取⑤中少量产物于试管中,加适量蒸馏水,再滴加石蕊溶液,溶液变蓝
10.(2024·四川泸县二中模拟)氮和氮的化合物与人类有密切关系。
(1)下列属于氮的固定的是________(填序号)。
①工业上N 和H 合成NH
2 2 3
②N 和O 放电条件下生成NO
2 2
③NH 催化氧化生成NO
3
写出反应③的化学方程式:_____________________________________________
________________________________________________________________________。
(2)①治理NO污染通常是在氧化剂作用下,将NO氧化成溶解度高的NO ,然后用水或碱液吸收
2
脱氮。下列物质可以用于氧化NO的是________(填字母)。
A.NaCl溶液 B.KCrO 溶液
2 2 7
C.Na CO 溶液 D.KMnO 溶液
2 3 4
②NO也可用NaClO碱性溶液氧化并将其转化为硝酸盐化肥,写出该反应的离子方程式:
________________________________________________________________________
________________________________________________________________________。
③目前处理柴油车尾气中NO 和PM 等的方法之一是用车用尿素[CO(NH )]溶液在选择性催化
x 2.5 2 2
还 原 系 统 中 将 NO 无 害 化 处 理 , 写 出 该 系 统 无 害 化 处 理 NO 的 化 学 方 程 式 :
x
________________________________________________________________________
________________________________________________________________________。
11.氨水是常见的化学试剂,可将氨气(NH)溶于水制得。
3
(1)用固体试剂制氨气的发生装置可以选择如图 1 中的________,反应的化学方程式为
________________________________________________________________________
________________________________________________________________________。
(2) 欲 收 集 一 瓶 干 燥 的 氨 气 , 选 择 如 图 中 的 装 置 , 其 连 接 顺 序 为 发 生 装 置
→____________________(按气流方向,用小写字母表示)。
(3)小华为探究氨气溶于水是否发生化学反应,设计并完成如表实验(填写表中空白):
实验操作 实验现象及结论
将浸有酚酞溶液的滤纸干燥后,放
无明显现象
入盛有干燥氨气的集气瓶中
(4) 小 明 将 滴 有 酚 酞 的 稀 氨 水 加 热 , 观 察 到 溶 液 颜 色 变 浅 , 原 因 可 能 是
________________________________________________________________________
________________________________________________________________________。(5)为研究氨气的还原性,小兰做了以下实验:将(2)收集到的NH 充入注射器X中,硬质玻璃管Y
3
中加入少量催化剂,充入NO (两端用夹子K、K 夹好)。在一定温度如图2所示装置进行实验。
2 1 2
操作步骤 实验现象 解释原因
①Y管中 ②反应的化学方程式为
打开K,推动注射器活塞,
1
__________________ ____________________
使X中的气体缓慢充入Y管中
________________ ____________________
将注射器活塞退回原处并固定,
Y管中有少量水珠 生成的气态水凝聚
待装置恢复到室温
打开K ③__________ ④__________
2
课时检测(二十六)
1.B 汽车尾气排放的氮氧化物是在汽车发动机气缸内高温富氧环境下氮气和氧气的反应,不是
汽油不完全燃烧造成的,故B符合题意。
2.B ①中N 与O 反应生成NO是自然固氮,A错误;②中N 与H 在高温、高压、催化剂条件下
2 2 2 2
反应产生NH ,属于人工固氮,B正确;③中细菌还原硝酸根中正五价的氮,生成无污染的0价的N,
3 2
所以③中氮元素化合价降低,得到电子被还原,C错误;如N 在放电条件下与O 直接化合生成无色且
2 2
不溶于水的NO气体,氧元素参与了反应,二氧化氮易与水反应生成硝酸(HNO )和NO,也有氧元素参
3
加反应,D错误。
3.C NO极易与氧气反应生成一种红棕色气体NO ,反应原理为2NO+O===2NO,A正确;实
2 2 2
验室中,可利用铜与稀硝酸反应制取NO,反应原理为3Cu+8HNO (稀)===3Cu(NO ) +2NO↑+
3 3 2
4HO,B正确;人体吸入大量NO气体,NO与血红蛋白结合,造成人中毒甚至死亡,C错误;雷雨天气,
2
氮气和氧气在放电的条件下反应生成NO,反应原理为N+O=====2NO,D正确。
2 2
4.B 铜丝溶解于稀HNO ,生成硝酸铜、NO、水,无色气体为NO,不会生成氢气,故A错误;
3
NH 能使热的氧化铜产生红色物质,原理是3CuO+2NH =====N+3Cu+3HO,说明氨气具有还原
3 3 2 2
性,故B正确;N 与H 混合,在高温、高压、催化剂的条件下反应生成氨气,没有催化剂时,反应速率
2 2
慢,生成物的含量少,但不能说明N的非金属性弱,故C错误;NO 被NaOH溶液吸收,生成硝酸钠、
2
亚硝酸钠和水,发生歧化反应,体现NO 的氧化性和还原性,没有体现酸性氧化物的性质,故D错误。
2
5.D NO 不一定为成盐氧化物,故A错误;五氧化二氮和硝酸中的氮的化合价相同,所以反应②
x
是非氧化还原反应,故B错误;氨气参与反应生成铵盐,为反应物,不是催化剂,故C错误;NH 可能来
3自过度施用氮肥,铵盐不稳定,易分解产生氨气,故D正确。
6.B 因为氨水中存在氨分子,加热氨逸出,也能使湿润的红色石蕊试纸变蓝,不能证明是铵根离
子与氢氧化钠反应产生了氨,B错误;挥发出的氨气在红热的Pt丝作催化剂条件下和O 发生反应
2
4NH +5O=====4NO+6HO,生成的NO遇到O 发生反应2NO+O===2NO,生成红棕色的NO ,
3 2 2 2 2 2 2
D正确。
7.A 将一盛有等体积NO、NO 的试管倒立在水槽中,发生的反应为3NO +HO===2HNO +
2 2 2 3
NO,水既不是氧化剂又不是还原剂,溶液体积占试管容积的×=,A错误,B正确;试管内溶液中溶质
是硝酸,设试管容积为V L,浓度为= mol·L-1,C正确;若将试管中的气体换为氯化氢或者氨气,二者
均易溶于水,因此水充满试管,D正确。
8.A 实验时,为防止氢气和氧气混合后加热爆炸,用氮气排出装置内的空气后再加热铁粉,所以
点燃a处酒精灯一段时间后,再点燃c处酒精喷灯,A项错误;b装置的作用是吸收氨气并干燥气体,
碱石灰不能吸收氨气,b处装置不能用盛有碱石灰的U形管代替,B项正确;硬质玻璃管中的石棉可增
大混合气体与铁粉的接触面积,加快反应速率,C项正确;氨气溶于水,溶液呈碱性,若d处锥形瓶中
溶液变红,则说明硬质玻璃管中有NH 生成,D项正确。
3
9.C 浓硫酸是干燥剂,可以除去氮气中的水蒸气杂质,但在除去氮气中的气体杂质时应在其他
气体杂质全部除去后再通入浓硫酸中除水蒸气杂质,否则还会引入水蒸气杂质,故③④中应依次盛装
酸性氯化亚铁溶液、浓HSO ,故B正确;②的作用为安全瓶,停止加热时可以防止③中的溶液进入①
2 4
中,故C错误;实验结束后,取⑤中少量产物于试管中,加适量蒸馏水,发生水解生成Ca(OH) 和
2
NH ,再滴加石蕊溶液,溶液变蓝,故D正确。
3
10.解析:(1)固氮是指将游离态的氮元素转化为化合态的氮元素,N 和H 合成NH 、N 和O 放电
2 2 3 2 2
条件下生成NO符合固氮的定义,故选①②;反应③NH 催化氧化生成NO和水,反应的化学方程式
3
为4NH +5O=====4NO+6HO。(2)①氧化NO需要氧化剂,NaCl溶液、Na CO 溶液均不与NO反
3 2 2 2 3
应,KCrO、KMnO 溶液具有强氧化性,可以氧化NO,故选B、D。
2 2 7 4
答案:(1)①② 4NH +5O=====4NO+6HO
3 2 2
(2)①BD ②2NO+3ClO-+2OH-===2NO+3Cl-+HO
2
③2CO(NH )+6NO===5N +2CO +4HO
2 2 2 2 2
11.解析:(1)实验室制备氨气,可以利用氯化铵和氢氧化钙固体加热反应生成,选择装置A进行,
反应的化学方程式为2NH Cl+Ca(OH) =====CaCl +2NH ↑+2HO。(2)欲收集一瓶干燥的氨气,需
4 2 2 3 2
要发生装置制备出氨气,通过碱石灰(不能用浓硫酸)吸收水蒸气,通过向下排空气法收集,剩余氨气需
要吸收并防倒吸,装置连接顺序为发生装置→d→c→f→e→i。(3)将浸有酚酞溶液的滤纸湿润后,放入
盛有干燥氨气的集气瓶中,滤纸变红,说明氨气遇水形成的溶液呈碱性。(4)小明将滴有酚酞的稀氨水
加热,观察到溶液红色变浅,原因可能是氨水不稳定受热易分解生成氨气和水,导致溶液碱性减弱,则
溶液颜色变浅。(5)将(2)收集到的NH 充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO ,
3 2
打开K,推动注射器活塞,使X中的气体缓慢充入Y管中,二氧化氮和氨气发生氧化还原反应生成氮
1
气和水,反应的化学方程式为8NH +6NO =====7N+12HO,红棕色气体颜色变浅,最后褪为无色;
3 2 2 2
该反应是气体体积减小的反应,Y管内压强降低,打开K,Z中的NaOH溶液倒吸入Y管中。
2
答案:(1)A 2NH Cl+Ca(OH) =====CaCl +2NH ↑+2HO (2)d→c→f→e→i
4 2 2 3 2
(3)将浸有酚酞溶液的滤纸湿润后,放入盛有干燥氨气的集气瓶中 滤纸变红,说明氨气遇水形成
溶液呈碱性(4)氨水不稳定,受热易分解生成氨气和水,导致溶液碱性减弱,溶液颜色变浅 (5)①红棕色气体
慢慢变浅,最后褪为无色
②8NH +6NO =====7N+12HO
3 2 2 2
③Z中的NaOH溶液倒吸入Y管中
④该反应是气体体积减小的反应,Y管内压强降低,在大气压的作用下发生倒吸