文档内容
课时检测(二十八) 以气体制备为主体的实验探究
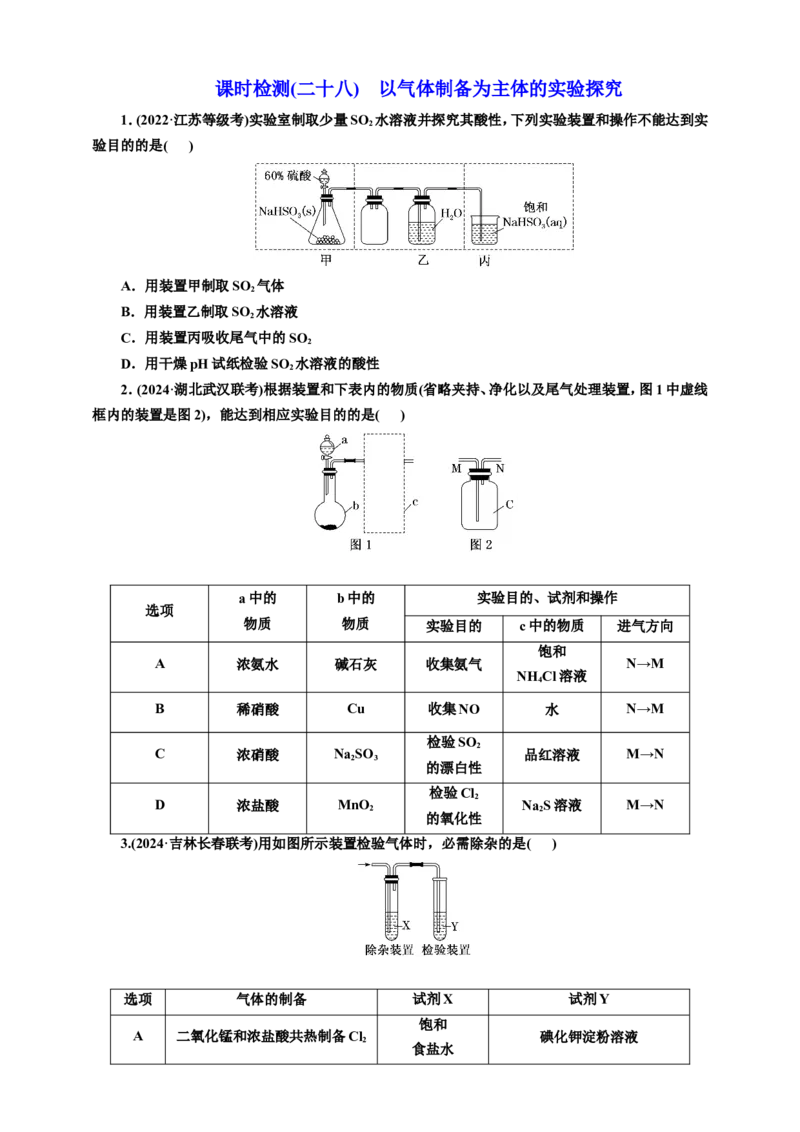
1.(2022·江苏等级考)实验室制取少量SO 水溶液并探究其酸性,下列实验装置和操作不能达到实
2
验目的的是( )
A.用装置甲制取SO 气体
2
B.用装置乙制取SO 水溶液
2
C.用装置丙吸收尾气中的SO
2
D.用干燥pH试纸检验SO 水溶液的酸性
2
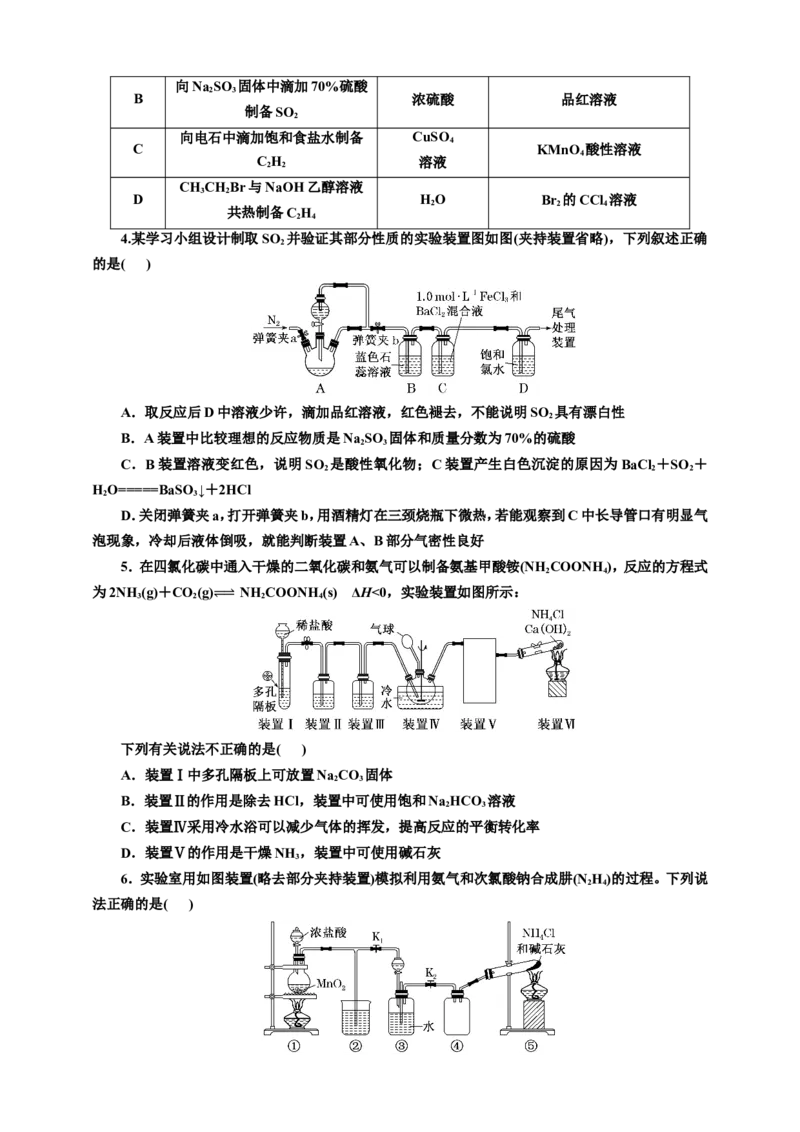
2.(2024·湖北武汉联考)根据装置和下表内的物质(省略夹持、净化以及尾气处理装置,图1中虚线
框内的装置是图2),能达到相应实验目的的是( )
a中的 b中的 实验目的、试剂和操作
选项
物质 物质 实验目的 c中的物质 进气方向
饱和
A 浓氨水 碱石灰 收集氨气 N→M
NH Cl溶液
4
B 稀硝酸 Cu 收集NO 水 N→M
检验SO
2
C 浓硝酸 Na SO 品红溶液 M→N
2 3
的漂白性
检验Cl
2
D 浓盐酸 MnO Na S溶液 M→N
2 2
的氧化性
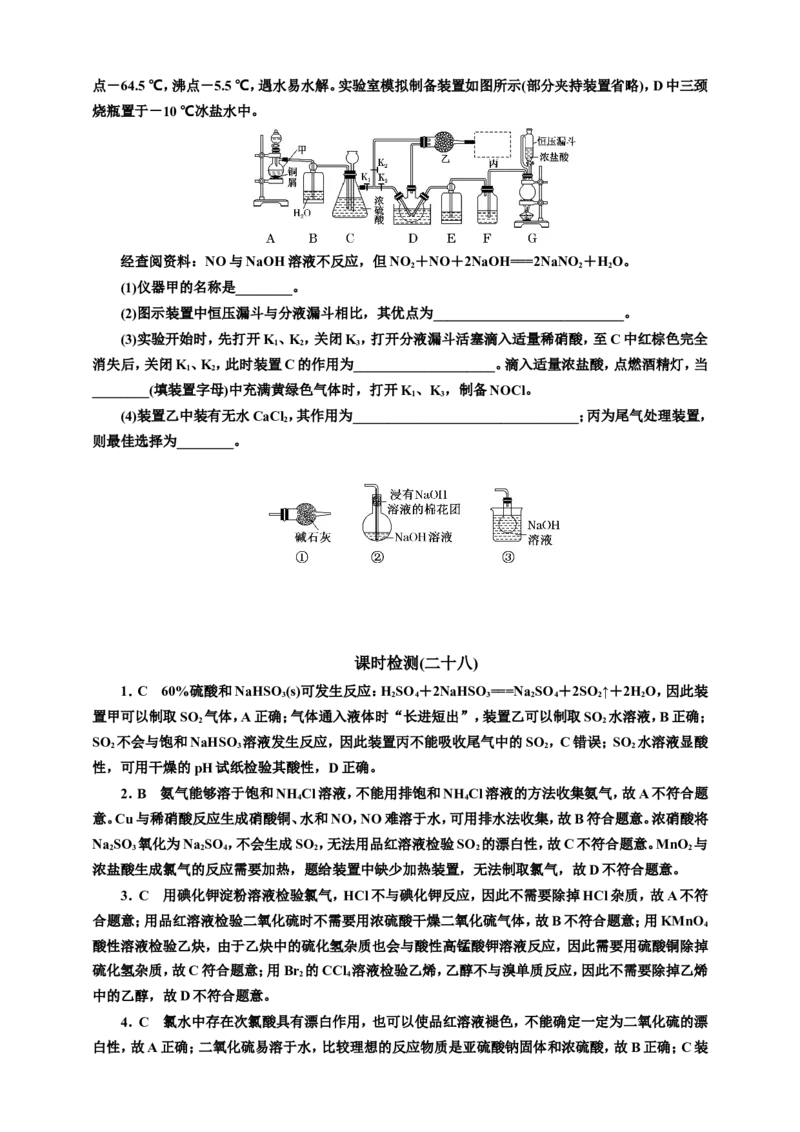
3.(2024·吉林长春联考)用如图所示装置检验气体时,必需除杂的是( )
选项 气体的制备 试剂X 试剂Y
饱和
A 二氧化锰和浓盐酸共热制备Cl 碘化钾淀粉溶液
2
食盐水向Na SO 固体中滴加70%硫酸
2 3
B 浓硫酸 品红溶液
制备SO
2
向电石中滴加饱和食盐水制备 CuSO
4
C KMnO 酸性溶液
4
CH 溶液
2 2
CH CH Br与NaOH乙醇溶液
3 2
D HO Br 的CCl 溶液
2 2 4
共热制备CH
2 4
4.某学习小组设计制取SO 并验证其部分性质的实验装置图如图(夹持装置省略),下列叙述正确
2
的是( )
A.取反应后D中溶液少许,滴加品红溶液,红色褪去,不能说明SO 具有漂白性
2
B.A装置中比较理想的反应物质是Na SO 固体和质量分数为70%的硫酸
2 3
C.B装置溶液变红色,说明SO 是酸性氧化物;C装置产生白色沉淀的原因为BaCl +SO +
2 2 2
HO=====BaSO ↓+2HCl
2 3
D.关闭弹簧夹a,打开弹簧夹b,用酒精灯在三颈烧瓶下微热,若能观察到C中长导管口有明显气
泡现象,冷却后液体倒吸,就能判断装置A、B部分气密性良好
5.在四氯化碳中通入干燥的二氧化碳和氨气可以制备氨基甲酸铵(NHCOONH ),反应的方程式
2 4
为2NH (g)+CO (g) NH COONH (s) ΔH<0,实验装置如图所示:
3 2 2 4
⥫⥬
下列有关说法不正确的是( )
A.装置Ⅰ中多孔隔板上可放置Na CO 固体
2 3
B.装置Ⅱ的作用是除去HCl,装置中可使用饱和Na HCO 溶液
2 3
C.装置Ⅳ采用冷水浴可以减少气体的挥发,提高反应的平衡转化率
D.装置Ⅴ的作用是干燥NH ,装置中可使用碱石灰
3
6.实验室用如图装置(略去部分夹持装置)模拟利用氨气和次氯酸钠合成肼(N H)的过程。下列说
2 4
法正确的是( )A.将装置①中浓盐酸换成稀盐酸,反应仍可进行
B.②中盛装NaOH溶液,用于吸收多余的Cl
2
C.③分液漏斗中盛装饱和食盐水
D.当反应结束时,④中可收集一瓶纯净的NH
3
7.ClO 是一种极易溶于水且几乎不与冷水反应的黄绿色气体(沸点11 ℃),实验室制备纯净ClO
2 2
溶液的装置如图所示:
已知下列反应:NaClO +HCl→NaCl+ClO +Cl +HO;NaClO +HCl→NaCl+ClO +HO;
3 2 2 2 2 2 2
NaClO +Cl →NaCl+ClO (均未配平)。下列说法正确的是( )
2 2 2
A.a中通入的N 可用CO 或SO 代替
2 2 2
B.b中NaClO 可用饱和食盐水代替
2
C.c中广口瓶最好放在冰水浴中冷却
D.d中吸收尾气后只生成一种盐
8.实验室常用的几种气体发生装置如图A、B、C所示:
(1)实验室可以用B或C装置制取氧气:
①如果用B装置,通常使用的试剂是_______________________________________
_____________________;如果用C装置,通常使用的试剂是_________________。
②检查B装置气密性的操作方法是________________________________________
________________________________________________________________________。
(2)气体的性质是气体收集方法选择的主要依据。下列性质与收集方法无关的是________(填字母)。
a.密度 b.颜色 c.溶解性
d.热稳定性 e.与氧气反应
(3)若用A装置与D装置相连制取并收集X气体,则X可能是下列气体中的________。
a.CO b.H c.Cl
2 2 2
①写出A装置中发生反应的离子方程式:_________________________________
________________________________________________________________________。
②D装置中烧杯中应盛放_____________,目的是_______________。
③若要收集干燥纯净的X气体,上述装置应如何改进:_______________________
________________________________________________________________________。
9.亚硝酰氯(NOCl)是有机合成中重要试剂,可由NO与Cl 在常温常压(或稍低温度)下合成,其熔
2点-64.5 ℃,沸点-5.5 ℃,遇水易水解。实验室模拟制备装置如图所示(部分夹持装置省略),D中三颈
烧瓶置于-10 ℃冰盐水中。
经查阅资料:NO与NaOH溶液不反应,但NO +NO+2NaOH===2NaNO +HO。
2 2 2
(1)仪器甲的名称是________。
(2)图示装置中恒压漏斗与分液漏斗相比,其优点为___________________________。
(3)实验开始时,先打开K、K,关闭K,打开分液漏斗活塞滴入适量稀硝酸,至C中红棕色完全
1 2 3
消失后,关闭K、K,此时装置C的作用为____________________。滴入适量浓盐酸,点燃酒精灯,当
1 2
________(填装置字母)中充满黄绿色气体时,打开K、K,制备NOCl。
1 3
(4)装置乙中装有无水CaCl ,其作用为________________________________;丙为尾气处理装置,
2
则最佳选择为________。
课时检测(二十八)
1.C 60%硫酸和NaHSO (s)可发生反应:HSO +2NaHSO ===Na SO +2SO ↑+2HO,因此装
3 2 4 3 2 4 2 2
置甲可以制取SO 气体,A正确;气体通入液体时“长进短出”,装置乙可以制取SO 水溶液,B正确;
2 2
SO 不会与饱和NaHSO 溶液发生反应,因此装置丙不能吸收尾气中的SO ,C错误;SO 水溶液显酸
2 3 2 2
性,可用干燥的pH试纸检验其酸性,D正确。
2.B 氨气能够溶于饱和NH Cl溶液,不能用排饱和NH Cl溶液的方法收集氨气,故A不符合题
4 4
意。Cu与稀硝酸反应生成硝酸铜、水和NO,NO难溶于水,可用排水法收集,故B符合题意。浓硝酸将
Na SO 氧化为Na SO ,不会生成SO ,无法用品红溶液检验SO 的漂白性,故C不符合题意。MnO 与
2 3 2 4 2 2 2
浓盐酸生成氯气的反应需要加热,题给装置中缺少加热装置,无法制取氯气,故D不符合题意。
3.C 用碘化钾淀粉溶液检验氯气,HCl不与碘化钾反应,因此不需要除掉HCl杂质,故A不符
合题意;用品红溶液检验二氧化硫时不需要用浓硫酸干燥二氧化硫气体,故B不符合题意;用KMnO
4
酸性溶液检验乙炔,由于乙炔中的硫化氢杂质也会与酸性高锰酸钾溶液反应,因此需要用硫酸铜除掉
硫化氢杂质,故C符合题意;用Br 的CCl 溶液检验乙烯,乙醇不与溴单质反应,因此不需要除掉乙烯
2 4
中的乙醇,故D不符合题意。
4.C 氯水中存在次氯酸具有漂白作用,也可以使品红溶液褪色,不能确定一定为二氧化硫的漂
白性,故A正确;二氧化硫易溶于水,比较理想的反应物质是亚硫酸钠固体和浓硫酸,故B正确;C装置中产生的白色沉淀为BaSO ,故C错误;D选项中检验装置中A、B两部分的气密性进行的操作正确。
4
5.A 多孔隔板上应该放置难溶性固体,而Na CO 易溶于水,所以多孔隔板上应该放置CaCO
2 3 3
固体,与稀盐酸制备CO ,A错误;装置Ⅱ的作用是除去CO 中的HCl杂质,可使用的是饱和的
2 2
NaHCO 溶液,B正确;氨气是易挥发的气体,冷水浴可以减少NH 的挥发,且反应2NH (g)+
3 3 3
CO (g)NHCOONH (s) ΔH<0为放热反应,利用冷水浴降低温度,可促使平衡向正反应方向移动,
2 2 4
从而提高反应的平衡转化率,C正确;浓硫酸与NH 可反应,所以不能用浓硫酸干燥NH ,干燥NH 用
3 3 3
装有碱石灰的干燥装置,D正确。
6.B 由题图可知,①中发生的反应为MnO +4HCl(浓)=====MnCl +Cl ↑+2HO,打开K,Cl
2 2 2 2 1 2
能和③分液漏斗中的NaOH溶液反应生成NaCl、NaClO,⑤用来制取NH ,④装置作安全瓶,能防倒
3
吸,在③中NH 和NaClO反应生成NH,发生反应ClO-+2NH ===N H+Cl-+HO,最后关闭K,
3 2 4 3 2 4 2 1
②中盛装的NaOH溶液用于吸收多余的Cl 。装置①中浓盐酸换成稀盐酸,MnO 与稀盐酸不反应,故
2 2
A错误;Cl 有毒,不能排放到环境中,则②中盛装NaOH溶液,用于吸收多余的Cl ,故B正确;③分液
2 2
漏斗中应该盛装NaOH溶液,利用Cl 与NaOH溶液反应制备NaClO,故C错误;反应结束后,关闭
2
K,多余的NH 可收集在④中,但两导管无“短进长出”而气体不纯,故D错误。
2 3
7.C a中通入N 的目的是将a中产生的ClO 和Cl 吹出并进入后续装置,继续实验,二氧化硫
2 2 2
具有还原性,可将ClO 、NaClO 等物质还原,故A错误;b中NaClO 的作用是吸收ClO 中混有的氯
2 3 2 2
气和氯化氢杂质气体,用饱和食盐水可吸收氯化氢,但不能吸收氯气,故B错误;ClO 是一种极易溶于
2
水且几乎不与冷水反应的黄绿色气体,故c中广口瓶最好放在冰水浴中冷却,有利于吸收ClO ,故C
2
正确;d中氢氧化钠和ClO 发生歧化反应生成NaCl和NaClO ,产物至少两种盐,故D错误。
2 3
8.解析:(1)①如果用B装置,实验室制取氧气常用高锰酸钾或氯酸钾与二氧化锰在加热条件下分
解制备氧气;如果用C装置,反应不需要加热,则可以用过氧化氢溶液在二氧化锰作催化剂条件下分
解制备氧气。(2)收集气体方法的选择可依据气体的密度、溶解性、是否与氧气反应,如气体与氧气反应
则只能用排水法收集,气体是否有颜色、气体热稳定性与收集方法无关。(3)A与D连接是利用向上排
空气法收集气体;吸收装置是用液体吸收气体防止污染空气;制取CO 时不需要加热也不必处理尾气
2
H 不能用向上排空气法收集,且尾气处理时一般采用点燃的方法,故X可能是Cl 。①A装置中二氧
2 2
化锰和浓盐酸加热反应生成氯气、氯化锰和水。②D装置中连接烧杯的目的是用来吸收尾气,防止污
染空气,实验室一般用NaOH溶液吸收多余的Cl 。③生成的氯气中含氯化氢气体和水蒸气,通过饱和
2
食盐水除去HCl,通过浓硫酸除去水蒸气,若要收集干燥纯净的Cl ,装置应在盛有浓硫酸的洗气瓶前
2
加一个装有饱和NaCl溶液的洗气瓶。
答案:(1)①氯酸钾和二氧化锰(或高锰酸钾) 过氧化氢溶液和二氧化锰 ②连接一段导气管并将
其插入水中,用酒精灯微热(或用手捂住)试管,如果导管口有气泡产生,松开手或停止加热,冷却后,在
导管里回升一段水柱,且保持一段时间不下降,则说明B装置气密性良好 (2)bd (3)c
①MnO +4H++2Cl-=====Mn2++Cl ↑+2HO
2 2 2
②NaOH溶液 吸收尾气Cl ,防止污染空气
2
③在盛有浓硫酸的洗气瓶前加一个装有饱和NaCl溶液的洗气瓶
9.解析:(1)由题图可知,仪器甲的名称是蒸馏烧瓶。(2)图示装置中的恒压分液漏斗,可以平衡分
液漏斗内外压强,便于液体顺利流下。(3)关闭K、K,A中依然产生NO气体,故此时C可以作为安全
1 2
瓶,储存A中产生的NO气体;滴入适量浓盐酸,点燃酒精灯,当D中充满黄绿色气体时,打开K、K,
1 3
制备NOCl。(4)亚硝酰氯(NOCl)遇水发生水解反应,装置乙中无水氯化钙可以吸收水蒸气,防止水蒸气进入D中使NOCl水解,丙为尾气处理装置,尾气主要为NO、Cl 和NOCl、NO ,故在尾气吸收时可
2 2
以选用NaOH溶液,同时为了防止NOCl和NO 挥发逸出,可以在上方加一个浸有NaOH溶液的棉花
2
团,①中碱石灰固体不能吸收NOCl和NO气体,③中不能避免挥发出来的气体污染空气,则最佳选择
为②。
答案:(1)蒸馏烧瓶 (2)平衡压强,便于液体顺利流下
(3)储存A中产生的NO D (4)防止水蒸气进入D,使NOCl水解 ②