文档内容
课时检测(二十) 氯及其化合物的基本知能评价
1.下列关于氯及其化合物的性质与用途具有对应关系的是( )
A.Cl 易液化,可用于生产盐酸
2
B.ClO 有强氧化性,可用于自来水消毒
2
C.CCl 难溶于水,可用作灭火剂
4
D.HCl极易溶于水,可用于检验NH
3
2.有关Cl 的性质,下列说法不正确的是( )
2
A.Cl 在通常状况下呈黄绿色、液氯具有漂白性
2
B.能与NaOH溶液反应
C.铁丝在Cl 中燃烧,反应不生成FeCl
2 2
D.H 在Cl 中燃烧,产生苍白色火焰
2 2
3.(2023·江苏南通市三模)NaClO是家用消毒液的有效成分,这是利用了NaClO的( )
A.碱性 B.强氧化性
C.还原性 D.受热后不稳定性
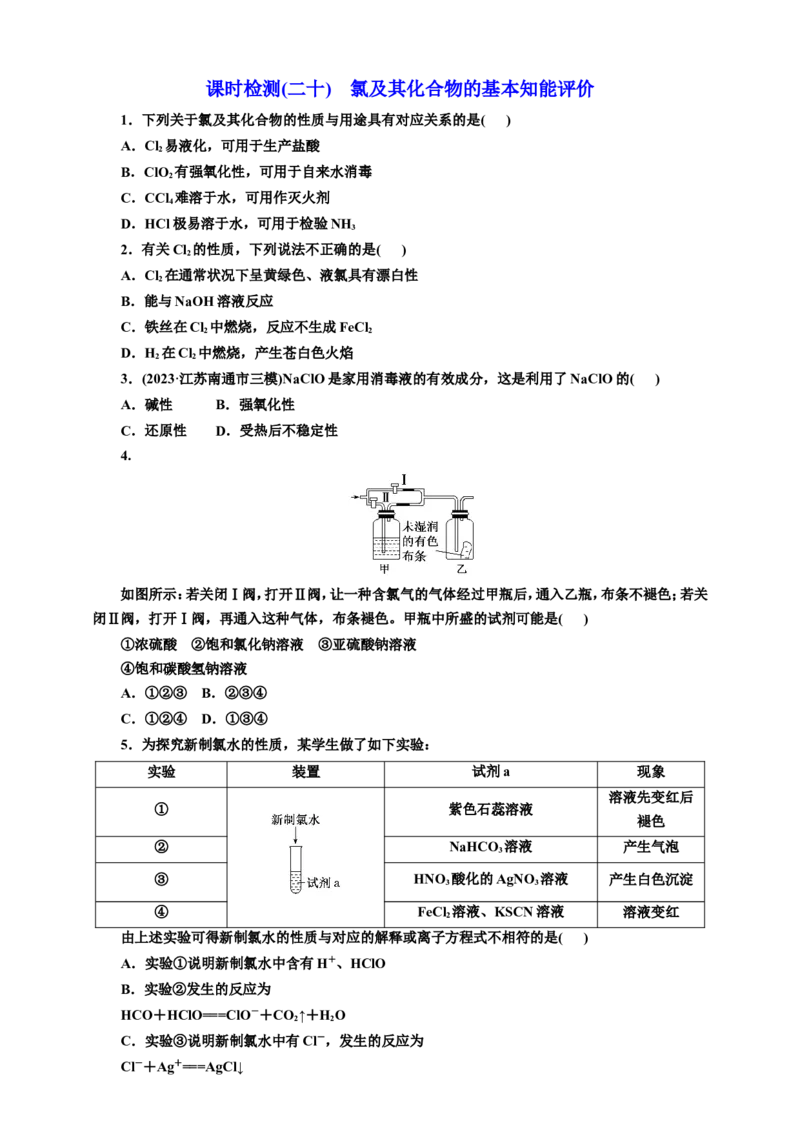
4.
如图所示:若关闭Ⅰ阀,打开Ⅱ阀,让一种含氯气的气体经过甲瓶后,通入乙瓶,布条不褪色;若关
闭Ⅱ阀,打开Ⅰ阀,再通入这种气体,布条褪色。甲瓶中所盛的试剂可能是( )
①浓硫酸 ②饱和氯化钠溶液 ③亚硫酸钠溶液
④饱和碳酸氢钠溶液
A.①②③ B.②③④
C.①②④ D.①③④
5.为探究新制氯水的性质,某学生做了如下实验:
实验 装置 试剂a 现象
溶液先变红后
① 紫色石蕊溶液
褪色
② NaHCO 溶液 产生气泡
3
③ HNO 酸化的AgNO 溶液 产生白色沉淀
3 3
④ FeCl 溶液、KSCN溶液 溶液变红
2
由上述实验可得新制氯水的性质与对应的解释或离子方程式不相符的是( )
A.实验①说明新制氯水中含有H+、HClO
B.实验②发生的反应为
HCO+HClO===ClO-+CO ↑+HO
2 2
C.实验③说明新制氯水中有Cl-,发生的反应为
Cl-+Ag+===AgCl↓D.实验④说明氯气具有强氧化性,发生的反应为
Cl +2Fe2+===2Cl-+2Fe3+
2
6.(2023·广州市三模)某溶液的主要成分为NaClO(含有一定量的NaOH),既能杀菌消毒又能漂白。
下列用来解释事实的离子方程式不正确的是( )
A.该溶液可用NaOH溶液吸收Cl 制备:
2
Cl +2OH-===Cl-+ClO-+HO
2 2
B.该溶液与洁厕灵(主要成分为HCl)混合产生Cl :
2
2H++Cl-+ClO-===Cl↑+HO
2 2
C.该溶液与过氧化氢溶液混合产生O:
2
2ClO-+HO===2Cl-+O↑+2OH-
2 2 2
D.该溶液加白醋可增强漂白作用:
CH COOH+ClO-===HClO+CH COO-
3 3
7.在新制饱和氯水中,若只改变某一条件,下列叙述正确的是( )
A.再通入少量氯气,减小
B.通入少量SO ,溶液漂白性增强
2
C.加入少量的碳酸钠粉末,pH增大,溶液漂白性增强
D.光照过程中,有气泡冒出,溶液的导电性减弱
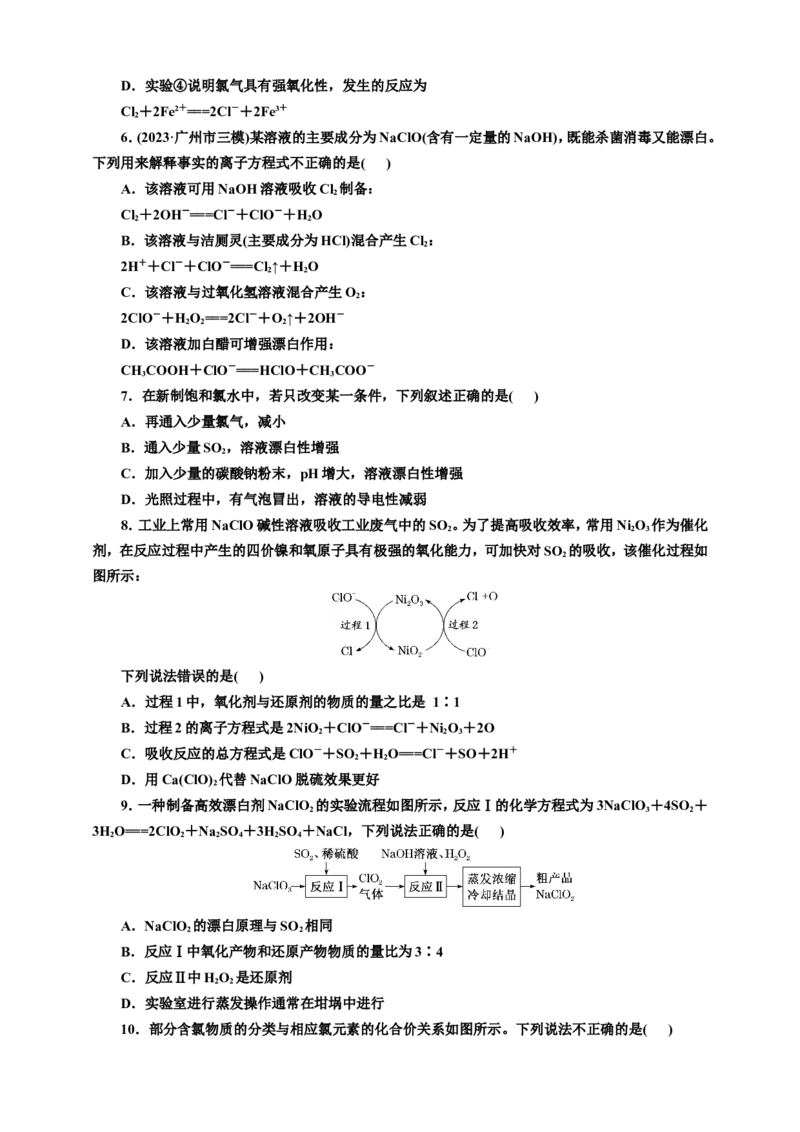
8.工业上常用NaClO碱性溶液吸收工业废气中的SO 。为了提高吸收效率,常用Ni O 作为催化
2 2 3
剂,在反应过程中产生的四价镍和氧原子具有极强的氧化能力,可加快对SO 的吸收,该催化过程如
2
图所示:
下列说法错误的是( )
A.过程1中,氧化剂与还原剂的物质的量之比是 1∶1
B.过程2的离子方程式是2NiO +ClO-===Cl-+Ni O+2O
2 2 3
C.吸收反应的总方程式是ClO-+SO +HO===Cl-+SO+2H+
2 2
D.用Ca(ClO) 代替NaClO脱硫效果更好
2
9.一种制备高效漂白剂NaClO 的实验流程如图所示,反应Ⅰ的化学方程式为3NaClO +4SO +
2 3 2
3HO===2ClO +Na SO +3HSO +NaCl,下列说法正确的是( )
2 2 2 4 2 4
A.NaClO 的漂白原理与SO 相同
2 2
B.反应Ⅰ中氧化产物和还原产物物质的量比为3∶4
C.反应Ⅱ中HO 是还原剂
2 2
D.实验室进行蒸发操作通常在坩埚中进行
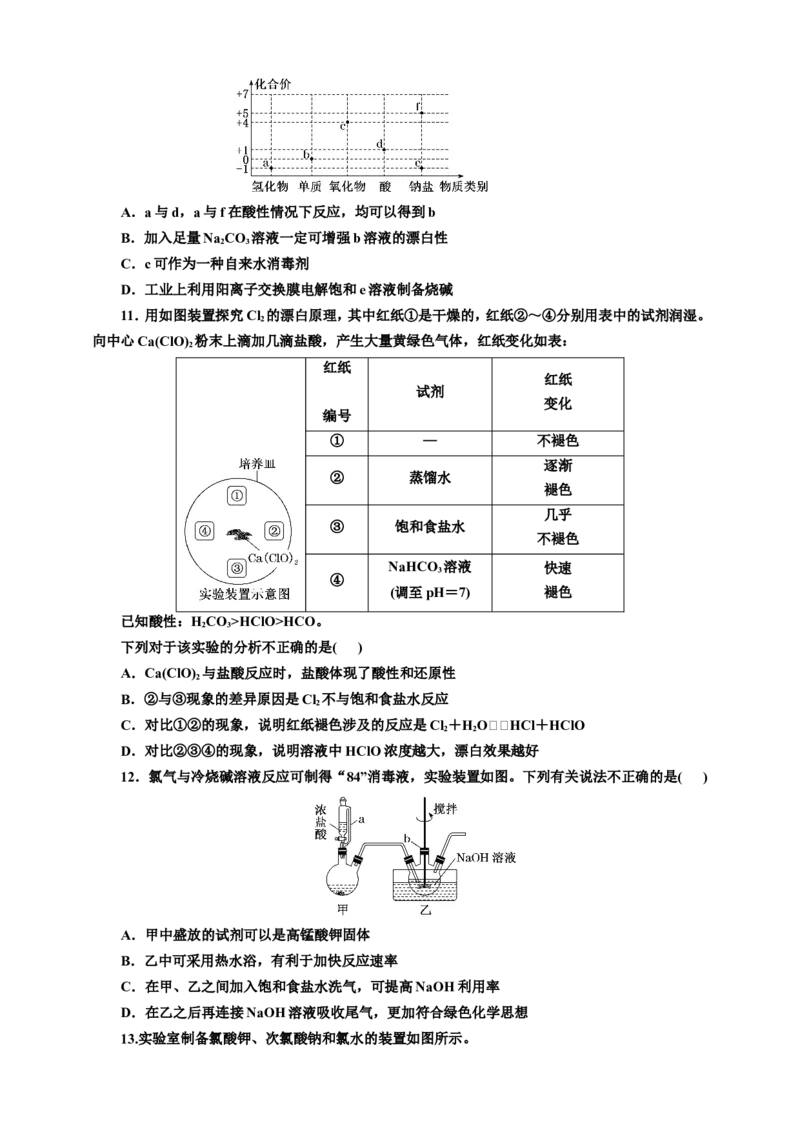
10.部分含氯物质的分类与相应氯元素的化合价关系如图所示。下列说法不正确的是( )A.a与d,a与f在酸性情况下反应,均可以得到b
B.加入足量Na CO 溶液一定可增强b溶液的漂白性
2 3
C.c可作为一种自来水消毒剂
D.工业上利用阳离子交换膜电解饱和e溶液制备烧碱
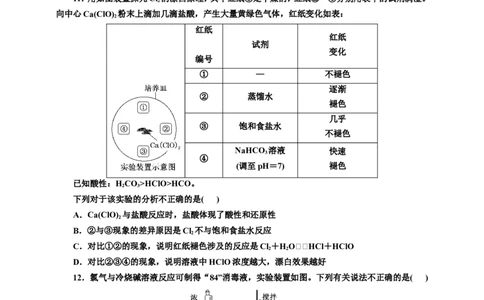
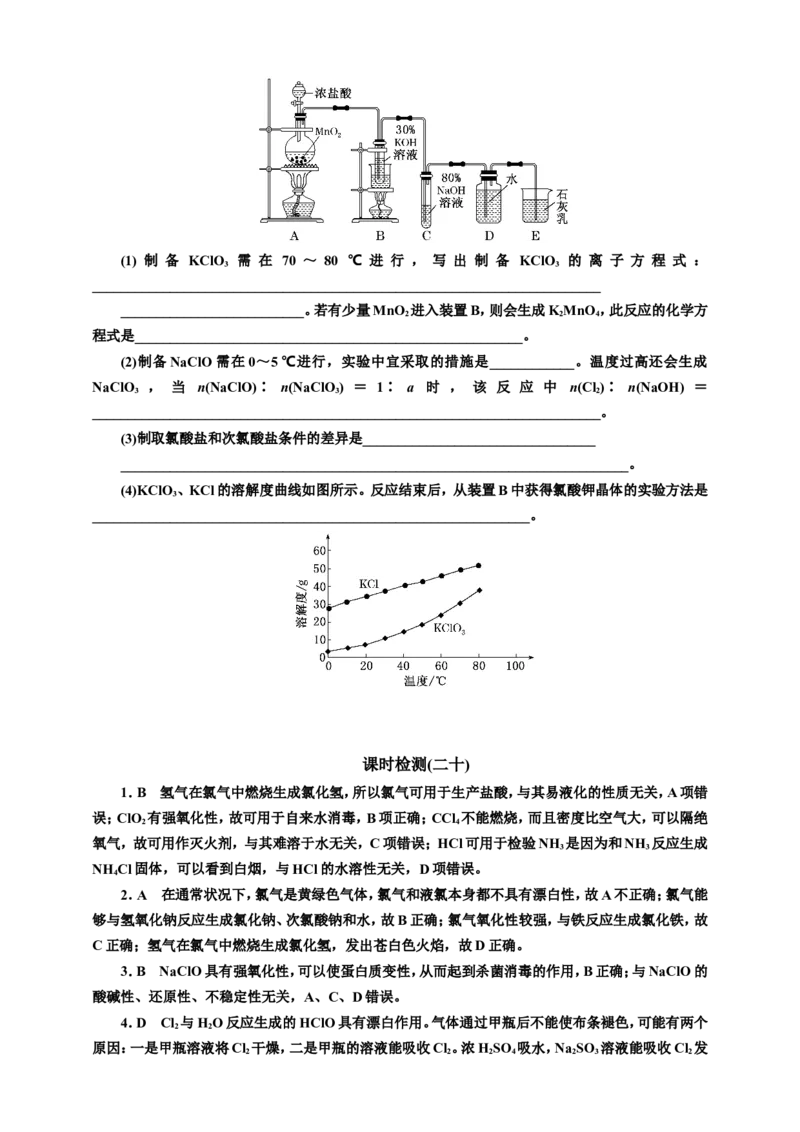
11.用如图装置探究Cl 的漂白原理,其中红纸①是干燥的,红纸②~④分别用表中的试剂润湿。
2
向中心Ca(ClO) 粉末上滴加几滴盐酸,产生大量黄绿色气体,红纸变化如表:
2
红纸
红纸
试剂
变化
编号
① — 不褪色
逐渐
② 蒸馏水
褪色
几乎
③ 饱和食盐水
不褪色
NaHCO 溶液 快速
3
④
(调至pH=7) 褪色
已知酸性:HCO >HClO>HCO。
2 3
下列对于该实验的分析不正确的是( )
A.Ca(ClO) 与盐酸反应时,盐酸体现了酸性和还原性
2
B.②与③现象的差异原因是Cl 不与饱和食盐水反应
2
C.对比①②的现象,说明红纸褪色涉及的反应是Cl +HOHCl+HClO
2 2
D.对比②③④的现象,说明溶液中HClO浓度越大,漂白效果越好
12.氯气与冷烧碱溶液反应可制得“84”消毒液,实验装置如图。下列有关说法不正确的是( )
A.甲中盛放的试剂可以是高锰酸钾固体
B.乙中可采用热水浴,有利于加快反应速率
C.在甲、乙之间加入饱和食盐水洗气,可提高NaOH利用率
D.在乙之后再连接NaOH溶液吸收尾气,更加符合绿色化学思想
13.实验室制备氯酸钾、次氯酸钠和氯水的装置如图所示。(1) 制 备 KClO 需 在 70 ~ 80 ℃ 进 行 , 写 出 制 备 KClO 的 离 子 方 程 式 :
3 3
________________________________________________________________________
__________________________。若有少量MnO 进入装置B,则会生成KMnO ,此反应的化学方
2 2 4
程式是_______________________________________________________。
(2)制备NaClO需在0~5 ℃进行,实验中宜采取的措施是____________。温度过高还会生成
NaClO , 当 n(NaClO)∶ n(NaClO ) = 1∶ a 时 , 该 反 应 中 n(Cl)∶ n(NaOH) =
3 3 2
________________________________________________________________________。
(3)制取氯酸盐和次氯酸盐条件的差异是_________________________________
________________________________________________________________________。
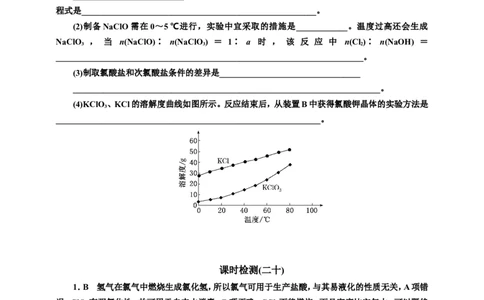
(4)KClO 、KCl的溶解度曲线如图所示。反应结束后,从装置B中获得氯酸钾晶体的实验方法是
3
______________________________________________________________。
课时检测(二十)
1.B 氢气在氯气中燃烧生成氯化氢,所以氯气可用于生产盐酸,与其易液化的性质无关,A项错
误;ClO 有强氧化性,故可用于自来水消毒,B项正确;CCl 不能燃烧,而且密度比空气大,可以隔绝
2 4
氧气,故可用作灭火剂,与其难溶于水无关,C项错误;HCl可用于检验NH 是因为和NH 反应生成
3 3
NH Cl固体,可以看到白烟,与HCl的水溶性无关,D项错误。
4
2.A 在通常状况下,氯气是黄绿色气体,氯气和液氯本身都不具有漂白性,故A不正确;氯气能
够与氢氧化钠反应生成氯化钠、次氯酸钠和水,故B正确;氯气氧化性较强,与铁反应生成氯化铁,故
C正确;氢气在氯气中燃烧生成氯化氢,发出苍白色火焰,故D正确。
3.B NaClO具有强氧化性,可以使蛋白质变性,从而起到杀菌消毒的作用,B正确;与NaClO的
酸碱性、还原性、不稳定性无关,A、C、D错误。
4.D Cl 与HO反应生成的HClO具有漂白作用。气体通过甲瓶后不能使布条褪色,可能有两个
2 2
原因:一是甲瓶溶液将Cl 干燥,二是甲瓶的溶液能吸收Cl 。浓HSO 吸水,Na SO 溶液能吸收Cl 发
2 2 2 4 2 3 2生氧化还原反应,饱和NaHCO 溶液能与Cl 发生反应生成CO 。
3 2 2
5.B 紫色石蕊溶液先变红,说明有H+存在,后褪色,说明有HClO存在,A正确;碳酸的酸性比
HClO的酸性强,根据强酸制弱酸原理,正确的离子方程式为HCO+H+===CO↑+HO,B错误;新制
2 2
氯水中有Cl-,和银离子反应生成白色沉淀,C正确;Cl 具有强氧化性,可以氧化亚铁离子,D正确。
2
6.C 该溶液与过氧化氢溶液混合产生O ClO-+HO===Cl-+O↑+ HO,C错误。
2: 2 2 2 2
7.C 饱和氯水不能再溶解氯气,各成分的浓度不变,A项错误;通入少量SO ,发生反应SO +
2 2
Cl +2HO===2HCl+HSO ,Cl +HOH++Cl-+HClO的平衡左移,HClO的浓度减小,漂白性
2 2 2 4 2 2
减弱,B项错误;加入少量的碳酸钠粉末,消耗H+,使平衡正向移动,HClO的浓度增大,C项正确;光
照过程中,HClO分解,生成O 和HCl,溶液中的离子浓度增大,导电性增强,D项错误。
2
8.C 过程1中,ClO-转化为Cl-,Cl元素化合价降低,ClO-作氧化剂,Ni O 转化为NiO ,Ni元
2 3 2
素化合价升高,Ni O 作还原剂,根据得失电子守恒可得,氧化剂与还原剂的物质的量之比是1∶1,A
2 3
项正确;过程2中,NiO 和ClO-反应生成Ni O 、Cl-和O,离子方程式为2NiO +ClO-===Cl-+
2 2 3 2
Ni O+2O,B项正确;用NaClO 碱性溶液吸收工业废气中的SO ,离子方程式为ClO-+SO +2OH-
2 3 2 2
===Cl-+SO+HO,C项错误;Ca2+与SO结合生成微溶的CaSO ,有利于反应的进行,因此用
2 4
Ca(ClO) 代替NaClO脱硫效果更好,D项正确。
2
9.C NaClO 中氯元素的化合价为+3价,该物质具有强的氧化性,因而具有漂白性,NaClO 的
2 2
漂白是氧化漂白,而SO 能与某些有色物质结合,产生不稳定的无色物质,因此NaClO 和SO 的漂白
2 2 2
原理不相同,A错误;由反应Ⅰ知,氧化产物是Na SO 和HSO ,还原产物是ClO 和NaCl,氧化产物
2 4 2 4 2
和还原产物物质的量比为4∶3,B错误;反应Ⅰ产生的ClO 气体进入反应Ⅱ装置,发生反应2ClO +
2 2
HO+2NaOH===2NaClO +O+2HO,HO 中氧元素的化合价由反应前的-1价变为反应后O 中
2 2 2 2 2 2 2 2
的0价,化合价升高,失去电子,HO 是还原剂,C正确;实验室进行结晶操作通常是在蒸发皿中进行,
2 2
坩埚是灼烧使用的仪器,D错误。
10.B 根据价类二维图可知:b、c、d分别为Cl 、ClO 、HClO,a、e、f分别为HCl、NaCl、NaClO 。
2 2 3
HCl与HClO,HCl与NaClO 在酸性情况下发生归中反应,均可以得到Cl ,A正确;Cl 的水溶液中存
3 2 2
在平衡:Cl +HOHCl+HClO,加入足量Na CO 溶液,既消耗HCl,又与HClO反应,漂白性减弱,
2 2 2 3
B错误;氯碱工业中使用阳离子交换膜,它可将阴极产生的氢氧化钠和阳极产生的氯气隔离,避免二者
发生反应,D正确。
11.B 次氯酸钙与盐酸反应的化学方程式为Ca(ClO) +4HCl===CaCl +2Cl ↑+2HO,盐酸既体现
2 2 2 2
了酸性又体现了还原性,A正确;氯气与水的反应为可逆反应,存在平衡:Cl +HO HCl+HClO,
2 2
饱和食盐水中氯离子浓度很大,促使反应逆向进行,次氯酸的量很少,所以③中红纸⥫几⥬乎不褪色,B错
误;①说明干燥氯气没有漂白性,②红纸褪色,①②说明氯水有漂白性,涉及的反应为Cl +HO
2 2
HCl+HClO,C正确;④中反应为Cl +HCO===CO+HClO+Cl-,④中次氯酸的浓度最大,②③⥫④⥬
2 2
中次氯酸浓度大小为④>②>③,由红纸变化可知,HClO浓度越大,漂白效果越好,D正确。
12.B A项,高锰酸钾和浓盐酸常温下反应可以制取氯气,没有加热装置,所以甲中盛放的试剂
可以是高锰酸钾固体,正确;B项,氯气与冷烧碱溶液反应可制得“84”消毒液,所以乙中不可采用热
水浴,否则会有其他反应发生,会生成杂质氯酸钠,错误;C项,在甲、乙之间加入饱和食盐水洗气,可
以除去浓盐酸挥发出来的氯化氢气体,可提高NaOH利用率,正确;D项,氯气有毒,不能随意排放到
大气中,所以在乙之后再连接NaOH溶液吸收尾气,更加符合绿色化学思想,正确。13.解析:(2)当n(NaClO)∶n(NaClO )=1∶a时,依据得失电子守恒和元素守恒,得化学方程式
3
(3a+1)Cl +(6a+2)NaOH===aNaClO +NaClO+(5a+1)NaCl+(3a+1)H O,该反应中
2 3 2
n(Cl)∶n(NaOH)=1∶2。(4)由溶解度曲线分析可知,同一温度下,KCl的溶解度比KClO 大,温度越
2 3
高溶解度越接近,故从装置B中获得氯酸钾晶体的实验方案是冷却结晶、过滤、洗涤。
答案:(1)3Cl+6OH-=====5Cl-+ClO+3HO
2 2
3MnO +KClO +6KOH===3K MnO +KCl+3HO(或Cl +4KOH+MnO ===K MnO +2KCl
2 3 2 4 2 2 2 2 4
+2HO) (2)将装置C放在冰水浴中 1∶2 (3)碱溶液(或反应物)的浓度不同,反应温度不同
2
(4)将装置B中的试管放在冰水中冷却,过滤,用少量冰水洗涤晶体2~3次