文档内容
课时检测(四十四) 新型化学电源
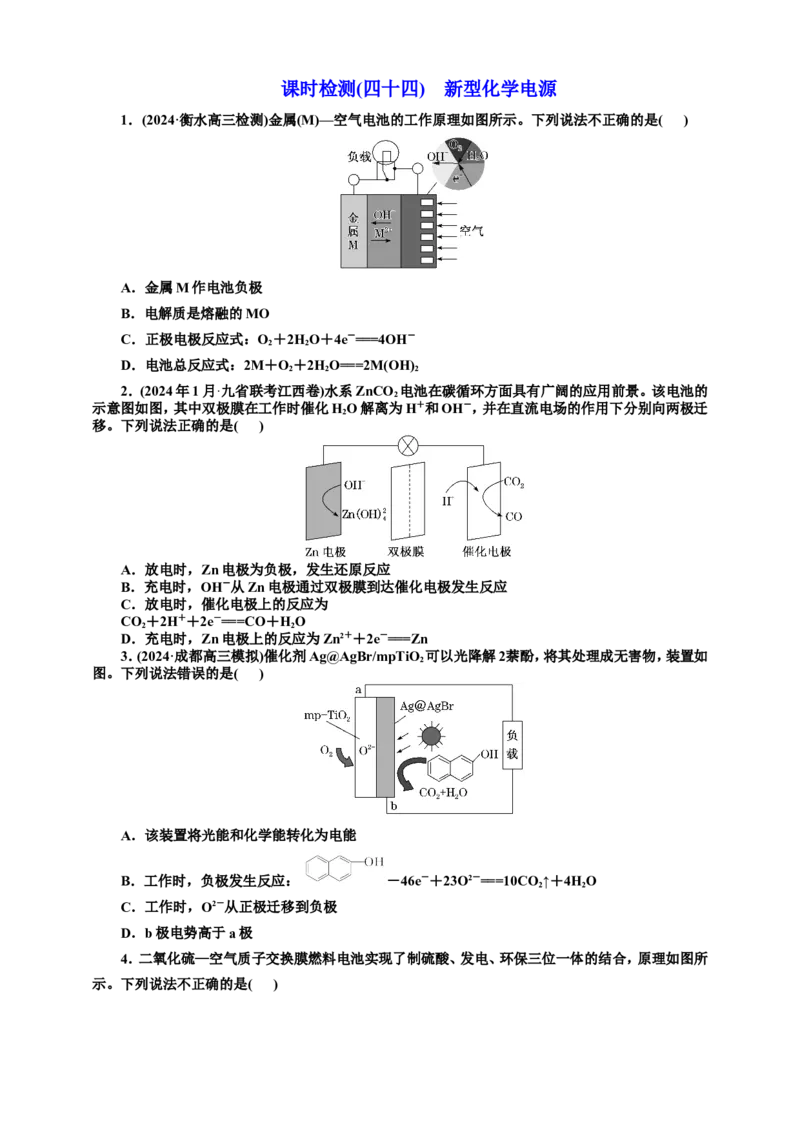
1.(2024·衡水高三检测)金属(M)—空气电池的工作原理如图所示。下列说法不正确的是( )
A.金属M作电池负极
B.电解质是熔融的MO
C.正极电极反应式:O+2HO+4e-===4OH-
2 2
D.电池总反应式:2M+O+2HO===2M(OH)
2 2 2
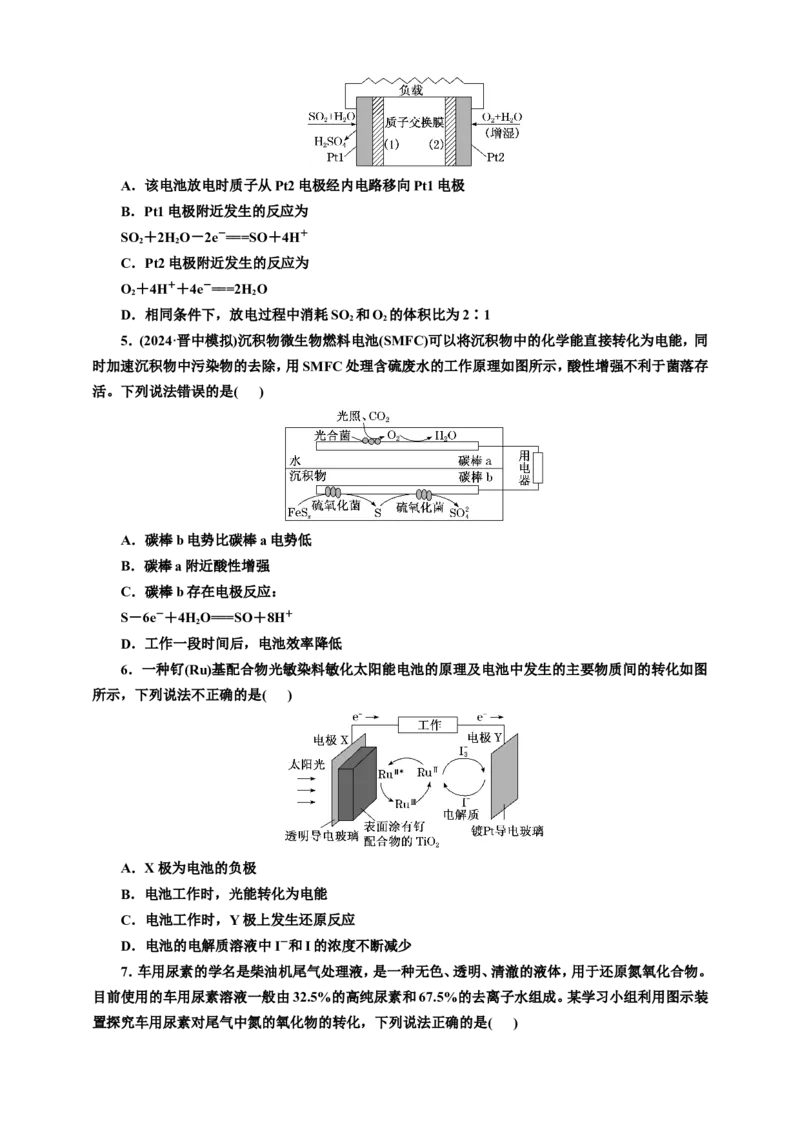
2.(2024年1月·九省联考江西卷)水系ZnCO 电池在碳循环方面具有广阔的应用前景。该电池的
2
示意图如图,其中双极膜在工作时催化HO解离为H+和OH-,并在直流电场的作用下分别向两极迁
2
移。下列说法正确的是( )
A.放电时,Zn电极为负极,发生还原反应
B.充电时,OH-从Zn电极通过双极膜到达催化电极发生反应
C.放电时,催化电极上的反应为
CO +2H++2e-===CO+HO
2 2
D.充电时,Zn电极上的反应为Zn2++2e-===Zn
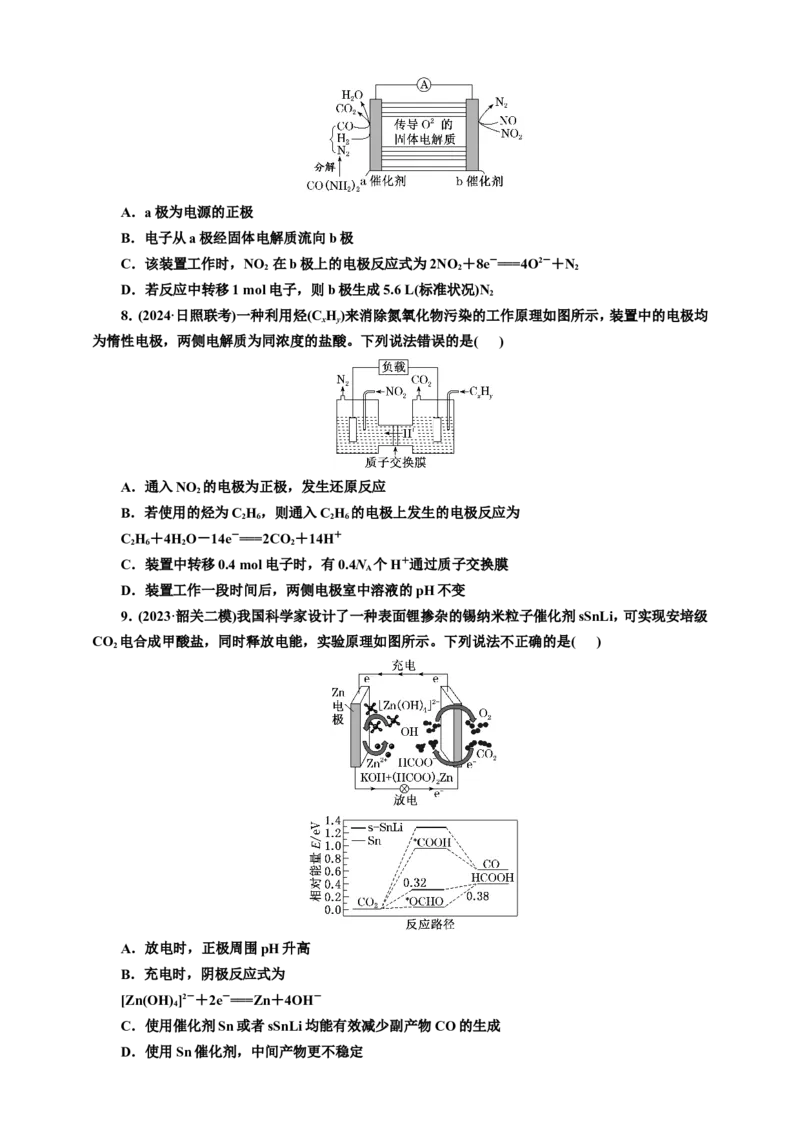
3.(2024·成都高三模拟)催化剂Ag@AgBr/mpTiO 可以光降解2萘酚,将其处理成无害物,装置如
2
图。下列说法错误的是( )
A.该装置将光能和化学能转化为电能
B.工作时,负极发生反应: -46e-+23O2-===10CO↑+4HO
2 2
C.工作时,O2-从正极迁移到负极
D.b极电势高于a极
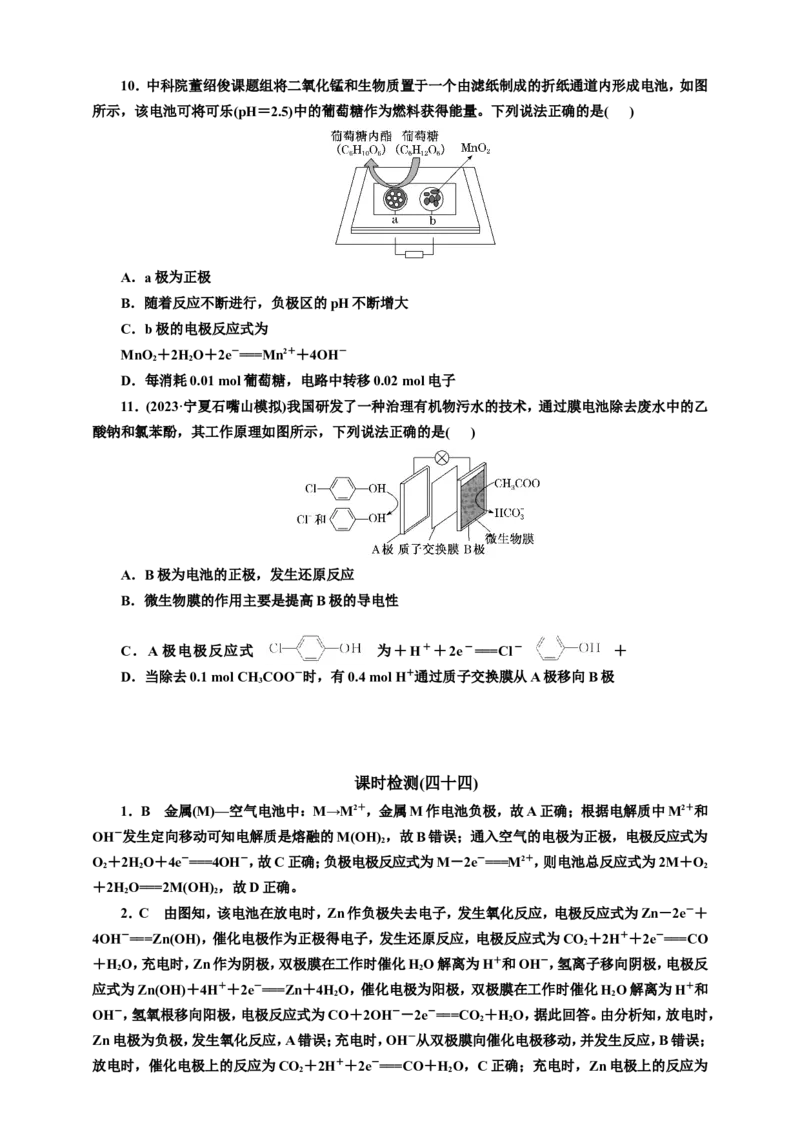
4.二氧化硫—空气质子交换膜燃料电池实现了制硫酸、发电、环保三位一体的结合,原理如图所
示。下列说法不正确的是( )A.该电池放电时质子从Pt2电极经内电路移向Pt1电极
B.Pt1电极附近发生的反应为
SO +2HO-2e-===SO+4H+
2 2
C.Pt2电极附近发生的反应为
O+4H++4e-===2H O
2 2
D.相同条件下,放电过程中消耗SO 和O 的体积比为2∶1
2 2
5.(2024·晋中模拟)沉积物微生物燃料电池(SMFC)可以将沉积物中的化学能直接转化为电能,同
时加速沉积物中污染物的去除,用SMFC处理含硫废水的工作原理如图所示,酸性增强不利于菌落存
活。下列说法错误的是( )
A.碳棒b电势比碳棒a电势低
B.碳棒a附近酸性增强
C.碳棒b存在电极反应:
S-6e-+4HO===SO+8H+
2
D.工作一段时间后,电池效率降低
6.一种钌(Ru)基配合物光敏染料敏化太阳能电池的原理及电池中发生的主要物质间的转化如图
所示,下列说法不正确的是( )
A.X极为电池的负极
B.电池工作时,光能转化为电能
C.电池工作时,Y极上发生还原反应
D.电池的电解质溶液中I-和I的浓度不断减少
7.车用尿素的学名是柴油机尾气处理液,是一种无色、透明、清澈的液体,用于还原氮氧化合物。
目前使用的车用尿素溶液一般由32.5%的高纯尿素和67.5%的去离子水组成。某学习小组利用图示装
置探究车用尿素对尾气中氮的氧化物的转化,下列说法正确的是( )A.a极为电源的正极
B.电子从a极经固体电解质流向b极
C.该装置工作时,NO 在b极上的电极反应式为2NO +8e-===4O2-+N
2 2 2
D.若反应中转移1 mol电子,则b极生成5.6 L(标准状况)N
2
8.(2024·日照联考)一种利用烃(C H)来消除氮氧化物污染的工作原理如图所示,装置中的电极均
x y
为惰性电极,两侧电解质为同浓度的盐酸。下列说法错误的是( )
A.通入NO 的电极为正极,发生还原反应
2
B.若使用的烃为CH,则通入CH 的电极上发生的电极反应为
2 6 2 6
CH+4HO-14e-===2CO+14H+
2 6 2 2
C.装置中转移0.4 mol电子时,有0.4N 个H+通过质子交换膜
A
D.装置工作一段时间后,两侧电极室中溶液的pH不变
9.(2023·韶关二模)我国科学家设计了一种表面锂掺杂的锡纳米粒子催化剂sSnLi,可实现安培级
CO 电合成甲酸盐,同时释放电能,实验原理如图所示。下列说法不正确的是( )
2
A.放电时,正极周围pH升高
B.充电时,阴极反应式为
[Zn(OH) ]2-+2e-===Zn+4OH-
4
C.使用催化剂Sn或者sSnLi均能有效减少副产物CO的生成
D.使用Sn催化剂,中间产物更不稳定10.中科院董绍俊课题组将二氧化锰和生物质置于一个由滤纸制成的折纸通道内形成电池,如图
所示,该电池可将可乐(pH=2.5)中的葡萄糖作为燃料获得能量。下列说法正确的是( )
A.a极为正极
B.随着反应不断进行,负极区的pH不断增大
C.b极的电极反应式为
MnO +2HO+2e-===Mn2++4OH-
2 2
D.每消耗0.01 mol葡萄糖,电路中转移0.02 mol电子
11.(2023·宁夏石嘴山模拟)我国研发了一种治理有机物污水的技术,通过膜电池除去废水中的乙
酸钠和氯苯酚,其工作原理如图所示,下列说法正确的是( )
A.B极为电池的正极,发生还原反应
B.微生物膜的作用主要是提高B极的导电性
C.A 极电极反应式 为+H++2e-===Cl- +
D.当除去0.1 mol CH COO-时,有0.4 mol H+通过质子交换膜从A极移向B极
3
课时检测(四十四)
1.B 金属(M)—空气电池中:M→M2+,金属M作电池负极,故A正确;根据电解质中M2+和
OH-发生定向移动可知电解质是熔融的M(OH) ,故B错误;通入空气的电极为正极,电极反应式为
2
O+2HO+4e-===4OH-,故C正确;负极电极反应式为M-2e-===M2+,则电池总反应式为2M+O
2 2 2
+2HO===2M(OH) ,故D正确。
2 2
2.C 由图知,该电池在放电时,Zn作负极失去电子,发生氧化反应,电极反应式为Zn-2e-+
4OH-===Zn(OH),催化电极作为正极得电子,发生还原反应,电极反应式为CO +2H++2e-===CO
2
+HO,充电时,Zn作为阴极,双极膜在工作时催化HO解离为H+和OH-,氢离子移向阴极,电极反
2 2
应式为Zn(OH)+4H++2e-===Zn+4HO,催化电极为阳极,双极膜在工作时催化HO解离为H+和
2 2
OH-,氢氧根移向阳极,电极反应式为CO+2OH--2e-===CO+HO,据此回答。由分析知,放电时,
2 2
Zn电极为负极,发生氧化反应,A错误;充电时,OH-从双极膜向催化电极移动,并发生反应,B错误;
放电时,催化电极上的反应为CO +2H++2e-===CO+HO,C正确;充电时,Zn电极上的反应为
2 2Zn(OH)+4H++2e-===Zn+4HO,D错误。
2
3.D 该装置为原电池,a极:O→O2-,氧元素化合价降低得电子,故a极为正极,b极为负极,a
2
极电势高于b极,D错误。
4.A 放电时为原电池,质子向正极移动,Pt1电极:SO →HSO 发生氧化反应,为负极,则该电
2 2 4
池放电时质子从Pt1电极移向Pt2电极,A错误;Pt1电极为负极,发生反应:SO +2HO-2e-===SO
2 2
+4H+,硫酸应拆为离子形式,B正确;Pt2电极为正极,电解质溶液呈酸性,故电极反应为O+4e-+
2
4H+===2H O,C正确;根据正、负极电极反应可知,相同条件下,放电过程中消耗SO 和O 的体积比
2 2 2
为2∶1,D正确。
5.B 光合菌产生的O 得电子结合H+生成HO,碳棒a为正极,FeS 在硫氧化菌的作用下被氧
2 2 x
化为S,S在硫氧化菌的作用下被氧化为SO,碳棒b为负极,正极的电势高于负极,A正确;碳棒a为
正极,电极反应为O+4e-+4H+===2H O,酸性减弱,B错误;根据图示,碳棒b存在电极反应:S-6e
2 2
-+4HO===SO+8H+,C正确;酸性增强不利于菌落存活,负极失电子发生的氧化反应会减慢,故工
2
作一段时间后,电池效率降低,D正确。
6.D 由题图中电子的移动方向可知,电极X为原电池的负极,发生氧化反应,电极Y为原电池
的正极,发生还原反应,A、C正确;电池工作时,光能转化为电能,B正确;由题图可知,电池放电过程
中,I和I-相互转化,RuⅡ、RuⅡ*、RuⅢ间循环转化,所有化学物质都没有被损耗,D错误。
7.C a极:H→HO、CO→CO 发生氧化反应,b极:NO→N、NO →N 发生还原反应,则a极为
2 2 2 2 2 2
电源的负极,b极为电源的正极,电子从a极经导线流向b极,故A错误,B错误;根据题图信息得出
NO 在b极上的电极反应式为2NO +8e-===4O2-+N,故C正确;反应中转移1 mol 电子时,若全为
2 2 2
NO 参与电极反应,根据2NO +8e-===4O2-+N 知,生成N 的体积为2.8 L(标准状况),若全为NO
2 2 2 2
参与电极反应,根据2NO+4e-===2O2-+N 知,生成N 的体积为5.6 L(标准状况),故D错误。
2 2
8.D 通入NO 的电极上NO 转化为N,发生还原反应,该电极为正极,A项正确;若使用的烃为
2 2 2
CH,CH 转化为CO ,结合电解质溶液显酸性,可知通入CH 的电极上发生的电极反应为CH+
2 6 2 6 2 2 6 2 6
4HO-14e-===2CO+14H+,B项正确;为平衡电荷,装置中转移0.4 mol电子时,有0.4N 个H+通
2 2 A
过质子交换膜,C项正确;结合B项中负极反应和正极反应:2NO +8e-+8H+===N +4HO知,装置
2 2 2
工作一段时间后,左室中溶液pH增大,右室中溶液pH减小,D项错误。
9.D 根据题干图示信息可知,放电时,Zn 电极作负极,电极反应为 Zn-2e-+4OH-
===[Zn(OH) ]2-,另一电极为正极,电极反应为CO +2e-+HO===OH-+HCOO-,故正极周围pH
4 2 2
升高,A正确;充电时,Zn电极为阴极,电极反应为[Zn(OH) ]2-+2e-===Zn+4OH-,另一电极为阳极,
4
电极反应为4OH--4e-===2H O+O↑,B正确;由题干图示信息可知,使用催化剂Sn或者sSnLi时,
2 2
生成CO的活化能均高于生成HCOOH的活化能,故均能有效减少副产物CO的生成,C正确;由题
干图示信息可知,使用sSnLi催化剂时的中间产物具有的总能量比使用Sn催化剂时的中间产物的总
能量高,能量越高越不稳定,故使用sSnLi催化剂时的中间产物更不稳定,D错误。
10.D 由题图可知,a极上CH O 转化成CH O,碳元素化合价升高,发生氧化反应,b极上二
6 12 6 6 10 6
氧化锰发生还原反应生成Mn2+,a极为负极,b极为正极,A项错误;依题意知,负极的电极反应式为
CH O-2e-===C H O+2H+,负极区的pH不断减小,B项错误;b极为正极,电极反应为MnO +
6 12 6 6 10 6 2
4H++2e-===Mn2++2HO,C项错误;由负极的电极反应式知,每消耗0.01 mol葡萄糖,电路中转移
2
0.02 mol电子,D项正确。11.C A极: → ,发生得氢的还原反应,则A极为电池的正极,B极为
电池的负极;A极电极反应式为 +H++2e-===Cl-+ ,B极电极反应式为
CH COO--8e-+4HO===2HCO+9H+,A错误,C正确。微生物膜主要作催化剂,催化反应的进行,
3 2
B错误。由B极电极反应式可知,当除去0.1 mol CH COO-时,转移电子的物质的量为0.8 mol,故有
3
0.8 mol H+通过质子交换膜从B极移向A极,D错误。