文档内容
氮及其化合物作业题
作业题目难度分为 3 档:三星☆☆☆(基础题目)
四星☆☆☆☆(中等题目)
五星☆☆☆☆☆(较难题目)
本套作业题目 1-6,17-25,28-29 题为三星,7-16,26-27,30-31 为四星,32-35
为五星
1.下列变化中不属于氮的固定的是( ) ☆☆☆
A.工业上将 NH 与 CO 在高温高压下制成[CO(NH)]
3 2 2 2
B.空气中的 O 和 N 在闪电时化合成 NO
2 2
C.豆科植物的根瘤菌把氮气变为 NH
3
D.工业上用 N 和 H 来合成 NH
2 2
3
【解答】
氮的固定指的是游离态的氮变成氮的化合物
故选:A.
2.N 的下列用途:①合成氨的原料;②焊接金属的保护气;③填充灯泡;④保
2
存水果、粮食,这些性质是利用它的化学稳定性的是( ) ☆☆☆
A.②③ B.①④ C.①② D.②③④
【解答】
氮气对金属、灯丝、粮食水果等起了保护作用,N 没有参加反应,体现了它的化
2
学稳定性,N 是作为合成氨的原料,发生了化学反应,没有体现它的化学稳定性。
2
故选:D.
第 1页(共 19页)3.雷雨天 N 会发生一系列的反应,电闪雷鸣的雨天,一般不可能生成的是( )
2
☆☆☆
A.NH B.HNO C.NO D.NO
3 3 2
【解答】
在电闪雷鸣的雨天,空气中发生的化学反应有:①N+O 2NO,②2NO+O═
2 2 2
2NO,③3NO+HO═2HNO+NO,故一般不可能生成的是:NH
2 2 2 3
3
故选 A.
4.下列关于氮的说法正确的是( ) ☆☆☆
A.N 分子的结构较稳定,因而氮气不能支持任何物质燃烧
2
B.23 g NO 和 NO 混合气含有 0.5N 个氮原子(N 表示阿伏加德罗常数)
2 2 4 A A
C.NO 可用向上排空气法或者排水法收集
D.浓硝酸保存在棕色瓶内是因为硝酸易挥发
【解答】
A、虽然氮气分子的结构较稳定,镁能在氮气中燃烧生成氮化镁,所以氮气能支
持燃烧,故 A 错误.
B、NO 和 NO 的最简式都是 NO,所以可以把混合气体当作二氧化氮分析不影响
2 2 4 2
氮原子的个数,二氧化氮的物质的量= =0.5mol,每个二氧化氮分子中含
有 1 个 N,所以 23g NO 和 NO 混合气含有 0.5N 个氮原子(N 表示阿伏加德罗常
2 2 4 A A
数),故 B 正确.
C、NO 和氧气反应,和水不反应,所以 NO 不能用排空气法收集,只能用排水法
收集,故 C 错误.
D、浓硝酸见光易分解,所以要保存在棕色试剂瓶中,故 D 错误.
故选 B.
5.下列关于 NO 和 NO 的叙述正确的是( ) ☆☆☆
2
A.NO 是一种红棕色气体
B.NO 与水反应生成硝酸,所以 NO 是硝酸的酸酐
2 2
第 2页(共 19页)C.NO 和 NO 是引发光化学烟雾的主要污染源
2
D.NO 可用排水法收集
2
【解答】
A.NO 为无色气体,而 NO 为红棕色气体,故 A 错误;
2
B.NO 与水反应生成硝酸,但硝酸的酸酐为 NO,酸酐中 N 元素的化合价与硝酸
2 2 5
中 N 元素的化合价相同,故 B 错误;
C.NO 和 NO 均为常见的空气污染物,是引发光化学烟雾的主要污染源,故 C 正
2
确;
D.NO 与水反应,不能用排水法收集,故 D 错误;
2
故选 C.
6.关于氮的变化关系图如下,则下列说法不正确的是( ) ☆☆☆
A.路线①②③是工业生产硝酸的主要途径
B.路线Ⅰ、Ⅱ、Ⅲ是雷电固氮生成硝酸的主要途径
C.上述所有反应都是氧化还原反应
D.氮气可在足量的氧气中通过一步反应生成 NO
2
【解答】
A.工业生产硝酸:氨气催化氧化生成一氧化氮,一氧化氮氧化生成二氧化氮,
二氧化氮与水反应生成硝酸,故 A 正确;
B.氮的固定是指游离态氮转化为化合态,雷电条件下氮气与氧气反应生成一氧
化氮,一氧化氮氧化生成二氧化氮,二氧化氮与水反应生成硝酸,故 B 正确;
C.上述所有反应都有化合价的变化,都属于氧化还原反应,故正确;
D.氮气与氧气反应生成一氧化氮,与氧气的量无关,故 D 错误;
故选:D.
7.已知 X、Y、Z、W(含同一元素)有如下转化关系,且 X 能与 W 发生反应生成
一种易溶于水的盐,则 X 可能是( ) ☆☆☆☆
第 3页(共 19页)A.N B.NO
2
2
C.NH D.NO
3
【解答】
X、Y、Z、W(含同一元素),其中 X 能经过两步氧得 Z,Z 再与水反应可以生成对
应的酸或碱,则 X 可以含有 C、N、S、Na 等元素,X 能与 W 发生反应生成一种易
溶于水的盐,符合此条件的 X 只能为 NH,NH 能与氧气生成 NO,NO 再与氧气反
3 3
应生成 NO,NO 与水反应生成 HNO,HNO 与 NH 反应生成 NHNO,NHNO 是一种易
2 2 3 3 3 4 3 4 3
溶于水的盐,根据上面的分析可知,应选 C。
故选 C.
8.甲、乙、丙、丁四种物质,甲、乙、丙含同一种元素.下列各组物质可按下
图转化的是( ) ☆☆☆☆
① ② ③ ④
甲 C N S Fe
2
丙 CO NO SO Fe(NO)
2 2 3 3
3
A.①② B.②③ C.①④ D.③④
【解答】
①假设甲是 C,丙是二氧化碳,则丁是氧气,乙为一氧化碳,碳在少量氧气中燃
烧生成一氧化碳,在过量氧气中燃烧生成二氧化碳,一氧化碳燃烧生成二氧化碳,
所以符合转化关系,故正确;
②假设甲是氮气,丙是二氧化氮,氮气和氧气反应生成一氧化氮,一氧化氮和氧
气反应生成二氧化氮,但氮气不能一步转化为二氧化氮,故错误;
③假设甲是 S,丙是三氧化硫,硫燃烧生成二氧化硫,二氧化硫被氧化生成三氧
化硫,但硫不能一步转化为三氧化硫,故错误;
④假设甲是铁,丙是硝酸铁,则丁是硝酸,乙为硝酸亚铁,铁和少量稀硝酸反应
生成硝酸亚铁,硝酸亚铁和硝酸反应生成硝酸铁,铁和过量稀硝酸反应实现硝酸
铁,所以符合转化关系,故正确;
第 4页(共 19页)故选 C.
9.如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的
水槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观
察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中
盛装的不可能是( ) ☆☆☆☆
A.N 与 NO 的混和气体 B.O 与 NO 的混和气体
2 2 2 2
C.NO 与 NO 的混和气体 D.NO 一种气体
2 2
【解答】
A、N 和水不反应且不溶于水,试管内不能完全被水充满,故 A 选;
2
B、O 与 NO 的混和气体可在溶液中发生反应 4NO+O+2HO=4HNO,试管内能完全
2 2 2 2 2 3
被水充满,故 B 不选;
C、NO 与 NO 的混和气体,当向试管内鼓入氧气后,可在溶液中发生反应
2
4NO+3O+2HO=4HNO,4NO+O+2HO=4HNO,试管内能完全被水充满,故 C 不选;
2 2 3 2 2 2 3
D、O 与 NO 可在溶液中发生反应 4NO+O+2HO=4HNO,试管内能完全被水充满,
2 2 2 2 2 3
故 D 不选.
故选 A.
10.同温同压下,在 3 支相同体积的试管中分别充有等体积混合的 2 种气体,它
们是①NO 和 O,②NO 和 O,③NH 和 N.现将 3 支试管均倒置于水槽中,充分反
2 2 2 3 2
应后,试管中剩余气体的体积分别为 V、V、V,则下列关系正确的是( )
1 2 3
☆☆☆☆
A.V>V>V B.V>V>V C.V>V>V D.V>V>V
1 2 3 1 3 2 3 2 1 3 1
2
【解答】
分别充满等体积混合的 2 种气体,则设每种气体各占 L,①组合发生反应:
4NO+3O+2HO=4HNO,剩余气体的体积为: L,
2 2 3
第 5页(共 19页)②组合发生反应:4NO+O+2HO=4HNO,剩余气体的体积为 L,
2 2 2 3
③组合 NH 全部溶于水,剩余 N 为 L,
3 2
所以:V>V>V,
3 2 1
故选 C.
11.在相同状况下,将下列四种混合气体:(1)体积比为 3:1 的 NH 和 N (2)
3 2
体积比为 1:1 的 NO 和 NO (3)体积比为 1:1 的 NO 和 O (4)体积比为 4:3
2 2 2
的 NO 和 O 分别置于完全相同的试管里,并倒置于水槽中.充分反应后,液面上
2
升的高度分别为 h、h、h、h,则下列关系正确的是( ) ☆☆☆☆
1 2 3 4
A.h>h>h>h B.h>h>h>h
1 2 3 4 4 3 2
1
C.h>h>h>h D.h>h>h>h
4 1 3 2 2 1 3
4
【解答】
设完全相同的试管的体积为 V,充分反应后,液面上升的高度取决于剩余气体的
体积,剩余气体越多,液面高度越低,
1)体积比为 3:1 的 NH 和 N 中只有氨气能完全溶于水,氮气不溶于水,则液面
3 2
高度为 V=h;
1
2)体积比为 1:1 的 NO 和 NO 中,由 3NO+HO═2HNO+NO 可知,NO 不溶于水,
2 2 2 3
则液面高度为 V=h;
2
3)体积比为 1:1 的 NO 和 O 中由 4NO+O+2HO═4HNO 可知,则液面高度为 V=h;
2 2 2 2 2 3 3
4)体积比为 4:3 的 NO 和 O 中由 4NO+3O+2HO═4HNO 可知,气体无剩余,液体
2 2 2 3
充满试管,液面高度为 V,
显然 h>h>h>h
4 1 3
2
故选 C.
12.将盛有 N 和 NO 的混合气体的试管倒立于水中经过足够时间后,气体体积
2 2
减少为原来的一半,则原混合气体中 N 和 NO 的体积比是( ) ☆☆☆☆
2 2
A.1:1 B.1:2 C.1:3 D.3:1
第 6页(共 19页)【解答】
设原混合气体中含有 x mol N,y mol NO,
2 2
盛有 N 和 NO 的混合气体的试管倒立于水中发生 3NO+HO=2HNO+NO,则
2 2 2 2 3
3NO+HO=2HNO+NO
2 2 3
3 1
y
则(x+ ):(x+y)=1:2,
解得 x:y=1:3,
故选 C.
13.将体积为 V mL 的试管充满 NO 气体,按如图所示进行实验.当通入相同条件
下 O 49mL 时,液面仍在原来位置,则试管体积 V 为( ) ☆☆☆☆
2
A.49mL B.28 mL C.30mL D.24.5mL
【解答】
通入氧气发生 4NO+3O+2HO=4HNO,如 NO 过量,则体积不可能与原来相等,应为
2 2 3
氧气过量,则
4NO+3O+2HO=4HNO,
2 2 3
4 3
V V
49﹣ V=V,
V=28,
故选 B.
14.NO、NO、O 按照一定比例通入水中,能被完全吸收,无剩余气体,若 NO、
2 2
NO、O 的气体体积分别为 a、b、c、则 a:b:c 可能为( ) ☆☆☆☆
2 2
A.1:5:2 B.2:5:1 C.5:1:2 D.5:2:1
第 7页(共 19页)【解答】
根据反应后无剩余气体,即全部生成了硝酸,根据反应中电子得失守恒:
n(NO)×3+n(NO)=n(O)×4 来判断即可.
2 2
A.NO、NO、O 的气体体积比为 1:5:2,物质的量之比为 1:5:2,
2 2
B.此时 1×3+5=2×4,故 A 正确;
B.NO、NO、O 的气体体积比为 2:5:1,物质的量之比为 2:5:1,
2 2
此时 2×3+5≠1×4,故 B 错误;
C.NO、NO、O 的气体体积比为 5:1:2,物质的量之比为 5:1:2,
2 2
此时 5×3+1≠2×4,故 C 错误;
D.NO、NO、O 的气体体积比为 5:2:1,物质的量之比为 5:2:1,
2 2
此时 5×3+2≠1×4,故 D 错误;
故选 A.
15.相同条件下,两个容积相同的试管分别装满 NO 和 NO 气体,分别倒置于水
2
槽中,然后通过导管缓慢通入氧气,边通边慢慢摇动试管,直到两个试管内充满
液体.假设试管内的溶质不向水槽中扩散,则两个试管内溶液物质的量浓度之比
为( ) ☆☆☆☆
A.1:1 B.5:7
C.7:5 D.4:3
【解答】
两只试管中分别发生 4NO+O+2HO=4HNO、4NO+3O+2HO=4HNO,则试管体积相同,
2 2 2 3 2 2 3
则生成的硝酸的物质的量相同,且溶液的体积相同,所以两试管的硝酸的浓度相
同。
故选 A.
16.将标准状况下 NO 和 O 按体积比 4:1 混合后充入一干燥烧瓶中,把烧瓶倒
2 2
置于水中,瓶内液体逐渐上升,假设烧瓶内溶液不扩散,最终烧瓶内溶液溶质的
第 8页(共 19页)物质的量浓度为( ) ☆☆☆☆
A. mol•L﹣1 B. × mol•L﹣1
C. × mol•L﹣1 D. mol•L
﹣1
【解答】
设混合气体中含有 4VL NO,1VL O,则烧瓶的体积为 5V L,
2 2
4NO + O +2HO = 4HNO
2 2 2
3
mol mol mol
c(HNO)= = × mol/L,
3
故选 C.
17.下列叙述不正确的是( ) ☆☆☆
A.稀 HNO 和金属反应时主要得到氢气
3
B.NH 易液化,液氨常用作制冷剂
3
C.利用氨气极易溶于水,氨气可以做喷泉实验
D.铵盐受热易分解,贮存氨态氮肥时要密封保存,并放在阴凉通风处
【解答】
A.硝酸具有强的氧化性,与金属反应不生成氢气,故 A 错误;
B.氨很容易液化,液态氨汽化时要吸收大量的热,使周围物质的温度急剧下降,
所以氨常作为制冷剂,故 B 正确;
C.氨气极易溶于水,能够使瓶内外在短时间内产生较大的气压差,所以能够形
成喷泉实验,故 C 正确;
D.铵盐受热易分解,因此贮存氨态氮肥时要密封保存,并放在阴凉通风处,故
D 正确;
故选:A.
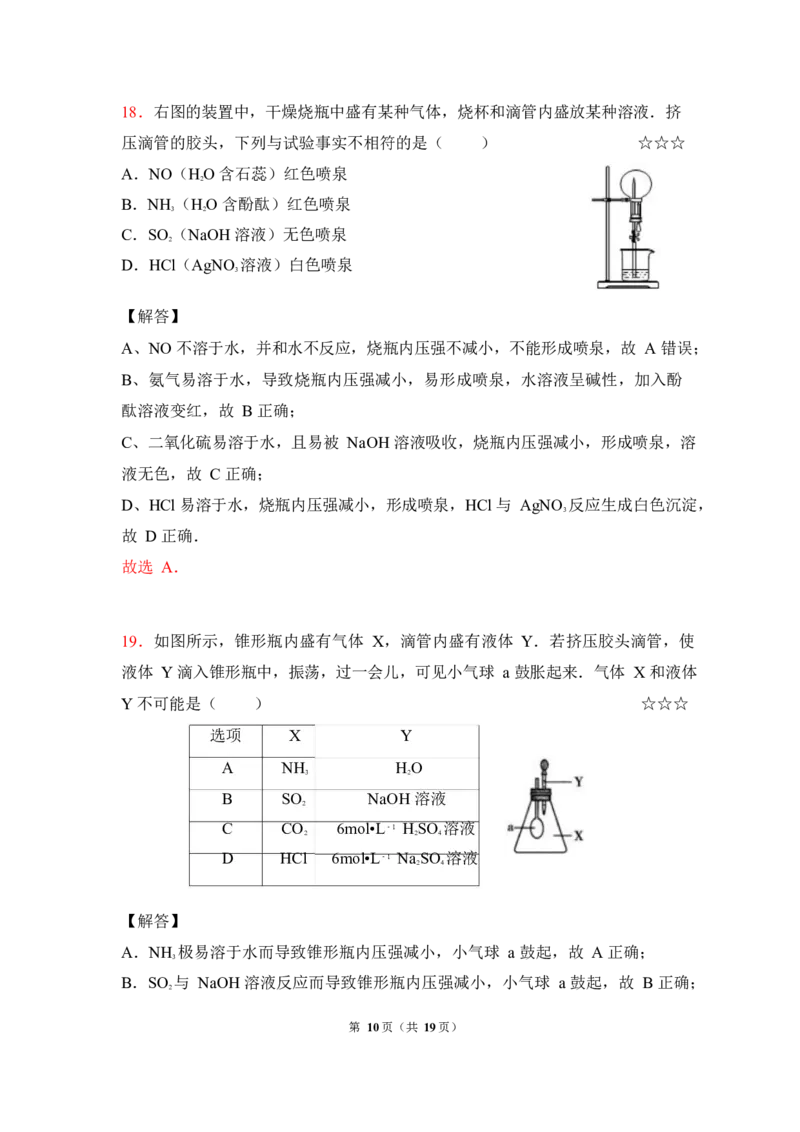
第 9页(共 19页)18.右图的装置中,干燥烧瓶中盛有某种气体,烧杯和滴管内盛放某种溶液.挤
压滴管的胶头,下列与试验事实不相符的是( ) ☆☆☆
A.NO(HO 含石蕊)红色喷泉
2
B.NH(HO 含酚酞)红色喷泉
3 2
C.SO(NaOH 溶液)无色喷泉
2
D.HCl(AgNO 溶液)白色喷泉
3
【解答】
A、NO 不溶于水,并和水不反应,烧瓶内压强不减小,不能形成喷泉,故 A 错误;
B、氨气易溶于水,导致烧瓶内压强减小,易形成喷泉,水溶液呈碱性,加入酚
酞溶液变红,故 B 正确;
C、二氧化硫易溶于水,且易被 NaOH 溶液吸收,烧瓶内压强减小,形成喷泉,溶
液无色,故 C 正确;
D、HCl 易溶于水,烧瓶内压强减小,形成喷泉,HCl 与 AgNO 反应生成白色沉淀,
3
故 D 正确.
故选 A.
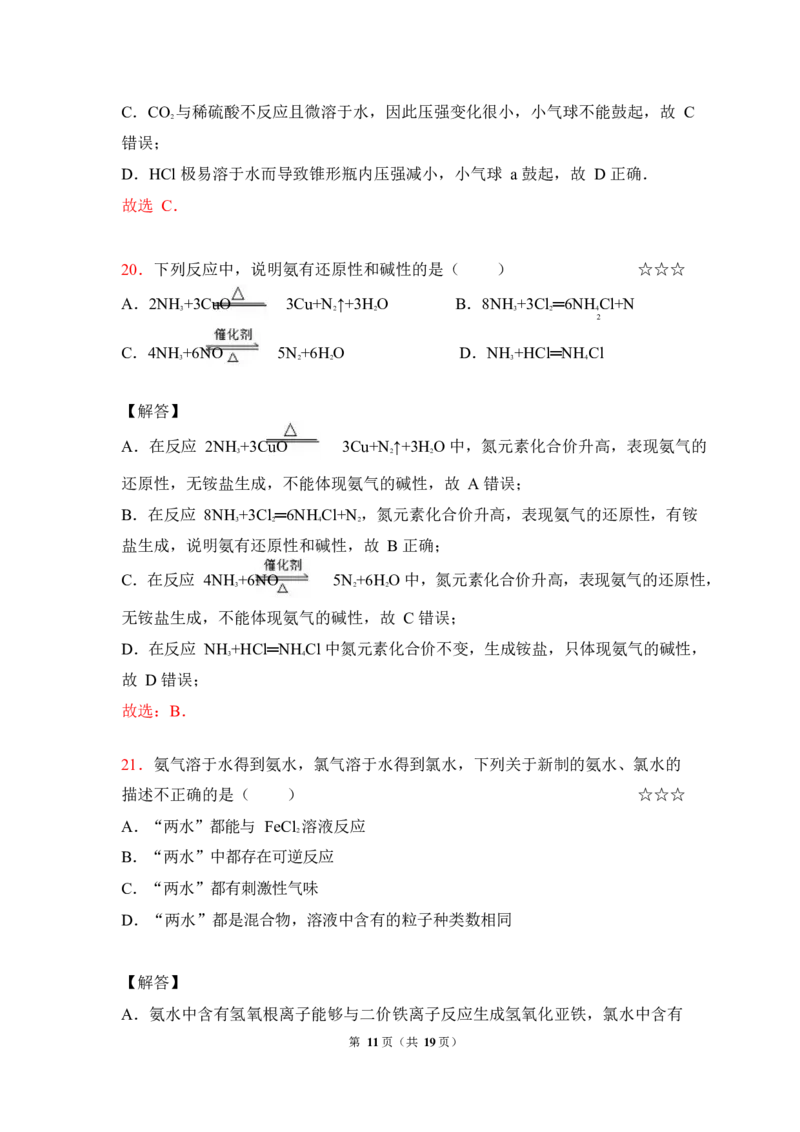
19.如图所示,锥形瓶内盛有气体 X,滴管内盛有液体 Y.若挤压胶头滴管,使
液体 Y 滴入锥形瓶中,振荡,过一会儿,可见小气球 a 鼓胀起来.气体 X 和液体
Y 不可能是( ) ☆☆☆
选项 X Y
A NH HO
3 2
B SO NaOH 溶液
2
C CO 6mol•L﹣1 HSO 溶液
2 2 4
D HCl 6mol•L﹣1 NaSO 溶液
2 4
【解答】
A.NH 极易溶于水而导致锥形瓶内压强减小,小气球 a 鼓起,故 A 正确;
3
B.SO 与 NaOH 溶液反应而导致锥形瓶内压强减小,小气球 a 鼓起,故 B 正确;
2
第 10页(共 19页)C.CO 与稀硫酸不反应且微溶于水,因此压强变化很小,小气球不能鼓起,故 C
2
错误;
D.HCl 极易溶于水而导致锥形瓶内压强减小,小气球 a 鼓起,故 D 正确.
故选 C.
20.下列反应中,说明氨有还原性和碱性的是( ) ☆☆☆
A.2NH+3CuO 3Cu+N↑+3HO B.8NH+3Cl═6NHCl+N
3 2 2 3 2 4
2
C.4NH+6NO 5N+6HO D.NH+HCl═NHCl
3 2 2 3 4
【解答】
A.在反应 2NH+3CuO 3Cu+N↑+3HO 中,氮元素化合价升高,表现氨气的
3 2 2
还原性,无铵盐生成,不能体现氨气的碱性,故 A 错误;
B.在反应 8NH+3Cl═6NHCl+N,氮元素化合价升高,表现氨气的还原性,有铵
3 2 4 2
盐生成,说明氨有还原性和碱性,故 B 正确;
C.在反应 4NH+6NO 5N+6HO 中,氮元素化合价升高,表现氨气的还原性,
3 2 2
无铵盐生成,不能体现氨气的碱性,故 C 错误;
D.在反应 NH+HCl═NHCl 中氮元素化合价不变,生成铵盐,只体现氨气的碱性,
3 4
故 D 错误;
故选:B.
21.氨气溶于水得到氨水,氯气溶于水得到氯水,下列关于新制的氨水、氯水的
描述不正确的是( ) ☆☆☆
A.“两水”都能与 FeCl 溶液反应
2
B.“两水”中都存在可逆反应
C.“两水”都有刺激性气味
D.“两水”都是混合物,溶液中含有的粒子种类数相同
【解答】
A.氨水中含有氢氧根离子能够与二价铁离子反应生成氢氧化亚铁,氯水中含有
第 11页(共 19页)氯气能够氧化二价铁离子生成三价铁离子,所以“两水”都能与 FeCl 溶液反应,
2
故 A 正确;
B.一水合氨、次氯酸都是弱电解质,都是部分电离,存在电离平衡,故 B 正确;
C.氨水中含有氨气、氯水中含有氯气,氨气和氯气都具有刺激性气味,故 C 正
确;
D.均为混合物,但氨水中含 6 种微粒,氯水中含 7 种微粒,故 D 错误;
故选:D.
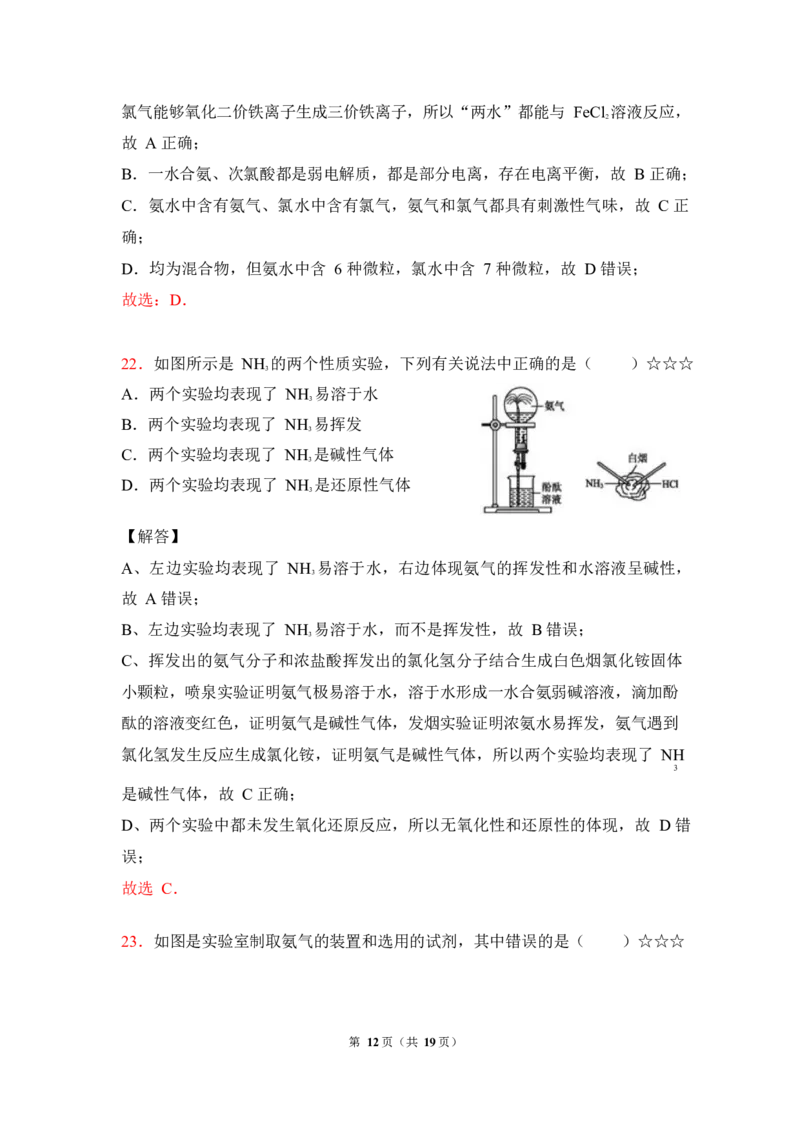
22.如图所示是 NH 的两个性质实验,下列有关说法中正确的是( )☆☆☆
3
A.两个实验均表现了 NH 易溶于水
3
B.两个实验均表现了 NH 易挥发
3
C.两个实验均表现了 NH 是碱性气体
3
D.两个实验均表现了 NH 是还原性气体
3
【解答】
A、左边实验均表现了 NH 易溶于水,右边体现氨气的挥发性和水溶液呈碱性,
3
故 A 错误;
B、左边实验均表现了 NH 易溶于水,而不是挥发性,故 B 错误;
3
C、挥发出的氨气分子和浓盐酸挥发出的氯化氢分子结合生成白色烟氯化铵固体
小颗粒,喷泉实验证明氨气极易溶于水,溶于水形成一水合氨弱碱溶液,滴加酚
酞的溶液变红色,证明氨气是碱性气体,发烟实验证明浓氨水易挥发,氨气遇到
氯化氢发生反应生成氯化铵,证明氨气是碱性气体,所以两个实验均表现了 NH
3
是碱性气体,故 C 正确;
D、两个实验中都未发生氧化还原反应,所以无氧化性和还原性的体现,故 D 错
误;
故选 C.
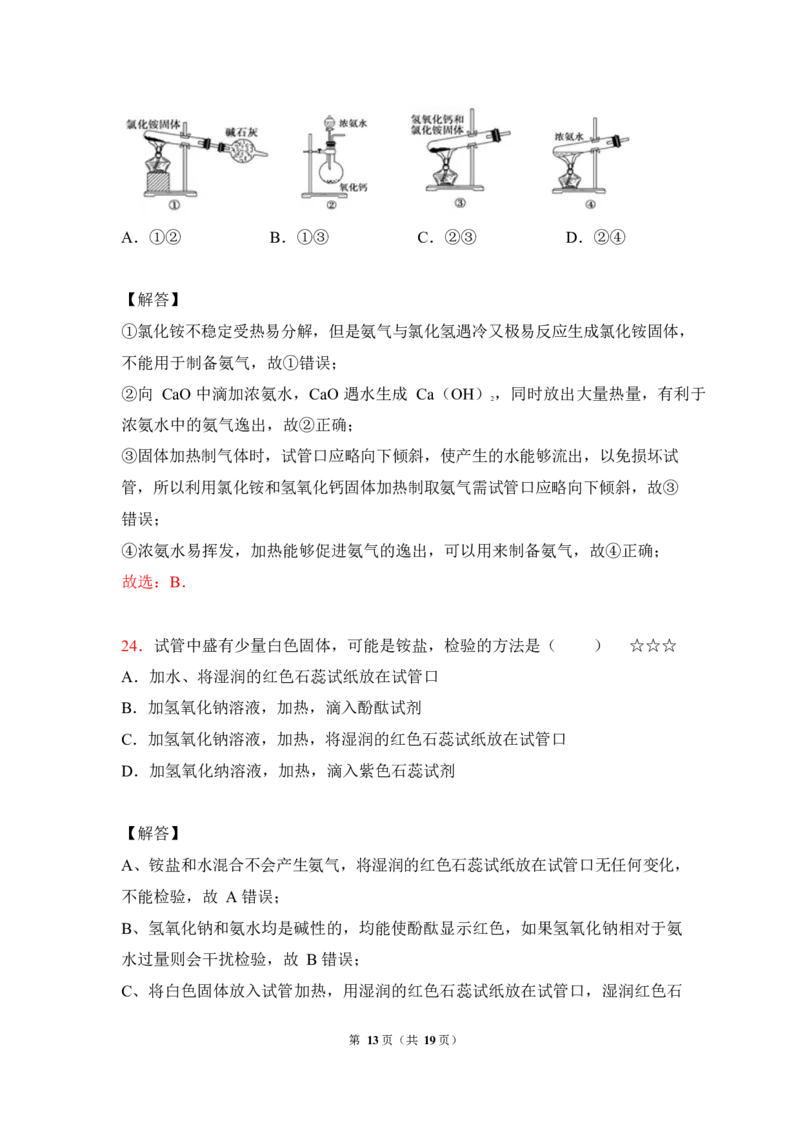
23.如图是实验室制取氨气的装置和选用的试剂,其中错误的是( )☆☆☆
第 12页(共 19页)A.①② B.①③ C.②③ D.②④
【解答】
①氯化铵不稳定受热易分解,但是氨气与氯化氢遇冷又极易反应生成氯化铵固体,
不能用于制备氨气,故①错误;
②向 CaO 中滴加浓氨水,CaO 遇水生成 Ca(OH),同时放出大量热量,有利于
2
浓氨水中的氨气逸出,故②正确;
③固体加热制气体时,试管口应略向下倾斜,使产生的水能够流出,以免损坏试
管,所以利用氯化铵和氢氧化钙固体加热制取氨气需试管口应略向下倾斜,故③
错误;
④浓氨水易挥发,加热能够促进氨气的逸出,可以用来制备氨气,故④正确;
故选:B.
24.试管中盛有少量白色固体,可能是铵盐,检验的方法是( ) ☆☆☆
A.加水、将湿润的红色石蕊试纸放在试管口
B.加氢氧化钠溶液,加热,滴入酚酞试剂
C.加氢氧化钠溶液,加热,将湿润的红色石蕊试纸放在试管口
D.加氢氧化纳溶液,加热,滴入紫色石蕊试剂
【解答】
A、铵盐和水混合不会产生氨气,将湿润的红色石蕊试纸放在试管口无任何变化,
不能检验,故 A 错误;
B、氢氧化钠和氨水均是碱性的,均能使酚酞显示红色,如果氢氧化钠相对于氨
水过量则会干扰检验,故 B 错误;
C、将白色固体放入试管加热,用湿润的红色石蕊试纸放在试管口,湿润红色石
第 13页(共 19页)蕊试纸会变蓝色,证明产生的气体是氨气,证明该盐中含有铵根离子,这是检验
铵盐的方法,故 C 正确;
D、氢氧化钠和氨水均是碱性的,均能使石蕊试液显示蓝色,如果氢氧化钠相对
于氨水过量则会干扰检验,故 D 错误.
故选 C.
25.下列反应中硝酸既能表现出酸性又表现出氧化性的是( ) ☆☆☆
A.使石蕊试液变红
B.与铜反应放出 NO 气体,生成 Cu(NO)
3
2
C.与 NaCO 反应放出 CO 气体,生成 NaNO
2 3 2
3
D.与 S 单质混合共热时生成 HSO 和 NO
2 4
2
【解答】
A.使石蕊变红,只能说明硝酸具有酸性,不能说明氧化性,故 A 错误;
B.与铜反应生成 Cu(NO) 和 NO 气体,生成硝酸铜表现酸性,生成 NO 表现硝
3 2
酸的氧化性,故 B 正确;
C.与 NaCO 反应放出 CO 气体生成 NaNO,说明硝酸的酸性比碳酸强,不发生氧
2 3 2 3
化还原反应,不能说明氧化性,故 C 错误;
D.与 S 单质混合共热时生成 HSO 和 NO,只表现硝酸的氧化性,不表现酸性,
2 4 2
故 D 错误.
故选:B.
26.从降低成本和减少环境污染的角度考虑,制取硝酸铜最好的方法是( )
☆☆☆☆
A.铜和浓硝酸反应 B.铜和稀硝酸反应
C.氧化铜和硝酸反应 D.氯化铜和硝酸银反应
【解答】
A、铜和浓硝酸反应的方程式为:Cu+4HNO(浓)=Cu(NO)+2NO ↑+2HO,该反
3 3 2 2 2
应中产生有毒气体二氧化氮,所以对环境有污染,不符合“绿色化学”理念,且
第 14页(共 19页)硝酸的利用率不高,故 A 错误.
B、铜和稀硝酸反应方程式为:Cu+ HNO=Cu(NO)+ NO↑+ HO,该反应中产
3 3 2 2
生有毒气体一氧化氮,所以对环境有污染,不符合“绿色化学”理念,且硝酸的
利用率不高,故 B 错误.
C、氧化铜和硝酸反应的方程式为:CuO+2HNO=Cu(NO)+HO,没有污染物,且
3 3 2 2
硝酸的利用率 100%,符合“绿色化学”和“降低成本”理念,故 C 正确.
D、氯化铜和硝酸银反应方程式为:CuCl+2AgNO=2AgCl↓+Cu(NO),该反应虽
2 3 3 2
有硝酸铜生成,但硝酸银价格较贵,不符合“降低成本”理念,故 D 错误.
故选 C.
27.下列标有横线的物质在给定的条件下不能完全溶解的是( )☆☆☆☆
①1mol Zn 与含 1mol HSO 的稀硫酸溶液反应
2 4
②1mol Cu 与含 2mol HSO 的浓硫酸溶液共热
2 4
③1mol Cu 与含 4mol HNO 的浓硝酸溶液反应
3
④1mol MnO 与含 4mol HCl 的浓盐酸溶液共热.
2
A.①③ B.①② C.②④ D.③④
【解答】
①1mol 锌与含 1mol HSO 的稀硫酸溶液恰好完全反应,故不选;
2 4
②随反应的进行浓硫酸变在稀硫酸,稀硫酸与铜不反应,故选;
③1mol 铜转移 2mol 的电子,生成 2mol 的铜离子与 2mol 硝酸结合成硫酸盐,而
2mol HNO 的硝酸作氧化剂,得电子的量为 2mol~6mol,所以铜不足,故不选;
3
④随着反应的进行,盐酸浓度逐渐降低,稀盐酸与二氧化锰不反应,故选.
故选 C.
28.某溶液中仅含有一种溶质,若在该溶液中加入 BaCl 溶液出现白色沉淀再加
2
稀 HNO 沉淀不消失,则该溶液不可能含有的溶质是( ) ☆☆☆
3
A.AgNO B.CuSO C.KSO D.NaCO
3 4 2 3 2
3
第 15页(共 19页)【解答】
如溶液中含有 SO
2﹣,能被硝酸氧化为 SO 2﹣,加入 BaCl 溶液生成
BaSO, 2
4 3 4
因加入的为 BaCl,可能生成 AgCl,二者都不溶于水,所以溶液中可能含有
2
SO 2﹣、SO
CuSO, 2﹣ 、Ag + 离子中的一种,即:该溶液可能为 AgNO 3 或 K 2 SO 3 或
4 4 3
由于碳酸钡能够溶于稀硝酸,所以该溶液不可能为碳酸钠溶液,
故选 D.
29.取三张蓝色石蕊试纸放在玻璃片上,然后按顺序分别滴加 65%的 HNO、98%
3
的 HSO 和新制的氯水,三张试纸呈现的颜色分别是( ) ☆☆☆
2 4
A.白、红、白 B.红、黑、白 C.红、红、红 D.白、黑、白
【解答】
硝酸具有强氧化性,将试纸中的有色物质氧化成无色的;
浓硫酸具有脱水性,试纸和其中的有色物质都是有机物,浓硫酸夺取水分,只剩
下黑色的碳;
新制氯水漂白性,将试纸漂白;
故选:D.
30.下列反应所得溶液中一定只含有一种溶质的是( ) ☆☆☆☆
A.向稀硝酸中加入铁粉
B.向稀盐酸中滴入少量的 NaAlO 溶液
2
C.向 NaOH 溶液中通入 CO 气体
2
D.向 MgSO、HSO 的混合溶液中加入过量的 Ba(OH) 溶液
4 2 4 2
【解答】
A.铁粉与稀硝酸反应可生成 Fe2+或 Fe3+,可能为二者的混合物,故 A 错误;
B.向稀盐酸中滴入少量的 NaAlO 溶液反应生成氯化钠、氯化铝溶液,溶质有两
2
种,故 B 错误;
C.向 NaOH 溶液中通入 CO 气体可生成 NaHCO 或 NaCO,可能为二者的混合物,
2 3 2 3
故 C 错误;第 16页(共 19页)D.向 MgSO、HSO 的混合溶液中加入过量的 Ba(OH) 溶液,生成 Mg(OH) 和
4 2 4 2 2
BaSO,溶质只有 Ba(OH),故 D 正确.
4 2
故选 D.
31.物质的量之比为 2:5 的锌与稀硝酸反应,若硝酸被还原的产物为 NO,反应
2
结束后锌没有剩余,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比
是( ) ☆☆☆☆
A.1:4 B.1:5 C.2:3 D.2:5
【解答】
锌与稀硝酸反应时硝酸既表现酸性又表现氧化性,根据原子守恒和电子守恒,
2mol 锌失去 4mol 电子,生成 2mol 锌离子,由于生成硝酸锌,则其结合的硝酸
根离子是 4mol,则剩余的 1mol 的硝酸被还原得到 4mol 电子,硝酸也全部反应,
则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是 1:4,
故选 A.
32.将 2.56g Cu 和一定量的浓 HNO 反应,随着 Cu 的不断减少,反应生成气体
3
的颜色逐渐变浅,当 Cu 反应完毕时,共收集到气体 1.12L(标准状况),则反应
中消耗 HNO 的物质的量为( ) ☆☆☆☆☆
3
A.0.05 mol B.1 mol C.1.05 mol D.0.13 mol
【解答】
铜和硝酸反应,随着浓度的减少,硝酸的还原产物的价态越低,铜和浓硝酸反应
生成 NO,而与稀硝酸反应时则生成 NO,故生成的气体有 NO 和 NO,
2 2
则 n(NO)+n(NO)= =0.05mol,即被还原的硝酸的物质的量为 0.05mol,
2
n(Cu)= =0.04mol,则生成 n(Cu(NO))=0.04mol,
3 2
可知表现酸性的硝酸的物质的量为 0.04mol×2=0.08mol,
则参加反应的硝酸的物质的量为:0.05mol+0.08mol=0.13mol.
故选 D.
第 17页(共 19页)33.将一定质量铜与 100mL 一定浓度的硝酸反应,铜完全溶解时产生的 NO 和 NO
2
混合气体在标准状况下的体积为 11.2L.待产生的气体全部释放后,向溶液加入
140mL 5mol•L﹣1 的 NaOH 溶液,恰好使溶液中的 Cu2+全部转化成沉淀,则原硝酸
溶液的物质的量浓度是( ) ☆☆☆☆☆
A.5mol/L B.7mol/L C.10mol/L D.12mol/L
【解答】
向反应后溶液中加入 NaOH 溶液,恰好使溶液中的 Cu2+全部转化成沉淀,此时溶
液中溶质为 NaNO,由钠离子守恒 n(NaNO)=n(NaOH)=0.14L×5mol/L=0.7 mol,
3 3
生成混合气体物质的量为 n(NO+NO)= =0.5mol,根据氮原子守恒可
2
知 n(HNO)=n(NaNO)+n(NO+NO)=0.7 mol+0.5mol=1.2mol,
3 3 2
故原有硝酸的物质的量浓度为 =12mol/L
故选 D.
34.在含有 1mol HNO 和 2molHSO 的混合稀溶液中,加入 1.5molCu,加热充分
3 2 4
反应,产生的气体在标准状况下的体积约为( ) ☆☆☆☆☆
A.5.6L B.11.2L C.22.4L D.44.8L
【解答】
混合酸中:n(H
+
)=1mol+2mol×2=5mol,n(NO ﹣)=n(HNO
3
)=1mol,
3
3Cu+2NO ﹣+8H
+
=3Cu2++2NO↑+4H
2
O
3
3 2 8 2
1.5mol 1mol 4mol 1mol
故 H
+
剩余,Cu、NO ﹣完全反应,由方程式可知生成 NO 的物质的量是 1mol,故标
3
况下,生成 NO 的体积=1mol×22.4L/mol=22.4L,
故选 C.第 18页(共 19页)35.将一定量硫酸、硝酸和 KNO 溶液混合成 100ml 溶液,其中 HSO、HNO 和 KNO
3 2 4 3
3
的物质的量浓度分别是 6mol/L,2mol/L 和 1mol/L,向其中加入过量的铁粉,可
产生标准状况下的混合气体体积为( ) ☆☆☆☆☆
A.11.2 L B.6.72 L C.8.96 L D.4.48 L
【解答】
100ml 溶 液 中 含 有 氢 离 子 的 物 质 的 量 为 : 0.1L × 6mol/L × 2+0.1L ×
2mol/L=1.4mol;含有的硝酸根离子为:0.1L×2mol/L+0.1L×1mol/L=0.3mol,
加入过量的铁粉,发生反应的离子方程式为:3Fe+2NO ﹣+8H
+
=3Fe2++2NO↑+4H
2
O
3
和反应 Fe+2H
+
=Fe2++H
2
↑,则:
3Fe+2NO ﹣+8H
+
=3Fe2++2NO↑+4H
2
O
3
2 8 2
0.3mol 1.2mol 0.3mol
剩余的氢离子的物质的量为:1.4mol﹣1.2mol=0.2mol,
Fe+2H
+
=Fe2++H
2
↑,
2 1
0.2mol 0.1mol
产生气体的物质的量为:0.3mol+0.1mol=0.4mol,标况下体积为:0.4mol×
22.4L/mol=8.96L
故选:C.
第 19页(共 19页)