文档内容
盐类水解作业题
作业题目难度分为 3 档:三星☆☆☆(基础题目)
四星☆☆☆☆(中等题目)
五星☆☆☆☆☆(较难题目)
本套作业题目 1-9,18-20 题为三星,10-17 题为四星,21-31 题为五星。
1.下列有关盐类水解的叙述中正确的是( ) ☆☆☆
A.溶液呈中性的盐一定是强酸、强碱生成的盐
B.含有弱酸根盐的水溶液一定呈碱性
C.盐溶液的酸碱性主要决定于形成盐的酸和碱的相对强弱
D.强酸强碱盐的水溶液一定呈中性
【解答】
A、如果弱酸、弱碱的电离程度相当,生成的盐的水溶液呈中性,如 CHCOONH
3
4
溶液呈中性,故 A 错误;
B、含有弱酸根盐的水溶液不一定呈碱性,如 NaHSO 溶液呈酸性,故 B 错误;
3
C、酸和碱反应生成的盐溶液的酸碱性取决于酸和碱的相对强弱,谁强显谁性是
水解的规律,故 C 正确;
D、强酸强碱盐的水溶液不一定呈中性,例如 NaHSO 溶液显酸性,故 D 错误。
4
故选 C.
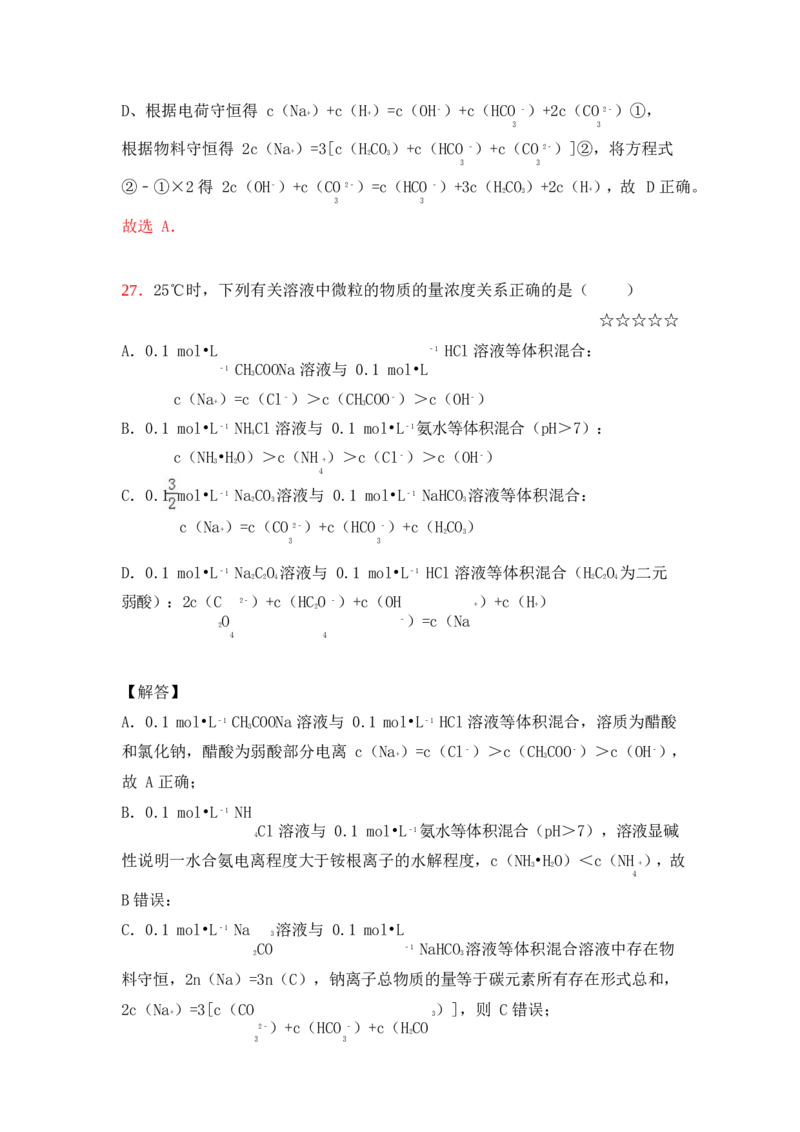
2.如图表示的是某离子 X 的水解过程示意图,则离子 X 可能是( ) ☆☆☆
A.CO 2﹣ B.HCO ﹣ C.Na
+
D.NH
+
3 3 4第 1页(共 21页)【解答】
根据盐的水解原理结合图示的内容可以知道 X 离子水解显示酸性.
A、碳酸根水解,显示碱性,故 A 错误;
B、碳酸氢根离子水解显示碱性,故 B 错误;
C、钠离子不会发生水解,故 C 错误;
D、铵根离子水解溶液显示酸性,故 D 正确。
故选 D.
3.常温下,有下列盐:①FeCl②NaClO ③NaCl,其水溶液的 pH 由大到小排列
3
正确的是( ) ☆☆☆
A.①>③>② B.②>③>① C.③>②>① D.①>②>③
【解答】
常温下,盐溶液酸碱性根据其对应的酸、碱的相对强弱判断,强酸强碱盐溶液呈
中性,强酸弱碱盐溶液呈酸性,强碱弱酸盐溶液呈碱性,溶液的酸性越强其 pH
越小、碱性越强 pH 越大,
①是强酸弱碱盐,溶液呈酸性,常温下 pH<7;
②是强碱弱酸盐,溶液呈酸性,常温下 pH>7;
③是强酸强碱盐,溶液呈中性,常温下 pH=7;
所以这三种溶液 pH 大小顺序是②>③>①。
故选 B.
4.有溶质的物质的量浓度均为 0.1mol/L 的下列八种溶液①HCl ②HSO ③
2 4
CHCOOH ④Ba(OH) ⑤KOH ⑥NaF ⑦KCl ⑧NHCl 这些溶液的 pH 由小到大
3 2 4
的顺序是( ) ☆☆☆
A.②①③⑧⑦⑥⑤④ B.②①③⑥⑦⑧⑤④
C.①②③⑧⑦⑥④⑤ D.②①⑧③⑦⑥④⑤
第 2页(共 21页)【解答】
酸性溶液:①HCl 为一元强酸;
②HSO 为二元强酸;
2 4
③CHCOOH 为一元弱酸;
3
⑧NHCl 溶液中,铵根离子水解,溶液显示酸性;
4
所以溶液的 pH 由小到大的顺序:②①③⑧;
碱性溶液:
④Ba(OH) 为二元强碱;
2
⑤KOH 为一元强碱;
⑥NaF 为强碱弱酸盐,溶液显示碱性;
所以溶液的 pH 由小到大的顺序:⑥⑤④;
⑦KCl 是强酸强碱盐,其溶液呈中性;
通过以上分析知,这几种溶液的 pH 由小到大的排列顺序是:②①③⑧⑦⑥⑤④,
故选 A.
5.下列离子方程式中,属于水解反应的是( ) ☆☆☆
A.HCOOH+H O +HO═HCO ﹣+H
3 2 2
O═HCOO﹣+H B.CO
2 +
+
3
C.CO 2﹣+HO═HCO ﹣+OH﹣ D.HS﹣═S2﹣+H
2
+
3 3
【解答】
A.为甲酸的电离,甲酸电离生成甲酸根和氢离子,故 A 不选;
B.二氧化碳与水反应生成碳酸,碳酸电离生成碳酸氢根与氢离子,不是水解,
故 B 不选;
C.碳酸根水解生成碳酸氢根与氢氧根,为水解方程式,故 C 选;
D.为硫氢根离子电离生成硫离子和氢离子,故 D 不选。
故选 C.
6.下列物质在常温下发生水解时,对应的水解方程式正确的是( ) ☆☆☆
A.Na
2
CO
3
:CO 2﹣+H
2
O
⇌
2OH﹣+CO
2
↑
3第 3页(共 21页)B.NH
4
NO
3
:NH
+
+H
2
O
⇌
NH
3
•H
2
O+H
+
4
C.CuSO
4
:Cu2++2H
2
O
⇌
Cu(OH)
2
↓+2H
+
D.KF:F
﹣+HO═HF+OH﹣
2
【解答】
A.碳酸钠溶液中,碳酸根离子水解分步进行,主要以第一步为主,碳酸根离子
水解的方程式为:CO 2﹣+H
2
O
⇌
HCO ﹣+OH﹣,故 A 错误;
3 3
B.铵根离子水解的离子方程式为:NH
+
+H
2
O
⇌
NH
3
•H
2
O+H
+
,故 B 正确;
4
C.铜离子水解生成的不是氢氧化铜沉淀,铜离子水解方程式为:
Cu2++2H +2H
2
2
O
⇌
Cu(OH)
+
,故 C 错误;
D.水解反应为可逆反应,应该用可逆号,氟离子水解的方程式为:
F﹣+H
2
O
⇌
HF+OH﹣,故 D 错误。
故选 B.
7.室温下,将碳酸钠溶液加热至 70℃,其结果是( ) ☆☆☆
A.溶液中 c(CO 2﹣)增大 B.水的电离程度不变
3
C.K(水的离子积)将变小 D.溶液的碱性增强
W
【解答】
A、碳酸钠溶液中碳酸根离子水解促进水的电离,水解过程是吸热反应,升温促
进水解,溶液中 c(CO 2﹣)减小,故 A 错误;
3
B、碳酸钠溶液中碳酸根离子水解促进水的电离,水的电离程度增大,故 B 错误;
C、温度升高离子积常数增大,故 C 错误;
D、升温促进水解平衡正向进行,溶液碱性增强,故 D 正确。
故选 D.
8.在 CH
3
COO﹣+H
2
O
⇌
CH
3
COOH+OH﹣的平衡中,要使水解平衡向右移动,应采取的措施是( ) ☆
☆☆
第 4页(共 21页)A.加水稀释 B.加入冰醋酸 C.加入 NaOH 固体 D.降低温度
【解答】
在醋酸根离子的水解平衡中,要使水解平衡向右移动,反应是吸热过程,
A、加水会促进电离平衡正向移动,越稀越电离,故 A 正确;
B、加入冰醋酸电离大于水解,醋酸分子浓度增大程度大,水解程度减小,故 B
错误;
C、加入氢氧化钠固体,溶解后氢氧根离子浓度增大,平衡逆向进行,故 A 错误;
D、水解是吸热过程,降温抑制水解正向进行,平衡逆向移动,故 D 错误。
故选 A.
9.向 NaCN 的水溶液中加入下列物质,可使 NaCN 水解程度增大的是( )
☆☆☆
①NaOH ②NaCN ③NHCl ④NaCO ⑤HO ⑥HCN ⑦HCl
4 2 3 2
A.①②③ B.①⑤⑥ C.①③⑤ D.③⑤⑦
【解答】
NaCN 的水溶液中存在下列平衡:CN﹣+H
2
O
⇌
HCN+OH﹣,
①NaOH 会抑制水解,水解程度减小,故错误;
②NaCN 的加入会使得溶液浓度增大,水解程度减弱,故 C 错误;
③NHCl 中的铵根离子可以和氢氧根离子之间反应,消耗氢氧根离子,促使水解
4
平衡正向移动,故正确;
④NaCO 水解显示碱性,所以会抑制氰化钠的水解,水解程度减小,故错误;
2 3
⑤加 HO 可以将溶液稀释,水解程度增大,故正确;
2
⑥HCN 的加入可以抑制化学平衡正向进行,故错误;
⑦HCl 的加入可以消耗氢氧根离子,促使化学平衡正向进行,故正确。
故选 D.
第 5页(共 21页)10.将浓度为 0.1mol/L NaCO 溶液加水稀释,下列结论错误的是( )
2 3
☆☆☆☆
A.水解平衡正向移动 B.各微粒浓度均变小(除 HO 外)
2
C.溶液中离子数目增多 D. 比值增大
【解答】
0.1mol•L CO 溶液中存在水解平衡:CO
2 3
﹣1 的 Na 2﹣+H 2 O ⇌ HCO ﹣+OH﹣
3 3
A、加水稀释,碳酸根离子水解平衡正向移动,故 A 正确;
B、加水稀释,氢氧根浓度减小,氢离子浓度增大,故 B 错误;
C、加水稀释,碳酸根离子水解平衡正向移动,阴离子数增加,溶液中离子数目
增多,故 C 正确;
D、加水稀释,碳酸根离子水解平衡正向移动,浓度之比等于其物质的量之比,
比值增大,故 D 正确。
故选 B.
11.一定条件下,Na
2
CO
3
溶液中存在 CO 2﹣+H
2
O
⇌
HCO ﹣+OH﹣平衡.下列说法不正确
3 3
的是( ) ☆☆☆☆
A.稀释溶液, 增大
B.加入 NaOH 固体, 减小
C.升高温度,平衡常数增大
D.通入 CO,溶液 pH 减小
2
【解答】
A.碳酸根离子的水解平衡常数 K= ,温度不变,则该比值不
h第 6页(共 21页)变,故 A 错误;
B.加入 NaOH 固体,溶液中氢氧根离子浓度增大,则水解平衡向着逆向移动,碳
酸氢根离子浓度减小,碳酸根离子浓度增大, 的比值减小,故 B 正确;
C.水解是吸热反应,升高温度,水解平衡正向移动,所以平衡常数
K= 增大,故 C 正确;
h
D.二氧化碳与氢氧根离子反应,导致溶液中氢氧根离子浓度减小,溶液的 pH
减小,故 D 正确;
故选 A.
12.欲使 0.1mol∙L﹣1 的 NaHCO
3
溶液中 c(H
+
)、c(CO 2﹣)、c(HCO
3
¯)都减少,其
3
方法是( ) ☆☆☆☆
A.通入二氧化碳气体 B.加水稀释
C.通入氯化氢气体 D.加入饱和石灰水溶液
【解答】
A.CO 与水反应生成碳酸,c(H)、c(HCO ﹣)增大,故 A 错误;
2 +
3
B.加水稀释使氢氧根离子的浓度减小,氢离子浓度增大,故 B 错误;
C.HCl+NaHCO=NaCl+HO+CO↑,所以通入氯化氢气体后,碳酸氢根离子浓度减
3 2 2
小,碳酸根离子浓度减小,碳酸氢钠溶液呈碱性,通入氯化氢后溶液碱性减弱,
所以氢离子浓度增大,故 C 错误;
D.Ca(OH)+NaHCO=CaCO↓+HO+NaOH,所以加入饱和石灰水溶液后,碳酸氢根
2 3 3 2
离子转化为碳酸钙沉淀,所以碳酸氢根离子浓度、碳酸根离子浓度都减小,溶液
由弱碱性变为强碱性,所以氢离子浓度也减小,故 D 正确。
故选 D.
13.在 NHCl 饱和溶液中分别加入①Mg;②NHCl(固);③NHHCO;④HO;⑤氯
4 4 4 3 2
水;⑥Cu.能使该溶液的 pH 值增大的是( ) ☆☆☆☆
第 7页(共 21页)A.②③ B.①②⑤ C.②③⑥ D.①③④
【解答】
NH
4
Cl 饱和溶液中存在 NH
+
+H
2
O
⇌
NH
3
•H
2
O+H
+
,
4
①Mg 可以 H反应:Mg+2H =Mg2++H↑,氢离子参加反应导致 c(H)降低,pH 增大;
+ + 2 +
②饱和的 NH Cl 不溶解,故溶液中 c(H
4
Cl 溶液继续加入 NHCl 固体,NH )不变,
4 4 +
所以理论上不会影响溶液 pH 值;
③加入 NHHCO,由于 HCO 的酸性比盐酸弱,所以其溶液中水解生成的碳酸酸性
4 3 2 3
比盐酸弱,因此溶液的 pH 值就会比较高,往 NHCl 中加入它就会使 pH 值升高;
4
④加入大量的水后,促进 NHCl 水解,但 NHCl 水解增大程度小于溶液体积增大
4 4
程度,所以溶液中 c(H)降低,pH 增大;
+
⑤氯水是酸性的,且酸性大于 NHCl 溶液,加入后溶液中 c(H)增大,则溶液
4 +
的 pH 值会下降;
⑥Cu 不与 NHCl 反应,所以不影响 NHCl 水解,溶液中 c(H)不变,则 pH 值理
4 4 +
论上没影响,
所以能使该溶液的 pH 增大的是 Mg、NHHCO、HO
4 3 2
故选 D.
14.对于某酸的酸式盐 NaHY 的水溶液的下列叙述中,正确的是( )
☆☆☆☆
A.该酸式盐的水溶液一定显酸性
B.在该盐溶液中,离子浓度为:c(Na)>c(Y2﹣)>c(HY﹣)>c(OH﹣)>c
+
(H)
+
C.若 HY ﹣+H
2
O
⇌
Y2﹣+H
﹣能水解,水解方程式为:HY O
3
+
D.若 HY﹣能电离,电离方程式为:HY
﹣+H
2
O
⇌
Y2﹣+H
3
O
+
【解答】
A、如果 HY﹣的水解程度大于电离程度,溶液呈碱性,如果电离大于水解溶液呈酸性,故 A 错误;
第 8页(共 21页)B、不知电离和水解程度的大小,所以无法比较 c(Y2﹣)和 c(HY﹣)、c(OH﹣)
和 c(H)的大小,故 B 错误;
+
C、若 HY
﹣能水解,水解是结合水中的氢离子,水解方程式为:HY﹣+H
2
O
⇌
H
2
Y+OH﹣,
故 C 错误;
D、若 HY﹣能电离,电离方程式为:HY﹣+H
2
O
⇌
Y2﹣+H
3
O
+
,故 D 正确。
故选 D.
15.常温下,将 NHNO 溶于水得无色溶液,为使该溶液中的 c(NH ):c(NO -)
4 3 +
4 3
=1:1,可以采取的下列措施是( ) ☆☆☆☆
A.加入适量的 HNO
,抑制 NH 水解
3 +
4
B.加入适量的氨水,使溶液的 pH 等于 7
C.再加入适量的 NHNO(s)
4 3
D.加入适量的 NaOH,使溶液的 pH 等于 7
【解答】
A.加入硝酸,氢离子的浓度增大能抑制铵根离子的水解,但硝酸中有硝酸根离
子导致硝酸根离子的浓度增大,铵根离子与硝酸根离子的浓度不是 1:1,故 A
错误;
B.加入氨水使溶液的 PH=7,溶液中氢离子浓度等于氢氧根离子浓度,溶液呈中
性,溶液中阴阳离子所带的电荷相等,所以 c(NH ):c(NO ﹣)=l:l,故 B 正
+
4 3
确;
C.再加入适量的 NHNO,不能抑制铵根离子的水解,仍存在 c(NH ):c(NO ﹣)
4 3 +
4 3
小于 l:l,故 C 错误;
D.加入适量的 NaOH,使溶液的 pH=7,溶液中氢离子浓度等于氢氧根离子浓度,
溶液呈中性,溶液中阴阳离子所带的电荷相等,[c(NH )+C(Na )]:c(NO ﹣)
+ +
4 3
=l:l,所以 c(NH ):c(NO ﹣)小于 l:l,故 D 错误。
+
4 3
故选 B.16.下列关于电解质溶液的叙述正确的是( ) ☆☆☆☆
第 9页(共 21页)A.在 pH=3 的溶液中,Na、Cl﹣、Fe2+、ClO﹣可以大量共存
+
B.pH=11 的 NaOH 溶液与 pH=3 的醋酸溶液等体积混合,滴入石蕊溶液呈红色
C.常温下,pH=7 的 NH
Cl 与氨水的混合溶液中:c(Cl﹣)>c(NH )>c(H)
4 + +
4
=c(OH﹣)
D.向 0.1mol•L
﹣1 的氨水中加入少量硫酸铵固体,则溶液中 c(OH﹣)/c(NH•HO)
3 2
增大
【解答】
A、在 pH=3 的溶液中,Fe2+、ClO﹣可以发生氧化还原反应不能大量共存,故 A 错
误;
B、pH=11 的 NaOH 溶液与 pH=3 的醋酸溶液等体积混合,酸剩余,溶液显示酸性,
滴入石蕊溶液呈红色,故 B 正确;
C、常温下,pH=7 的 NHCl 与氨水的混合溶液中 c(H)=c(OH﹣),存在电荷守恒:
4 +
c(Cl﹣)+c(OH﹣)=c(NH )+c(H),所以:c(Cl﹣)=c(NH )>c(H)=c
+ + + +
4 4
(OH﹣),故 C 错误;
D、向 0.1mol/L 的氨水中加入少量硫酸铵固体,溶液中铵根离子浓度增大,抑制
了一水合氨的电离,则一水合氨的浓度增大,氢氧根离子的浓度减小,则溶液中
氢氧根离子浓度和一水合氨浓度比值是减小的,故 D 错误;
故选 B.
17.常温下,体积相同、物质的量浓度相同的三种盐 NaX、NaY、NaZ 的溶液 pH
分别为 7、9、10,则下列说法不正确的是( ) ☆☆☆☆
A.酸性强弱 HX>HY>HZ
B.有两种盐能发生水解
C.分别稀释上述三种溶液,pH 均变小
D.三种溶液中离子总数不相同
【解答】
A.相同物质的量浓度的钠盐溶液,溶液的 pH 越大,酸根离子的水解程度越大,第 10页(共 21页)其相应的酸的酸性越弱,根据题意知,在三种酸 HX、HY、HZ 中酸性强弱为 HX>
HY>HZ,故正确;
B.NaX、NaY、NaZ 水溶液 pH 分别为 7、9、10,说明后两种盐都是强碱弱酸盐,
能水解,pH=7 的钠盐不水解,故正确;
C.相同物质的量浓度的三种溶液,分别稀释,pH=7 的钠盐不水解,稀释后 pH
不变,故 C 错误;
D.NaX、NaY、NaZ 水溶液 pH 分别为 7、9、10,后两种盐都是强碱弱酸盐,能水
解,pH=7 的钠盐不水解,溶质在溶液中的粒子数也不一定相同,三种溶液中离
子总数不一定相同,故 D 正确。
故选 C.
18.下列应用与盐类的水解无关的是( ) ☆☆☆
A.纯碱溶液可去除油污
B.NaCl 可用作防腐剂和调味剂
C.TiCl 溶于大量水加热制备 TiO
4
2
D.FeCl 饱和溶液滴入沸水中制 Fe(OH) 胶体
3 3
【解答】
A、纯碱水解,溶液显碱性,有利于油脂的水解,与盐类水解有关,故 A 不选;
B、氯化钠溶液不发生水解,故 B 符合题意,故 B 选;
C、TiCl
4
溶于大量水发生反应 TiCl
4
+(2+x)H
2
O
⇌
TiO
2
•xH
2
O+4HCl,加入大量水
并加热,HCl 挥发,促使水解正向进行,故 C 不选;
D、制 Fe(OH) 胶体利用是溶液中三价铁离子的水解,故 D 不选。
3
故选 B.
19.在空气中直接蒸发下列盐的溶液:①Fe(SO)②NaCO③KCl④CuCl⑤NaHCO
4 3 2 3 2
2 3
可以得到相应盐的晶体(可以含有结晶水)的是( ) ☆☆☆
A.①③⑤ B.①②③ C.②④ D.①③④⑤
第 11页(共 21页)【解答】
①Fe(SO) 加热时虽发生水解,但硫酸难挥发,加入溶液可生成 Fe(SO),
2 4 3 2 4 3
故正确;
②NaCO 水解生成氢氧化钠,但氢氧化钠不稳定,在空气中仍生成碳酸钠,故正
2 3
确;
③KCl 性质稳定,加热溶液可生成 KCl,故正确;
④CuCl 溶液水解生成氢氧化铜和盐酸,盐酸挥发,最后生成氢氧化铜,故错误;
2
⑤NaHCO 不稳定,加热分解生成碳酸钠,故错误。
3
故选 B.
20.将 AlCl 溶液和 NaAlO 溶液分别蒸干灼烧,对产物的主要成分叙述正确的是
3 2
( ) ☆☆☆
A.均为 Al(OH) B.前者为 AlO,后者为 NaAlO
3 2 3
2
C.均为 AlO D.前者为 AlCl,后者为 NaAlO
2 3 3
2
【解答】
AlCl 溶液加热时水解生成 Al(OH),生成的 HCl 易挥发,最终生成 Al(OH),
3 3 3
在加强热时,Al(OH) 不稳定,分解生成 AlO;
3 2 3
NaAlO 溶液加入水解生成 Al(OH) 与 NaOH,最终又反应生成 NaAlO,NaAlO 溶
2 3 2 2
液蒸发并灼烧得到 NaAlO
2
故选 B.
21.在 20mL 0.1mol•L HCl 溶液中加入同体积、同物质的量浓度的 NH•HO 溶液,
3 2
反应后溶液中各粒子浓度的关系错误的是( ) ☆☆☆☆☆
A.c(H)+c(NH )=c(OH﹣)+c(Cl﹣)
+ +
4
B.c(H)=c(OH﹣)+c(NH •HO)
+ 3 2
C.c(Cl﹣)>c(NH )>c(OH﹣)>c(H)
+ +
4
D.c(Cl﹣)=c(NH
+
)+c(NH
3
•H
2
O)
4第 12页(共 21页)【解答】
A.根据电荷守恒可知:c(H)+c(NH )=c(OH﹣)+c(Cl﹣),故 A 正确;
+ +
4
B.反应后溶质为 NH
Cl,根据 NHCl 溶液中的质子守恒可得 c(H)=c(OH﹣)
4 4 +
+c(NH •HO),故 B 正确;
3 2
C.二者恰好反应生成 NHCl,铵根离子水解溶液呈酸性,则 c(H)>c(OH﹣),
4 +
结合电荷守恒可知 c(Cl﹣)>c(NH ),则反应后溶液中离子浓度大小为 c(Cl
+
4
﹣)>c(NH )>c(H)>c(OH﹣),故 C 错误;
+ +
4
D.根据 NH •HO),故 D
3 2
4
Cl 溶液中的物料守恒可知:c(Cl﹣)=c(NH
+
)+c(NH
4
正确。
故选 C.
22.常温下,下列溶液中的微粒浓度关系正确的是( ) ☆☆☆☆☆
A.pH=8.3 的 NaHCO 溶液:c(Na)>c(HCO ﹣)>c(CO 2﹣)>c(HCO)
3 + 2 3
3 3
B.pH=2 的 HPO 溶液:c(H)=c(HPO ﹣)+2c(HPO 2﹣)+3c(PO 3﹣)
3 4 + 2
4 4 4
+c(OH﹣)
C.pH=11 氨水与 pH=3 的盐酸等体积混合:
c(C1﹣)=c(NH )>c(OH﹣)=c(H)
+ +
4
D.0.2mol/L CHCOOH 溶液与 0.1mol/L NaOH 溶液等体积混合
3
c(Na
)=c(CHCOO﹣)+c(CHCOOH)
+ 3 3
【解答】
A、pH=8.3 的 NaHCO 溶液呈碱性,说明 HCO ﹣的水解程度大于其电离程度,则 c
3
3
(HCO)>c(CO 2﹣),正确的离子浓度大小为:
2 3
3
c(Na
)>c(HCO ﹣)>c(HCO)>c(CO 2﹣),故 A 错误;
+ 2 3
3 3
B、根据 pH=2 的 HPO 溶液中的质子守恒可知:
3 4c(H)=c(HPO ﹣)+2c(HPO 2﹣)+3c(PO 3﹣)+c(OH﹣),故 B 正确;
+ 2
4 4 4
C、pH=11 的氨水与 pH=3 的盐酸等体积混合,氨水过量导致溶液呈碱性:
第 13页(共 21页)c(NH )>c(C1﹣)>c(OH﹣)>c(H),故 C 错误;
+ +
4
D、二者混合时,溶液中的溶质是等物质的量浓度的 CHCOOH 和 CHCOONa,溶液
3 3
中存在物料守恒:2c(Na)=c(CHCOO﹣)+c(CHCOOH),故 D 错误;
+ 3 3
故选 B.
23.室温下,下列溶液中粒子浓度关系正确的是( ) ☆☆☆☆☆
A.NaS 溶液:c(Na)>c(HS﹣)>c(OH﹣)>c(HS)
2 + 2
B.NaCO 溶液:c(OH﹣)=c(H)+c(HCO ﹣)+c(HCO)
2 2 4 + 2 2 2 4
4
C.NaCO 溶液:c(Na)+c(H)=2c(CO 2﹣)+c(OH﹣)
2 3 + +
3
D.CHCOONa 和 CaCl 混合溶液:c(Na)+2c(Ca2+)=c(CHCOO﹣)+c(CHCOOH)
3 2 + 3 3
+c(Cl﹣)
【解答】
A.Na
2
S 溶液中硫离子分步水解,S2﹣+H
2
O
⇌
HS﹣+OH﹣,HS﹣+H
2
O
⇌
H
2
S+OH﹣,溶液中
离子浓度大小为:c(Na)>c(OH﹣)>c(HS﹣)>c(HS),故 A 错误;
+ 2
B.NaCO 溶液中存在质子守恒:c(OH﹣)=c(H)+c(HCO ﹣)+2c(HCO),故
2 2 4 + 2 2 2 4
4
B 错误;
C.碳酸钠溶液中存在电荷守恒,c(Na)+c(H)=2c(CO 2﹣)+c(OH﹣)
+ +
3
+c(HCO ﹣),故 C 错误;
3
D.CHCOONa 和 CaCl 混合溶液中存在物料守恒,醋酸根离子和醋酸分子浓度总
3 2
和和钠离子浓度相同,氯化钙溶液中氯离子浓度为钙离子浓度 2 倍,CHCOONa
3
和 CaCl 混合溶液:c(Na)+2c(Ca2+)=c(CHCOO﹣)+c(CHCOOH)+c(Cl﹣),
2 + 3 3
故 D 正确;
故选 D.
24.常温常压时,下列叙述不正确的是( ) ☆☆☆☆☆
A.20mL 0.1mol/L CHCOONa 溶液与 10mL 0.1 mol/L HCl 溶液混合后溶液呈酸性,
3
所得溶液中:c(CHCOO﹣)>c(Cl﹣)>c(CHCOOH)>c(H)
3 3 +
B.含等物质的量的 NaHC 2 O 4 和 Na 2 C 2 O 4 的混合溶液:2c(Na + )=3[c(HC 2 O ﹣)+c
4第 14页(共 21页)(CO CO
2 2 2
2﹣)+c(H )]
4
4
C.PH=1 的 NaHSO ﹣)
4
溶液:c(H
+
)=c(SO 2﹣)+c(OH
4
D.CO 的水溶液:c(H)>c(HCO ﹣)=2c(CO 2﹣)
2 +
3 3
【解答】
A.20mL 0.1mol/L CHCOONa 溶液与 10mL 0.1 mol/L HCl 溶液混合后,溶质为等
3
浓度的 CHCOOH、NaCl、CHCOONa,溶液呈酸性,说明 CHCOOH 的电离程度大于
3 3 3
CHCOO﹣的水解程度,则 c(CHCOO﹣)>c(CHCOOH),结合物料守恒可知:
3 3 3
c(CHCOO﹣)>c(Cl﹣)>c(CHCOOH),所得溶液中粒子浓度大小为:
3 3
c(CHCOO﹣)>c(Cl﹣)>c(CHCOOH)>c(H),故 A 正确;
3 3 +
B.含等物质的量的 NaHCO 和 NaCO 的混合溶液中,根据物料守恒可得:
2 4 2 2 4
2c(Na)=3[c(HCO ﹣)+c(CO 2﹣)+c(HCO)],故 B 正确;
+ 2 2 2 2 4
4 4
C.pH=1 的 NaHSO 溶液中,根据物料守恒可得:c(Na)=c(SO 2﹣),根据电荷
4 +
4
守恒可得:c(H)+c(Na)=2c(SO 2﹣)+c(OH﹣),二者结合可得:
+ +
4
c(H)=c(SO 2﹣)+c(OH﹣),故 C 正确;
+
4
D.CO 的水溶液中,由于碳酸氢根离子的电离程度较小,
2
则 c(HCO ﹣)>>c(CO 2﹣),所以正确的离子浓度大小为:c(H)>c(HCO ﹣)
+
3 3 3
>2c(CO 2﹣),故 D 错误;
3
故选 D.
25.下列溶液中,微粒浓度关系正确的是( ) ☆☆☆☆☆
A.含有 NH 、Cl﹣、H、OH﹣的溶液中,其离子浓度一定是:c(Cl﹣)>c(NH )
+ + +
4 4
>c(H)>c(OH﹣)
+
B.pH=6 的醋酸与醋酸钠的混合溶液中,c(Na)>c(CHCOO﹣)
+ 3
C.0.1 mol/L 的 NaS 溶液中,c(OH )+c(HS
2 +
﹣)=c(H ﹣)+2c(HS)
2
D.pH=3 的一元酸和 pH=11 的一元碱等体积混和后的溶液中,一定是 c(OH﹣)=
c(H)
+【解答】
第 15页(共 21页)A、含有 NH 、Cl﹣、H、OH﹣的溶液中,其组成情况可以是盐酸和氯化铵的混合液,
+ +
4
可能存在 c(Cl﹣)>c(H)>c(NH )>c(OH﹣),故 A 错误;
+ +
4
B、pH=6 的醋酸与醋酸钠的混合溶液中,说明醋酸的电离程度大于水解程度,
c(OH ),根据电荷守恒 c(OH
+
﹣)<c(H ﹣)+c(CHCOO﹣)=c(H)+c(Na),
3 + +
则 c(Na)<c(CHCOO﹣),故 B 错误;
+ 3
C、NaS 溶液中,遵循质子守恒:c(OH﹣)=c(H)+c(HS﹣)+2c(HS),故 C
2 + 2
正确;
D、pH=3 的一元酸和 pH=11 的一元碱等体积混和后的溶液的酸碱性和酸碱的强弱
有关,当酸是弱酸时,则 c(OH﹣)<c(H),碱是弱碱时,c(OH﹣)>c(H),
+ +
只有是强酸强碱时,才存在 c(OH﹣)=c(H),故 D 错误.
+
故选 C.
26.将标准状况下 2.24L CO 缓慢通入 1L 0.15mol•L﹣1 的 NaOH 溶液中,气体被
2
充分吸收,下列关系不正确的是( ) ☆☆☆☆☆
A.c(Na)>c(CO 2﹣)>c(HCO ﹣)>c(OH﹣)>c(H)
+ +
3 3
B.c(Na)+c(H)=c(OH﹣)+c(HCO ﹣)+2c(CO 2﹣)
+ +
3 3
C.2c(Na)=3[c(HCO)+c(HCO ﹣)+c(CO 2﹣)]
+ 2 3
3 3
D.2c(OH﹣)+c(CO 2﹣)=c(HCO ﹣)+3c(HCO)+2c(H)
2 3 +
3 3
【解答】
n(CO)= =0.1mol,n(NaOH)=1L×0.15mol/L=0.15mol,分析可得
2
产物生成 0.05mol NaCO 和 0.05mol NaHCO,
2 3 3
A、CO 2﹣的水解程度>HCO ﹣的且水解程度都较小,则 c(HCO ﹣)>c(CO 2﹣)>
3 3 3 3
c(OH﹣),则有 c(Na)>c(HCO ﹣)>c(CO 2﹣)>c(OH﹣)>c(H),故 A 错
+ +
3 3
误;
B、溶液呈电中性,溶液中阴阳离子所带电荷相等,所以 c(Na)+c(H)=
+ +
c(OH﹣)+c(HCO ﹣)+2c(CO 2﹣),故 B 正确;
3 3
C、n(CO ﹣)+n(HCO
2
2﹣)+n(HCO )=0.1mol,n(Na)=0.15mol,根据物料守
3 +
3 3恒得,2C(Na)=3[c(HCO)+c(HCO ﹣)+c(CO 2﹣)],故 C 正确;
+ 2 3
3 3
第 16页(共 21页)D、根据电荷守恒得 c(Na)+c(H)=c(OH﹣)+c(HCO ﹣)+2c(CO 2﹣)①,
+ +
3 3
根据物料守恒得 2c(Na)=3[c(HCO)+c(HCO ﹣)+c(CO 2﹣)]②,将方程式
+ 2 3
3 3
②﹣①×2 得 2c(OH﹣)+c(CO 2﹣)=c(HCO ﹣)+3c(HCO)+2c(H),故 D 正确。
2 3 +
3 3
故选 A.
27.25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
☆☆☆☆☆
A.0.1 mol•L ﹣1 HCl 溶液等体积混合:
﹣1 CHCOONa 溶液与 0.1 mol•L
3
c(Na)=c(Cl﹣)>c(CHCOO﹣)>c(OH﹣)
+ 3
B.0.1 mol•L﹣1 NHCl 溶液与 0.1 mol•L﹣1 氨水等体积混合(pH>7):
4
c(NH•HO)>c(NH )>c(Cl﹣)>c(OH﹣)
3 2 +
4
C.0.1 mol•L﹣1 NaCO 溶液与 0.1 mol•L﹣1 NaHCO 溶液等体积混合:
2 3 3
c(Na)=c(CO 2﹣)+c(HCO ﹣)+c(HCO)
+ 2 3
3 3
D.0.1 mol•L﹣1 NaCO 溶液与 0.1 mol•L﹣1 HCl 溶液等体积混合(HCO 为二元
2 2 4 2 2 4
弱酸):2c(C 2﹣)+c(HCO ﹣)+c(OH )+c(H)
2 + +
O ﹣)=c(Na
2
4 4
【解答】
A.0.1 mol•L﹣1 CHCOONa 溶液与 0.1 mol•L﹣1 HCl 溶液等体积混合,溶质为醋酸
3
和氯化钠,醋酸为弱酸部分电离 c(Na)=c(Cl﹣)>c(CHCOO﹣)>c(OH﹣),
+ 3
故 A 正确;
B.0.1 mol•L﹣1 NH
Cl 溶液与 0.1 mol•L﹣1 氨水等体积混合(pH>7),溶液显碱
4
性说明一水合氨电离程度大于铵根离子的水解程度,c(NH•HO)<c(NH ),故
3 2 +
4
B 错误:
C.0.1 mol•L﹣1 Na 溶液与 0.1 mol•L
3
CO ﹣1 NaHCO 溶液等体积混合溶液中存在物
2 3
料守恒,2n(Na)=3n(C),钠离子总物质的量等于碳元素所有存在形式总和,
2c(Na)=3[c(CO )],则 C 错误;
+ 3
2﹣)+c(HCO ﹣)+c(HCO
2
3 3D.0.1 mol•L﹣1 Na
CO 溶液与 0.1 mol•L﹣1 HCl 溶液等体积混合得到等浓度 NaCl
2 2 4
和 NaHCO,溶液中存在电荷守恒,2c(CO 2﹣)+c(HCO ﹣)+c(OH﹣)+c(Cl﹣)
2 4 2 2
4 4
=c(Na)+c(H),故 D 错误。
+ +
第 17页(共 21页)故选 A.
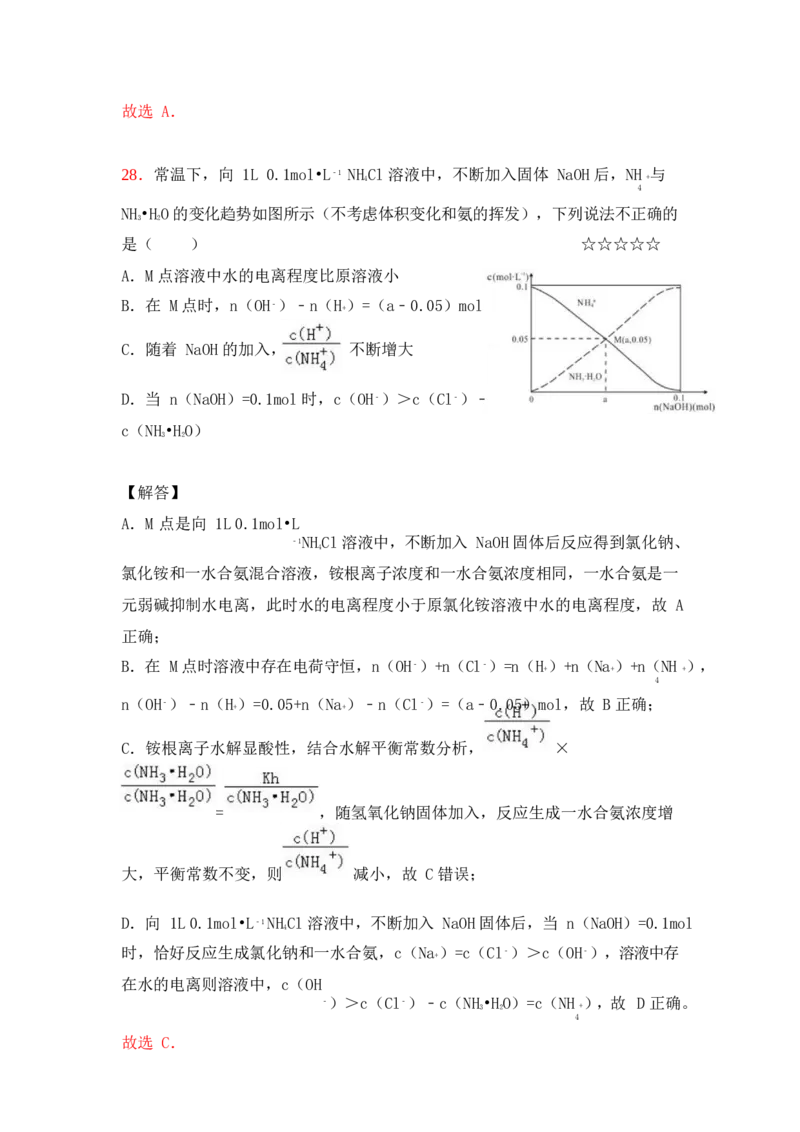
28.常温下,向 1L 0.1mol•L﹣1 NH
4
Cl 溶液中,不断加入固体 NaOH 后,NH
+
与
4
NH•HO 的变化趋势如图所示(不考虑体积变化和氨的挥发),下列说法不正确的
3 2
是( ) ☆☆☆☆☆
A.M 点溶液中水的电离程度比原溶液小
B.在 M 点时,n(OH﹣)﹣n(H)=(a﹣0.05)mol
+
C.随着 NaOH 的加入, 不断增大
D.当 n(NaOH)=0.1mol 时,c(OH﹣)>c(Cl﹣)﹣
c(NH•HO)
3 2
【解答】
A.M 点是向 1L 0.1mol•L
﹣1NHCl 溶液中,不断加入 NaOH 固体后反应得到氯化钠、
4
氯化铵和一水合氨混合溶液,铵根离子浓度和一水合氨浓度相同,一水合氨是一
元弱碱抑制水电离,此时水的电离程度小于原氯化铵溶液中水的电离程度,故 A
正确;
B.在 M 点时溶液中存在电荷守恒,n(OH﹣)+n(Cl﹣)=n(H)+n(Na)+n(NH ),
+ + +
4
n(OH﹣)﹣n(H)=0.05+n(Na)﹣n(Cl﹣)=(a﹣0.05)mol,故 B 正确;
+ +
C.铵根离子水解显酸性,结合水解平衡常数分析, ×
= ,随氢氧化钠固体加入,反应生成一水合氨浓度增
大,平衡常数不变,则 减小,故 C 错误;
D.向 1L 0.1mol•L﹣1 NHCl 溶液中,不断加入 NaOH 固体后,当 n(NaOH)=0.1mol
4
时,恰好反应生成氯化钠和一水合氨,c(Na)=c(Cl﹣)>c(OH﹣),溶液中存
+
在水的电离则溶液中,c(OH
﹣)>c(Cl﹣)﹣c(NH•HO)=c(NH ),故 D 正确。
3 2 +
4
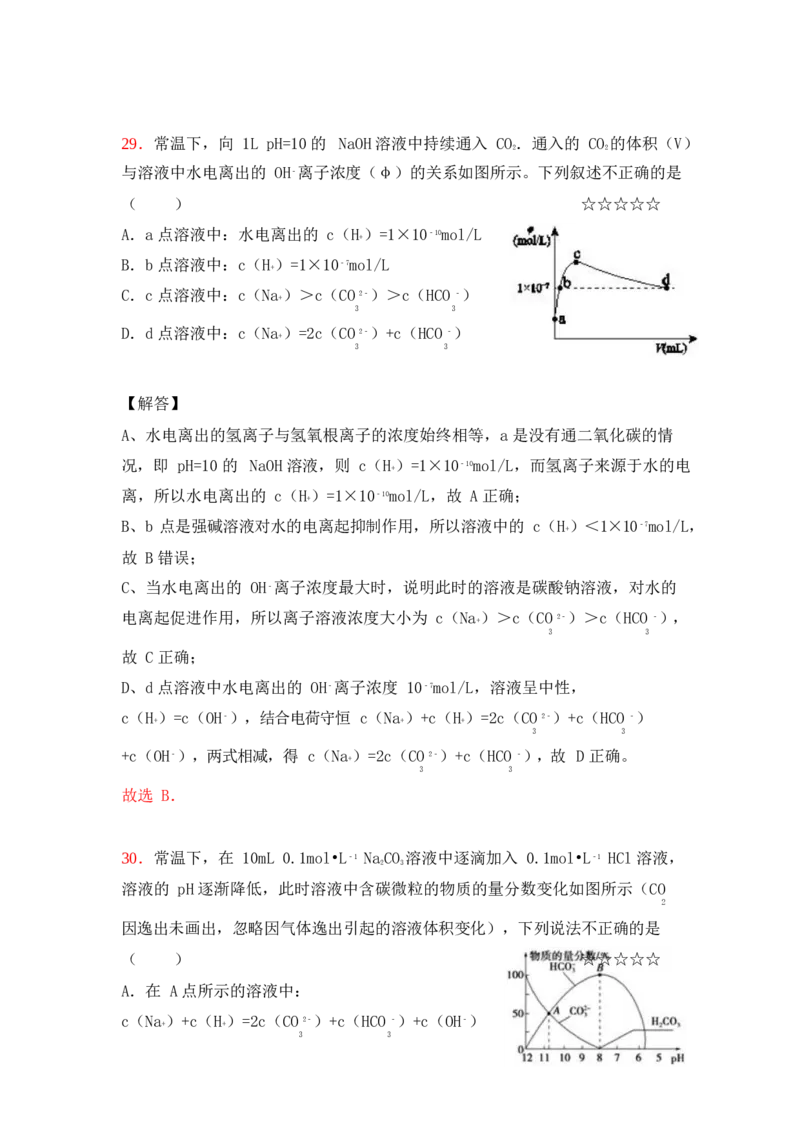
故选 C.第 18页(共 21页)29.常温下,向 1L pH=10 的 NaOH 溶液中持续通入 CO.通入的 CO 的体积(V)
2 2
与溶液中水电离出的 OH﹣离子浓度(φ)的关系如图所示。下列叙述不正确的是
( ) ☆☆☆☆☆
A.a 点溶液中:水电离出的 c(H)=1×10﹣10mol/L
+
B.b 点溶液中:c(H)=1×10﹣7mol/L
+
C.c 点溶液中:c(Na)>c(CO 2﹣)>c(HCO ﹣)
+
3 3
D.d 点溶液中:c(Na)=2c(CO 2﹣)+c(HCO ﹣)
+
3 3
【解答】
A、水电离出的氢离子与氢氧根离子的浓度始终相等,a 是没有通二氧化碳的情
况,即 pH=10 的 NaOH 溶液,则 c(H)=1×10﹣10mol/L,而氢离子来源于水的电
+
离,所以水电离出的 c(H)=1×10﹣10mol/L,故 A 正确;
+
B、b 点是强碱溶液对水的电离起抑制作用,所以溶液中的 c(H)<1×10﹣7mol/L,
+
故 B 错误;
C、当水电离出的 OH﹣离子浓度最大时,说明此时的溶液是碳酸钠溶液,对水的
电离起促进作用,所以离子溶液浓度大小为 c(Na)>c(CO 2﹣)>c(HCO ﹣),
+
3 3
故 C 正确;
D、d 点溶液中水电离出的 OH﹣离子浓度 10﹣7mol/L,溶液呈中性,
c(H)=c(OH﹣),结合电荷守恒 c(Na)+c(H)=2c(CO 2﹣)+c(HCO ﹣)
+ + +
3 3
+c(OH﹣),两式相减,得 c(Na)=2c(CO 2﹣)+c(HCO ﹣),故 D 正确。
+
3 3
故选 B.
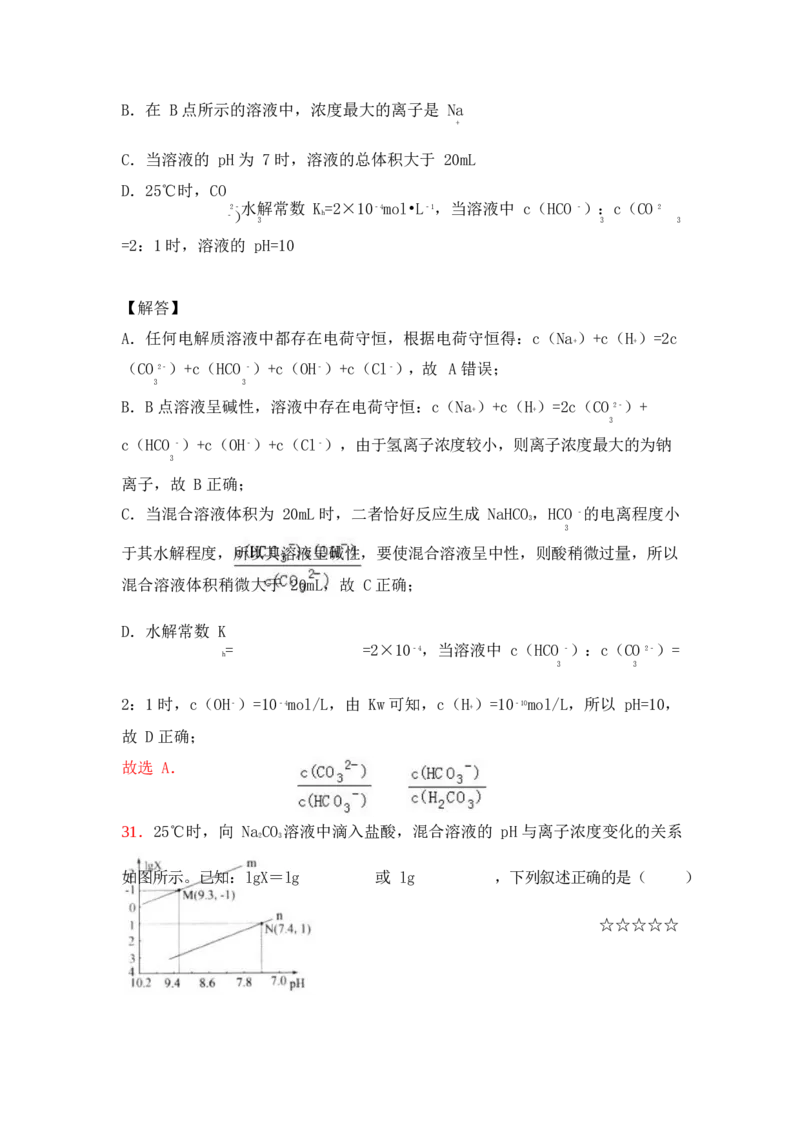
30.常温下,在 10mL 0.1mol•L﹣1 NaCO 溶液中逐滴加入 0.1mol•L﹣1 HCl 溶液,
2 3
溶液的 pH 逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示(CO
2
因逸出未画出,忽略因气体逸出引起的溶液体积变化),下列说法不正确的是
( ) ☆☆☆☆☆
A.在 A 点所示的溶液中:
c(Na)+c(H)=2c(CO 2﹣)+c(HCO ﹣)+c(OH﹣)
+ +
3 3第 19页(共 21页)B.在 B 点所示的溶液中,浓度最大的离子是 Na
+
C.当溶液的 pH 为 7 时,溶液的总体积大于 20mL
D.25℃时,CO
2﹣水解常数 K=2×10﹣4mol•L﹣1,当溶液中 c(HCO ﹣):c(CO 2
﹣) h
3 3 3
=2:1 时,溶液的 pH=10
【解答】
A.任何电解质溶液中都存在电荷守恒,根据电荷守恒得:c(Na)+c(H)=2c
+ +
(CO 2﹣)+c(HCO ﹣)+c(OH﹣)+c(Cl﹣),故 A 错误;
3 3
B.B 点溶液呈碱性,溶液中存在电荷守恒:c(Na)+c(H)=2c(CO 2﹣)+
+ +
3
c(HCO ﹣)+c(OH﹣)+c(Cl﹣),由于氢离子浓度较小,则离子浓度最大的为钠
3
离子,故 B 正确;
C.当混合溶液体积为 20mL 时,二者恰好反应生成 NaHCO,HCO ﹣的电离程度小
3
3
于其水解程度,所以其溶液呈碱性,要使混合溶液呈中性,则酸稍微过量,所以
混合溶液体积稍微大于 20mL,故 C 正确;
D.水解常数 K
= =2×10﹣4,当溶液中 c(HCO ﹣):c(CO 2﹣)=
h
3 3
2:1 时,c(OH﹣)=10﹣4mol/L,由 Kw 可知,c(H)=10﹣10mol/L,所以 pH=10,
+
故 D 正确;
故选 A.
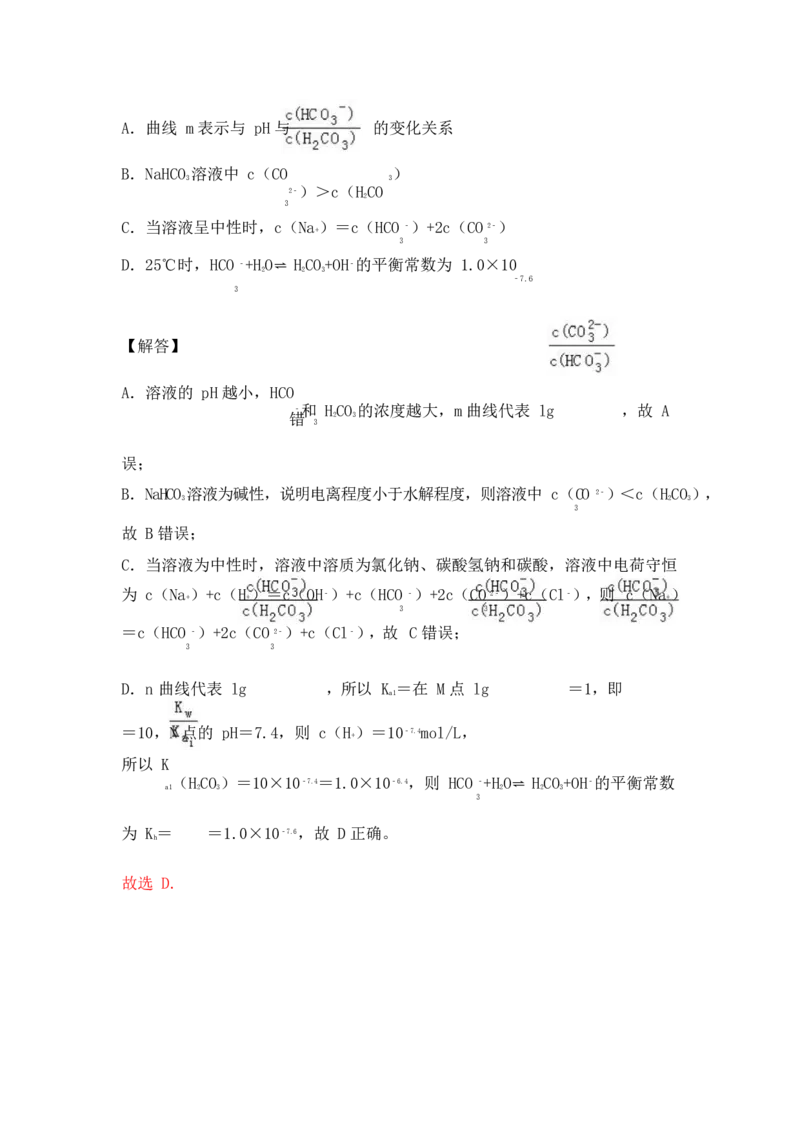
31.25℃时,向 NaCO 溶液中滴入盐酸,混合溶液的 pH 与离子浓度变化的关系
2 3
如图所示。已知:lgX=lg 或 lg ,下列叙述正确的是( )
☆☆☆☆☆第 20页(共 21页)A.曲线 m 表示与 pH 与 的变化关系
B.NaHCO 溶液中 c(CO )
3 3
2﹣)>c(HCO
2
3
C.当溶液呈中性时,c(Na)=c(HCO ﹣)+2c(CO 2﹣)
+
3 3
D.25℃时,HCO ﹣+H
2
O
⇌
H
2
CO
3
+OH﹣的平衡常数为 1.0×10
﹣7.6
3
【解答】
A.溶液的 pH 越小,HCO
﹣和 HCO 的浓度越大,m 曲线代表 lg ,故 A
错 2 3
3
误;
B.NaHCO 溶液为碱性,说明电离程度小于水解程度,则溶液中 c(CO 2﹣)<c(HCO),
3 2 3
3
故 B 错误;
C.当溶液为中性时,溶液中溶质为氯化钠、碳酸氢钠和碳酸,溶液中电荷守恒
为 c(Na)+c(H)=c(OH﹣)+c(HCO ﹣)+2c(CO 2﹣)+c(Cl﹣),则 c(Na)
+ + +
3 3
=c(HCO ﹣)+2c(CO 2﹣)+c(Cl﹣),故 C 错误;
3 3
D.n 曲线代表 lg ,所以 K =在 M 点 lg =1,即
a1
=10,N 点的 pH=7.4,则 c(H)=10﹣7.4mol/L,
+
所以 K
a1
(H
2
CO
3
)=10×10﹣7.4=1.0×10﹣6.4,则 HCO ﹣+H
2
O
⇌
H
2
CO
3
+OH﹣的平衡常数
3
为 K= =1.0×10﹣7.6,故 D 正确。
h
故选 D.第 21页(共 21页)