文档内容
硫及其化合物作业题
作业题目难度分为3档:三星☆☆☆(基础题目)
四星☆☆☆☆(中等题目)
五星☆☆☆☆☆(较难题目)
本套作业题目1-4,6,8,10-11,17,23题为三星,5,7,9,12-16,18-22为四星。
1.有关硫及其化合物说法正确的是( ) ☆☆☆
A.有浓硫酸参与的反应都是氧化还原反应
B.硫在足量空气中燃烧生成大量 SO
3
C.SO 能使酸性高锰酸钾溶液褪色,体现了漂白性
2
D.二氧化硫可用于抑制酒类中细菌生长,可在葡萄酒中微量添加
【解答】
A、根据是否有化合价的变化,如氢氧化钠与浓硫酸反应是酸碱中和反应,非氧
化还原反应,故A错误;
B、硫与氧气反应只生成二氧化硫,不能生成三氧化硫,故 B错误;
C、SO 能使酸性高锰酸钾溶液褪色,是氧化还原反应,是还原性,而不是漂白性,
2
故C错误;
D、二氧化硫具有较强的还原性,故常用作葡萄酒的抗氧化剂,所以二氧化硫可
用于抑制酒类中细菌生长,故 D正确;
故选D.
2.下列关于硫及其化合物的说法中正确的是( ) ☆☆☆
A.SO 和Cl 按1:1混合通入水中后可能使品红褪色
2 2
B.二氧化硫的排放会导致光化学烟雾和酸雨的产生
C.单质硫在自然界只以化合态存在
D.浓硫酸可用来干燥SO、CO、Cl 等气体
2 2
第1页(共14页)【解答】
A.SO 和 Cl 混合通入水中发生氧化还原反应生成盐酸和硫酸,都不具有漂白性,
2 2
故A错误;
B.二氧化硫导致酸雨,氮氧化物导致光化学烟雾,故 B错误;
C.自然界中存在游离态的硫,如火山口存在游离态的硫,故 C错误;
D.SO、Cl 等为酸性气体,CO为中性气体,且都与浓硫酸不发生氧化还原反应,
2 2
可用浓硫酸来干燥,故D正确.
故选D.
3.下列关于硫及含硫化合物的叙述正确的是( ) ☆☆☆
A.SO 的漂白原理与次氯酸相同
2
B.硫在足量空气中燃烧生成大量 SO
3
C.浓硫酸可以干燥H、HS、CO 等气体
2 2 2
D.可用铝槽储运浓硫酸
【解答】
A.二氧化硫的漂白性是利用有色物质和二氧化硫反应生成无色物质,次氯酸的
漂白性是利用次氯酸的强氧化性,所以二者漂白原理不同,故 A错误;
B.硫在空气中燃烧生成二氧化硫而不是三氧化硫,故 B错误;
C.浓硫酸具有强氧化性,硫化氢具有还原性,浓硫酸可以氧化硫化氢生成单质
硫,不能用来干燥硫化氢,可以干燥中性气体H 和酸性气体CO,故C错误;
2 2
D.常温下,铝与浓硫酸发生钝化,在表面生成一层致密的氧化膜,阻止反应进
行,故D正确;
故选D.
4.下列物质能将品红氧化使品红溶液褪色的是( ) ☆☆☆
①活性炭 ②过氧化钠 ③氯水 ④二氧化硫 ⑤漂白粉
A.①②③④⑤ B.②③④⑤ C.②③④ D.②③⑤
第2页(共14页)【解答】
过氧化钠、氯水中的次氯酸、漂白粉具有强的氧化性,能够氧化有机色素生成无
色物质,所以具有漂白性,活性炭是因为吸附性而使物质漂白,二氧化硫与有色
物质化合生成无色物质而具有漂白性,所以能将品红氧化使品红溶液褪色的是过
氧化钠、氯水、漂白粉,
故选:D.
5.下列实验用来证明气体SO 的存在,其中正确的是( ) ☆☆☆☆
2
①能使品红溶液褪色
②能使湿润的蓝色石蕊试纸变红
③能使澄清的石灰水变浑浊
④通入足量的NaOH溶液中,再滴入BaCl 溶液,有白色沉淀生成,该沉淀溶于
2
盐酸
⑤通入到溴水使其褪色,再滴入 Ba(NO) 溶液,有白色沉淀生成.
3 2
A.①②④⑤ B.都不能证明 C.①⑤能证明 D.只有⑤能证明
【解答】
①能使品红溶液褪色的不一定为二氧化硫,可为氯气等,故错误;
②能使湿润的蓝色石蕊试纸变红的为酸性气体,不一定为二氧化硫,故错误;
③能使澄清的石灰水变浑浊也可能为二氧化碳等,故错误;
④通入足量的 NaOH 溶液中,再滴入 BaCl 溶液,有白色沉淀生成,该沉淀溶于
2
盐酸,不一定为二氧化硫,也可能为二氧化碳,故错误;
⑤通入溴水,溴水褪色,再加入Ba(NO) 溶液有白色沉淀生成,白色沉淀为硫
3 2
酸钡,则使溴水褪色的气体为二氧化硫,二氧化硫与溴水发生氧化还原反应,故
正确.
故选D.
第3页(共14页)6.下列说法正确的是( ) ☆☆☆
A.SO 能使品红溶液、溴水和酸性高锰酸钾溶液褪色是因为 SO 具有漂白性
2 2
B.SO 和 Cl 都有漂白作用,将等物质的量的两种气体同时作用于潮湿的有色物
2 2
质时,可增强漂白作用
C.活性炭使有色物质褪色是利用了碳单质具有还原性,使有色物质发生还原反
应
D.SO 使品红溶液褪色后,将褪色后的溶液加热,溶液重新变为红色
2
【解答】
A.SO 能使溴水和酸性高锰酸钾溶液褪色,均发生氧化还原反应,与二氧化硫的
2
还原性有关,故A错误;
B.等物质的量的两种气体,反应生成硫酸和盐酸,不具有漂白性,故 B错误;
C.活性炭使有色物质褪色,与吸附性有关,与碳的还原性无关,故 C错误;
D.SO 使品红溶液褪色,化合生成无色的物质,为暂时性漂白,将褪色后的溶液
2
加热,溶液重新变为红色,故 D正确;
故选D.
7.下列各组物质中,常温下Y既能与X反应又能与Z反应的是( )
☆☆☆☆
选项 X Y Z
A SO NaClO溶液 CO
2 2
B 盐酸 浓硫酸 Cu
C NH O Mg
3 2
D NaO HO SiO
2 2 2 2
【解答】
A、次氯酸钠是具有强氧化性的强碱弱酸盐,二氧化硫与次氯酸钠发生氧化还原
反应,与二氧化碳反应生成次氯酸,故A符合;
B、浓硫酸与盐酸不反应,常温下浓硫酸也不与Cu反应,故B不符合;
第4页(共14页)C、常温下氨气与氧气不反应,在点燃的条件下生成氮气,催化氧化生成一氧化
氮,故C不符合;
D、二氧化硅与水不反应,故 D不符合;
故选A.
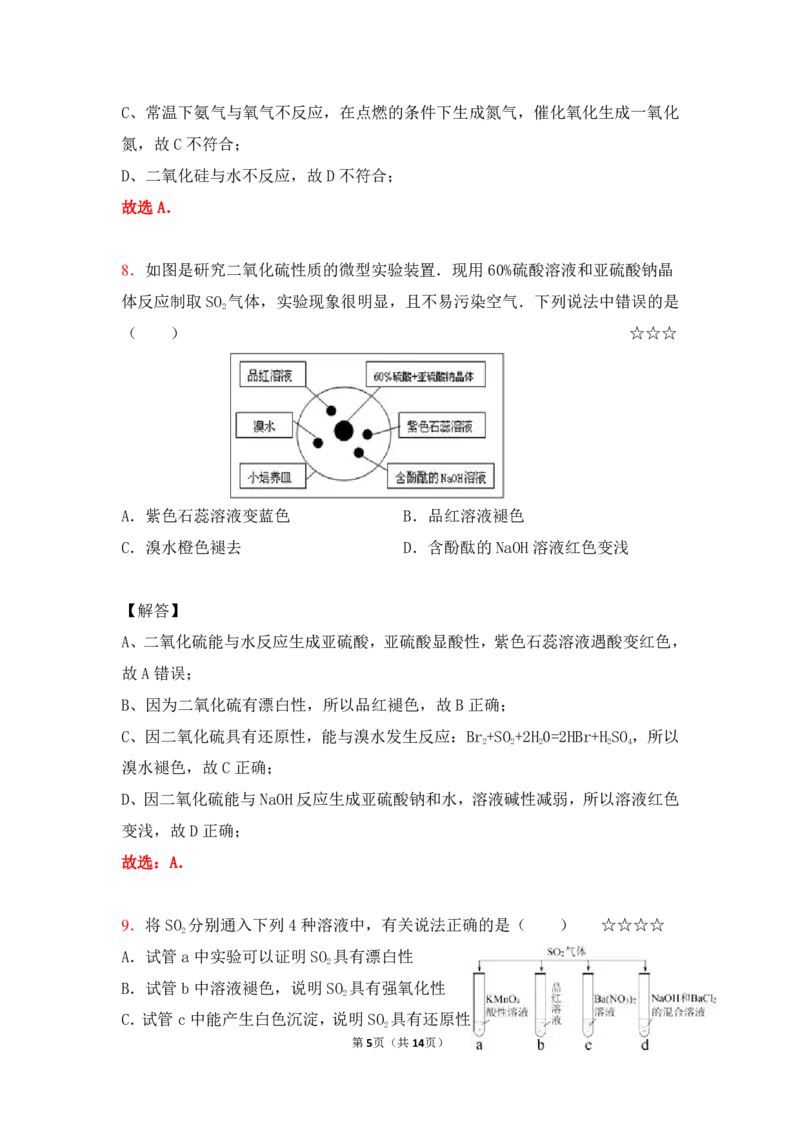
8.如图是研究二氧化硫性质的微型实验装置.现用60%硫酸溶液和亚硫酸钠晶
体反应制取SO 气体,实验现象很明显,且不易污染空气.下列说法中错误的是
2
( ) ☆☆☆
A.紫色石蕊溶液变蓝色 B.品红溶液褪色
C.溴水橙色褪去 D.含酚酞的NaOH溶液红色变浅
【解答】
A、二氧化硫能与水反应生成亚硫酸,亚硫酸显酸性,紫色石蕊溶液遇酸变红色,
故A错误;
B、因为二氧化硫有漂白性,所以品红褪色,故B正确;
C、因二氧化硫具有还原性,能与溴水发生反应:Br+SO+2H0=2HBr+HSO,所以
2 2 2 2 4
溴水褪色,故C正确;
D、因二氧化硫能与NaOH反应生成亚硫酸钠和水,溶液碱性减弱,所以溶液红色
变浅,故D正确;
故选:A.
9.将SO 分别通入下列4种溶液中,有关说法正确的是( ) ☆☆☆☆
2
A.试管a中实验可以证明SO 具有漂白性
2
B.试管b中溶液褪色,说明SO 具有强氧化性
2
C.试管c中能产生白色沉淀,说明SO 具有还原性
2
第5页(共14页)D.试管d中能产生白色沉淀,该沉淀完全溶于稀硝酸
【解答】
A.SO 与KMnO 酸性溶液发生氧化还原反应,表现了SO 的还原性,故A错误;
2 4 2
B.SO 使品红溶液褪色,表现了SO 的漂白性,故B错误;
2 2
C.SO 被溶液中的NO﹣和H+氧化为 SO2﹣,表现了SO 的还原性,故C正确;
2 3 4 2
D.SO 与NaOH 和BaCl 混合溶液反应生成BaSO,BaSO 被硝酸氧化为BaSO,BaSO
2 2 3 3 4 4
难溶于稀硝酸,故D错误;
故选C.
10.某冶炼厂利用炼铜产生的SO 生产硫酸,变废为宝,化害为利.其原理是( )
2
☆☆☆
A.利用了SO 的水溶性,将SO 直接通入水中
2 2
B.利用了SO 的氧化性,将SO 直接通入水中
2 2
C.利用了SO 的氧化性,使其与 O 反应而转化为SO,再与水反应
2 2 3
D.利用了SO 的还原性,使其与 O 反应而转化为SO,再与水反应
2 2 3
【解答】
二氧化硫直接通入水中得到的是亚硫酸;二氧化硫转化成硫酸,硫元素化合价升
高,二氧化硫发生氧化反应,体现了二氧化硫的还原性;
故选:D.
11.下列有关物质性质和应用的因果关系正确的是( ) ☆☆☆
A.二氧化硫具有漂白性,能使氯水褪色
B.浓硫酸具有较强酸性,能使 Cu转化为Cu2+
C.硅具有还原性,一定条件下能将铁从其氧化物中置换出来
D.二氧化锰具有强氧化性,能将双氧水氧化为氧气
【解答】
第6页(共14页)A.二氧化硫与氯水反应生成硫酸和盐酸,使氯水褪色,体现二氧化硫的还原性,
与漂白性无关,故A错误;
B.铜与浓硫酸反应生成硫酸铜、二氧化硫和水,硫酸中部分硫元素化合价降低、
部分化合价不变,浓硫酸表现强的氧化性和酸性,使铜化合价升高体现浓硫酸的
强的氧化性,故B错误;
C.硅单质中硅化合价为 0,处于低价,一定条件下能将铁从其氧化物中置换出
来,体现其还原性,故C正确;
D.过氧化氢分解生成氧气和水,反应中二氧化锰起催化作用,故 D错误;
故选:C.
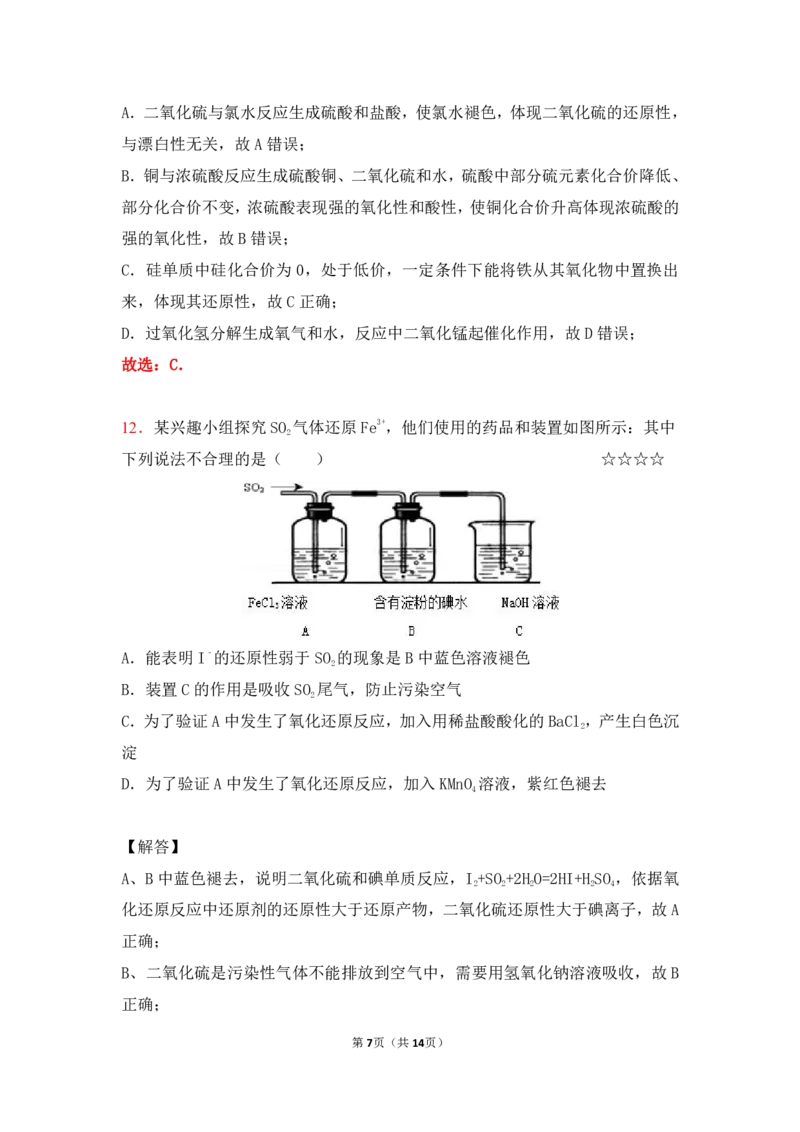
12.某兴趣小组探究SO 气体还原 Fe3+,他们使用的药品和装置如图所示:其中
2
下列说法不合理的是( ) ☆☆☆☆
A.能表明I﹣的还原性弱于SO 的现象是 B中蓝色溶液褪色
2
B.装置C的作用是吸收SO 尾气,防止污染空气
2
C.为了验证A中发生了氧化还原反应,加入用稀盐酸酸化的BaCl,产生白色沉
2
淀
D.为了验证A中发生了氧化还原反应,加入KMnO 溶液,紫红色褪去
4
【解答】
A、B中蓝色褪去,说明二氧化硫和碘单质反应,I+SO+2HO=2HI+HSO ,依据氧
2 2 2 2 4
化还原反应中还原剂的还原性大于还原产物,二氧化硫还原性大于碘离子,故A
正确;
B、二氧化硫是污染性气体不能排放到空气中,需要用氢氧化钠溶液吸收,故 B
正确;
第7页(共14页)C、铁离子氧化二氧化硫为硫酸,2Fe3++SO+2HO=2Fe2++SO2﹣+4H+,加入氯化钡生
2 2 4
成沉淀说明反应进行生成了硫酸根离子,故C正确;
D、二氧化硫、亚铁离子都具有还原性,都可以和高锰酸钾溶液发生反应使之褪
色,不能验证A中发生了氧化还原反应,故D错误;
故选D.
13.下列说法正确的是( ) ☆☆☆☆
A.SO 能使KMnO 水溶液迅速褪色
2 4
B.可以用澄清石灰水鉴别SO 和 CO
2 2
C.硫粉在过量的纯氧中燃烧可以生成SO
3
D.少量SO 通过浓的CaCl 溶液能生成白色沉淀
2 2
【解答】
A、因SO 中硫为+4价,具有较强的还原性.在水溶液中 SO 可以将氧化剂KMnO
2 2 4
等迅速还原而使溶液褪色,故 A正确;
B、因SO 通入澄清石灰水跟CO 通入澄清石灰水反应现象类似:Ca(OH)+SO=CaSO
2 2 2 2 3
↓+HO,CO+Ca(OH)═CaCO↓+HO,都产生白色沉淀,故B错误;
2 2 2 3 2
C、因硫粉在过量的纯氧中燃烧只生成SO 不生成SO,故C错误;
2 3
D、因SO 的水化物为 HSO,其酸性比盐酸弱,不能与CaCl 溶液反应生成白色沉
2 2 3 2
淀,故D错误;
故选A.
14.向溶液X中持续通入气体Y,会产生“浑浊→澄清”现象的是( )
☆☆☆☆
A.X:漂白粉溶液 Y:二氧化硫 B.X:硝酸钡溶液 Y:二氧化硫
C.X:氯化铝溶液 Y:氨气 D.X:偏铝酸钠溶液 Y:二氧化氮
【解答】
第8页(共14页)A.漂白粉溶液中通入二氧化硫,发生氧化还原反应生成硫酸钙,溶液变浑浊,
不会变澄清,故A错误;
B.硝酸钡溶液中通入二氧化硫,发生氧化还原反应生成硫酸钡,溶液变浑浊,
不会变澄清,故B错误;
C.氯化铝溶液中通入氨气,生成的氢氧化铝,不能溶解在氨水中,溶液变浑浊,
不会变澄清,故C错误;
D.偏铝酸钠溶液中通入二氧化氮,二氧化氮与水反应生成硝酸,与偏铝酸钠反
应生成氢氧化铝,然后溶解在硝酸中生成硝酸铝,则会产生“浑浊→澄清”现象,
故D正确;
故选D.
15.下列变化的实质相似的是( ) ☆☆☆☆
①浓硫酸和浓盐酸在空气中敞口放置时浓度均减小
②二氧化硫和氯气均能使品红溶液褪色
③二氧化硫能使品红溶液、溴水褪色
④氨气和碘化氢气体均不能用浓硫酸干燥
⑤常温下浓硫酸用铁制容器存放、加热条件下浓硫酸能与木炭反应
⑥浓硫酸能在白纸上写字,氢氟酸能在玻璃上刻字
⑦二氧化碳、二氧化硫使澄清石灰水变混浊.
A.只有②④⑤ B.只有⑤⑦ C.只有①③⑦ D.只有①②
【解答】
①浓硫酸具有吸水性、浓盐酸具有挥发性,浓硫酸和浓盐酸在空气中敞口放置时
浓度均减小,但原理不同,故错误;
②二氧化硫具有漂白性、次氯酸具有强氧化性,二者都能使品红溶液褪色,但漂
白原理不同,故错误;
③二氧化硫具有漂白性和还原性,二氧化硫使品红溶液褪色体现漂白性、使溴水
褪色体现还原性,故错误;
④氨气能和浓硫酸反应生成盐,碘化氢气体能被浓硫酸氧化,所以前者浓硫酸体
第9页(共14页)现酸性、后者浓硫酸体现氧化性,故错误;
⑤浓硫酸具有强氧化性,能和C、Fe发生氧化还原反应,所以能用同一原理解释,
故正确;
⑥前者浓硫酸体现脱水性、后者氢氟酸体现酸性,所以反应原理不同,故错误;
⑦二氧化碳、二氧化硫都能和澄清石灰水反应生成难溶性钙盐而使澄清石灰水变
浑浊,故正确;
故选B.
16.盛有氯化钡稀溶液的甲乙两试管分别通入SO 至饱和,若向甲试管中加入足
2
量氯水,乙试管中加入足量氢氧化钠溶液,则下列叙述正确的是( )
☆☆☆☆
A.甲、乙两试管都有白色沉淀生成 B.甲、乙两管都没有白色沉淀生成
C.甲管没有白色沉淀生成而乙试管有 D.甲管有白色沉淀而乙试管没有
【解答】
甲中加入足量氯水,氯气和二氧化硫发生氧化还原反应生成硫酸和稀盐酸,硫酸
和氯化钡反应生成硫酸钡沉淀;乙中加入足量氢氧化钠,氢氧化钠和二氧化硫生
成亚硫酸钠,亚硫酸钠和氯化钡发生复分解反应生成亚硫酸钡白色沉淀,所以看
到的现象是甲、乙中都产生白色沉淀,
故选A.
17.同温同压下,将1L SO 和1L Cl 充分混合后通入加有品红的BaCl 溶液中,
2 2 2
可观察到的现象为( ) ☆☆☆
A.溶液褪色 B.产生白色沉淀 C.无明显现象 D.产生黄色沉淀
【解答】
同温同压,体积相同时,物质的量相同,则等物质的量的 SO 和 Cl 在溶液中发
2 2
生了氧化还原反应,离子反应为SO+Cl+2HO═4H++SO2﹣+2Cl﹣,品红不褪色,但
2 2 2 4
硫酸根离子与钡离子结合生成硫酸钡白色沉淀,
第10页(共14页)故选B.
18.下列关于SO 的叙述中,正确的是( ) ☆☆☆☆
2
A.可以用碱石灰来干燥SO 气体
2
B.通入BaCl 溶液中,无明显现象
2
C.因为SO 有漂白性,所以它能使品红溶液、溴水褪色
2
D.将1.12L的SO 气体通入装有 100mL 1mol/L的FeCl 溶液的试管里,恰好完
2 3
全反应
【解答】
A.碱石灰为碱性干燥剂,能够与二氧化硫反应,所以不能干燥二氧化硫,故 A
错误;
B.亚硫酸酸性弱于盐酸,依据强酸制备弱酸规律,所以二氧化硫与氯化钡溶液
不反应,故B正确;
C.二氧化硫使品红褪色体现其漂白性,二氧化硫使溴水褪色体现其还原性,故
C错误;
D.状况不知无法求二氧化硫的物质的量,所以不确定反应是否完全,故D错误;
故选:B.
19.在含有FeCl 和BaCl 的酸性溶液中,通入足量的SO 后有白色沉淀生成,过
3 2 2
滤后,向溶液中滴加KSCN溶液,无明显现象,下列叙述不正确的是( )
☆☆☆☆
A.白色沉淀不含BaSO B.溶液的酸性减弱
3
C.白色沉淀是BaSO D.FeCl 全部被还原为FeCl
4 3 2
【解答】
在FeCl 的酸性溶液中,通入足量的 SO 后,发生反应为:
3 2
2Fe3++SO+2HO═2Fe2++SO2﹣+4H+,反应后溶液显示酸性,Ba2++SO2﹣=BaSO ↓,过滤
2 2 4 4 4
后,向溶液中滴加KSCN溶液,溶液无明显现象,说明溶液中不存在铁离子,
第11页(共14页)A.亚硫酸酸性小于盐酸,所以不可能生成BaSO,故A正确;
3
B.根据以上分析知,溶液中生成硫酸,所以溶液的酸性增强,故 B错误;
C.氯化铁和二氧化硫生成的硫酸根离子与钡离子反应生成 BaSO 沉淀,故 C 正
4
确;
D.通过以上分析知,溶液中氯化铁完全被氧化生成氯化亚铁,故 D正确;
故选B.
20.下列实验现象正确的是( ) ☆☆☆☆
A.将SO 气体通入Ba(NO) 溶液中有白色沉淀生成
2 3 2
B.将足量的SO 气体通入Ba(OH) 溶液中有白色沉淀生成
2 2
C.将SO 气体通入BaCl 溶液中有白色沉淀生成
2 2
D.将NaSO 与BaCl 溶液混合后生成白色沉淀,加稀硝酸沉淀全部溶解
2 3 2
【解答】
A.将SO 气体通入Ba(NO) 溶液中发生反应生成硫酸钡白色沉淀,故A正确;
2 3 2
B.足量二氧化硫与氢氧化钡反应生成亚硫酸氢钡,亚硫酸氢钡溶于水,得不到
沉淀,故B错误;
C.亚硫酸酸性弱于盐酸,将SO 气体通入BaCl 溶液不发生反应,不会有白色沉
2 2
淀生成,故C错误;
D.亚硫酸钠与氯化钡反应生成亚硫酸钡沉淀,亚硫酸钡具有还原性,能够被硝
酸氧化生成硫酸钡沉淀,所以沉淀不会消失,故A正确;
故选:A.
21.除去CO 中混有的少量SO 气体,最好选用的试剂是( ) ☆☆☆☆
2 2
A.澄清石灰水 B.品红溶液 C.NaOH溶液 D.饱和NaHCO 溶液
3
【解答】
A.氢氧化钙与二氧化硫、二氧化碳都反应,故A不选;
B.品红微溶于水,即使达到饱和,溶解度也不大,而且品红和 SO 反应生成的
2
第12页(共14页)物质不稳定,很容易分解,因此不适合用作吸收剂,故 B不选;
C.二氧化硫、二氧化碳都能与氢氧化钠溶液反应,被氢氧化钠溶液吸收,故 C
不选;
D.SO 可与饱和NaHCO 溶液反应生成CO,但CO 不反应,可用于除杂,故D选;
2 3 2 2
故选:D.
22.下列说法正确的是( ) ☆☆☆☆
A.SO 和Cl 使品红溶液褪色的原理相同
2 2
B.浓硫酸分别使胆矾变白、蔗糖变黑时,浓硫酸表现的性质相同
C.浓硝酸和浓硫酸露置在空气中,浓度都降低的原因相同
D.浓硫酸与稀硫酸都能与金属锌反应放出气体,两个反应的氧化产物相同
【解答】
A.氯气的漂白作用是氯气和水反应生成的次氯酸的漂白作用,是次氯酸的强氧
化性的体现;二氧化硫的漂白作用是二氧化硫与水生成的亚硫酸和有色物质结合
为不稳定的无色物质,加热会恢复原来的颜色,褪色原理不同,故 A错误;
B.蔗糖变黑时能够使蔗糖脱水生成碳,表现的是脱水性,胆矾遇浓硫酸变白色,
体现浓硫酸的吸水性,浓硫酸表示的性质不同,故B错误;
C.浓硝酸易挥发出硝酸分子,溶液浓度减小,浓硫酸是难挥发性的酸具有吸水
性使你的减小,浓硝酸和浓硫酸露置在空气中,浓度都降低的原因不相同,故C
错误;
D.浓硫酸和锌发生氧化还原反应生成硫酸锌、二氧化硫和水,稀硫酸和锌反应
生成硫酸锌和氢气,元素化合价升高失电子发生氧化反应D正确,氧化产物为硫
酸锌,故D正确;
故选D.
23.下列各组气体中,在通常状况下能共存,并且都能用浓硫酸干燥的是( )
☆☆☆
A.SO、HS、Cl B.SO、O、NH
2 2 2 2 2 3
第13页(共14页)C.NO、O、H D.SO、CO、O
2 2 2 2 2
【解答】
A.硫化氢具有还原性,能够与浓硫酸反应,不能用浓硫酸干燥,故 A错误;
B.氨气为碱性气体,能够与浓硫酸反应,不能用浓硫酸干燥,故 B错误;
C.一氧化氮与氧气常温下反应生成二氧化氮,不能共存,故 C错误;
D.二氧化硫、二氧化碳、氧气相互不反应,且都与浓硫酸不反应,能够用浓硫
酸干燥,故D正确;
故选D.
第14页(共14页)